稀有金属 2013,37(02),312-319
金属铪的制备方法研究进展
柳旭 王力军 陈松 吴延科 王鑫
北京有色金属研究总院矿物资源与冶金材料研究所
摘 要:
铪因其优异的性能而具有非常重要的应用价值。总结了国内外金属铪的制备方法和研究现状,主要介绍了热还原法(包括镁还原、钙还原、铝还原)和熔盐电解法(包括传统的熔盐电解及直接熔盐电脱氧)制备铪的工艺流程及研究进展,并对各种方法的优劣进行了分析。热还原法利用金属镁、钙等为还原剂还原金属的氯化物或氧化物制备铪,其中,镁还原法因工艺成熟、产品质量稳定,目前是工业上生产铪的主要方法,存在的问题是工序复杂且为间歇性生产;钙还原法虽然有着过程简单,回收率高的优点,但对原料的纯度要求很高,产品纯度一般也较差;铝还原法因易生成铝铪合金不利于工业应用。熔盐电解法是在熔盐电解质中电解铪的化合物制备铪,其中,传统的熔盐电解法具有工艺流程短、操作简单、成本低的优点,存在的问题是电流效率较低;新型的熔盐电脱氧法为铪的制备提供了新思路,进一步缩短了工艺流程,存在的问题是电流效率低,脱氧不完全会导致产品中含氧量较高,这将在一定程度上限制其工业应用。除镁还原法外,目前这些制备方法多限于实验室规模的研究,今后最有希望在工业上应用的是传统的熔盐电解法,但距离产业化应用尚需进行深入研究和扩大实验验证。
关键词:
铪;制备;进展;
中图分类号: TG146.414
作者简介:柳旭(1986-),女,河南驻马店人,博士;研究方向:有色金属冶金;王力军(E-mail:gold@grinm.com);
收稿日期:2012-10-07
基金:国家自然科学基金(50674015);北京有色金属研究总院青年基金项目(53141)资助;
Research Progress in Preparation of Hafnium Metal
Abstract:
Owing to its excellent properties,hafnium has very important application values.The technologies for producing hafnium metal and the present research state at home and abroad was summarized,which mainly introduced the process flow and research progress of metallothermic reduction(including magnesium reduction,calcium reduction,aluminum reduction) and molten salt electrolysis(including general molten salt electrolysis and direct electro-deoxidation).Moreover the advantages and disadvantages analysis for them was performed.Metallothermic reduction was defined as reducing metal-chlorine or metal-oxide to prepare hafnium with magnesium or calcium as reducing agent.The magnesium reduction process was mature and the quality of its product was steady,so it was the main method for producing hafnium.However,the existing problem was that the procedure was complex and discontinuous;although calcium reduction procedure was simple and the recovery rate was high,it had high request for the raw material and the quality of the product was poor.Aluminum reduction was not proper for industrial application because it was easy to produce aluminum-hafnium alloys.Molten salt electrolysis was defined as electrolysis hafnium compounds in electrolyte to produce hafnium,in that,the general molten salt electrolysis had the virtue of short process flow,simple operation and low cost,but it existed the problem of low current efficiency.The new direct electro-deoxidation method provided a new way for producing hafnium,but there not only existed the problem of low current efficiency but also had high oxygen content in the product if not completely deoxidised,which would restrict its industrial application.Except for magnesium reduction process,other technologies were only limited to laboratory scale,the general molten salt electrolysis was the most probable to be applied in industry,and deepening research and expanding experiments should be done before commercialization.
Keyword:
hafnium;preparation;progress;
Received: 2012-10-07
铪位于元素周期表中第ⅣB族,在地壳的丰度超过了Hg,Nb和U,但由于其用途特殊,提取方法复杂,产量较少,价格昂贵,加之熔点较高,因而被称为稀有难熔金属[1]。
铪对中子具有较强的吸收能力,其热中子俘获截面为115b(1b=1×10-28m2),可用作核反应的控制棒、反应堆中的保护涂层、通量衰减器等。金属铪具有较好的耐腐蚀性能,在热水和蒸气混合物中的耐腐蚀性高于钛、锆,可以用作化工的特殊结构材料。另外,铪具有高抗氧化性、良好的导电导热性和较低的电子逸出功,可用于等离子切割电极的等离子发射体。添加了铪元素的合金,其材料强度、耐腐蚀性等会有显著的改善,如含钽、钼的铪基合金可用于抗1650℃高温的飞行器;铌-铪-钨合金可用于火箭和燃气透平。铪还是一种很好的吸气剂,铪钛合金作为吸气剂应用于灯泡、电子管等电气产品中[2,3,4]。
随着经济的迅速发展,研究金属铪的制备方法具有重要的理论和现实意义。自20世纪50年代以来,金属铪的制备相继成为世界各国研究的热点[5,6,7,8]。由于原子能级铪要求铪材料含锆小于2.1%,所以制备满足技术要求的金属铪仍然是当今较难的任务。本文主要比较了铪的各种冶金方法及其应用。目前铪的制备方法主要有金属热还原法和熔盐电解法。
1 金属热还原法
金属热还原法根据原料和还原剂的不同主要分为以下几种方法:镁(钠)还原四氯化铪制备海绵铪(Kroll法);钙、氢化钙还原二氧化铪生产金属铪粉;铝还原二氧化铪法。
1.1 镁(钠)还原四氯化铪制备海绵铪(Kroll法)
1940年,卢森堡科学家W.J.克劳尔发明了镁还原四氯化钛制取海绵钛的方法,因铪与钛性质相似,镁还原法被应用于还原四氯化铪[8]。
镁热还原四氯化铪在800℃,氩气保护下,以金属镁为还原剂反应制取海绵铪。镁还原法的主要工艺流程见图1,反应方程式为:
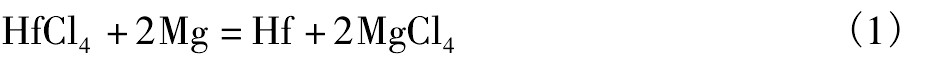
镁还原法工艺主要包括由二氧化铪碳化氯化制备四氯化铪、粗四氯化铪的提纯、四氯化铪的镁还原、海绵铪与氯化镁及过量镁的真空蒸馏分离等几个方面。
1954年,Holmes等[8]应用镁还原制备锆的设备制备出了海绵铪。由于铪比锆的吸水性更强,因此对氯化及提纯过程有更高的要求。镁过量40%,得到硬度为20~25 HRC的海绵铪,可直接进行热铸、加工成板材。
1960年,Gerald等[9]将氧氯化铪、二氧化铪及气态的四氯化铪在有碳存在的条件下逐渐升高温度,得到氯化铪及一氧化碳;氯化铪再被金属镁还原。还原温度控制在750~850℃,镁过量两倍。制取的海绵铪在960℃下真空蒸馏18 h后,铪中氧含量为600×10-6,而用传统的方法制备的海绵铪氧含量为1800×10-6。
2012年,叶章根等[10]报道了铪的制备方法为镁还原法,主要研究了海绵铪的电解精炼,在合理控制电解质的纯度及密度、电流密度、电解时间的条件下,海绵铪精炼后铪的粒度可小至40~90μm。
目前该法工艺成熟、生产出来的铪产品质量稳定,是工业上生产金属铪的主要方法,但此法还存在以下的问题:(1)生产过程为间歇生产,影响效率;(2)工艺流程长、操作复杂;(3)生产过程中会产生氯气,产生环境污染。
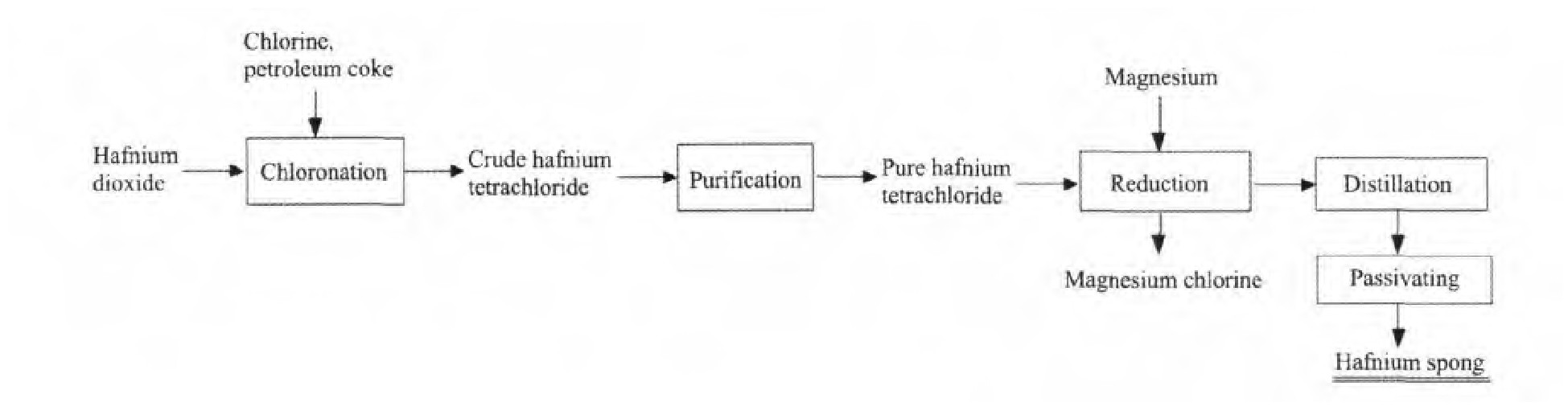
图1 镁还原法制备金属铪的工艺流程图Fig.1 Process flow diagram of preparation of hafnium by magnesium reduction
1.2 钙、氢化钙还原二氧化铪生产金属铪粉
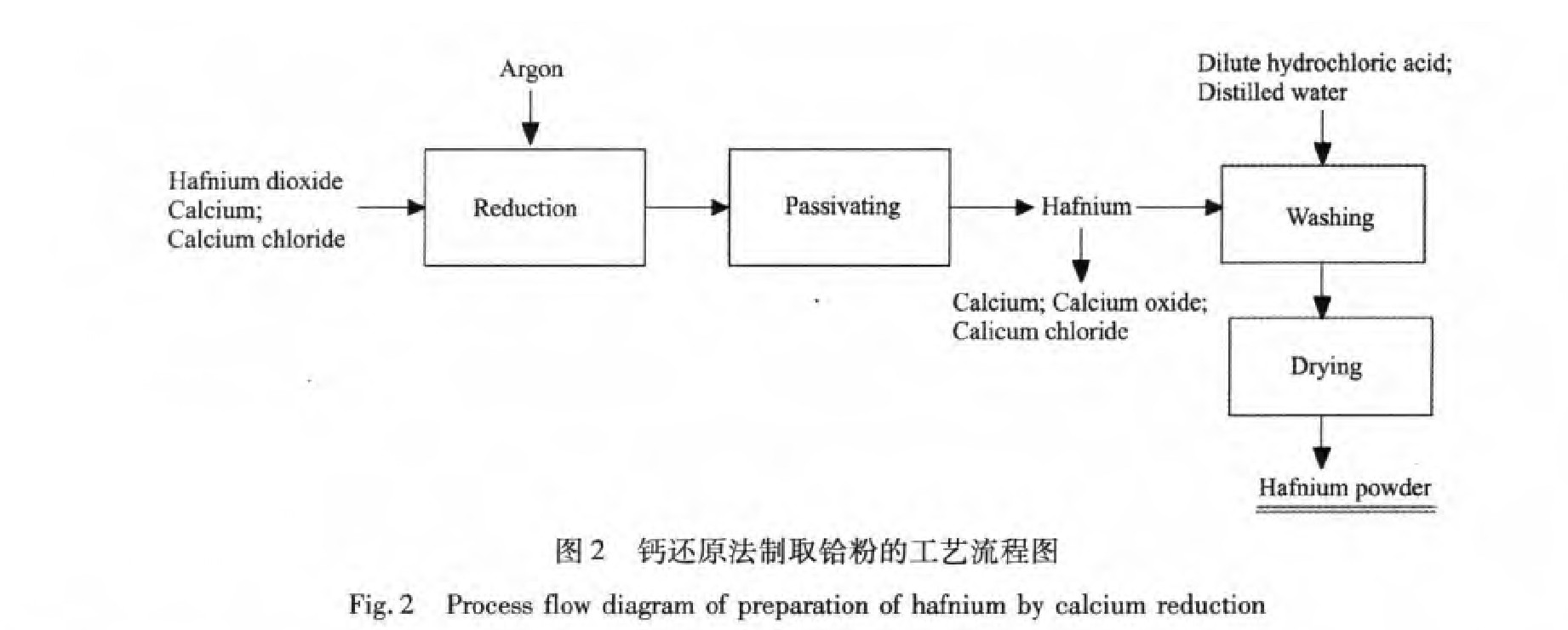
钙还原法是以Hf O2为原料,钙或氢化钙为还原剂,Ca Cl2为助剂,抽真空在氩气保护下在1000℃左右进行还原反应。还原产物经酸洗、水洗、过滤、干燥即得到金属铪。主要发生的化学反应为:

钙还原法工艺流程如图2所示。
Sharma等[11]研究了用氢化钙及金属镁还原二氧化铪制备金属铪。氢化钙还原法是先将过量80%的Ca H2磨成粉后,再与Hf O2混合,在925℃下在密闭反应器中进行还原。镁还原是在镁过量50%,1000℃下密闭反应器中进行还原。但研究表明,与钙还原相比,Ca H2和Mg还原的效果不如Ca还原所得的铪纯度高。
选择钙作还原剂的原因主要有以下几点:(1)氧化钙的热稳定性比二氧化铪高,在热力学上具有可行性;(2)生成的氧化钙易与产品分离;(3)钙在铪中的溶解性低,未参与反应的钙不易与产物铪形成合金;(4)钙的价格低廉。
早在20世纪70年代,Sharma等[11]研究了钙还原二氧化铪制备金属铪。研究表明,用过量70%的钙,在960℃下反应2 h得到含氧量为6000×10-6,含氮量为147×10-6的铪粉。进一步的研究发现用Ca Cl2作为钙还原过程中的助溶剂可降低所制备的金属中的氧含量,残余氧以Ca O的形式存在,因此目前研究较多的是钙和氯化钙及二氧化铪体系。
钙还原二氧化铪体系的操作温度需控制在900~1200℃,而钙的熔点为842℃,Ca Cl2的熔点为775℃,在还原过程中熔盐表面的部分钙及氯化钙熔盐会挥发掉,从而在一定程度上减小了产率、增加了成本。Na Cl可降低体系的熔点,2009年,Abdelkader等[5]向上述体系中加入了Na Cl大大降低了体系的熔点,新体系的熔点为504℃,很好的解决了因温度过高带来的一系列问题。他们利用30%Na Cl、70%Ca Cl2、过量50%钙的体系中还原二氧化铪,产物铪的含氧量为960×10-6。在这种改进的体系中进行钙还原,操作温度比较低、还原过程更容易控制、得到的产品中氧含量有所降低,开辟了钙还原的新思路。
钙还原法具有过程简单、回收率高的优点,但此法对原料的纯度要求很高,产品纯度有待于提高,需要进一步研究才能应用于工业生产。
1.3 铝还原二氧化铪法
铝还原法制备金属铪一般先将铪的氧化物经铝热还原制得铪铝合金[12],然后铪铝合金再经高温真空脱除铝和电子束熔炼脱除其他残余杂质而得到较纯的金属铪。其工艺流程如图3所示。主要发生的化学反应为:
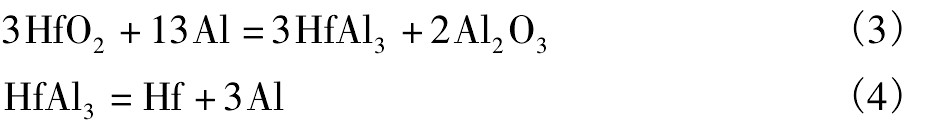
1965年,Gosse和Albert报道了一种通过铝热还原二氧化铪制备金属铪的方法[13]。该方法首先是在真空状态,温度高于2773 K条件下,将铪的氧化物(Hf O2)与铝进行反应还原得到铝铪合金,然后再将得到的铝铪合金进行脱铝得到粗金属铪。20世纪80年代,Juneja等[14]研究了铝还原第Ⅳ族金属氧化物制备其金属。与铝还原法相似,Gosse等[13,15]用硅、碳来还原二氧化铪制备铪,均不太成功。
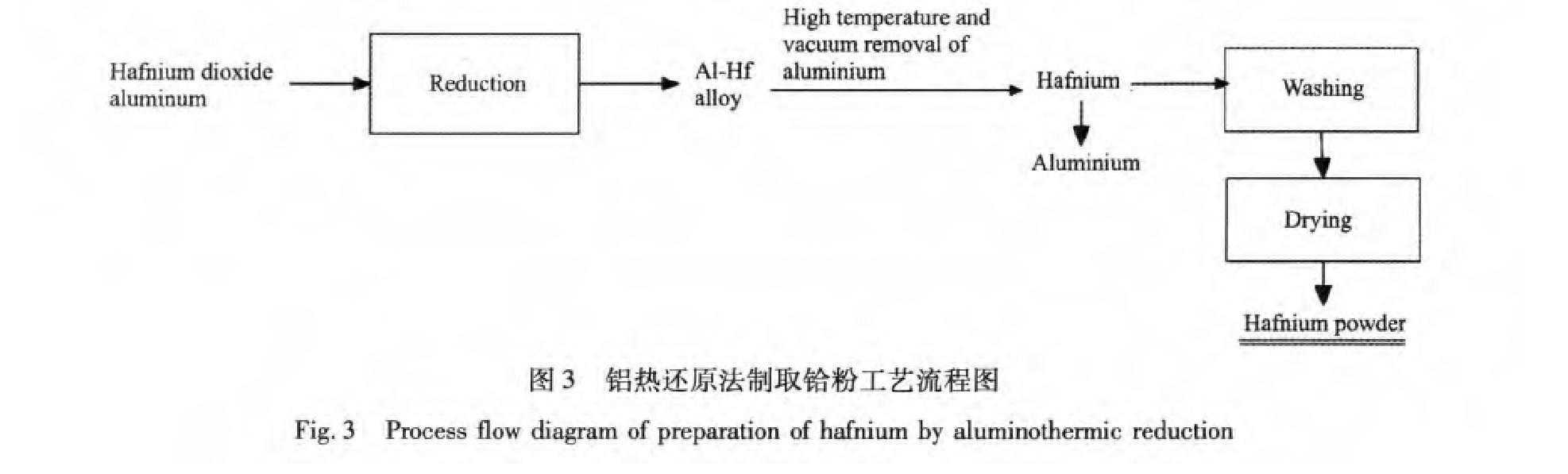
与其他制备方法相比,铝还原法具有以下优点:(1)铝价格相对便宜,比较容易加工;(2)用量较少;(3)熔融的氧化铝废渣可以回收利用。铝还原法的还原温度较高,具有较高的能耗,易形成铝-铪合金,加上铝还原的技术还不够成熟,目前此法还无法得到应用。
2 熔盐电解法
2.1 传统的熔盐电解法
热还原法存在工序复杂、能耗高等问题,因此研究流程短、成本低及对环境友好的制备方法受到各国的重视。由于电能是一种清洁的能源,且电解操作简单,所以电化学法制备金属铪近年来得到了一定的关注[16,17,18,19,20,21,22]。
熔盐电解法制备金属铪,常以K2Hf F6或者HfCl4为原料,以石墨为阳极,不锈钢棒为阴极,碱金属氯化物为电解质进行电解,四价的铪离子将被还原在阴极沉积,还原的产物经破碎、水洗得到所需金属。由于与钛和锆的氯化物(低共价性)相比,四氯化铪在熔盐中能保持更长时间,即铪的氯化物比较稳定[21]。熔盐电解制备金属铪的电解过程中主要的反应为:
阴极:Hf4++4e-=Hf(5)阳极:4Cl--4e-=2Cl2(6)总反应:Hf4++4Cl-=Hf+2Cl2(7)
铪的制备有不同的电解质体系,以Hf Cl4-Na Cl-KCl体系为例,熔盐电解法的工艺流程见图4。
一些研究者报道了铪在不同的碱金属熔盐中的电沉积,早期的一些研究及其研究的相关结果列于表1。
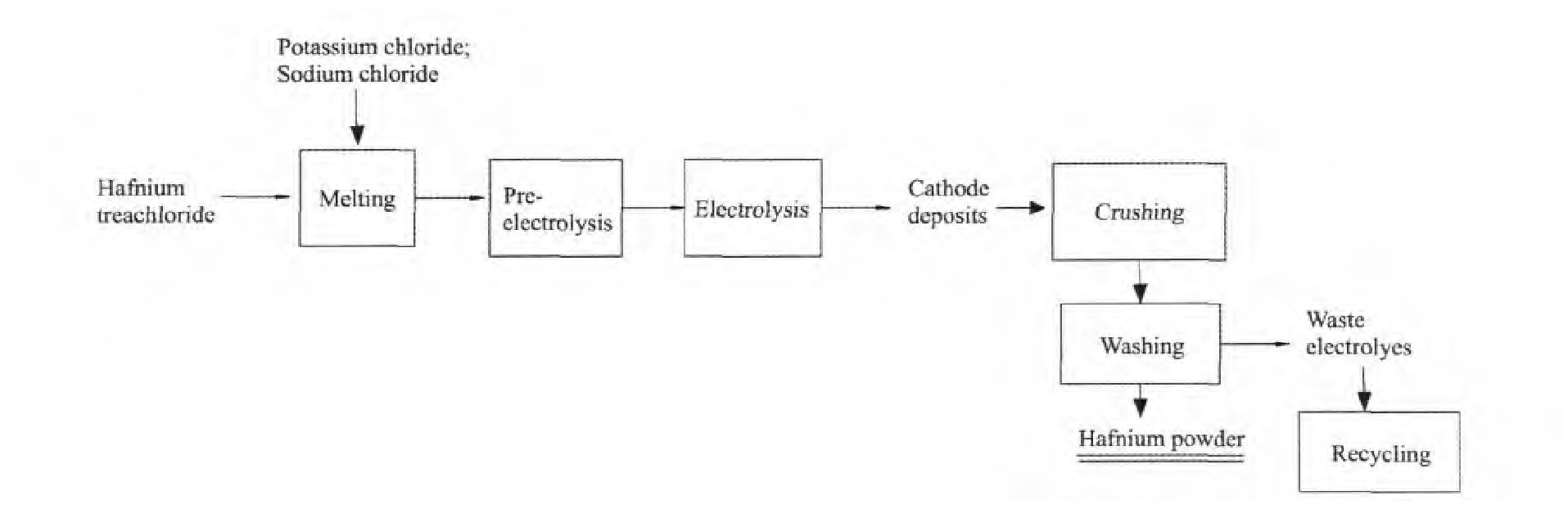
图4 熔盐电解法制取铪粉工艺流程图Fig.4 Process flow diagram of preparation of hafnium by molten salt electrolysis
表1 熔盐电沉积铪的研究Table 1 Research of electrowinning hafnium 下载原图
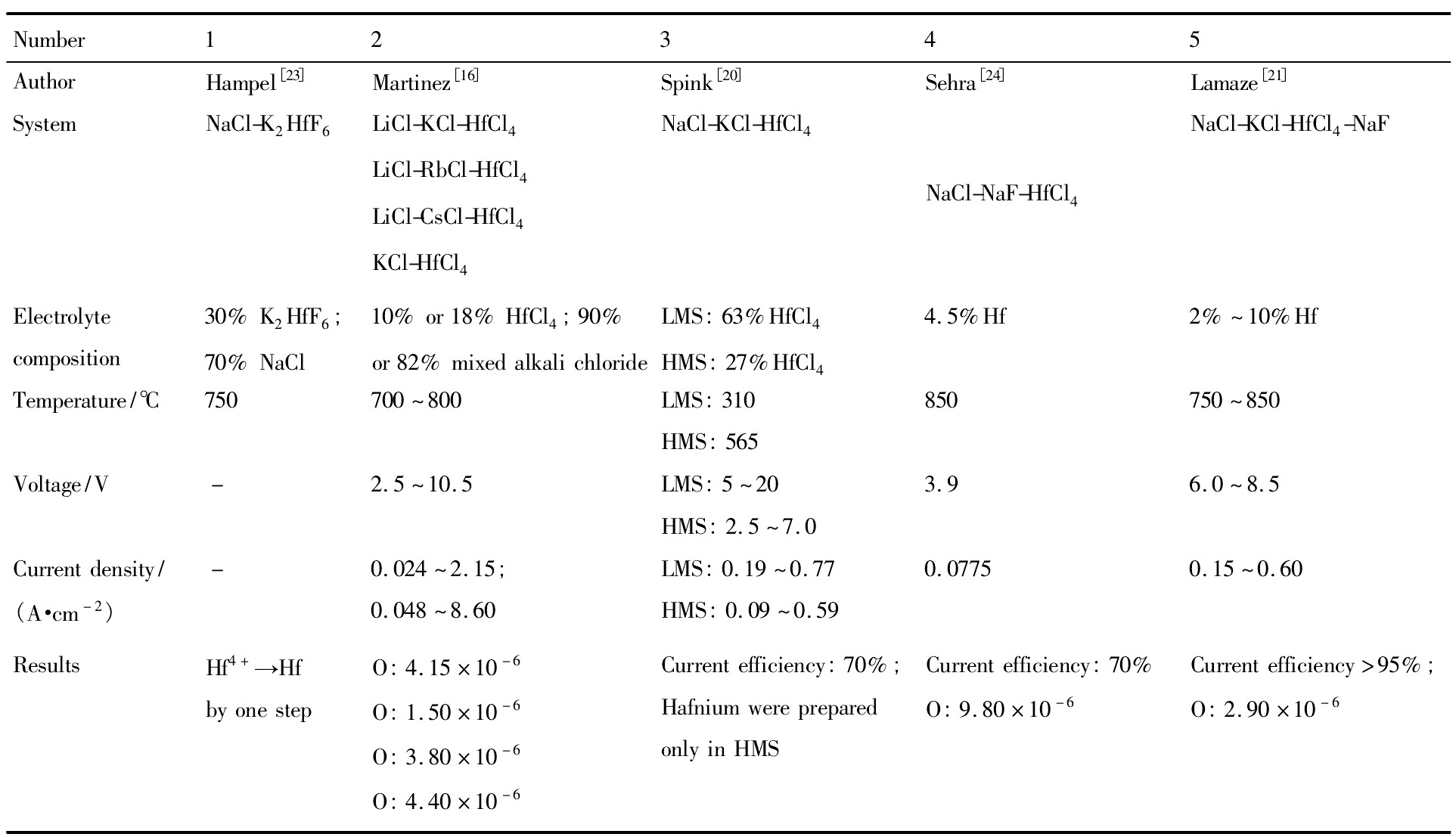
Notes:LMS-Low temperature melt system;HMS-High temperature melt system
表1 熔盐电沉积铪的研究Table 1 Research of electrowinning hafnium
由表1可见,传统的熔盐电解法可成功制备出金属铪,这一过程成功的关键在于控制好原料如Hf Cl4中的氧含量及其他杂质的含量。熔盐电解法具有设备造价低、原材料易制备、电解操作容易等优点,缺点是高温下进行电解过程中电解质易挥发、多种价态铪离子在阴极不完全放电和反复电解导致电流效率低下,另外由于铪具有较高的熔点,电解只能在其熔点以下进行,产物为固体粉末状,部分产物弥散在电解质中,影响电解质性能。2.2新型的熔盐电解法-二氧化铪直接电脱氧法
20世纪90年代末,剑桥大学的Fray等[25]在研究减少钛表面的氧化膜时发现了可以用电化学的方法直接将金属的氧化物还原为金属粉末的方法。2000年Fray等[25]在Nature杂志上首次报道了此方法,该方法是基于熔盐电解法利用金属氧化物制备其单质的方法,又称FFC法。FFC法可以生产的公斤级金属有Ti,Cr,Ta,可以成功制备的金属有Zr,Hf,Be,Mg,Ca,Ba,V,Nb,W,Fe,Cu等[25~31]。FFC工艺是将单一或混合金属氧化物压制成块作为阴极,在熔盐中(通常为Ca Cl2熔盐)经一步电解得到杂质含量低得金属单质或合金。该法的工艺流程如图5所示[26]。

图5 FFC法工艺流程Fig.5 Process flow diagram of preparation of hafnium by FFC method
用此法来制备金属铪,以二氧化铪为原料,以氯化钙或氯化钙与其他碱金属氯化物为电解质,二氧化铪压制成块作为阴极,石墨或其他惰性电极作为阳极,直接进行电解即可。以石墨作为阳极为例,可能发生的反应为:
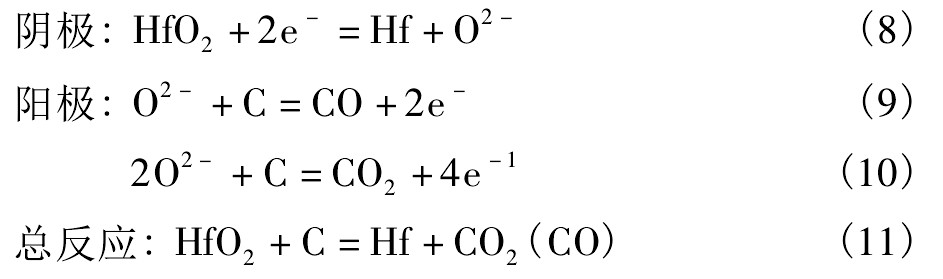
该法生产工艺简单,阳极产生的气体为CO,CO2,以氧化物为原料经一步电解得到杂质很低的金属,不仅缩短了工艺流程,也减少了能耗和环境污染。存在的问题是电流效率低、反应过程中随着含氧量的降低电脱氧效率也越来越低。目前应用此法制备铪还处于实验研究阶段。
3 结语
1.金属热还原法中,钙还原法虽然具有工艺简单,回收率高的优点,但也存在较大的缺点:对原料的纯度要求很高、产品纯度一般也较差。目前,克劳尔法是一种比较成熟的方法,也是工业上生产铪的主要方法,但也存在工序复杂、间歇生产、污染严重等一系列问题。
2.传统的熔盐电解法电解法具有工序简单、污染小等优点,缺点是电流效率低、铪与熔盐难分离、电极过程复杂;FFC法是近几年发展的一种新方法,操作简单,要得到氧含量低的产品需延长电解时间,但这在一定程度上又降低了电流效率,因此使用此工艺需要很好平衡两者之间的关系。
3.目前金属铪的制备大多尚处于实验阶段,今后最有希望在工业上应用的是传统的熔盐电解法,如何将其工业化是今后努力的一个方向。对铪的进一步研究需要改进实验方法、运用更先进的技术手段等。
参考文献
[1] Xiong B K.Zirconium and Hafnium─twin sisters inthe rare metals kingdom[J].Rare Metals Letters,2005,24(1):41.(熊炳昆.稀有金属王国中的姊妹花―锆和铪[J].稀有金属快报,2005,24(1):41.)
[2] Luo X W,Luo F C.The properties,application,man-ufacturing techniques and developing prospect of zirconi-um and hafnium materials[J].Jiangxi Metallurgy,2009,29(4):39.(罗新文,罗方承.锆铪材料的性质、应用、生产技术与发展前景[J].江西冶金,2009,29(4):39.)
[3] Xiong B K.The preparation and application of hafnium[J].Rare Metals Letters,2005,24(5):46.(熊炳昆.金属铪的制备及应用[J].稀有金属快报,2005,24(5):46.)
[4] Xiong B K,Yang X M,Luo F C,Luo F C,Zhang W.Zirconium and Hafnium Compounds Application[M].Beijing:Metallurgical Industry Press,2002.1.(熊炳昆,杨新民,罗方承,张伟.锆铪及其化合物应用[M].北京:冶金工业出版社,2002.1.)
[5] Abdelkader A M,Daher A.Preparation of hafniumpowder by calciothermic reduction of HfO2 in moltenchloride bath[J].Journal of Alloys and Compounds,2009,469(1-2):571.
[6] Kuznetsov S A.Electrochemistry of refractory metals inmolten salts:application for the creation of new andfunctional materials[J].Pure Applied Chemistry,2009,81(8):1423.
[7] Sehra J C,Vijay P L.Refractory metals extraction byfused salt electrolysis,the present status and the futureprospects[J].Mineral Processing and Extractive Metal-lurgy Review,1998,19(1):523.
[8] Holmes H P,Barr M M,Gilbert H L.Production ofhafnium[R].American:U.S.Bureau of Mines,1954.
[9] Gerald W E,Albany O,Richard W B.Produc-tion of hafnium metal[P].United States:96058,1960.
[10] Ye Z G,Chen S,Li W L,Wu Y K,Wang L J.Elec-tro-refining of hafnium in KCl-NaCl-K2HfF6 molten salt[J].Chinese Journal of Rare Metals,2012,36(5):791.(叶章根,陈松,李文良,吴延科,王力军.熔盐电解精炼铪的研究[J].稀有金属,2012,36(5):791.)
[11] Sharma I G,Vijay P L,Sehra J C,Sundaram C V.Preparation of hafnium metal by calciothermic reductionof HfO2[R].Bhabha Atomic Research Center,Bhabha,India,1975.
[12] Sharma I G,Majumdar S,Chakraborty S P,Suri A K.Aluminothermic preparation of Hf-Ta and Nb-10Hf-1Tialloys and their characterization[J].Journal of Alloysand Compounds,2003,350:184.
[13] Gosse G,Albert P,Leh P R.Production of hafnium bydirect reduction of its oxide in the electron bombardmentfurnace[J].Memoires Scientifiques de la revue de Met-allurgie,1965,62(57):407.
[14] Juneja J M,Vijay P L,Sehra J.Studies on the alumi-nothermic reduction of pure strontium oxide[in]Pro-ceedings of the symposium on metallothermic processesin metal and alloy extraction.Conference,Nagpur,1983.102.
[15] Sundaram C V,Mukherjee T K,Sharma B P.Openaluminothermic reduction of columbium(Nb)pentoxideand purification of the reduced metal[A].Proceeding ofthe International Symposium on Fifty Years of Metallurgy[C].Banaras,1973.1.
[16] Martinez G M,Wong M M,Couch D E.Electrowin-ning of hafnium from hafnium tetrachloride[J].Trans.Met.Soc.AIME,1969,245(10):2237.
[17] Nettle J R,Hiege J M,Baker D H.Hafnium electrore-fining[J].High-Temperature Refractory Metals,1969,34(1):385.
[18] Sharma I G,Gupta C K.Study on electrorefining ofcalciothermic hafnium[J].Journal of Nuclear Materi-als,1978,74(1):19.
[19] Sehra J C,Suri A K.Refractory and reactive met-al extraction by fused salts electrolysis[J].HighTemperature Materials and Processes,1993,11(1-4):255.
[20] Spink D R,Vijayan C P.Hafnium electrowinningstudies[J].Journal of the Electrochemical Society,1974,121(7):879.
[21] Lamaze A P,Charquet D.Development of hafnium tet-rachloride electrolysis[A].Refractory Metals-Extrac-tion,Processing and Applications[C].Warrendale,1990.231.
[22] Moriyama.Metallurgy of zirconium and hafnium(Ⅳ):a historical review[J].Transactions of the Mining andMetallurgical Association,Kyoto,1993,21(10):682.
[23] Hampel C A.The Encyclopedia of Electrochemis-try[M].Reinhold Pub.Corp.New York,1964.692.
[24] Sehra J C,Rakhasia R H,Shah V D.Studies onthe preparation and purification of hafnium metal[J].High Temperature Materials and Process,1997,16(2):123.
[25] Fray D G,Farthing T W,Chen G Z.Direct electro-chemical reduction of titanium dioxide to titanium in mol-ten calcium chloride[J].Nature,2000,407(6802):361.
[26] Fenn A J,Cooley G,Fray D J.Exploiting the FFCcambridge process[J].Advanced Materials and Proces-ses,2004,162(2):51.
[27] Hu X F,Xu Q.Preparation of tantalum by electro-de-oxidation in CaCl2-NaCl melt[J].Acta MetallurgicaSinica,2006,42(3):285.(胡小峰,许茜.CaCl2-NaCl熔盐电脱氧法制备金属Ta[J].金属学报,2006,42(3):285.)
[28] Okabe T H,Oda T,Mitsuda Y.Titanium powder pro-duction by preform reduction process[J].Journal of Al-loys and Compounds,2004,364(1-2):156.
[29] Chen G Z,Gordo E,Fray D J.Direct electrolyticpreparation of chromium powder[J].Metallurgical andMaterials Transactions,2004,35B(2):223.
[30] Yana X Y,Fray D J.Electrochemical studies on re-duction of solid Nb2O5 in molten CaCl2-NaCl eutectic[J].Journal of the Electrochemical Society,2005,152(10):D12.
[31] Chen G Z,Fray D J.A morphological study of the FFCchromium and titanium powders[J].Mineral Processingand Extractive Metallurgy,2006,1115(1):49.