直接电氧化合成乙基香兰素
刘万民1, 2,胡国荣2,肖鑫1,钟萍1,许律1
(1. 湖南工程学院 化学化工学院,湖南 湘潭,411104;
2. 中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘要:在硫酸介质中,以3-乙氧基-4-羟基苯乙醇酸为原料,在Pt电极上直接电氧化合成乙基香兰素。采用极化曲线技术确定该阳极过程的速度控制步骤为扩散传质步骤,结合循环伏安技术和恒电位电解技术确定直接电氧化合成乙基香兰素的合适反应条件:在35 ℃下,以Pt电极为阳极,Ni电极为阴极,0.5 mol/L 3-乙氧基-4-羟基苯乙醇酸+0.25 mol/L硫酸溶液为电解液,控制阳极电位于1.35 V恒电位电解1 h,乙基香兰素的产率可达66.68%,电流效率可达54.72%。
关键词:3-乙氧基-4-羟基苯乙醇酸;乙基香兰素;直接电氧化;极化曲线;循环伏安
中图分类号:O646 文献标志码:A 文章编号:1672-7207(2012)03-0842-06
Synthesis of ethylvanillin by direct electrooxidation
LIU Wan-min1, 2, HU Guo-rong2, XIAO Xin1, ZHONG Ping1, XU Lü1
(1. College of Chemistry and Chemical Engineering, Hunan Institute of Engineering, Xiangtan 411104, China;
2. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Ethylvanillin was prepared by direct electrooxidation of 3-ethoxy-4-hydroxy mandelic acid dissolved in sulfuric acid solution. The diffusion step was confirmed as the rate determining step by means of polarization curves. Combining cyclic voltammograms with the constant potential electrolysis method, the feasible conditions of direct electrooxidation synthesis of ethylvanillin are determined as follows: anode Pt electrode, cathode Ni electrode, electrolyte 0.5 mol/L 3-ethoxy-4-hydroxy mandelic acid and 0.25 mol/L sulfuric acid solution, temperature 35 ℃, time 1 h and anode potential 1.35 V. The yield of ethylvanillin is 66.68% and the current efficiency is 54.72%.
Key words: 3-ethoxy-4-hydroxy mandelic acid; ethylvanillin; direct electrooxidation; polarization curve; cyclic voltammogram
乙基香兰素,化学名3-乙氧基-4-羟基苯甲醛,无天然来源,是当今世界上最重要的合成香料之一。由于乙基香兰素的香气浓,单位使用量少,可降低成本,是香兰素在香料应用领域的替代品[1-4]。目前,国际市场上的乙基香兰素大部分采用邻乙氧基苯酚-乙醛酸法生产[5-6]。邻乙氧基苯酚-乙醛酸法制取乙基香兰素均需经过缩合、氧化和脱羧3个步骤,即首先在碱性条件下将邻乙氧基苯酚与乙醛酸缩合生成3-乙氧基- 4-羟基苯乙醇酸(简称EHMA),进而在高温条件下用硫酸铜或氧化铜催化氧化碱性介质中的EHMA生成3-乙氧基-4-羟基苯乙酮酸,然后于酸性介质中脱羧得到乙基香兰素。该法中的氧化步骤采用的是化学氧化法,作为氧化剂或催化剂的硫酸铜或氧化铜在反应完成后必须除去,这一后处理过程不仅复杂,而且影响产品的质量。如果在氧化步骤采用电化学氧化法来氧化EHMA,则无须外加氧化剂或催化剂,而是以最清洁的电子作氧化剂。相对于化学氧化法而言,电化学氧化法还具有工艺流程短、操作简单、节省原料、提高产品纯度和无环境污染等优点[7]。迄今为止,关于电氧化EHMA制备乙基香兰素的报道极少[8-9]。本文作者在碱性介质中用聚邻甲苯胺-Cu2+膜电极间接电氧化EHMA制备乙基香兰素[10]。尽管此法相对于化学氧化法具有上述优势,但氧化步骤完成后,仍需脱羧处理以获得乙基香兰素。为此,本文作者采用Pt电极直接电氧化酸性介质中的EHMA,将氧化步骤与脱羧步骤合二为一,缩短了乙基香兰素的制备工艺流程,并获得了良好的效果。
1 实验
1.1 仪器与试剂
CHI660B型电化学工作站(上海辰华仪器公司),76-1型恒温水浴槽(金坛市金南仪器厂),PS-1型恒电位/恒电流仪(北京欧亚中兴科技有限公司),WQF-410型傅里叶变换红外光谱仪(北京第二光学仪器厂)。硫酸,分析纯;EHMA,根据文献[11]自制;溶液均用二次去离子水配制。
1.2 极化曲线、循环伏安及恒电位电解实验
在H型双极室三电极电解槽内,以Pt电极作工作电极,极化曲线和循环伏安实验电极尺寸(长×宽)为4 mm×5 mm(非工作面用环氧树脂封闭),电解实验电极尺寸(长×宽)为40 mm×20 mm;极化曲线和循环伏安实验中采用尺寸为30 mm×40 mm的Pt片作辅助电极,电解实验中采用尺寸为30 mm×40 mm的Ni片作辅助电极;以饱和甘汞电极为参比电极,通过鲁金毛细管与工作电极相连。极化曲线和循环伏安曲线均在电化学工作站上测定;恒电位电解实验在恒电 位/恒电流仪上进行。文中所述电位均相对于饱和甘汞电极。
1.3 乙基香兰素的分析
采用WQF-410型傅里叶变换红外光谱仪表征乙基香兰素;采用亚硫酸氢钠-碘量法测乙基香兰素的含量[12]。
2 结果与讨论
2.1 EHMA在Pt电极上电氧化电位的确定
图1所示为35 ℃时,将Pt电极分别置于0.25 mol/L硫酸溶液(底液)及0.5 mol/L EHMA+0.25 mol/L硫酸溶液(研究液)中,以100 mV/s扫描速率测得的循环伏安曲线。由图1可知:在底液(曲线1)中,当正向扫描至1.35 V时有氧化电流产生,扫描至1.5 V后,氧化电流迅速增大,并且伴随着大量氧气气泡的析出。而在研究液(曲线2)中,正向扫描至0.7 V附近时就有氧化电流产生,扫描至1.1 V后氧化电流明显增大,在1.35 V处出现一个氧化峰,随后氧化电流逐渐衰减;扫描至1.55 V后,氧化电流重新开始升高,继续扫描时,Pt电极上有氧气气泡析出。通过对底液及研究液中的循环伏安曲线分析可知:硫酸介质中的EHMA在Pt电极上于0.7 V附近开始氧化,随着电位的变正,氧化电流迅速增大,直至电极表面的EHMA浓度趋近零,氧化电流于1.35 V 处达到最大值,亦即EHMA的氧化反应速度达到最大值;而当电位达到1.55 V 后,氧气的析出占据了主要地位。因此,硫酸介质中EHMA在Pt电极上的电氧化电位应控制在1.0~1.5 V 之间,尤其以1.35 V最好。
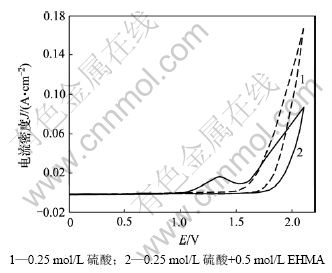
图1 0.25 mol/L 硫酸及0.25 mol/L硫酸+0.5 mol/L EHMA溶液的循环伏安曲线
Fig.1 Cyclic voltammograms of 0.25 mol/L H2SO4 and 0.25 mol/L H2SO4 + 0.5 mol/L EHMA solutions
2.2 不同硫酸浓度中的循环伏安实验
由2.1节分析可知:在阳极电位1.35 V下,Pt电极在溶有EHMA的硫酸介质中主要包括以下电极反应或化学反应。
(1) 阳极区
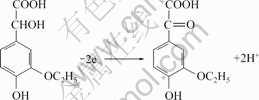 (1)
(1)
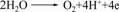 (2)
(2)
(2) 阴极区
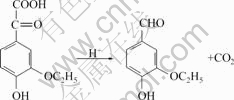 (3)
(3)
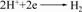 (4)
(4)
H+不仅参与了阳极反应与阴极反应,而且对EHMA脱去CO2具有催化作用。因此,为了考察硫酸浓度对实验结果的影响,在控制其他条件不变(温度35 ℃,EHMA浓度0.5 mol/L,扫描速度100 mV/s)的情况下,测定了不同硫酸浓度中的循环伏安曲线,如图2所示。
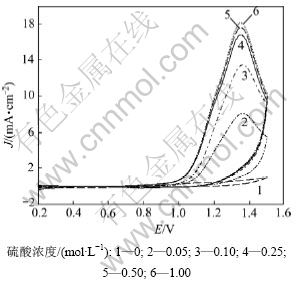
图2 不同浓度硫酸+0.5 mol/L EHMA溶液的循环伏安曲线
Fig.2 Cyclic voltammograms of H2SO4 with different concentrations and 0.5 mol/L EHMA solutions
由图2可知:当硫酸浓度为0 mol/L时,在1.35 V处几乎没有氧化电流产生;硫酸浓度由0增大至0.25 mol/L时,氧化电流增加很快,峰电流与硫酸浓度之间几乎呈线性关系;而当硫酸浓度大于0.25 mol/L时,氧化电流增加很小。这是因为硫酸在该电化学体系中主要起3个方面的作用:作为支持电解质增强溶液的电导率、参与电极反应以及加快脱羧反应的速度。溶液中没有硫酸时,电导率很小,EHMA在Pt电极上几乎不发生电氧化;硫酸浓度较小时,溶液的电导率较小,EHMA的电氧化速度也较小,表现出氧化电流也较小;硫酸浓度较大时,虽然溶液的电导率和脱羧反应的速度均得到了提高,但由反应式(1)可知:H+浓度增加不利于EHMA的电氧化,致使氧化电流增加较小。因此,在硫酸所起的这3个作用之间有一个平衡浓度,根据图2确定为0.25 mol/L。
2.3 电化学合成过程中速度控制步骤的确定
硫酸介质中的EHMA在Pt电极上直接电氧化合成乙基香兰素的阳极过程至少由以下步骤串联组成。
(1) 反应前液相传质步骤:溶液本体中的EHMA分子向Pt电极表面附近液层迁移。
(2) 电化学反应步骤:高过电位下,EHMA分子在Pt电极/溶液界面上一次失去2个电子生成3-乙氧基-4-羟基苯乙酮酸分子;或者,低过电位下,EHMA分子在Pt电极/溶液界面上依次失去2个电子生成3-乙氧基-4-羟基苯乙酮酸分子。
(3) 随后转化步骤:Pt电极表面及其附近液层中的3-乙氧基-4-羟基苯乙酮酸分子在硫酸作用下脱去CO2生成乙基香兰素分子。
(4) 反应后的液相传质步骤:Pt电极及其附近液层中的乙基香兰素分子向溶液本体中迁移。
在上述4个串联步骤中,第(3)步和第(4)步的速度较快,速度控制步骤可能是第(1)步或第(2)步或是第(1)步和第(2)步同时作为控制步骤。
为了确定电化学合成过程中的速度控制步骤,测定了不同温度下Pt电极在0.5 mol/L EHMA+0.25 mol/L硫酸溶液体系中的稳态极化曲线和阳极极化曲线,如图3和4所示。
由图3可知:该体系的静止电位为0.685 V。在过电位较大时,还原反应可以忽略,阳极过电位与电流密度之间符合塔菲尔(Tafel)关系。将Tafel区线性部分外推得虚线8,其与静止电位线(虚线7)的交点即是交换电流密度的对数值lg J0[13],由此可计算出不同温度下的交换电流密度J0,如表1所示。

图3 不同温度时0.5 mol/L EHMA+0.25 mol/L硫酸溶液的稳态极化曲线
Fig.3 Steady state polarization curves of 0.5 mol/L EHMA and 0.25 mol/L H2SO4 solution at different temperatures
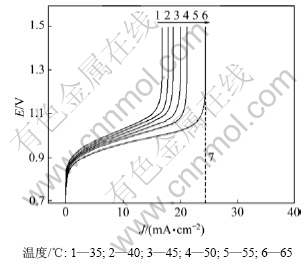
图4 不同温度时0.5 mol/L EHMA+0.25 mol/L硫酸溶液的阳极极化曲线
Fig.4 Anodic polarization curves of 0.5 mol/L EHMA and 0.25 mol/L H2SO4 solution at different temperatures
由图4可知:随着电极电位的增大,电流密度逐渐出现了一个极限值,即极限扩散电流密度Jd。作极化曲线极限值部分的切线得虚线7,其与横轴的交点即是极限扩散电流密度Jd,由此可求出不同温度下的极限扩散电流密度Jd,如表1所示。
表1 不同温度下的交换电流密度J0和极限扩散电流密度Jd
Table 1 Exchange current density J0 and limited diffusion current density Jd of different temperatures

由表1可知:在35~65 ℃之间,该电化学体系的交换电流密度很小,极限扩散电流密度的温度系数也很小,而同一温度下的极限扩散电流密度远远大于交换电流密度。因此,当外加电流密度趋近于极限扩散电流密度时,很容易出现浓差极化现象,即扩散传质步骤很容易成为整个电极过程的速度控制步骤。
为了进一步确定电化学合成过程中的速度控制步骤,测定了35 ℃下,Pt电极在不同EHMA浓度的研究液中的阳极极化曲线,如图5所示。

图5 不同EHMA浓度下的阳极极化曲线
Fig.5 Anodic polarization curves of EHMA with different concentrations
由图5可知:在没有外力搅拌作用下,当EHMA的浓度从0.1 mol/L增加至0.5 mol/L时,其极限扩散电流密度相应地成倍数增加,符合浓差极化中Jd=nFDc0/δ(式中:n为参与电极反应的电子数;F为法拉第常数;D为扩散系数;c0为反应物本体浓度;δ为扩散层厚度)的关系。而当EHMA的浓度继续增大至0.75 mol/L乃至1.0 mol/L时,极限扩散电流密度增加较少。这可能是由于EHMA分子的基团较多,体积较大,溶液中EHMA的浓度较大时,空间阻碍作用彰显出来,造成极限扩散电流密度增大不多。此外,对比曲线3和曲线6可知:在其他条件均不变的情况下,增加搅拌时,极限扩散电流密度增大很多,这也符合浓差极化的动力学特征。
因此,综合上述分析,可以断定:将Pt电极/ EHMA+硫酸电化学体系的阳极电位控制在1.35 V进行恒电位电解时,速度控制步骤为扩散传质步骤。
2.4 EHMA恒电位电解合成乙基香兰素
根据上述实验及分析,在35 ℃时,以Pt电极为阳极,Ni电极为阴极,0.5 mol/L EHMA+0.25 mol/L硫酸溶液为电解液,在一定搅拌速度下,控制阳极电位于1.35 V恒电位电解不同时间,实验结果见表2。其中产率为实际生成的目的产物乙基香兰素与起始EHMA的摩尔比,电流效率为实际生成目的产物乙基香兰素在理论上所用电量与实际所用电量之比。
表2 EHMA恒电位电解实验结果
Table 2 Results of constant potential electrolysis of EHMA

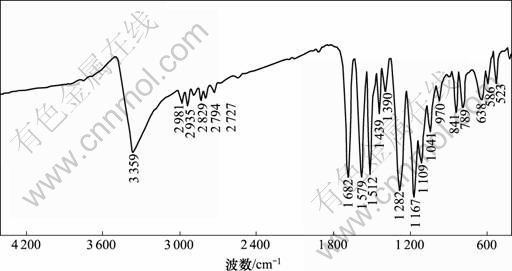
图6 乙基香兰素的红外谱
Fig.6 IR spectrum of ethylvanillin
由表2可知:随着电解时间的延长,乙基香兰素的产率和电流效率都呈现先增后减的趋势,但都不怎么高,这主要是由于Pt电极对EHMA的电催化活性不够(表1中的电流密度也说明了这一点),存在着较多的副反应所引起的。综合衡量2个指标,以恒电位电解1.0 h为宜。
2.5 红外光谱分析
图6所示为乙基香兰素的红外谱。其主要基团的特征峰可分别归属为:1 682 cm-1(醛基CHO);3 359 cm-1(酚羟基Ar―OH);1 282 cm-1,1 167 cm-1(C― O―C);1 579 cm-1(芳环氢Ar―H);2 981~2 727 cm-1(甲基C―H);1 512 cm-1(亚甲基C―H);1 109 cm-1,1 041 cm-1(苯环1,3和4位取代特征峰);与Sadtler标准谱图一致,可以确定产物为乙基香兰素。
3 结论
(1) 采用循环伏安技术确定了EHMA在Pt电极上的电氧化电位及硫酸浓度对直接电氧化合成乙基香兰素的影响。
(2) 采用极化曲线技术计算了35~65 ℃下,Pt电极在0.5 mol/L EHMA+0.25 mol/L硫酸溶液体系中的交换电流密度和极限扩散电流密度,并确定了该电化学合成过程中的速度控制步骤为扩散传质步骤。
(3) 在35 ℃时,以Pt电极为阳极,Ni电极为阴极,0.5 mol/L EHMA+0.25 mol/L硫酸溶液为电解液,在一定搅拌速度下,控制阳极电位于1.35 V恒电位电解1 h,乙基香兰素的产率可达66.68%,电流效率可达54.72%。从应用角度看,硫酸介质中电氧化EHMA合成乙基香兰素具有很好的前景,但其产率和电流效率还有待进一步提高。
参考文献:
[1] Egawa T, Kameyama A, Takeuchi H. Structural determination of vanillin, isovanillin and ethylvanillin by means of gas electron diffraction and theoretical calculations[J]. Journal of Molecular Structure, 2006, 794(1/2/3): 92-102.
[2] Knez Z, Skerget M, Uzunalic A P. Phase equilibria of vanillins in compressed gases[J]. Journal of Supercritical Fluids, 2007, 43(2) 237-248.
[3] Ohashi M, Omae H, Hashida M, et al. Determination of vanillin and related flavor compounds in cocoa drink by capillary electrophoresis[J]. Journal of Chromatography A, 2007, 1138(1/2): 262-267.
[4] Meropi T P, Antony C C. Chemiluminometric determination of vanillin in commercial vanillin products[J]. Talanta, 2007, 71(1): 208-212.
[5] Soucek J, Hora A, Kluger A, et al. Improved catalysts for oxidation of phenylglycolic acids to benzaldehydes: CS, 265937[P]. 1990-04-13.
[6] Stange H, Matschiner H, Mendow E, et al. Preparation of aromatic hydyoxyaldehydes by copper catalyzed oxidation of arylglycolic acids: DD, 301512[P]. 1993-02-18.
[7] 马淳安. 有机电化学合成导论[M]. 北京: 科学出版社, 2002: 5-6.
MA Chun-an. Introduction to synthetic organic electrochemistry [M]. Beijing: Science Press, 2002: 5-6.
[8] 蒲兰芳. 有机电解合成乙基香兰素[J]. 河南化工, 1997(8): 15.
PU Lan-fang. Ethylvanillin prepared by organic electrolysis[J]. Henan Hua Gong, 1997(8): 15.
[9] 其乐木格, 丁绍民, 宋华付. 用邻乙氧基苯酚电化学合成乙基香兰素的研究[J]. 化学研究与应用, 2001, 13(3): 340-342.
QI LE Mu-ge, DING Shao-min, SONG Hua-fu. Study of ethylvanillin electro-synthesized from o-ethoxyphenol[J]. Chemical Research and Application, 2001, 13(3): 340-342.
[10] 刘万民, 陈范才, 惠海军, 等. EHMA在聚邻甲苯胺-Cu2+膜电极上的电氧化[J]. 化学研究, 2008, 19(3): 74-78.
LIU Wan-min, CHEN Fan-cai, HUI Hai-jun, et al. Electrooxidation of 3-ethoxy-4-hydroxy-mandelic acid on poly(o-toluidine)/Cu2+ film electrode[J]. Chemical Study, 2008, 19(3): 74-78.
[11] 刘万民, 陈范才, 叶一鸣, 等. EHMA的合成工艺研究[J]. 香料香精化妆品, 2005(3): 17-19.
LIU Wan-min, CHEN Fan-cai, YE Yi-ming, et al. Study on synthesis of 3-ethoxy-4-hydroxy mandelic acid[J]. Flavour Fragrance Cosmetics, 2005(3): 17-19.
[12] 刘晓航, 马楠, 袁履冰. 亚硫酸氢钠-碘量法在乙基香兰素合成控制中的应用[J]. 化学研究与应用, 1997, 9(4): 381-384.
LIU Xiao-hang, MA Nan, YUAN Lü-bing. Application of sodium bisulfite iodinmetry to monitor process of preparation of ethylvanillin[J]. Chemical Research and Application, 1997, 9(4): 381-384.
[13] 李荻. 电化学原理[M]. 北京: 北京航空航天大学出版社, 2008: 217.
LI Di. Principles of electrochemistry[M]. Beijing: Beihang University Press, 2008: 217.
(编辑 陈爱华)
收稿日期:2011-05-04;修回日期:2011-07-09
基金项目:湖南省教育厅资助科研项目(09C260)
通信作者:刘万民(1979-),男,湖南安化人,博士研究生,讲师,从事应用电化学研究;电话:13787101796;E-mail: mwliu22@yahoo.com.cn