���±�ţ�1004-0609(2012)04-1201-08
��������������Li[Li0.2Ni0.2Mn0.6]O2�ĺϳɼ��绯ѧ����
�� �£��� ϼ�������٣����Ҷ�
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժҪ����LiOH��H2O��Ni(OH)2��Mn3O4Ϊԭ�ϣ����ù��෨�ϳ�����ӵ����������Li[Li0.2Ni0.2Mn0.6]O2��ͨ��X��������(XRD)��ɨ���������(SEM)��������Ʒ�Ľṹ����ò���б������������˸ò��ϵı������ܺߵ������ܡ����������900 �����ս�10 h ��ɻ�þ���ϸС���ȵIJ�״Li[Li0.2Ni0.2Mn0.6]O2���ϣ����������õĵ绯ѧ���ܣ��ŵ�������߿ɴ�235.9 mA��h/g����50 ���²���ʱ�ò��ϵķŵ������ߴ�284.4 mA��h/g�������ֳ����õ�ѭ�����ܣ��䱶�����ܺ͵������ܻ��д���һ�����ơ�
�ؼ��ʣ�����ӵ�أ��������ϣ����෨���绯ѧ����
��ͼ����ţ�TM 912.9 ���� ���ױ�־�룺A
Synthesis and electrochemical properties of Li[Li0.2Ni0.2Mn0.6]O2 as high capacity cathode material
DU Ke, HUANG Xia, HU Guo-rong, PENG Zhong-dong
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Li[Li0.2Ni0.2Mn0.6]O2 was synthesized by solid state method using LiOH��H2O, Ni(OH)2 and Mn3O4 as starting materials. The structure and morphologies of products were characterized by XRD and SEM. The electrochemical performances were also investigated at different rates and temperatures. It is found that the sandwich Li[Li0.2Ni0.2Mn0.6]O2 material obtained at 900 �� for 10 h exhibits uniform and fine particle sizes, indicating high electrochemical capacity and good cycling stability. The maximum discharge capacity is 235.9 mA��h/g. The discharge capacity can reach as high as 284.4 mA��h/g at 50��, and an excellent cyclability is also obtained, while the performance deteriorated at low temperature and the rate capability needs to be improved.
Key words: lithium-ion battery; cathode material; solid state method; electrochemical performance
����ӵ�����ִ�����Ӧ��Խ��Խ�㷺����Ҫ��������ӵ�ز�Ʒ��ɳɷ��У���������ռ������Ҫ�ĵ�λ���������ϵĺû�ֱ�Ӿ�������ӵ�ز�Ʒ������ָ�ꡣĿǰ������ӵ������������Ҫ������״�ṹLiCoO2��LiNiO2��LiMnO2���⾧ʯ�ͽṹLiMn2O4[1]�����ʯ�ͽṹLiFePO4[2]�Լ�LiNixCoyO2��LiNixCoyMnzO2[3]�Ⱥ�﮸����������Щ�������ϱ�����һ����200 mA��h/g���£�������ȶ���350 mA��h/g����ʱ̼����[4]��˵���ѳ�Ϊ��һ���������ӵ�������ܶȵ�ƿ�����д��������������������������ϡ�
�̻��������������Ͽ���ͨʽxLi[Li1/3- Mn2/3]O2��(1-x)LiMO2���������MΪ���ɽ�����0��x��1����ṹ������LiCoO2�����״γ���ѹ������������ӵ������ѹʱ�������̻���������ϻ���4.5 V���ҳ���һ�����ƽ̨���Ӷ�������������״�����й��ɽ���Ԫ��������ԭ�����õ��������ɴ�200 mA��h/g����[5-6]���������ڲ�����ʹ���˴�����MnԪ�أ���LiCoO2����Ԫ����Li[Ni1/3- Mn1/3Co1/3]O2��ȣ������۸�ͣ����Ұ�ȫ�Ժá��Ի����Ѻá���ˣ�xLi[Li1/3Mn2/3]O2��(1-x)LiMO2���ϱ��ڶ�ר��ѧ����Ϊ��һ������ӵ���������ϵ�����֮ѡ[7-8]��
���У�xLi[Li1/3Mn2/3]O2��(1-x)Li[Ni1/2Mn1/2]O2 (0�� x��1)ϵ������ӵ�ظ����������ϲ���ʹ���˴�����MnԪ�أ�������ȫ����CoԪ�أ���˼۸�õ���һ�����ͣ����Ұ�ȫ�Ժá��Ի����Ѻã����кܺõķ�չǰ��[9]��KIM��[10]���ϳɵ�0.3Li[Li1/3Mn2/3]- O2��0.7Li[Ni1/2Mn1/2]O2������2.5~4.6 V��ѹ��Χ��ŵ磬�״ηŵ������ﵽ260 mA��h/g������ѹ����Ϊ1.45~4.6 Vʱ�״ηŵ������ߴ�320 mA��h/g��LU ��[11]�ϳɵ�xLi[Li1/3Mn2/3]O2��(1-x)Li[Ni1/2Mn1/2]O2 (x=1/6)������10 mA/g��3.0~4.8 V��ŵ�ʱ�����ֳ����õĵ绯ѧ���ܣ�20��ѭ����ŵ������ﵽ225 mA��h/g�����������ʸߴ�98%��LEE��[12]�ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2������2.0~4.6 V��ŵ�ʱ�״ηŵ������ߴ�270 mA��h/g�����ǣ����ϱ����еIJ��϶���ȡ���������ϳɣ����̽ϳ������������ƣ����ײ�����Һ����Ⱦ�������ڴˣ�����������ͨ���Ľ����෨�Ʊ�����ӵ����������Li[Li0.2Ni0.2Mn0.6]O2���о����������������¶ȶԸò��ϵ绯ѧ���ܵ� Ӱ�졣
1 ʵ��
1.1 ��Ʒ�ϳ�
��LiOH�� H2O(�Ű������ҵ�Ƽ�����˾��������ؼ�)Ϊ�Դ�����ɽ���ԭ�ϲ��ý���Ni��Mn�������Ni(OH)2(��ɳ��ұ�о�Ժ��������ؼ�)��Mn3O4 (��ɳ�����²��ϿƼ��ɷ�����˾��������ҵ��)����һ��������ϣ�����ĥ���л�е�4 h��֮������е���Ļ��ǰ��������60������к�ɺ������ɸ���ٷ�������¯����2 ��/min�������ٶ����¶�Ϊ800~950 ������������4~24 h����Ȼ��ȴ�����£�ȡ��ĥϸ�õ�Li[Li0.2Ni0.2Mn0.6]O2�������ϡ�
1.2 ���ϱ���
�����ձ�Rigaku��˾����Minflex�͵�X���Զ������ǶԲ���Ľṹ���в��ԣ�ʵ���������£�Cu K�����䣻�ܵ�ѹ40 kV���ܵ���250 mA��ɨ���ٶ�10 (��)/min��2�� 10��~80�㣻����0.02�㡣
�����ձ�JEOL��˾������JSM-5600LV��ɨ����������Բ���Ŀ�����С�ͱ�����ò���й۲졣
1.3 ���ϵ绯ѧ���ܲ���
����Ʒ����Ȳ�ڡ�PVDF�����������8:1:1���Ȼ�ϣ��ټ��������л��ܼ�N-��������ͪ(NMP)������ĥ����ɫ��״���ʡ�����״�����Ϳ������ �ϣ�������60 ��ĺ�����1~2 h��֮������120 ���������ո���24 h��Ȼ�����Ƴ�����Ƭ���Խ����Ϊ�Ը�����Celgard 2400�����ϩĤΪ��Ĥ��1 mol/L LiPF6��EC��DMC��EMC(�����1:1:1)�Ļ����Һ��Ϊ���Һ����ˮ��������������1��10-6�ij��������������(�Ϻ������ǻ��缼������˾������Universal 2440/750)����װ�ɿ�ʽʵ���أ��õ�ز���ϵͳ(�人�н�ŵ��������˾������LAND CT2001A)�Կ�ʽ��ؽ��к����ѭ����ŵ���ԣ���ѹ��ΧΪ2.0~4.8 V������ڲ�ͬ�¶��µij�ŵ�����ʵ���ں�����(�����Դ���������豸����˾������DW7005P)�н��С�
2 ���������
2.1 �ϳ��¶ȶ�Li[Li0.2Ni0.2Mn0.6]O2�������ܵ�Ӱ��
ͼ1��ʾΪ�ֱ���800��850��900��950 ���·�Ӧ10 h �ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��XRD�ס���ͼ1���Կ��������������ϵ�XRD���Թ���Ϊ�ռ�ȺΪ �͵Ħ�-NaFeO2�Ͳ�״�ṹ�����У���2��=20��~28�㷶Χ�ڵ���������ɹ������Ӳ�Li+��Mn4+�ij�������������ġ�800 ��ʱ�ϳɵ���Ʒ�Ѿ��д���Li[Li0.2Ni0.2Mn0.6]O2 �IJ�״�ṹ���������ǿ�����������źϳ��¶����ߣ�����Ľᾧ�ȼ�ǿ��900 ��ʱ�ϳ���Ʒ��(006)��(102)��(018)��(110)�����ķ������ԣ������ڴ������ºϳɵIJ��Ͼ������õIJ�״�ṹ��
�͵Ħ�-NaFeO2�Ͳ�״�ṹ�����У���2��=20��~28�㷶Χ�ڵ���������ɹ������Ӳ�Li+��Mn4+�ij�������������ġ�800 ��ʱ�ϳɵ���Ʒ�Ѿ��д���Li[Li0.2Ni0.2Mn0.6]O2 �IJ�״�ṹ���������ǿ�����������źϳ��¶����ߣ�����Ľᾧ�ȼ�ǿ��900 ��ʱ�ϳ���Ʒ��(006)��(102)��(018)��(110)�����ķ������ԣ������ڴ������ºϳɵIJ��Ͼ������õIJ�״�ṹ��
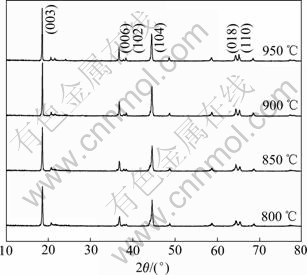
ͼ1 ��ͬ�¶��·�Ӧ10 h�ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��XRD��
Fig. 1 XRD patterns of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at different temperatures for 10 h
��XRDͼ������Ϣ�������Ʒ�ľ�������(a��c)��c/aֵ�Լ�I003/I104ǿ�ȱȣ�����Ʒ�ľ������ݼ���1���ӱ�1���Կ������ڸ��¶������ºϳɵ���Ʒ�ľ�������c/aֵ����������������ܶѻ��ṹ��c/aֵ(4.899)�����������Ʒ�����н�Ϊ�����IJ�״�ṹ��I003/I104ֵ�����������������е������ӻ��ų̶�[13]����ֵԽ�������ӻ��ų̶�Խ�ͣ�һ����Ϊ����ֵ����1.2ʱ���γɵIJ�״�ṹ�Ϻá�����1�и���Ʒ��I003/I104ֵ������1.5�������źϳ��¶ȵ����߶�����������������ӻ��ų̶������¶ȵ����߶����ͣ��γɵIJ�״�ṹ���롣
ͼ2��ʾΪ��ͬ�¶��ºϳɵ�Li[Li0.2Ni0.2- Mn0.6]O2��Ʒ��SEM��ͼ2���Կ�����800��850 ���ºϳɵ���Ʒ������С�����н����Ե��ž�����900 ��õ�����Ʒ�ᾧ��������ò��������Խ�С���ֲ���Ϊ���ȣ�950 ��õ�����Ʒ����������������һ��˵���¶ȵ������ڽϴ�̶��ϴٽ��˾������������γ��˽ϴ�Ŀ�����һ����Ϊ���������Ŀ������ϻᵼ��������ڹ�������ɢ��������ӣ��������ĵIJ��ֻ�������������Ƕﮣ������½���
��1 ��ͬ�¶��·�Ӧ10 h�ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2�ľ���������ǿ�ȱ�ֵ
Table 1 Lattice parameters, c/a ratio and I003/I104 intensity ratio of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at different temperatures for 10 h

ͼ3��ʾΪ��ͬ�¶��ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ�״γ�ŵ����ߡ���ͼ3���Կ�����Li[Li0.2Ni0.2Mn0.6]O2�������״γ��ʱ������������Ҫ������� 3.8~4.5 V ��S �������4.5 V ���ϵ�L������S �������Ӧ��Ԫ����Li[Ni1/2Mn1/2]O2 �е�Ni2+������ΪNi4+[14]����L�������ӦLi[Li0.2Ni0.2Mn0.6]O2������Li2MnO3��ֱ����Li2O�ѳ��������״γ��ʱ��4.5 V���ҳ���ƽ̨[15-16]�����״γ�ŵ��ó��ƽ̨��ʧ��800 ����Ʒ���״ηŵ������Ϊ115.6 mA��h/g��850 ����ƷΪ149.4 mA��h/g��900 ����ƷΪ164.4 mA��h/g���ɼ��������¶ȵ����ߣ�����ľ��������������950 ����Ʒ���״ηŵ���������½���115.4 mA��h/g���½����Ƚϴ�����������ڿ���������������µ������½���

ͼ2 ��ͬ�¶��·�Ӧ10 h�ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��SEM��
Fig. 2 SEM images of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at different temperatures for 10 h: (a) 800 ��; (b) 850 ��; (c) 900 ��; (d) 950 ��

ͼ3 ��ͬ�¶��·�Ӧ10 h�ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ���״γ�ŵ�����
Fig. 3 First charge-discharge curves of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at different temperatures for 10 h
ͼ4��ʾΪ��ͬ�¶��ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ�ij�ŵ�ѭ�����ߡ���ͼ4���Կ�������ͬ�¶����Ʊ�����Ʒ�����������Ե�����ѭ���Ľ���������������������900 ���·�Ӧ�ϳɵ���Ʒ�״ηŵ������Ϊ164.4 mA��h/g��ѭ��16�κ���ߴﵽ235.1 mA��h/g�����״α������д������������һ������xLi[Li1/3Mn2/3]O2��(1-x)Li[Ni1/2Mn1/2]O2������н�Ϊ�ձ顣KANG��[17]�����ܽ�-�������ϳɵ�Li[Li0.2Ni0.2- Mn0.6]O2��2.0~4.6 V��ѹ��Χ�ڳ�ŵ�ʱ���״ηŵ������Ϊ155 mA��h/g��ѭ��10�κ�ﵽ205 mA��h/g��֮��ѭ���ȶ������ҵ�[18]���õ��ȹ��෨��700 ��ϳ���xLi[Li1/3Mn2/3]O2��(1-x)Li[Ni1/2Mn1/2]O2 (x=0.3��0.5��0.7)�������ϣ�x=0.3��0.5ʱ��������ѭ���б�������������ѭ���ȶ��ԽϺá�������һ������ܵĽ������£��ڷŵ�ѭ���в��ϵĶѶ������Ƴ��������ӽ������ţ��������������������Ϲ��̶ܳ���ѭ�����ӡ��ṹ�����ǹ��ɽ������ӵ�������������ء���800��900 �棬����������ߣ�����Ҫ���������ߺϳ��¶���������߲��ϵľ����̶ȼ��������״�ṹ���Ӷ������绯ѧ���ܣ������ϳ��¶�������950 ��ʱ������Ʒ��������ѭ�����ܷ������ͣ������������һ������ߵ��¶���ɾ�������ij������ڲ����ڲ��Ļ������ʵij�����ã�����һ���棬���»������Li�ӷ����γ��˲���Liȱλ��������Ni2���ڿռ�Ⱥ��Li��λ�õ�ռ���ʣ���Li��λ�ϵ�Ni2������ɺ���������ѭ������˥������Ҫԭ��֮һ��Li��λ�ϵ�Ni2������﮺��ڽ������������Ӱ뾶��С��Ni4����������ɸ����Ӹ����ṹ���ݣ�������Ƕ﮹�����﮽�����Ƕ�������ݵ�λ�ã��Ӷ����Ƕ�����������С[19]��

ͼ4 ��ͬ�¶��·�Ӧ10 h�ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ�ķŵ�ѭ����������
Fig. 4 Cycle performance curves of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at different temperatures for 10 h
2.2 ��Ӧʱ���Li[Li0.2Ni0.2Mn0.6]O2�������ܵ�Ӱ��
ͼ5��ʾΪ900 ��ʱ4��10��16��24 h�ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��XRD�ס���ͼ5���Կ� ������900 ���·�Ӧ4 h���Ѿ����Եõ��ᾧ�����ĵ�һ�࣬�������ǿ������������Ӧʱ���ӳ���10 hʱ������Ľᾧ��������Ʒ(006)��(102)��(018)�� (110)�����ķ������ԣ������ڴ������ºϳɵIJ��Ͼ������õIJ�״�ṹ��
��XRDͼ������Ϣ�������Ʒ�ľ�������(a��c)��c/aֵ�Լ�I003/I104ǿ�ȱȣ�����Ʒ�ľ������ݼ���2���ӱ�2���Կ������ڸ���Ӧʱ��ϳɵ���Ʒ�ľ�������c/aֵ����������������ܶѻ��ṹ��c/aֵ(4.899)�����������Ʒ���Ѿ��н�Ϊ�����IJ�״�ṹ������Ʒ��I003/I104ֵ������1.5������Li���Ӻ��ɽ��������ӵĻ��ų̶Ⱥܵ�[20]���γɵIJ�״�ṹ�ܺá�
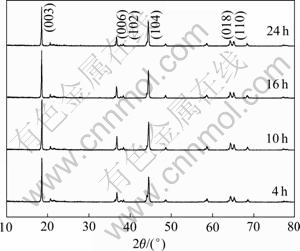
ͼ5 900 ��ʱ��ͬʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��XRD��
Fig. 5 XRD patterns of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at 900 �� for different reaction times
ͼ6��ʾΪ900 ��ʱ��ͬ��Ӧʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��SEM��ͼ6���Կ� ������Ӧʱ���Li[Li0.2Ni0.2Mn0.6]O2��Ʒ�ı�����òӰ���С����Ӧʱ��Ϊ4 h�õ�����Ʒ������С�����ž۽�Ϊ���ԣ���Ӧʱ��Ϊ10 h �õ�����Ʒ����ϸС���ֲ����ȣ����ŷ�Ӧʱ������ӣ����ɵ���Ʒ�Ŀ�����������
��2 900 ��ʱ��ͬʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2�ľ���������ǿ�ȱ�ֵ
Table 2 Lattice parameters, c/a ratio, I003/I104 intensity ratio of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at 900 �� for different reaction times

ͼ7��ʾΪ900 ��ʱ��ͬ��Ӧʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ���״ηŵ����ߡ���ͼ7���Կ��������ŷ�Ӧʱ������ӣ�Li[Li0.2Ni0.2Mn0.6]O2�ķŵ�����������Ӻ��С�����У�900 ��ʱ��Ӧ10 h���ɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ���״ηŵ������Ϊ164.4 mA��h/g������Ӧʱ��Ϊ4��16��24 h �õ���Li[Li0.2Ni0.2Mn0.6]O2��Ʒ���״ηŵ�������ֱ�Ϊ148.6��129.5��106.3 mA��h/g����Ӧʱ���Li[Li0.2- Ni0.2Mn0.6]O2��Ʒ�ĵ绯ѧ�����нϴ��Ӱ�졣�ʵ��ӳ���Ӧʱ����������ǿ���ϵĽṹ�ȶ��ԣ�ʹ��״�����������ԣ��������Ӧʱ�������������Li�ӷ������²���Ni2��ռ�ݾ���ṹ��Li����λ�ö��γ�С�ṹ�������������˲��ϵľ������䣬�Ӷ����·ŵ������½���

ͼ6 900 ��ʱ��ͬʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��SEM��
Fig. 6 SEM images of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at 900 �� for different reaction times: (a) 4 h; (b) 10 h; (c) 16 h; (d) 24 h

ͼ7 900 ��ʱ��ͬʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ���״γ�ŵ�����
Fig. 7 First charge-discharge curves of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at 900 �� for different reaction times
ͼ8��ʾΪ900 ��ʱ��ͬ��Ӧʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ�ij�ŵ�ѭ�����ߡ���ͼ8���Կ�����10 h ��Ӧʱ��ϳɵ���Ʒ��ѭ�����ܽ�������Ӧʱ��ϳɵ���Ʒ�����ܸ�������
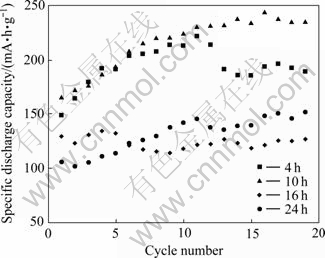
ͼ8 900 ��ʱ��ͬʱ���ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ��ѭ����������
Fig. 8 Cycle performance curves of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at 900 �� for different reaction times
2.3 �Ż������ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2���ϵ�����
ͼ9��ʾΪ�Ż������ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2���ϵı���ѭ�����ߡ���ͼ9���Կ������ò�����30 mA/g �������³�ŵ�ʱ����������ߴﵽ235.9 mA��h/g����������Ϊ60 mA/g�����ŵ�����ֱ�Ϊ60��150��300 mA/g ʱ���ŵ�������ֱ�Ϊ209.4��190.9��161.6 mA��h/g�����ű��ʵ����Ӷ��½����ԣ���������ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2���ϵı��������д���һ����ߡ�
ͼ10��ʾΪ�Ż������ºϳɵ�Li[Li0.2Ni0.2Mn0.6]O2������Ϊ�������ƳɵĿ�ʽ����Ⱥ���25��50��0 ������30 mA/g ��ŵ�ʱ�ķŵ�ѭ���������ߡ���ͼ10���Կ�������50 ����������£��ò��Ϸŵ�������ߴ�284.4 mA��h/g����ѭ�����ܺ��ȶ���17��ѭ������������û��˥��������¶�����߲��ϵ����������ǣ��ò�����0 ���µ����������½��������Li[Li0.2Ni0.2Mn0.6]O2���ϵĵ绯ѧ���ܶ��¶������Խ�ǿ��
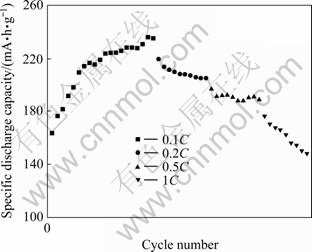
ͼ9 900 ���·�Ӧ10 h �ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2�ı���ѭ����������
Fig. 9 Cycle performance curves of Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at 900 �� for 10 h
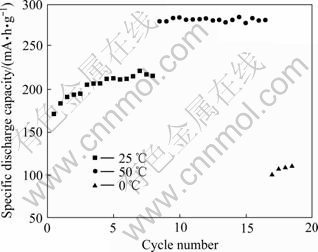
ͼ10 900 ���·�Ӧ10 h �ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2��Ʒ�ڲ�ͬ�¶��µķŵ�ѭ����������
Fig. 10 Cycle performance curves at 25, 50 and 0 �� for Li[Li0.2Ni0.2Mn0.6]O2 samples synthesized at 900 �� for 10 h
3 ����
1) ��LiOH��H2O��Ni(OH)2��Mn3O4Ϊԭ�ϣ����ù��෨�ϳ�������ӵ����������Li[Li0.2Ni0.2Mn0.6]O2���ϳ��¶Ⱥͷ�Ӧʱ���Li[Li0.2Ni0.2Mn0.6]O2���ϵľ���ṹ����ò�͵绯ѧ���ܶ��������Ե�Ӱ�졣�¶�Ϊ900 �桢��Ӧʱ��Ϊ10 hʱ�ϳɵ�Li[Li0.2Ni0.2Mn0.6]O2 ���ᄃ��ṹ����������ϸС���ȣ���30 mA/g�ĵ�����ŵ�ѭ�����κ��������ŵ�������ɴﵽ235.9 mA��h/g��
2) ��������Ϊ60 mA/g�����ŵ�����ֱ�Ϊ60��150��300 mA/g ʱ���ŵ�������ֱ�Ϊ209.4��190.9��161.6 mA��h/g�����ű��ʵ����Ӷ��½����ԣ������ò��ϵı��������д���һ�����ơ�
3) ��50 �������²���ʱ�ò��ϵķŵ�������ߴ�284.4 mA��h/g�������ֳ����õ�ѭ�����ܣ�����������ܽϲ
REFERENCES
[1] HOSONO E, KUDO T, HONMA I, MATSUDA H, ZHOU Hao-shen. Synthesis of single crystalline spinel LiMn2O4 nanowires for a lithium ion battery with high power density[J]. Nano Letters, 2009, 9(3): 1045-1051.
[2] Ф��ΰ, ������, �� ��, ���Ҷ�, ������. ���ܶ�����ӵ���������ϲ���LiFePO4/C[J]. �й���ɫ����ѧ��, 2007, 17(12): 2040-2045.
XIAO Zheng-wei, HU Guo-rong, DU Ke, PENG Zhong-dong, DENG Xin-rong. High density LiFePO4/C composite cathode material for lithium ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(12): 2040-2045.
[3] �� ƽ, �Ŵ���, �� ��, ������, տ ݼ, ��ΰ��. ��������Li(Ni1/3Mn1/3Co1/3)MxO2(M=Ti, Mg)�ĺϳɼ�����[J]. �й���ɫ����ѧ��, 2009, 19(1): 101-107.
YANG Ping, ZHANG Chuan-fu, DAI Xi, FAN You-qi, ZHAN Jing, JIANG Wei-yan. Synthesis of Li(Ni1/3Mn1/3Co1/3)MxO2 (M=Ti, Mg) cathode material by oxalate precursor and its properties[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(1): 101-107.
[4] �����j, �� ��, ������, Ф����. ����ӵ��[M]. ��ɳ: ���ϴ�ѧ������, 2002: 93-146.
GUO Bing-kun, XU Hui, WANG Xian-you, XIAO Li-xin. Lithium-ion battery[M]. Changsha: Central South University, 2002: 93-146.
[5] JOHNSON C S, LI NAICHAO, LEFIEF C, VAUGHEY J T, THACKERAY M M. Synthesis, characterization and electrochemistry of lithium battery electrodes: xLi2MnO3��(1-x)- LiMn0.333Ni0.333Co0.333O2 (0��x��0.7)[J]. Chem Mater, 2008, 20: 6095-6106.
[6] THACKERAY M M, KANG S H, JOHNSON C S, VAUGHEY J T, BENEDEK R, HACKNEY S A. Li2MnO3-stabilized LiMO2 (M=Mn, Ni, Co) electrodes for lithium-ion batteries[J]. Journal of Materials Chemistry, 2007, 17: 3112-3125.
[7] ZHENG J M, ZHANG Z R, WU X B, DONG Z X, ZHU Z, YANG Y. The effects of AlF3 coating on the performance of Li[Li0.2Mn0.54Ni0.13Co0.13]O2 positive electrode material for lithium-ion battery[J]. Journal of the Electrochemical Society, 2008, 155(10): A775-A782.
[8] GUO Xiao-jian, LI Yi-xiao, ZHENG Min, ZHENG Jian-ming, LI Jie, GONG Zheng-liang, YANG Yong. Structural and electrochemical characterization of xLi[Li1/3Mn2/3]O2��(1-x)Li- [Ni1/3Mn1/3Co1/3]O2 (0��x��0.9) as cathode materials for lithium ion batteries[J]. Journal of Power Sources, 2008, 184: 414-419.
[9] Ф ��, ����Ӣ, ���Ҷ�, �� ��, ������. ����ӵ����������LiNi0.5Mn0.5O2��ѭ������[J]. �й���ɫ����ѧ��, 2006, 16(8): 1439-1444.
XIAO Jin, ZENG Lei-ying, PENG Zhong-dong, ZHAO Hao, HU Guo-rong. Cycle performance of LiNi0.5Mn0.5O2 as cathode material for lithium secondary batteries[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(8): 1439-1444.
[10] KIM J S, JOHNSON C S, JOHN T. Electrochemical and structural properties of xLi2MnO3��(1-x)LiMn0.5Ni0.5O2 electrodes for lithium batteries(M��=Ti, Mn, Zr; 0��x��0.3)[J]. Chem Mater, 2004, 16: 1996-2006.
[11] LU Zhong-hua, BEAULIEU L Y, DONABERGER R A, THOMAS C L, DAHN J R. Synthesis, structure, and electrochemical behavior of Li[Li1/3-2x/3NixMn2/3-x/3]O2[J]. Journal of the Electrochemical Society, 2002, 149(6): A778-A791.
[12] LEE D K, PARK S H, AMINE K, BANG H J, PARAKASH J, SUN Y K. High capacity Li[Li0.2Ni0.2Mn0.6]O2 cathode materials via a carbonate co-precipitation method[J]. Journal of Power Sources, 2006, 162: 1346-1350.
[13] KIM Y, KIM H S, MARTIN S W. Synthesis and electrochemical characteristics of Al2O3-coated LiNi1/3Co1/3- Mn1/3O2 cathode materials for lithium ion batteries[J]. Electrochim Acta, 2006, 52: 1316-1322.
[14] KIM J H, PARK C W, SUN Y K. Synthesis and electrochemical behavior of Li[Li0.1Ni0.35 -x/2CoxMn0.55-x/2]O2 cathode materials[J]. Solid State Ionics, 2003, 164: 43-49.
[15] WU Y, MANTHIRAM A. High capacity, surface modified layered Li[Li(1 -x)/3Mn(2-x)/3Nix/3Cox/3]O2 cathodes with low irreversible capacity loss[J]. Electrochemical and Solid-State Letters, 2006, 9(5): A221-A224.
[16] JOHNSON C S, KIM J S, LEFIEF C, LI N, VAUGHEY J T, THACKERAY M M. The significance of the Li2MnO3 component in ��composite�� xLi2MnO3��(1-x)LiNi0.5Mn0.5O2 electrodes[J]. Electrochemistry Communications, 2004, 6: 1085-1091.
[17] KANG S H, SUN Y K, AMINE K. Electrochemical and ex situ X-ray study of Li[Li0.2Ni0.2Mn0.6]O2 cathode material for Li secondary batteries[J]. Electrochemical and Solid-State Letters, 2003, 6(9): A183-A186.
[18] �� ��, �� ��, �� ��, ������. (1-x)LiMnO2��xLi- [Ni1/2Mn1/2]O2�ĵ��¹����Ʊ����绯ѧ�����о�[J]. ����ʦ����ѧѧ��: ��Ȼ��ѧ��, 2009(����1): 10-12.
REN Yan, LIAN Fang, LI Dong, QIU Wei-hua. Eelectrochemical performance of (1-x)Li2MnO3��xLiMn1/2Ni1/2O2 prepared via low-heating solid-state reaction method[J]. Journal of South China Normal University: Science and Technology, 2009(S1): 10-12.
[19] �ռ���, ����, ���ǹ�, ����ͬ. LiNi1/3Co1/3Mn1/3O2�������ϵ��Ʊ��������[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2008, 39(2): 221-227.
SU Ji-tao, SU Yu-chang, LAI Zhi-guang, Fang Hui-tong. Preparation and characterization of LiNi1/3Co1/3Mn1/3O2 cathode material[J]. Central South University: Science and Technology, 2008, 39(2): 221-227.
[20] ZHANG Shi-chao, QIU Xin-ping, HE Zhi-qi, WENG Dang-sheng, ZHU Wen-tao. Nanoparticled Li(Ni1/3Co1/3Mn1/3)O2 as cathode material for high-rate lithium-ion batteries[J]. Power Sources, 2006, 153: 350-353.
(�༭ ������)
������Ŀ��������Ȼ��ѧ����������Ŀ(50604018)�����ϴ�ѧ�����У��������������Ŀ(2010QZZD0101)
�ո����ڣ�2011-05-21�������ڣ�2011-09-26
ͨ�����ߣ��� �£������ڣ��绰��0731-88830474��E-mail: duke22@csu.edu.cn