DOI: 10.11817/j.ysxb.1004.0609.2020-35915
�߰�ȫ����������ӵ����ƣ��ߵ�ѹ��״��������
��С��1, 2, 3��������3��������3��¬����1, 2���� ��3
(1. ���пƼ���������˾�����Ҷ�����ش������ģ����� 100088��
2. ������ɫ�����о���Ժ������ 100088��
3. ����ʱ������Դ�Ƽ��ɷ�����˾������ 352100)
ժ Ҫ���������������������Ϊ������������-�������ü���(TG-MS)���������������ϵ��ȷֽ⼰������Һ�ķ�Ӧ�����ԣ������˲�ͬ���̬�����Һ�Բ�״�����������ȶ��Ե�Ӱ�죬��ϵͳ������O2���ӵ�ԭ������������ų���ֹ��ѹ�����ӣ�����﮵����������״�ṹ�ƻ��̶ȼӾ磬�ȷֽ��ͷų������O2���Ա���4.4 V��LiNi0.33Mn0.33Co0.33O2(4.4 V-NMC111)��4.2 V��LiNi0.8Mn0.1Co0.1O2(4.2 V-NMC811)�����������ȶ��ԣ�����ȷ��4.4 V-NMC111��4.2 V-NMC811Ϊ����������ȫ��ؾ�������������ܶȣ���4.4 V-NMC111��ر��ֳ����õ������ԡ�
�ؼ��ʣ�����ӵ�أ��������ϣ��ߵ�ѹ�����ȶ��ԣ�����-�������ü���
���±�ţ�1004-0609(2020)-12-2912-08���� ��ͼ����ţ�TM9112.9���� ���ױ�־�룺A
����ӵ����Ϊһ�����ʹ��ܵ�Դ�����б������ߡ������¶ȷ�Χ���������Ѻá����С�����������ŵ㣬�ѹ㷺Ӧ���ڵ綯���������������Լ�������Ӳ�Ʒ��[1-4]��Ȼ��������ӵ������������ܶȵ�ͬʱ��Ҳ������һϵ�еİ�ȫ���⣬����������Լ������������ƹ�Ӧ�õ���Ҫƿ��֮һ[5-6]����ʵ�ϣ�����ӵ�صİ�ȫ�������ڵ�ػ��Բ���֮��ķ��ȷ�Ӧ[7-8]����������õĵ缫���������������ȶ������⣬��������Һ֮�仹�����Ż�ѧ��Ӧ������ڸ������������¾��ҷ�Ӧ���ȣ�������������ʹ�÷�Ӧ�Ӿ磬���������۵�һ���̶�ʱ���ͻ���ɵ����ʧ��[9-11]���о����������������ڸ����ȷֽ�����������������Ӧ��ʯī�������ϵ�3~4�������ǵ�������ӵ�����շ�����ʧ�ص���Ҫԭ��[12-14]��ͬʱ��������ҵ��﮵���������ϵĿ��������Ǹ������ϵ�һ�룬����������������Լ﮵�ؾ��и������ܶȵ���Ҫԭ��[15-16]��Ϊ�˻�ȡ�������ܶȵ�﮵�أ���ҵ��һ��ѡȡ�߿��������������ϣ����߸ߵ�ѹ���������ϡ���ˣ�������ͬ���������ڸߵ�ѹ�µ����ȶ��ԣ��Է�չ�߰�ȫ�������ܶȵ�����ӵ�ؾ�����Ҫ���塣
Ŀǰ���ѱ����Ŀ������о��缫���Բ��Ϸ�����Ϊ�ķ�����Ҫ�У��������ȷ�(ARC)����ʾɨ�����ȷ�(DSC)�Լ����ط�(TG)[17-19]��Ф�����Ȳ��õ�����������LAND��ز���ϵͳ���ü����������ڲ�ͬ�����¶Ⱥͱ����³��ŵ�ѭ�������еIJ������[3]����ϲ���ͨ�������ϲ��ϱ����������Ի�ȡ������ӵ�ص������Բ���[20]��Ȼ����������Щ�о��ֶ����������ƣ�ֻ�ܼ����ȷ�Ӧ��һЩ�ض�����(������¶ȡ��������ʡ���������)���������������ȷ�Ӧ�����в��������帱�����˲�������ԭλ�ط�ӳ﮵�ػ��Բ��Ϸ��ȷ�Ӧ���̡�
���Ľ�����ط�����������������-����(TG-MS)�о��ڲ�ͬ���״̬���������ϱ����Լ�����Һ֮��ķ������ԣ�ͬʱԭλ����ڷ��ȷ�Ӧ�����в���������ɷ֡��������������������ϣ������˲�ͬ���״̬LixCoO2(0��x��1.0)�����ȶ��ԡ����ȹ����Լ������ɷֺ�ԭ��ͬʱ��Ŀǰ�綯����ʹ��������Ԫ���������(NMC)��������Ϊ�о����Աȷ����������ܶ����ʱ���߿�����LiNi0.8- Mn0.1Co0.1O2�ߵ�ѹ���ڵ�LiNi0.33Mn0.33Co0.33O2�������ϵ����ȶ����ܡ�ͨ���ߵ�ѹ���������ϵ����ȶ��Է������Է�չ�߰�ȫ�������ܶȵ�﮵���ṩ����Ҫ���ݡ�
1 ʵ��
1.1 ��Ʒ�Ʊ�
������Ƭ�Ʊ����������Ϊ�����������ʣ�ƫ�۷���ϩ(PVDF, Solef6020)Ϊ�Ӽ�����Ȳ��Ϊ�������������96:2:2�������ȼ��뵽N-��������ͪ(NMP)���Ƴ��������ϣ�Ϳ����Al��������棬�����濾��ѹʵ��õ�����ӵ��������Ƭ�������������Ϊ�����������ʣ�����������ͬ�ķ�ʽ��ȡ�����������Ϊ�������ʵ�������Ƭ��������Ƭ���Բ��ϵ��ܶ�Ϊ20 mg/cm2��
���Һ���Ʊ�������̼����ϩ��(EC)/̼���ϩ ��/̼�������(DEC)(�����Ϊ10:40:50)�Ļ���ܼ�1000 mL�������ܼ��м���15.2 g LiPF6 (1.0 mol/L)�õ������Һ������û����Һ�м���1%��̼��������(VC)��3.0%���������ϩ��(PS)���Ʊ������Һ��
�����װ����������������Ƭ�����Һ����Ӧʯī����������Ĥ(����ϩ��16 ��m)��װ�ɷ���Ӳ��ȫ��أ���سߴ�Ϊ26.5 mm��148 mm��91 mm�����������Ϊ0.84 kg��Ϊ�˵õ���ͬ���̬��������Ƭ�����Ƚ������0.5C�����ʺ�����絽�趨�ĵ�ѹֵ���ٺ�ѹ�����0.05C��Ȼ����ڳ���������������ڲ�⣬֮���Ѽ�����������Ƭ��̼�������(DMC)��ϴ���Σ��Գ�ȥ�缫���������LiPF6�����յõ���ͬ���̬�ļ�Ƭ������ϴ���������Ƭ����պ�����60 �����2 h��ȥ����Ƭ�е�DMC������ܷⱣ�档
1.2 ��Ʒ����
��������������(TG-MS)�����ڲ��ϵ����ȶ��Բ��ԡ������¶ȷ�Χ��50~400 �棬��������Ϊ5 ��/min��������Ʒ������5~8 mg����Ʒ��TG�������ȹ����в����������������м�⣬����ʺ˱�(m/z)Ϊ18��32��44�������źš�
X�����������ڲ��ϵĽṹ�����������Բ��õ��豸ΪRigaku TTR-III��Cu K��������Ƕ�Ϊ15��~75�㡣
�������ʵ�飺�ڵ�ش��沼���¶ȸ����ߣ������������õ�ѹ�ߣ�����ط��������С�������5 ��/min���µ�100 �棬������1 h��֮����5 ��/min���£�ÿ����5 �棬����30 min��ֱ�����ʧЧ��
2 ���������
����������������﮵ı�����ò��ò��ͼ1(a)��ʾ���û������ʳʿ���״����ɢ���ȣ���������������m����ʮ��m֮��(��ͼ1(a))��ƽ������ԼΪ20 ��m(��ͼ1(b))����������ͬʱ������һЩ������ɢ��ϸ��������(��ͼ1(a)��ͼ)��������������(��ͼ1(c))�������京��AlԪ�ء�����Al2O3�����Ϊ������������ϵ��ȶ�����[20-21]��ͼ1(d)��ʾΪLixCoO2���ϼ�����Ƭ��XRD�ס���ͼ1(b)���Կ��������о�����ʹ�õ�����LiCoO2���ϳ��ֳ�խ�Ҽ��������壬��˵�������и߾����ȵIJ�״�ṹ�����⣬���������λ��LiCoO2(JSCPD R3m���ⷽ��ϵ)�ı���������һ�£�ͬʱδ����Al2O3������壬��˵����Al2O3Ϳ����ϱ������������Al2O3�ʷ�ɢ״С������������������״̬��ͬʱ�ı�LiCoO2�Ľṹ����˿�����Ϊ�����Ժ����������Ϸ�Ӧ�����о�����Ӱ�졣
Ϊ�˳�ַ�ӳ������������ʵʹ���е����ȶ����ܣ�����س����4.2 V�������������ϣ�����DMC��ϴ���֮��õ��������Һ��������Ƭ����TG-MS�����õ�4.2 V LixCoO2��TG-MSͼ����ͼ2(a)��ʾ����ͼ2(a)���Կ������ڼ�����231 ��ʱ��LixCoO2��ʼ�ȷֽ�ʧ�ء�ͨ��MSͼ���Ե�֪����Ӧ���������弸������O2������������ʧ��������Ҫ��O2�ͷ������ף���������������6.23%���������������г���LixCoO2�⣬ֻ����2%��Ȳ�ں�2%ƫ�۷���ϩ�ķǻ������ʣ������Ǿ����ͷ�O2����˻��Բ���LixCoO2���ȷֽⷴӦ��Ψһ���ܲ���O2�Ĺ��̡���400 ����Ⱥ��������ĩXRD���з���LiCoO2��Co3O4��������(��ͼ2(b))�����Ե�֪�������ϸ������ȷֽ⣬����������Co3O4�����������������ƶ����������ȷֽⷴӦʽ���£�
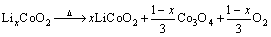 (1)
(1)
Ϊ�˸��ӳ�ֵط�ӳ���������ڲ�ͬ���״̬�²��ϵ����ȶ����ܣ���һ���о��˲�ͬ���״̬��LixCoO2�ڲ�ͬ�¶��µ���ʧ�ء�ͼ3(a)��ʾΪLixCoO2����������200~400 ��֮���в�ͬ�̶ȵ�������ʧ���ҳ���ֹ��ѹԽ�ߣ���ʧ����ʼ�¶�Խ�ͣ���������ʧԽ��Ϊ�˽�һ����ȷLixCoO2���ȷ�Ӧ�����Լ���ʧ������̬�Ĺ�ϵ������TG-MS�������������ϸ���ʱ�IJ��������������ȷ�ڲ�ͬ���̬�£�LixCoO2��x��ֵ�����Ӧ��ϵ���1��ʾ����xֵ���뵽ʽ(1)�У�����õ�O2�ͷ���������ֵ����ͼ3(b)������ʾ���������㲻ͬ���̬���O2��ʵ���ͷ�����ͼ3(b)ʵ����ʾ��ʵ��O2���ͷ�����ʽ(1)���������ֵ�����غϣ���Ҳ���˵��LixCoO2�������������Һ������£��ڲ�ͬ���̬������ʧ���������ϱ����ȷֽ����O2���[22-24]���ߵ�ѹ̬4.6 V��LixCoO2���������ͷ����䱾������10.5%��O2, ��4.2 V��O2��6.6%�߳���3.9%��������Ϊ���ų���ѹ������LixCoO2�е�(003)��λ���ͣ�������ͬʱ(104)��λ���ͣ�LixCoO2�Ľᾧ�����Ⱥ���������������Ƚ��ͣ�������LixCoO2��״�ṹ�ƻ��̶�����(��ͼ4)[25-26]��
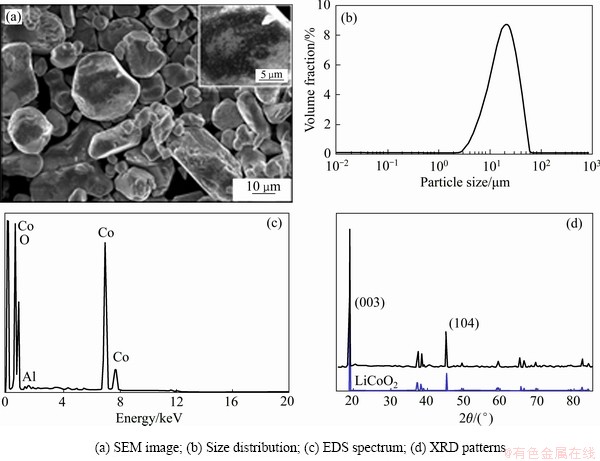
ͼ1 LiCoO2ԭ���ϻ�������
Fig. 1 Characterization of cathode material LiCoO2
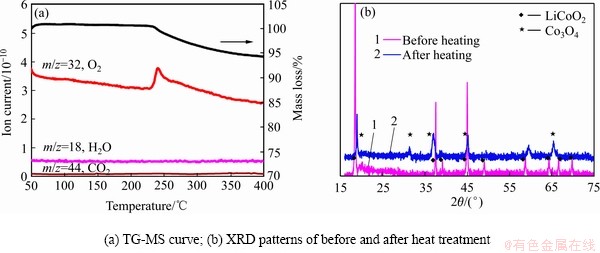
ͼ2 4.2 V����LixCoO2������Ƭ�����ȶ���
Fig. 2 Thermal stability of LixCoO2 at 4.2 V

ͼ3 ��ͬ���̬��LixCoO2�����ȶ���
Fig. 3 Thermal stability of LixCoO2 at different charging end-off voltages

ͼ4 ��ͬ���̬��LixCoO2��XRD��
Fig. 4 XRD patterns of LixCoO2 at different charging end-off voltages
��1 ȫ��صij�������ѹ��LixCoO2�е�x�Ĺ�ϵ
Table 1 Relationship between charging end-off voltage of full cell and x in LixCoO2


ͼ5 LixCoO2/���Һ�����ȶ���
Fig. 5 Thermal stability of LixCoO2 with electrolyte
����ʵ�ʵ��ʹ���У��������ϰ����˵��Һ����ˣ���һ������TG-MS�������е��Һ�������������о����Һ�������������ȶ����ܵ�Ӱ��[17]��ͼ5(a)��ʾΪ���е��Һ������̬(4.2 V)LixCoO2��TG-MSͼ����ͼ5(a)�п��Կ������¶ȴ�50 �浽400 �棬��������������ʧԼ10.3%�����⣬TG�������������Ե���ʧ�ؽΣ���һ����ʧ�ؽγ�����85~155 ��֮�䣬��Ӧ��������ʧΪ4.6%���ڶ�����ʧ�ؽη�����231~377 ��֮�䣬��Ӧ��������ʧΪ5.7%�����ͬʱ��������ԭλ�����Ƕ�50~400 �����¹����еIJ��������˼�⡣��4.2 V��LixCoO2���ƣ����ӵ��Һ���LixCoO2��231~377 ��֮��Ҳ�������Ե�������ʧ������85~155 �������������������塣���ӵ��Һ���������ϵ����������Դ��ڴ���������������ˣ�������Ϊ�������ϵ�������Ϊ������LixCoO2�����ȶ����йأ����Һ�Ĵ���Ҳ������Ҫ����(��ͼ5(b))�����⣬��������Ͽ��Ե�֪��LixCoO2/���Һ��85~155 ��֮����ͷų�CO2��������H2O��O2���Աȴ���LixCoO2����������Ե�֪CO2��Ҫ�����ڵ��Һ�ķֽ⣬ͬʱ���ܼ��������180 ��֮ǰ���ᷢ����ѧ��Ӧ[27-28]����85~ 155 ��֮��IJ���������ʧ����LixCoO2����Һ֮��Ļ�ѧ��Ӧ�����ġ����Ͽ�֪�����Һ�Ĵ��ڶ���������LixCoO2�����ȶ��ԣ��Ӿ�����������LixCoO2���������ȡ�
Ϊ�˸��ӳ�ֵط�ӳ�������ϵ����ȶ����ܣ�Ŀǰ�綯����ʹ��������Ԫ���������(NMC)��������Ҳ����TG-MS���������¶�50~400 ��֮�䣬����ѹΪ4.2 Vʱ��LiNi0.8Mn0.1Co0.1O2 (NMC(811))��LiNi0.33Mn0.33Co0.33O2 (NMC(111))��������ʧ�ֱ�Ϊ14.2%��4.8%(��ͼ6(a))��NMC(811)��NMC(111) ����ʼ�ֽ��¶ȷֱ�Ϊ215 ���290 �档�����������4.2 Vʱ��NMC(111)��NMC(811)�и��õ����ȶ����ܣ��ڳ��̬Ϊ4.2 Vʱ��NMC(111)��������ʧ��ΪNMC(811)��34%��﮵����ʵ��ʹ���У�����ڷ�����ȫ�¹�ʱ������������O2�������Ӿ�����ʧ�صķ���[29-30]����ˣ��ߵ�ѹ̬�������ϵ����ȶ����ܺ���O2��ȫ�������м�����Ҫ��ͼ6(b)��ʾΪNMC(811)��NMC(111)���������ڲ�ͬ���̬����O2�������������NMC�������ϵ���O2�������ų���ѹ���������������ͬ�ij��̬�£�NMC(111)����O2��ʼ�ս�NMC(811)�ͣ���ʹ��4.6 V�߳��̬�£�NMC(111)����O2��Ҳ��NMC(811)����O2��5.7%�����������4.6 V-MC(111)�����ȶ�����Ҳ����4.2 V-NMC(811)��
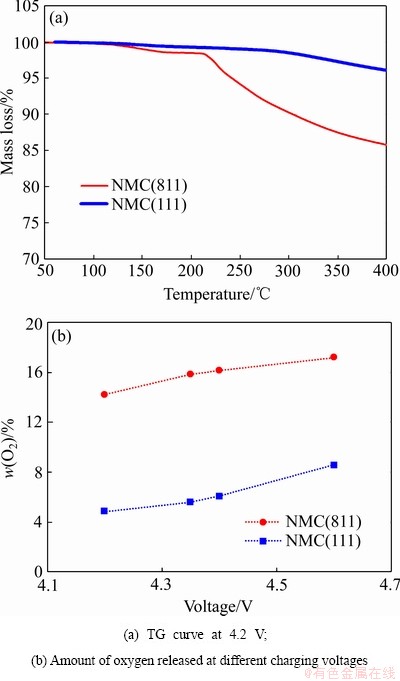
ͼ6 NMC(811)��NMC(111)�ڲ�ͬ�¶��µ����ȶ�����
Fig. 6 Thermal stability of NMC(811) and NMC(111) cathode material at different temperatures
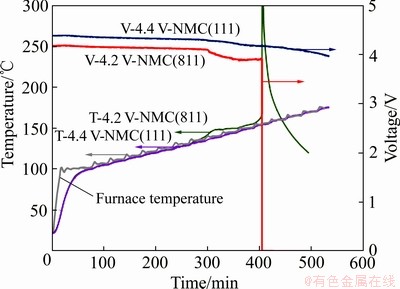
ͼ7 ����4.2-NMC(811)��4.4 V-NMC(111)����������װ�ĵ���������е����ȶ���
Fig. 7 Thermal stability of hot box based on batteries assembled 4.2 V-NMC(811) and 4.4 V-NMC(111) cathode material
��ø������ܶ�����ӵ�صķ�ʽ�����֣�һ������߲��ϵĿ���������һ��������������ϵĵ�ѹ��Ŀǰ��ҵ��ʹ����Ϊ�㷺�����������(NMC)�������ϣ�����������ϵĿ������ķ�ʽ���������������NMC(811)������ʹ�ø���������NMC(811)�ή��﮵�ص���ڵ�ѹ�����������������ϵ����ȶ��Է�����4.4 V-NMC(111)��������(6.0%)��Ϊ4.2 V- NMC(811)������(14.2%)��һ�롣��ˣ������Ʊ�������4.4 V-NMC(111)��4.2 V-NMC(811)�������ϵ�����ӵ�ء�����ȫ���4.4 V-NMC(111)��4.2 V- NMC(811)��������ֱ�Ϊ49��52 A��h�������ܶȷֱ�Ϊ218��228 W��h/kg����������������ҵ���е�ص��������ܵ�һ�ֳ��÷�����ͬʱҲ�Ǽ��缫�����ڵ���е����ȶ����ܵ���Ҫ�ֶΡ��������ֵ�ص���������ͼ7��ʾ����¯��135 ��ʱ��4.2 V- NMC(811)��ʼ�����ڶ�·����ѹ���½�����¯�´ﵽ150 ��ʱ��4.2 V-NMC(811)ʧЧ����4.4 V-NMC(111)ʧЧʱ��¯����180 �档����ʵ��������������4.4 V-NMC(111)��4.2 V-NMC(811)��﮵�ؾ��и��õ����ȶ����ܣ����Ӱ�ȫ������4.4 V-NMC(111)�������ܶȵ�һЩ����������и��ߵ����ȶ����ܣ�������ָ�����������߰�ȫ�ĵ����־����ش����塣
3 ����
1) ���ų���ֹ��ѹ�������������ϵ����ȶ������½������������ӡ�����LixCoO2�������ϣ�����ֹ��ѹ��������LixCoO2��״�ṹ���ƻ������ȶ��Ա��ֽ�����O2��ͬʱ�����Һ�Ĵ��ڣ�����������ϵ����ȶ��ԡ�
2) ����4.2 V-NMC (811)�������ϵ������ܶ�Ϊ228 W��h/kg��������4.4 V-NMC (111)�������ϵ������ܶ�Ϊ218 W��h/kg������4.4 V-NMC (111)�������ϵ������ܶ��Եͣ�����4.4 V-NMC (111)�������ϵ�����������4.2 V-NMC (811)����������������һ�롣
3) ����4.4 V-NMC (111)��4.2 V-NMC (811)����������װ�ĵ�ر�����4.4 V-NMC (111)�������ܸ��ã���ظ��Ӱ�ȫ����Ϊ��չ�������ܶȡ��߰�ȫ�Ե�����ӵ���ṩ���µ�˼·��
REFERENCES
[1] BRAUN P V, CHO J, PIKUL J H, KING W P, ZHANG H. High power rechargeable batteries[J]. Current Opinion in Solid State and Materials Science, 2012, 16(4): 186-198.
[2] ZHANG X, CHENG F, YANG J, CHEN J. LiNi0.5Mn1.5O4 porous nanorods as high-rate and long-life cathodes for Li-ion batteries[J]. Nano Letters, 2013, 13(6): 2822-2825.
[3] Ф����, ������, ������, ������, ¬����, �� ��. ����ӵ����������LiNi0.5Co0.2Mn0.3O2���ȵ绯ѧ[J]. �й���ɫ����ѧ��, 2017, 27(4): 739-746.
XIAO Zhong-liang, ZHOU Qing-qing, SONG Liu-bin, HU Chao-ming, LU Yi-peng, CAO Zhong. Thermo- electrochemistry on LiNi0.5Co0.2Mn0.3O2 cathode material for lithium ion battery [J]. The Chinese Journal of Nonferrous Metals, 2017, 27(4): 739-746.
[4] �� ��, ����ƽ, ��֥��. ����Ӷ�����ؼ�����״����չ����[J]. �й����¿Ƽ�, 2018, 7(4): 58-64.
LIU Yan, HU Qing-ping, TAO Zhi-yong. Current status and development trend of lithium ion power battery technology[J]. China High-Tech, 2018, 7(4): 58-64.
[5] LIU B H, JIA Y K, LI J, YIN S, YUAN C H, HU Z H, WANG L B, LI Y X, XU J. Safety issues caused by internal short circuits in lithium-ion batteries[J]. Journal of Materials Chemistry A, 2018, 43(6): 21475-21484.
[6] �� ��, ��ѧ��, ɣ ��, �� ��, ��˶��, ���˽�, �� ǿ. Li/CFx��ظ��´������ܺ�ʧЧ����[J]. �й���ɫ����ѧ��, 2019, 29(7): 1466-1473.
MA Ling, ZHONG Xue-qi, SANG Lin, DING Fei, ZHANG Shuo-qing, LIU Xing-jiang, XU Qiang. Storage performances and failure mechanisms of Li-CFx batteries at high temperature[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(7): 1466-1473.
[7] FINEGAN D P, DARCY E, KEYSER M, TJADEN B, HEENAN T. Characterising thermal runaway within lithium-ion cells by inducing and monitoring internal short circuits[J]. Energy & Environmental Science, 2017, 10(6): 1377-1388.
[8] AN Zhou-jian, JIA Li, WEI Li-ting, YANG Cheng-liang. Numerical modeling and analysis of thermal behavior and Li+ transport characteristic in lithium-ion battery[J]. International Journal of Heat and Mass Transfer, 2018, 127: 1351-1366.
[9] SHAHABEDDIN K, MOHAMMADIAN, ZHANG Yu-wen. Improving wettability and preventing Li-ion batteries from thermal runaway using microchannels[J]. International Journal of Heat and Mass Transfer, 2018, 118: 911-918.
[10] LIU Hua-qiang, WEI Zhong-bao, HE Wei-dong, ZHAO Ji-yun. Thermal issues about Li-ion batteries and recent progress in battery thermal management systems: A review[J]. Energy Conversion and Management, 2017, 150(15): 304-330.
[11] YANG S, WANG W W, LIN C, SHEN W X , LI Y D. Investigation of internal short circuits of lithium-ion batteries under mechanical abusive conditions[J]. Energies, 2019, 12(10): 1885-1890.
[12] CHOI N S, CHEN Z H, FREUNBERGER S A, SUN Y K. Challenges facing lithium batteries and electrical double- layer capacitors[J]. Angewandte Chemie International Edition, 2012, 51(40): 9994-10024.
[13] ���ƽ, ������, �̷�Բ, ������, ף ��, �� ��, �� ��. ��������LTO/G��LTO/Ag-G�ĺϳɼ���绯ѧ�� ��[J]. �й���ɫ����ѧ��, 2018, 28(2): 319-326.
ZHU Ji-ping, ZHANG Yang-yang, CHENG Fang-yuan, ZHANG Wen-lan, ZHU Jie, WANG Juan, WANG Jie. Synthesis and electrochemical properties of LTO/G and LTO/Ag-G anode materials[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(2): 319-326.
[14] MALEKI H, DENG G, ANANI A, HOWARD J. Thermal stability studies of Li-ion cells and components[J]. Journal of The Electrochemical Society, 1999, 146(9): 3224-3229.
[15] LU Xi-bin, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun, YAN Guo-chun, YIN Xing. A modified co-precipitation process to coat LiNi1/3Co1/3Mn1/3O2 onto LiNi0.8Co0.1Mn0.1O2 for improving the electrochemical performance[J]. Applied Surface Science, 2014, 279(4): 182-187.
[16] �� ��, �� ҫ, ��عȺ, �� ��. ����ӵ�ذ�ȫ�����о�[J]. ��ѧ��չ, 2011, 23(2/3): 401-409.
WU Kai, ZHANG Yao, ZENG Yu-qun, YANG Jun. Safety performance of lithium-ion battery[J]. Process in chemistry, 2011, 23(2/3): 401-409.
[17] FENG X N, FANG M, HE X M, OUYANG M, LU L G, WANG Hao, ZHANG M X. Thermal runaway features of large format prismatic lithium ion battery using extended volume accelerating rate calorimetry[J]. Journal of Power Sources, 2014, 255(1): 294-301.
[18] FENG X N, FANG M, HE X M, OUYANG M, LU L G, HAN X B, FANG M, PENG H Characterization of large format lithium ion battery exposed to extremely high temperature[J]. Journal of Power Sources, 2014, 272(25): 457-467.
[19] WANG Y D, JIANG J W, DAHN J R. The reactivity of delithiated Li(Ni1/3Co1/3Mn1/3)O2, Li(Ni0.8Co0.15Al0.05)O2 or LiCoO2 with non-aqueous electrolyte[J]. Electrochemistry Communications, 2007, 9(10): 2534-2540.
[20] ��ϲ��, �ź���, �� ��, �� ��, ���, ������. ����Ӳ������Ӷ�����ص������Բ���[J]. �й���ɫ����ѧ��, 2019, 29(12): 2747-2756.
CUI Xi-feng, ZHANG Hong-liang, GONG Yang, LI Jie, YANG Jian-hong, LI Wang-xing. Thermal properties of hard cased lithium-ion power battery [J]. The Chinese Journal of Nonferrous Metals, 2019, 29(12): 2747-2756.
[21] GABRISCH H, YAZAMI R, FULTZ B, Hexagonal to cubic spinel transformation in lithiated cobalt oxide TEM investigation[J]. Journal of Electrochemical Society, 2004, 151(6): A891-A897.
[22] YAMAKI J I, BABA Y, KATAYAMA N, TAKATSUJI H, EGASHIRA M, OKADA S. Thermal stability of electrolytes with LixCoO2 cathode or lithiated carbon anode[J]. Journal of Power Sources, 2003, 119/121(1): 789-793.
[23] LI Qiu-yuan, JIAO Shu-hong, LUO, Lang-li, DING M S, ZHENG Jian-ming, CARTMELL S S, WANG Chong-min, XU kang, ZHANG Ji-guang, XU Wu. Wide temperature electrolytes for lithium-ion batteries[J]. ACS Applied Materials & Interfaces, 2017, 9(22): 18826-18835.
[24] �� ��, ������, �� ��, ������, �� ��, �� ��. ����������ӵ�ع��ܵ��Һ���о���չ[J]. �й���ɫ����ѧ��, 2017, 27(6): 1208-1221.
HONG Bo, YAN Xiao-lin, HONG Shu, LAI Yan-qing, LI Jie, JIANG Feng. Review of functional electrolyte for lithium-ion battery working in wide temperature scope[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(6): 1208-1221.
[25] FURUSHIMA Y, YANAGISAWA C, NAKAGAWA T, AOKI Y, MURAKI N. Thermal stability and kinetics of delithiated LiCoO2[J]. Journal of Power Sources 2011, 196(4): 2260-2263.
[26] BABA Y, OKADA S, YAMAKI, J I. Thermal stability of LixCoO2 cathode for lithium ion battery[J]. Solid State Ionics, 2002, 148(3/4): 311-316.
[27] ����Ծ, ���º�, �� ��, ������, �� ��. ����������ӵ�ص��Һ��缫�ķ�Ӧ[J]. �й���ɫ����ѧ��, 2007, 17(4): 629-635.
HU Chuan-yue, LI Xin-hai, GUO Jun, WANG Xing-yan, YI Tao. Reactions between electrolyte and electrode of lithium ion batteries at elevated temperature[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(4): 629-635.
[28] BOTTLE G G, WHITE R E, ZHANG Z. Thermal stability of LiPF6�CEC:EMC electrolyte for lithium ion batteries[J]. Journal of Power Sources, 2001, 25(z1): 570-575.
[29] BAK S M, HU E Y, ZHOU Y N, YU X Q, SENANAYAKE S D, CHO S J, KIM K B, CHUNG K Y, YANG X Q, NAM K W. Structural changes and thermal stability of charged LiNixMnyCozO2 cathode materials studied by combined in situ time-resolved XRD and mass spectroscopy[J]. ACS Applied Materials & Interfaces, 2014, 6(24): 22594-22601.
[30] SANTANA I L, MOREIRA T F M, LELIS M F F, FREITAS M B J G. Photocatalytic properties of Co3O4/LiCoO2 recycled from spent lithium-ion batteries using citric acid as leaching agent[J]. Materials Chemistry and Physics, 2017, 190(1): 38-44.
Design of high-safety and high-energy density lithium ion battery: High voltage layered cathode materials
CHEN Xiao-bo1, 2, 3, CHEN Shi-long3, LIN Yong-shou3, LU Shi-gang1, 2, WU Kai3
(1. National Automotive Cell Innovation Center, GRINM Group Co., Ltd., Beijing 100088, China;
2. General Research Institute for Nonferrous Metals, Beijing 100088, China;
3. Contemporary Amperex Technology Co., Ltd., Ningde 352100, China)
Abstract: The thermogravimetry-mass spectrometry (TG-MS) technique was used to analyze the thermal stability of cathode materials, including the thermal decomposition, the reaction thermal characteristics with the electrolyte, and the effects of different states of charge and electrolyte. For the lithium cobaltate cathode material, the reason why the O2 increased in LixCoO2 was systematically explored. The results show that the layered structure of the cathode materials is broken with the cut-off voltage increasing, resulting in the thermal stability decreasing, and even the thermal decomposition to release more oxygen with the increase of the amount of delithiation. Comparing the thermal stability of the cathode material of the full battery based on the 4.4 V LiNi0.33Mn0.33Co0.33O2 (4.4 V-NMC111) and 4.2 V LiNi0.8Mn0.1Co0.1O2 (4.2 V-NMC811), it is demonstrated that despite the similar energy density of 4.4 V-NMC111 and 4.2 V-NMC811, the 4.4 V-NMC111 has better high temperature resistance performance.
Key words: lithium ion battery; cathode materials; high voltage; thermal stability; thermogravimetry-mass spectrometry technique
Foundation item: Project(2016YFB0100400) supported by the National Key Research and Development Plan, China
Received date: 2019-12-26; Accepted date: 2020-06-08
Corresponding author: LU Shi-gang; Tel: +86-10-82241199; E-mail: lusg8867@163.com
WU Kai; Tel: +86-593-8901380��E-mail: WuK@catlbattery.com
(�༭ ��ѧ��)
������Ŀ�������ص��з��ƻ�������Ŀ(2016YFB0100400)
�ո����ڣ�2019-12-26�������ڣ�2020-06-08
ͨ�����ߣ�¬���գ����ڣ���ʿ���绰��010-82241199��E-mail��lusg8867@163.com
�� ����������ʦ����ʿ���绰��0593-8901380��E-mail��WuK@catlbattery.com