DOI: 10.11817/j.ysxb.1004.0609.2021-35951
铁铝共生矿熔分还原过程矿相转变行为
于海燕1, 2,张继豪1, 2,潘晓林1, 2,魏伯文2,毕诗文2
(1. 东北大学 多金属共生矿生态化冶金教育部重点实验室,沈阳 110819;
2. 东北大学 冶金学院,沈阳 110819)
摘 要:本文基于“非高炉提铁-铝酸钙渣提铝”工艺,以铁铝共生矿预还原球团为原料,系统研究了温度、时间、碳氧比(C/O)和钙铝比(C/A)对熔分还原过程铁铝矿相生成转变行为和铝酸钙渣氧化铝浸出性能的影响。结果表明:当熔分温度高于1500 ℃时渣铁分离效果良好,且能获得自粉性能良好的铝酸钙渣;C/O过高不利于铁相聚集。在本文试验条件范围内,熔分还原条件对铝酸钙渣矿相种类影响不大,主要为12CaO・7Al2O3、γ-2CaO・SiO2,并含有少量β-2CaO・SiO2、2CaO・Al2O3・SiO2、3CaO・2FeO・3SiO2和20CaO・13Al2O3・3MgO・3SiO2。随着熔分温度和碳氧比的升高,铝酸钙渣中12CaO・7Al2O3含量逐渐降低,2CaO・Al2O3・SiO2含量逐渐增加,导致其氧化铝浸出率降低;随着C/A的升高,12CaO・7Al2O3含量逐渐增加,2CaO・Al2O3・SiO2含量显著降低,提高了铝酸钙渣的氧化铝浸出率,但当C/A提高到1.8以上时,3CaO・Al2O3的生成会导致氧化铝浸出率降低。熔分还原最佳条件为温度1500 ℃、时间30 min、C/O=0.6、C/A=1.7,此时渣铁分离效果良好,铝酸钙渣氧化铝浸出率达到89.03%。
关键词:铁铝共生矿;熔分还原;氧化铝浸出;铝酸钙;自粉
文章编号:1004-0609(2021)-02-0433-10 中图分类号:TF821 文献标志码:A
引文格式:于海燕, 张继豪, 潘晓林, 等. 铁铝共生矿熔分还原过程矿相转变行为[J]. 中国有色金属学报, 2021, 31(2): 433-442. DOI: 10.11817/j.ysxb.1004.0609.2021-35951
YU Hai-yan, ZHANG Ji-hao, PAN Xiao-lin, et al. Mineral transition of iron-aluminum symbiotic ore during melting reduction process[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(2): 433-442. DOI: 10.11817/j.ysxb.1004.0609.2021-35951
进入21世纪以来,我国氧化铝工业蓬勃发展,氧化铝产量连续多年占世界50%以上。然而,我国铝土矿资源储量只占世界总储量的不到3%,且普遍存在品位低、杂质多、冶炼成本高等问题,资源短缺问题日益突出,预计国内铝土矿的保障年限不足10年,与国外安全供矿50年以上的标准相差甚远。同时,我国铁矿石品位低且开采成本较高,使得国内所需的铁矿石消费大部分依赖于进口。目前我国50%以上的铝土矿和85%以上的铁矿石都依靠进口,对外依存度逐年攀升,而国际上矿产资源供给往往受到巨头垄断和政治形势双重制约和影响,其价格和供给量的大幅波动不仅对我国铝工业和钢铁工业造成严重影响,而且对国民经济的健康持续发展构成了巨大威胁[1-2]。因此,开发我国自有铁铝资源,对我国铝工业与钢铁工业的健康发展具有重大意义[3]。
我国拥有储量丰富的铁铝共生矿,仅广西已探明的资源储量就达10亿t以上。这种铁铝共生资源为多金属复合矿,氧化铝与氧化铁含量之和通常可达65%~80%以上[4-5],并含有镓、钒与稀土等稀散金属[6]。然而,由于我国绝大多数铁铝共生矿中,铁铝矿物粒度细且嵌布紧密,类质同相现象较为常见[7],铁铝矿物共生关系复杂,难以采取单一的铁铝提取方法进行提取,使得铁铝共生矿成为我国典型的难处理呆滞矿石。
针对铁铝共生资源的综合利用,国内许多研究单位提出了多种方案,大致可分为“先选后冶[8-10]”、“先铝后铁[11-13]”、“先铁后铝[14-15]”三种基本方案。先选后冶技术路线因铁铝共生资源多为矿物互相镶嵌,结构复杂,解离性能极差,难以获得理想的铁铝选矿分离效果;先铝后铁技术路线存在铝回收率低、赤泥炼铁时脱钠困难等问题[12]。因此,先铁后铝被认为是处理铁铝共生资源的可行性最好的技术路线。毕诗文等[16]提出“烧结-高炉冶炼提铁-铝酸钙渣提铝”工艺技术,在高炉内将铁矿物还原成铁水,铝矿物生成铝酸钙渣,并同时完成渣铁分离过程;LI等[17]通过钠化焙烧高铁铝土矿,在240 ℃浸出磁选后的非磁性物料,能够获得较高的氧化铝浸出率;LIU等[18]采用金属化还原和磁选处理高铁铝土矿,能够完成铁铝的分离过程,然而铁铝尖晶石的形成降低了金属铁的回收率;YUAN等[19]采用流态化氢悬浮焙烧并结合磁选工艺,能够去除高铁铝土矿85%以上的氧化铁,但获得铝精矿的拜耳法溶出性能还不知晓。以上综合利用铁铝共生资源的方案虽然可达到铁铝分离的技术指标,但由于环保、能耗等因素推广到工业生产仍有一定的难度。近年来,作者提出了“非高炉提铁-铝酸钙渣提铝”高效处理铁铝共生资源新工艺[20],技术路线如图1所示。该工艺将焦化、烧结和高炉冶炼三个工序缩短为熔融还原工序,简化了生产流程,以煤代焦直接生产铁水,可减轻对焦煤资源的依赖,显著降低炼铁成本;基于火法冶金使嵌布复杂的铝铁彻底分离,直接生产高质量铁水,铁回收率接近100%;炼铁的同时产生大量高质煤气,并完成构建铝酸钙渣矿物条件,有效提取氧化铝;提铝尾渣含碱量低,可生产水泥或硅酸钙粉体材料。
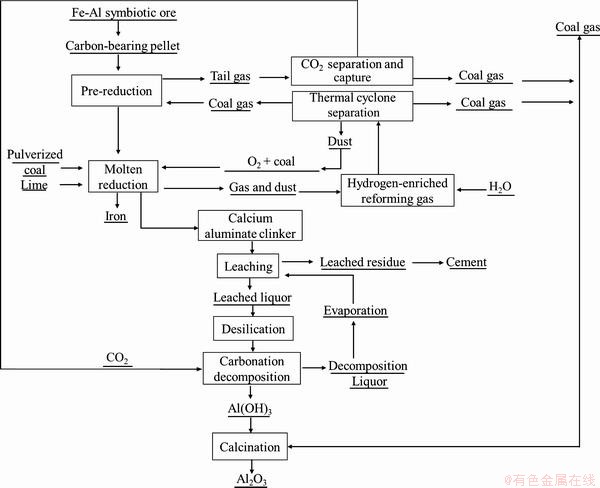
图1 铁铝共生矿生态化高效利用工艺流程
Fig. 1 Flow chart of ecological and efficient utilization of iron-aluminum symbiotic resources
作者前期研究铁铝共生矿碳热预还原过程矿相转变规律,并确定了最佳的预还原工艺条件[21]。本文以铁铝共生矿预还原球团为原料,系统研究不同条件下熔分还原过程中铁铝矿相的生成转变行为和铝酸钙渣氧化铝浸出性能,以期为高效综合利用我国储量巨大的铁铝共生资源提供实际指导。
1 实验
将煤粉与CaCO3配入铁铝共生矿使C/O=0.6,C/A=1.7在1250 ℃电炉中保温30 min完成预还原。物料研磨过150 μm筛即得到用于熔分还原的原料,预还原矿成分与XRD图谱分别见表1与图2所示。将预还原矿粉、煤粉与CaCO3按照试验所需不同碳氧比(C/O)、钙铝比(C/A)混合后放入石墨坩埚中,于高温炉中升温进行熔分还原,试验参数由试验所需条件确定。C/O,即n(C)/n(O),为配入煤中的碳与铁氧化物中氧的摩尔比;C/A,即n(CaO)/ n(Al2O3),为除去与SiO2结合成2CaO・SiO2和与TiO2结合成CaO・TiO2之外的CaO与Al2O3的摩尔比。当炉内温度降至室温后,取出熟料,通过磁选分离出磁性物料与非磁性铝酸钙渣。
表1 预还原矿的主要成分
Table 1 Compositions of pre-reduced ore (mass fraction, %)

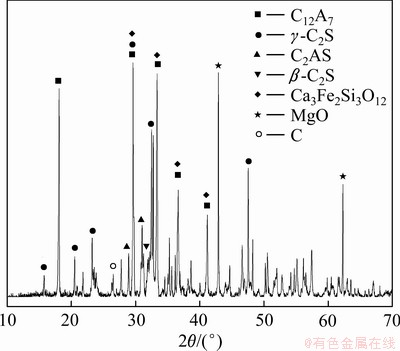
图2 预还原矿XRD谱
Fig. 2 XRD pattern of pre-reduced ore
将盛有Na2O浓度为80 g/L Na2CO3溶液的三口瓶固定在80 ℃水浴锅中按液固比10/1(Na2CO3溶液体积与铝酸钙渣的质量比,mL/g)加入铝酸钙渣,120 min后停止浸出试验,经过滤、洗涤、烘干、研磨粒径小于74 μm后制成待检测样品。取样经化学分析计算氧化铝的浸出率。氧化铝浸出率与矿相含量半定量计算公式分别见式(1)和(2)。
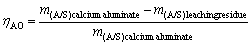 (1)
(1)
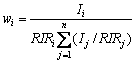 (2)
(2)
式中: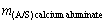 和
和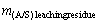 分别为铝酸钙渣和进行氧化铝浸出后渣中Al2O3和SiO2的质量比;wi为样品中i相的含量,%;Ii为i相最强衍射峰的强度;RIRi为i相的RIR值,
分别为铝酸钙渣和进行氧化铝浸出后渣中Al2O3和SiO2的质量比;wi为样品中i相的含量,%;Ii为i相最强衍射峰的强度;RIRi为i相的RIR值,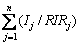 为样品中所有物相最强衍射峰强度与其参比强度之比的和[22]。
为样品中所有物相最强衍射峰强度与其参比强度之比的和[22]。
利用X射线荧光仪(XRF, ZSX100e)对预还原矿与铝酸钙渣的化学成分进行分析。在预还原矿与铝酸钙渣中加入10% MgO做为内标计算矿相含量,矿相分析采用X射线衍射仪(XRD, PANalytical PW3040/60),扫描速度(2θ)为3 (°)/min。利用扫描电子显微镜(SEM, Shimadzu SSX-550)研究铝酸钙渣的微观形貌和微区成分,加速电压为15 kV。
2 结果与讨论
2.1 熔分还原温度的影响
在C/A=1.5、C/O=1.0时分别在1450、1500、1550和1600 ℃条件下保温30 min,研究熔分还原温度对铝酸钙渣矿相形成与氧化铝浸出性能的影响。经熔分还原后的铝酸钙渣XRD谱如图3所示。
由图3可知,不同熔分温度下铝酸钙渣的矿相组成主要为12CaO・7Al2O3(C12A7)、γ-2CaO・SiO2(C2S)以及少量的β-2CaO・SiO2、2CaO・Al2O3・SiO2(C2AS)、3CaO・2FeO・3SiO2和20CaO・13Al2O3・3MgO・3SiO2。当熔分温度继续升高到1550 ℃时,体系中的12CaO・7Al2O3特征峰强逐渐减弱,2CaO・Al2O3・SiO2含量略微提高,含铝矿相主要为依然为12CaO・7Al2O3;当熔分温度为1600 ℃时部分12CaO・7Al2O3向3CaO・Al2O3(C3A)转化,3CaO・Al2O3含量有所提高。
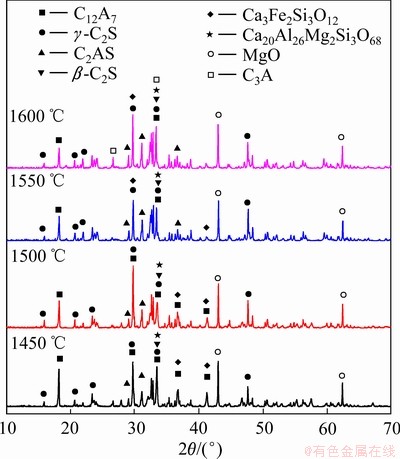
图3 不同熔分还原温度下铝酸钙渣XRD谱
Fig. 3 XRD patterns of calcium aluminate slag at different melting reduction temperatures
对于铝酸钙相,在升温过程中可能涉及以下反应:
CaO+Al2O3=CaO・Al2O3 (3)
12CaO+7Al2O3=12CaO・7Al2O3 (4)
3CaO+Al2O3=3CaO・Al2O3 (5)
7CaO・Al2O3+5CaO=12CaO・7Al2O3 (6)
CaO・Al2O3+2CaO=3CaO・Al2O3 (7)
12CaO・7Al2O3+9CaO=(7)3CaO・Al2O3 (8)
经热力学计算,式(6)的吉布斯自由能小于式(7) 的,在CaO充足的条件下,中间生成的CaO・Al2O3能够与CaO反应生成12CaO・7Al2O3。且式(6)在试验温度范围内可自发反应,当体系中铝酸钙相已充分转化为12CaO・7Al2O3相时,若体系中还有未反应完全的CaO,12CaO・7Al2O3便会与剩余的CaO继续反应生成3CaO・Al2O3。从以上反应过程可以看出,3CaO・Al2O3只会通过12CaO・7Al2O3进一步转化而来[23]。因此,3CaO・Al2O3在铝酸钙渣中的含量主要与配入的CaO量和不同铝酸钙相的转化速度有关。在熔分温度为1600 ℃的渣中,铝酸钙中12CaO・7Al2O3开始向3CaO・Al2O3转变,其原因应是更高的温度加快了不同铝酸钙相的转化速度。熔分温度由1550 ℃升高到1600 ℃后,铝酸钙相之间转化速度加快,由此推测,继续提高熔分温度时,部分12CaO・7Al2O3生成后将迅速转化为3CaO・Al2O3。
图4所示为1450和1500 ℃得到的铁珠及1500 ℃时的铝酸钙渣形貌。图4可以看出,1450 ℃磁选得到的铁珠中有明较多夹杂物,磁性物与非磁性物分离较差;而1500 ℃磁性物质表面无明显夹杂物,渣铁分离良好,且铝酸钙渣具有良好的自粉性能(见图4(c))。分析认为,1500 ℃熔分还原后得到的还原铁完全熔化并聚集成小铁珠渣铁分离效果良好,铝酸钙渣自粉良好,因此选择1500 ℃为熔分还原温度。对铝酸钙渣进行标准浸出试验,浸出结果如图5所示。
由图5可以看出,氧化铝浸出率随熔分温度的升高出现明显降低。当熔分温度由1450 ℃继续升高时,得到的铝酸钙渣浸出性能急剧恶化,这是由于在升温过程中部分12CaO・7Al2O向3CaO・Al2O3转化造成的。

图4 不同熔分温度下铁相与铝酸钙渣形貌
Fig. 4 Morphologies of iron and calcium aluminate slag at different melting reduction temperatures
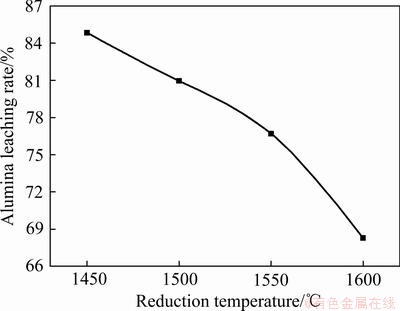
图5 不同熔分温度下铝酸钙渣氧化铝浸出率
Fig. 5 Alumina leaching rates of calcium aluminate slag at different melting reduction temperatures
2.2 熔分还原时间的影响
将预还原矿在1500 ℃、C/A=1.5、C/O=1.0时进行时间分别为15 min、30 min、45 min与60 min的熔分还原试验,研究熔分还原时间对铝酸钙渣矿相与氧化铝浸出性能的影响。经熔分还原后的铝酸钙渣XRD谱如图6所示,不同熔分时间下铝酸钙渣矿相组成基本相同且含量变化不大,主要矿相为12CaO・7Al2O3、γ-2CaO・SiO2、2CaO・Al2O3・SiO2,并含有少量的β-2CaO・SiO2、3CaO・2FeO・3SiO2、20CaO・13Al2O3・3MgO・3SiO2,但20CaO・13Al2O3・3MgO・3SiO2含量很低,未在XRD谱中标出。
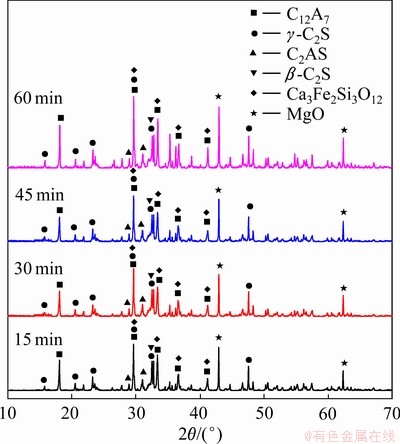
图6 不同熔分还原时间下铝酸钙渣XRD谱
Fig. 6 XRD patterns of calcium aluminate slag for different melting reduction durations
不同熔分时间获得的铝酸钙渣的氧化铝浸出性能如图7所示,随着熔分时间的延长,氧化铝的浸出率呈先上升后下降趋势。为探明保温时间影响铝酸钙渣浸出性能的机理,对影响氧化铝浸出的12CaO・7Al2O3和2CaO・Al2O3・SiO2含量进行了半定量计算,结果见表2。

图7 不同熔分还原时间下铝酸钙渣氧化铝浸出率
Fig. 7 Alumina leaching rates of calcium aluminate slag for different melting reduction durations
表2 不同熔分还原时间下铝酸钙渣矿相含量
Table 2 Mineral compositions of calcium aluminate slag for different melting reduction durations

由表2可知,随着熔分时间的延长,12CaO・7Al2O3和2CaO・Al2O3・SiO2均有小幅度变化。当保温时间由15 min提高至30 min时,12CaO・7Al2O3含量由13.58%升至15.91%,这是由于随着保温时间的延长,更多的Al2O3转化为12CaO・7Al2O3。利用Jade软件对图6中数据拟合并计算发现,12CaO・7Al2O3的半高峰宽呈现持续增加的趋势,根据Scherrer公式可知,其晶体尺寸逐渐增大,结晶度逐渐增加。说明随保温时间的延长,12CaO・7Al2O3晶粒逐渐长大且结晶趋于完整,晶体表面的缺陷更少,这些因素增加了12CaO・7Al2O3晶体在碱溶液中的稳定性,使 与H2O穿过晶体表面发生反应的能力降低[24]。由于不溶相2CaO・Al2O3・SiO2的含量在30 min后随时间延长而增加,导致30 min后铝酸钙渣的氧化铝浸出率下降。
与H2O穿过晶体表面发生反应的能力降低[24]。由于不溶相2CaO・Al2O3・SiO2的含量在30 min后随时间延长而增加,导致30 min后铝酸钙渣的氧化铝浸出率下降。
2.3 配碳量的影响
在熔分还原温度为1500 ℃、时间为30min、C/A =1.5时,通过加入不同量的煤粉使C/O分别为0.6、0.8、1.0和1.2,研究C/O对铝酸钙渣矿相转变和铁聚集的影响。对不同C/O时得到的铝酸钙渣进行XRD分析,结果如图8所示。
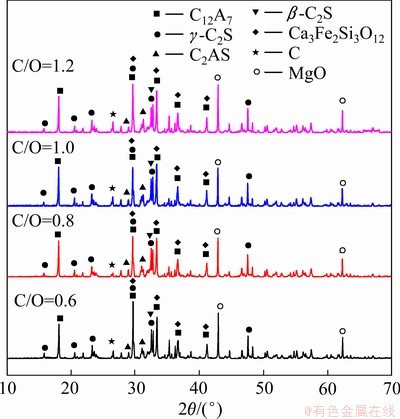
图8 不同C/O时铝酸钙渣XRD谱
Fig. 8 XRD patterns of calcium aluminate slag with different C/O values
由图8可知,不同C/O条件下,铝酸钙渣矿相组成基本相同,主要矿相为12CaO・7Al2O3、γ-2CaO・SiO2,并有少量2CaO・Al2O3・SiO2、β-2CaO・SiO2、Ca3Fe2Si3O12。随着C/O的提高,2CaO・Al2O3・SiO2含量略微升高。这可能是因为碳含量升高,渣相黏度增加,2CaO・Al2O3・SiO2与CaO的转熔反应进行难度增大,从而使大量2CaO・Al2O3・SiO2留在渣相中。
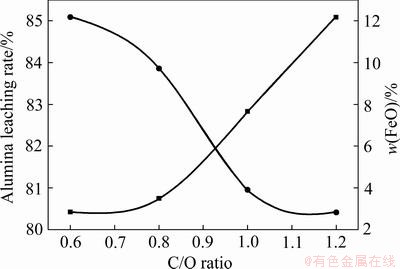
图9 不同C/O时铝酸钙渣氧化铝浸出率及FeO含量
Fig. 9 Alumina leaching rates and FeO contents of calcium aluminate slag with different C/O values
从图9可以看出,随着C/O的升高,铝酸钙渣氧化铝浸出率下降,而渣相中FeO含量逐渐升高。王波[25]认为当FeO残留量大于0.5%时,会消耗12CaO・7Al2O3生成6CaO4・Al2O3・FeO・SiO2。该四元系化合物的生成是降低铝酸钙中Al2O3浸出性能的主要原因。FeO残留量的增加反映了铁还原效果的变差。FeO的碳还原包括固体碳直接还原与CO间接还原。高温条件下CO2气体会与固体碳反应继续生成CO气体。在高温条件下,固体碳的还原能力又要强于CO的还原能力。分析认为本试验铁相的还原效果应主要与固体碳的直接还原有关。当物料的C/O达到0.6时,体系用于还原铁的碳量充足,增大碳含量会使物料黏度增大,碳扩散困难,不利于固体碳与铁氧化物的固固还原及固液还原,最终导致铝酸钙渣中残留较多的FeO。
为进一步考察碳阻碍铁相聚集的机理,将C/O=0.6磁选得到的铁珠从中心截开,通过扫描电子显微镜对其截面进行元素面扫描分析,结果如图10所示。
由图10可以看出,铁珠截面嵌布着大小、形状不一的条状碳单质,且数量较多。分析认为,出现此种表面形貌是铁的渗碳作用与小铁珠的相互聚合造成的。高温状态下,铁的渗碳反应使得最初形成的液态小铁珠表面附着了一层碳颗粒,随着还原反应的进行,液相小铁珠逐渐增多,物料孔隙率不断增大,小铁珠开始相互聚合形成大铁珠。在聚合过程中,表面附着碳单质的小铁珠被包裹在大铁珠中。当提高C/O时,初始形成的铁珠表面附着大量碳单质,在铁珠聚合过程中,这些碳单质会起到阻碍作用,这也是当配碳量过高时铁相聚合效果变差的原因。

图10 铁珠SEM像和元素面扫描图
Fig. 10 SEM and element scanning images of iron pellet
2.4 配钙量的影响
在熔分还原温度为1500 ℃、时间为30 min、C/O=0.6时,研究C/A分别为1.4、1.5、1.6和1.7时对熔分还原后铝酸钙渣矿相和浸出性能的影响。不同C/A时铝酸钙渣XRD谱如图11所示。当C/A介于1.4至1.7之间时,铝酸钙渣矿相种类基本相同,主要矿相为12CaO・7Al2O3、γ-2CaO・SiO2、2CaO・Al2O3・SiO2,并含有少量β-2CaO・SiO2、3CaO・2FeO・3SiO2、20CaO・13Al2O3・3MgO・3SiO2。随着C/A的升高,12CaO・7Al2O3、2CaO・Al2O3・SiO2、β-2CaO・SiO2含量有较明显变化。
表3中列出了不同C/A时得到的铝酸钙渣中主要矿相的含量,随着C/A的升高,12CaO・7Al2O3含量逐渐升高,β-2CaO・SiO2和2CaO・Al2O3・SiO2含量均逐渐降低。当C/A为1.8时铝酸钙渣中12CaO・7Al2O3含量相较C/A=1.7时下降约2%。造成此变化的原因可能是C/A=1.8时已有3CaO・Al2O3生成,但由于其含量低而未在XRD谱上显现出来,这是造成C/A=1.8时铝酸钙渣中12CaO・7Al2O3含量降低的原因。
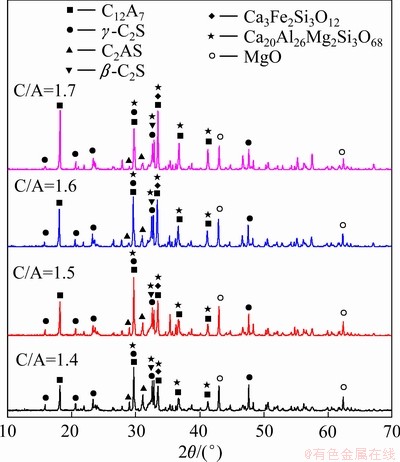
图11 不同C/A时铝酸钙渣XRD谱
Fig. 11 XRD patterns of calcium aluminate slag with different C/A values
表3 不同C/A时铝酸钙渣矿相含量
Table 3 Mineral compositions of calcium aluminate slag with different C/A values

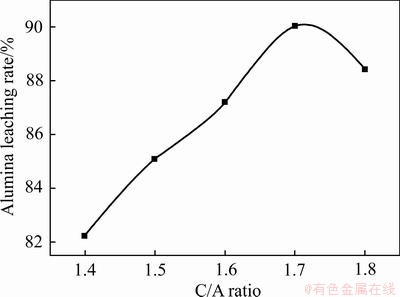
图12 不同C/A时铝酸钙渣氧化铝浸出率
Fig. 12 Alumina leaching rates of calcium aluminate slag with different C/A values
对铝酸钙渣进行氧化铝浸出试验,结果如图12所示。由图12可知,当C/A从1.4提高至1.7时,铝酸钙渣的氧化铝浸出率逐渐升高,在C/A=1.7时达到最大值,为89.03%;继续提高C/A时,氧化铝浸出率开始下降至88.42%。12CaO・7Al2O3的含量变化规律与氧化铝浸出率变化规律一致。
3 结论
1) 当熔分温度低于1500 ℃时渣铁分离效果不好,当熔分温度高于1500 ℃时渣铁分离效果良好,且能获得自粉性能良好的铝酸钙渣;C/O比过高不利于铁相聚集。
2) 当熔分还原温度为1450~1550 ℃、时间为15~60 min、配料C/O为0.6~1.2、C/A为1.4~1.7时,温度、时间、C/O与C/A对铝酸钙渣矿相种类影响不大,主要为12CaO・7Al2O3、γ-2CaO・SiO2,并含有少量的β-2CaO・SiO2、2CaO・Al2O3・SiO2、3CaO・2FeO・3SiO2和20CaO・13Al2O3・3MgO・3SiO2。
3) 随着熔分温度与C/O的升高,铝酸钙渣中12CaO・7Al2O3含量逐渐降低,2CaO・Al2O3・SiO2含量逐渐升高,导致其氧化铝浸出率降低;随着C/A的升高,12CaO・7Al2O3含量逐渐升高,2CaO・Al2O3・SiO2含量显著降低,提高了铝酸钙渣的氧化铝浸出率;但当C/A提高到1.8以上时,3CaO・Al2O3的生成会导致氧化铝浸出率降低。
4) 熔分还原过程最佳条件如下:熔分还原温度1500 ℃,保温时间30 min,C/O=0.6,C/A=1.7。此时渣铁分离效果良好,铝酸钙渣氧化铝浸出率为89.03%。
REFERENCES
[1] 韩跃新, 柳 晓, 何发钰, 等. 我国铝土矿资源及其选矿技术进展[J]. 矿产保护与利用, 2019, 4(8): 151-158.
HAN Yue-xin, LIU Xiao, HE Fa-yu, et al. Current situation of bauxite resource and its beneficiation technology in China[J]. Conservation and utilization of mineral resources, 2019, 4(8): 151-158.
[2] 陈喜峰. 中国铝土矿资源勘查开发现状及可持续发展建议[J]. 资源与产业, 2016, 18(3): 16-22.
CHEN Xi-feng. Exploration and sustainable development suggestions for China’s bauxite resource[J]. Resources&Industries, 2016, 18(3): 16-22.
[3] 田 丁, 申晓毅, 辛海霞, 等. 铁铝共生矿绿色化综合利用[J]. 轻金属, 2018(9): 13-16.
TIAN Ding, SHEN Xiao-yi, XIN Hai-xia, et al. Clean and integrated utilization of iron-aluminum paragenetic mineral[J]. Light Metals, 2018(9): 13-16.
[4] 何海洲, 杨志强, 郑 力. 广西铝土矿资源特征及利用现状[J]. 中国矿业, 2014, 23(5): 14-17, 22.
HE Hai-zhou, YANG Zhi-qiang, ZHENG Li. Analysis on the utilization status of Guangxi’s bauxite resources and its characteristics[J]. China mining magazine, 2014, 23(5): 14-17, 22.
[5] LIU Xue-fei, WANG Qing-fei, ZHANG Qi-zuan, et al. Mineralogical characteristics of the superlarge quaternary bauxite deposits in Jingxi and Debao counties, western Guangxi, China[J]. Journal of Asian Earth Sciences, 2012, 52: 53-62.
[6] 李殷泰, 毕诗文, 段振瀛, 等. 关于广西贵港三水铝石型铝土矿综合利用工艺方案的探讨[J]. 轻金属, 1992(9): 6-14.
LI Yin-tai, BI Shi-wen, DUAN Zhen-ying, et al. Reviews on the comprehensive utilization technology of bauxite in Guigang, Guangxi, China[J]. Light Metals, 1992(9): 6-14.
[7] 陈世益, 周 芳, 洪金益. 广西贵港三水型铝土矿针铁矿中铝的类质同象置换[J]. 中南矿冶学院学报, 1993, 24(3): 6-14.
CHEN Shi-yi, ZHOU Fang, HONG Jin-yi. Isomorphous substitution of aluminium in goethite of Guigang gibbsitic bauxite from Guangxi[J]. Journal of Central-South Institute of Mining and Metallurgy, 1993, 24(3): 283-288.
[8] YU Xin-yang, WANG Hao-lin, WANG Qiang-qiang, et al. Flotation of low-grade bauxite using organosilicon cationic collector and starch depressant[J]. Transactions of Nonferrous Metals Society of China, 2016, 26(4): 1112-1117.
[9] LI Guang-hui, JIANG Tao, LIU Mu-dan, et al. Beneficiation of high silica bauxite ores of India an innovative approach[J]. Mineral Processing and Extractive Metallurgy Review, 2010, 31(3): 150-164.
[10] HE Jing-feng, BAI Qiang, DU Tian-ye. Beneficiation and upgrading of coarse sized low-grade bauxite using a dry-based fluidized bed separator[J]. Advanced Powder Technology, 2020, 31(1): 181-189.
[11] YEH C H, ZHANG Guang-qing. Stepwise carbothermal reduction of bauxite ores[J]. International Journal of Mineral Processing, 2013, 124: 1-7.
[12] PAN Xiao-lin, YU Hai-yan, TU Gan-feng. Reduction of alkalinity in bauxite residue during Bayer digestion in high-ferrite diasporic bauxite[J]. Hydrometallurgy, 2015, 151: 98-106.
[13] 刘桂华, 张 明, 肖 伟, 等. 高铁一水硬铝石型铝土矿的低钙比烧结[J]. 中国有色金属学报, 2008, 18(10): 1903-1908.
LIU Gui-hua, ZHANG Ming, XIAO Wei, et al. Sintering process of diasporicbauxite with high iron content at low ratio of lime to silica for alumina production[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(10): 1903-1908.
[14] ZHANG Ying-yi, Lü Wei, QI Yuan-hong, ZOU Zong-shu. Recovery of iron and calcium aluminate slag from high-ferrous bauxite by high-temperature reduction and smelting process[J]. International Journal of Minerals, Metallurgy and Materials, 2016, 23(8): 881-890.
[15] 张作良, 李 强, 李明明, 等. 气基预还原处理高铝铁矿石[J]. 东北大学学报(自然科学版), 2013, 34(4): 556-559.
ZHANG Zuo-liang, LI Qiang, LI Ming-ming, et al. Treatment of high-aluminium content iron ore by gas-based prereduction[J]. Journal of Northeastern University(Natural Science), 2013, 34(4): 556-559.
[16] 毕诗文, 杨毅宏, 李殷泰, 等. 从高炉铝酸钙渣提取氧化铝的研究[J]. 轻金属, 1992(6): 10-16.
BI Shi-wen, YANG Yi-hong, LI Yin-tai, et al. Study on the extraction of alumina from blast-furnace calcium aluminate slag[J]. Light Metals, 1992(6): 10-16.
[17] LI Guang-hui, LUO Jun, JIANG Tao, et al. Digestion of alumina from non-magnetic material obtained from magnetic separation of reduced iron-rich diasporic bauxite with sodium salts[J]. Metals, 2016, 6(11): 2-9.
[18] LIU Zheng-gen, CHU Man-sheng, WANG Zheng, et al. Study on metallized reduction and magnetic separation of iron from fine particles of high iron bauxite ore[J]. High Temperature Materials and Processes, 2017, 36(1): 79-88.
[19] YUAN Shuai, XIAO Han-xin, YU Tian-yi, et al. Enhanced removal of iron minerals from high-iron bauxite with advanced roasting technology for enrichment of aluminum[J]. Powder Technology, 2020, 372: 1-7.
[20] 于海燕, 武建强, 潘晓林, 等. 一种铁铝共生矿的综合利用方法: 中国, 201210069914.4[P]. 2012-03-16.
YU Hai-yan, WU Jian-qiang, PAN Xiao-lin, et al. A comprehensive utilization method of iron-aluminum symbiotic ore: China, 201210069914.4[P]. 2012-03-16.
[21] 于海燕, 张继豪, 王明理, 等. 铁铝共生矿碳热预还原过程矿相转变行为[J]. 中国有色金属学报, 2020, 30(9): 2127-2135.
YU Hai-yan, ZHANG Ji-hao, WANG Ming-li, et al. Mineral transition of iron-aluminum symbiotic ore during carbothermal pre-reduction process[J]. The Chinese Journal of Nonferrous Metals, 2020, 30(9): 2127-2135.
[22] PAN Xiao-lin, YU Hai-yan, TU Gan-feng, et al. Effects of precipitation activity of desilication products (DSPs) on stability of sodium aluminate solution[J]. Hydrometallurgy, 2016, 165: 261-269.
[23] TONG Zhi-fang, XIE Sen-lin, ZHANG Li-heng, et al. Material ratio optimization of low mass ratio of alumina to silica of calcium aluminate slag based on thermodynamic calculation method[J]. Advanced Materials Research, 2012, 404: 288-292.
[24] 孙会兰, 于海燕, 王 波, 等. 12CaO・7Al2O3溶出动力学[J]. 中国有色金属学报, 2008, 18(10): 1924-1925.
SUN Hui-lan, YU Hai-yan, WANG Bo, et al. Leaching dynamics of 12CaO・7Al2O3[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(10): 1924-1925.
[25] 王 波. 钙铝硅化合物在铝酸钙炉渣形成过程相变规律和浸出性能的研究[D]. 沈阳: 东北大学, 2008: 55-56.
WANG Bo. Research on phase transformation law and leaching property of Ca, Al, Si compounds in the formation of calcium aluminate slag[D]. Shenyang: Northeastern University, 2008: 55-56.
Mineral transition of iron-aluminum symbiotic ore during melting reduction process
YU Hai-yan1, 2, ZHANG Ji-hao1, 2, PAN Xiao-lin1, 2, WEI Bo-wen2, BI Shi-wen2
(1. Key Laboratory for Ecological Metallurgy of Multimetallic Mineral (Ministry of Education), Northeastern University, Shenyang 110819, China;
2. School of Metallurgy, Northeastern University, Shenyang 110819, China)
Abstract: Based on the new technology of “non-blast furnace to extraction and calcium aluminate slag to extract alumina”, the effects of temperature, time, carbon-oxygen ratio(C/O) and calcium-aluminum ratio(C/A) on the formation and transformation behavior as well as the alumina leaching performance of calcium aluminate slag in the smelting reduction process were studied. The results show that when the melting temperature is higher than 1500 ℃, the separation performance of slag and iron is good, and the calcium aluminate slag with good self-pulverization performance can be obtained. Over high C/O value is not conducive to the aggregation of iron phase. The smelting reduction conditions have little effect on the mineral types of calcium aluminate slag, which mainly includes 12CaO・7Al2O3, γ-2CaO・SiO2, and a small amount of β-2CaO・SiO2, 2CaO・Al2O3・SiO2, 3CaO・2FeO・3SiO2 and 20CaO・13Al2O3・3MgO・3SiO2. With the increase of melting temperature and C/O value, the contents of 12CaO・7Al2O3 and 2CaO・Al2O3・SiO2 in calcium aluminate slag decrease, which result in the decrease of alumina leaching rate. With the increase of C/A value, the content of 12CaO・7Al2O3 increases, and the content of 2CaO・Al2O3・SiO2 decreases significantly, which improves the alumina leaching rate of calcium aluminate slag; but when C/A value increases to more than 1.8, the formation of 3CaO・Al2O3 decreases the alumina leaching rate. The optimum conditions of smelting reduction are as follows: temperature of 1500 ℃, time of 30 min, C/O value of 0.6, C/A value of 1.7. At this time, the separation of slag and iron is good, and the alumina leaching rate of calcium aluminate slag reaches 89.03%.
Key words: iron-aluminum symbiotic ore; melting reduction; alumina leaching; calcium aluminate; pulverization
Foundation item: Project(51374065) supported by the National Natural Science Foundation of China
Received date: 2020-04-15; Accepted date: 2020-11-24
Corresponding author: PAN Xiao-lin; Tel: +86-24-83686460; E-mail: panxl@smm.neu.edu.cn
(编辑 何学锋)
基金项目:国家自然科学基金资助项目(51374065)
收稿日期:2020-04-15;修订日期:2020-11-24
通信作者:潘晓林,副教授,博士;电话:024-83686460;E-mail:panxl@smm.neu.edu.cn