
DOIŁș 10.11817/j.issn.1672-7207.2020.04.003
Ëź»ŹÊŻ»ùNi(Mn, Cu)FežŽșÏŃő»ŻÎï”ÄÖƱžŒ°Æä”ÍÎÂNH3-SCRÓŠÓĂ
ŽÎłŹ1,¶ĆŃÇÀö2,Ń˩1,ŚȚŽșÀÙ1,ÎâĐń1
Łš1. Ì«ÔÀí耎óѧ »ŻŃ§»Żč€Ń§ÔșŁŹÉœÎś Ì«ÔŁŹ030024Ł»
2. œúÖĐѧÔș »ŻŃ§»Żč€Ń§ÔșŁŹÉœÎś œúÖĐŁŹ030619Ł©
ŐȘÒȘ:ÎȘÁËÌáÉęNiFežŽșÏŃő»ŻÎï(NiFe-LDO)Žß»ŻŒÁ”Ä”ÍÎÂÍŃÏőĐÔÄÜŁŹČÉÓĂÄòËŰËźÈȷ֜ⷚœ«čę¶ÉœđÊôMnșÍCuÔλÒęœűNiFeÀàËź»ŹÊŻ(NiFe-LDH)Čă°ćŁŹœèÖúNi(Mn, Cu)FeÀàËź»ŹÊŻ(Ni(Mn, Cu)Fe-LDH) Ÿ500 Ąæ±șÉŐŃÜÉúččÖțNi(Mn, Cu)FežŽșÏŃő»ŻÎï(Ni(Mn, Cu)Fe-LDO)Žß»ŻŒÁŁŹżŒČìĐÍŹčŠÄÜŚé·ÖMnșÍCuÔλÒęÈëNiFe-LDH¶ÔŃÜÉúččÖțžŽșÏŃő»ŻÎïŽß»ŻŒÁ”ÍÎÂÍŃÏőĐÔÄÜ”ÄÓ°ÏìĄŁŃĐŸżœáčû±íĂśŁșŸMnșÍCuČôÔÓŃÜÉúččÖț”ÄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁłÊÏÖłöžüșÔĔÍÎÂÍŃÏőĐÔÄÜŁŹNiCuFe-LDOŽß»ŻŒÁÔÚ210~360 ĄæʱŁŹNOŚȘ»ŻÂÊŸùłŹčę90%ŁŹN2ŃĄÔńĐԿɎï95%ÒÔÉÏŁ»¶űNiMnFe-LDOŽß»ŻŒÁÔÚ150 ĄæʱNOŚȘ»ŻÂÊżÉŽï90%ŁŹ180 ĄæʱNOŚȘ»ŻÂʜӜü99%ŁŹ150~360 Ąæ»îĐÔÎÂŽ°·¶Î§ÄÚŽß»ŻŒÁ”ÄN2ŃĄÔńĐÔŸùżÉÒÔÎȶšÔÚ96%ÒÔÉÏŁŹÍŹÊ±ŁŹÆä»čłÊÏÖœÏșÔĞ߿ŐËÙÊÊÓŠĐÔșÍœÏÇż”ÄżčËźżčÁòĐÔÄÜŁ»MnșÍCu”ÄÒęÈëȻ͏łÌ¶È”ŰÓĆ»ŻÁËNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄŃő»Ż»čÔĐÔșÍËáŒîĐÔŁŹŐâÊÇÒòÎȘNi3+șÍMn3+Œä”Ä”çŚÓŚȘÒÆŒÓËÙÁËŽß»ŻŒÁ±íĂæŃő»Ż»čÔŃ»·ŁŹ”ŒÖÂNiMnFe-LDOŸßÓĐžüÓĆÒì”Ä”ÍÎÂNH3-SCRĐÔÄÜĄŁ
čŰŒüŽÊ:Ëź»ŹÊŻŁ»Ni(Mn,Cu)FežŽșÏŃő»ŻÎïŁ»°±ÆűŃĄÔńĐÔŽß»Ż»čÔŁ»”ȘŃő»ŻÎïŁ»”ÍÎÂ
ÖĐÍŒ·ÖÀàșĆ:O643.32+2 ÎÄÏŚ±êÖŸÂë:A żȘ·ĆżÆѧ(ŚÊÔŽ·țÎń)±êʶÂë(OSID)
ÎÄŐ±àșĆ:1672-7207Łš2020Ł©04-0882-11
Preparation of Ni(Mn,Cu)Fe mixed metal oxides from LDH precursors and application in low-temperature NH3-SCR
CIĄĄChao1, DUĄĄYali2, YANGĄĄBaoshuan1, ZOUĄĄChunlei1, WUĄĄXu1
(1. College of Chemistry and Chemical Engineering, Taiyuan University of Technology, Taiyuan 030024, ChinaŁ»
2. College of Chemistry and Chemical Engineering, Jinzhong University, Jinzhong 030619, China)
Abstract: To improve the performance of NiFe-LDO in NH3-SCR at low temperatures, the transition metal Mn and Cu were in-situ doped into the NiFe-LDH laminates by the hydrothermal decomposition of urea. With the obtained NiMnFe-LDH and NiCuFe-LDH as precursors, the NiMnFe-LDO and NiCuFe-LDO catalysts were prepared after the calcination process at 500 Ąæ. Additionally, the effect of in-situ introduction of Mn and Cu on the denitration performances of the catalyst at low temperatures were investigated. The results show that the Mn-doped and Cu-doped Ni(Mn, Cu)Fe-LDO catalysts afford better redox property and remarkable denitration activity at low temperatures. For NiCuFe-LDO catalyst, the conversion of NO exceeds 90% and the selectivity of N2 reaches more than 95% in the range of 210ĄȘ360 Ąæ. Comparatively, except for its excellent N2 selectivity (>96%), NiMnFe-LDO catalyst possesses a wider active temperature window (150ĄȘ360 Ąæ) and higher NO conversion efficiency (with NO conversion beyond 90% at 150 Ąæ and around 99% at 180 Ąæ). Moreover, NiMnFe-LDO catalyst also presentes good high gas hourly space velocity adaptability and outstanding resistance ability to H2O and SO2. The introduction of Mn and Cu is beneficial to the redox as well as acid-base property optimization of Ni(Mn, Cu)Fe-LDO catalyst, which accelerates the redox cycle on the catalyst surface because of the electron transfer between Ni3+ and Mn3+ and thus endows the catalyst with superior denitration activity.
Key words: LDHs; Ni(Mn, Cu)Fe-LDO; NH3-SCR; NOx; low temperature
»ŻÊŻÈŒÁÏÈŒÉŐČúÉú”Ä”ȘŃő»ŻÎï(NOx)»áÔìłÉŃÏÖ۔Ļ·ŸłÎÊÌ⣏°üÀšËáÓêĄąč⻯ѧŃÌÎíșÍÎÂÊÒЧӊ”È[1-3]ĄŁËæŚĆÈËĂÇ»·±ŁÒâʶ”ÄČ»¶ÏÔöÇżŁŹÊÀœçžśčú·Ś·Ś°äČŒÏàÓŠ”Ä·šÂÉ·ščæżŰÖÆNOxĆĆ·ĆŁŹNOx”ÄžßЧÍŃłęÒŃłÉÎȘÏàčŰč€Ò”ÉúČú”„ÔȘ”ÄÖŰÒȘÈÎÎńĄŁÔÚÖÚ¶àÍŃÏőŒŒÊőÖĐŁŹ°±ŃĄÔńĐÔŽß»Ż»čÔŒŒÊő(NH3-SCR)ÒòÆäÍŃłęЧÂÊžßĄąÆűÌ掊ÀíÁżŽóĄą·ŽÓŠÌőŒțÒŚÓÚżŰÖÆ”ÈÓĆÊƶűÔÚ”±Ç°”Ă”œčúÄÚÍâčă·șÓŠÓĂŁŹ¶űžĂŒŒÊőÄÜ·ń·ą»ÓžßЧĐÔÄÜ”ÄčŰŒüÈĄŸöÓÚŽß»ŻŒÁ”ÄĐÔÄÜ[4-5]ĄŁŒűÓÚșܶàÆóÒ”ĆĆŃÌζÈÏà¶ÔœÏ”ÍŁŹÌœËśŃĐ·ą”ÍλîĐÔșĂĄąN2ŃĄÔńĐԞߥążčËźżčÁòĐÔÄÜÇż”ÄÍŃÏőŽß»ŻŒÁÒâÒćÖŰŽóĄŁNi»ùŃő»ŻÎïŽß»ŻŒÁŒÛžń”ÍÁźŁŹœ«ÆäÓëÆäËûœđÊôČôÔÓżÉÓĐЧ”śœÚŽß»ŻŒÁ”ÄŃő»Ż»čÔĐÔŒ°ËáŒîĐÔŁŹŽÓ¶űÒÖÖÆNH3”ÄčęŃő»ŻŁŹÌážßN2ŃĄÔńĐÔ[6]ĄŁFe»ùŃő»ŻÎïŽß»ŻŒÁŸßÓĐœÏžß”ÄÖĐžßÎÂÍŃÏő»îĐÔșÍœÏșÔĿčSO2ÖжŸĐÔÄÜ[7]ĄŁ»ùÓÚÀàËź»ŹÊŻŃÜÉúÎÌćÁŁŸ¶·ÖČŒŸùÔÈĄąÈÈÎȶšĐÔÁŒșĂșÍżčÉŐœá”ÈÓƔ㣏WANG”È[8]ÍščęŃĐŸż·ąÏÖŁŹŸNiFeÀàËź»ŹÊŻ(NiFe-LDH)ŃÜÉúÖƱž”ÄÄűÌúžŽșÏŃő»ŻÎï(NiFe-LDO)Žß»ŻŒÁŸßÓĐœÏșÔĿčÁòĐÔÄÜșÍŽß»ŻÎȶšĐÔŁŹ”«Æä”ÍÎÂÍŃÏő»îĐÔȹȻͻłöŁŹÈÔĐèÒȘœűÒ»ČœÓĆ»ŻĄŁLIU”È[9]ÖžłöœđÊôČôÔÓÄÜč»ÓĐЧ·ÖÉą»îĐÔÖĐĐÄŁŹÔöÇżŽß»ŻŒÁÓëÆűÌćÖźŒä”ÄÎüžœșͻŁŹÌáÉęŽß»ŻŒÁ”Ä”ÍÎÂÍŃÏő»îĐÔĄŁÔÚ”ÍÎÂSCR·ŽÓŠ”Ä»îĐÔŚé·ÖÖĐŁŹĂÌ»ùŃő»ŻÎïÓÉÓÚ·áž»¶à±ä”ÄŒÛÌŹșÍÁŒșĂ”ÄŃő»Ż»čÔÄÜÁŠ”Ă”œÁËÉîÈëŃĐŸż[10-12]ŁŹÍ»ùŃő»ŻÎïÔòÒòÆäÓ”ÓĐÊÊÖĐ”ÄŃő»Ż»čÔÄÜÁŠŒ°ĆäλȻ±„șÍ”ÄËáĐÔλ”ăÒȱžÊÜčŰŚąĄŁ»ùÓÚÒÔÉÏŃĐŸżÏÖŚŽŁŹ±ŸÎÄŚśŐßÔÚNiFe-LDHČă°ćÖĐÔλÒęÈëÊÊÁżĐÍŹčŠÄÜŚé·ÖMnșÍCuŁŹŸÍŹŸ§ÈĄŽúÖƱžNi(Mn, Cu)FeÀàËź»ŹÊŻ(Ni(Mn, Cu)Fe-LDHs)Ç°ÇęÌ棏œ«žßÎÂÍŰÆËŚȘ±äŃÜÉúččÖț”ÄNi(Mn, Cu)FežŽșÏŃő»ŻÎï(Ni(Mn, Cu)Fe-LDO)Žß»ŻŒÁÓŠÓĂÓÚNH3-SCR·ŽÓŠŁŹœèÖúһϔÁбíŐśŒŒÊőœÒÊŸMnșÍCuČôÔÓ¶ÔÄűÌú»ùžŽșÏŃő»ŻÎïÀí»ŻĐÔÄÜŒ°ÍŃÏőЧčû”ÄÓ°ÏìŁŹÓĆŃĄ”ÍÎÂSCRŽß»ŻŒÁĄŁ
1 Ê”Ńé
1.1ĄĄČÄÁÏŚŒ±ž
Ê”ŃéËùÓĂÔÁÏŁșNi(NO3)2Ą€6H2O(·ÖÎöŽżŁŹčúÒ©ŒŻÍĆ»ŻŃ§ÊÔŒÁÓĐÏȚč«ËŸ)Ł»Fe(NO3)3Ą€9H2O(·ÖÎöŽżŁŹÌìœòÊĐÌìÁŠ»ŻŃ§ÊÔŒÁÓĐÏȚč«ËŸ)Ł»Mn(NO3)2(ÖÊÁż·ÖÊęÎȘ50%(ÏÂÍŹ)·ÖÎöŽżŁŹÌìœòÊĐÌìÁŠ»ŻŃ§ÊÔŒÁÓĐÏȚč«ËŸ)Ł»Cu(NO3)2Ą€3H2O(·ÖÎöŽżŁŹÌìœòÊĐÌìÁŠ»ŻŃ§ÊÔŒÁÓĐÏȚč«ËŸ)Ł»ÄòËŰ(·ÖÎöŽżŁŹÌìœòÊб±łœ·œŐęÊÔŒÁł§)Ł»ÄûĂÊËáÄÆ(·ÖÎöŽżŁŹÌìœòÊп͚»ŻŃ§ÊÔŒÁÓĐÏȚč«ËŸ)șÍŐôÁóËź(Ì«ÔÀí耎óѧÖĐÊÔ»ù”Ű)ĄŁ
1.2ĄĄŽß»ŻŒÁ”ÄÖƱž
ČÉÓĂÄòËŰËźÈȷ֜ⷚŁŹÖƱžNiFe-LDHșÍNi(Mn, Cu)Fe-LDHsÇ°ÇęÌ楣ÖƱžNiFe-LDHʱŁŹ±ŁłÖn(Ni2+):n(Fe3+)ÎȘ4:1(ÆäÖĐŁŹnÎȘÎïÖÊ”ÄÁż)ŁŹœ«Ni(NO3)2Ą€6H2OșÍFe(NO3)3Ą€9H2OÈÜÓÚÈ„ÀëŚÓËźŁ»ÖƱžNi(Mn, Cu)Fe-LDHʱŁŹ±ŁłÖn(Ni2+):n(M2+):n(Fe3+)ÎȘ3:1:1ŁŹœ«Ni(NO3)2.6H2OŁŹFe(NO3)3.9H2OșÍMn(NO3)2(50%)ÈÜÒș(»òCu(NO3)2.3H2O)ÈÜÓÚÈ„ÀëŚÓËźŁŹłÆÈĄÉÙÁżÂçșÏŒÁÄûĂÊËáÄÆŒÓÈëÉÏÊö»ìșÏÈÜÒșÖĐŁŹ°Žn(NO ):n(ÄòËŰ)ÎȘ9:7ÏòÈÜÒșÖĐŒÓÈëÄòËŰŁŹœ«»ìșÏÈÜÒșÖĂÓÚŽĆÁŠœÁ°èÆśÉÏœÁ°è30 minșóŚȘÒÆÖÁžßŃč·ŽÓŠžȘŁŹÓÚ120 ĄăCËźÈÈ·ŽÓŠ24 hșóŸłéÂËĄąÏŽ”ÓșÍžÉÔï(80 ĄăCŁŹ12 h)ŁŹŒŽ”Ă”œNiFe-LDHșÍNi(Mn, Cu)Fe-LDHsÇ°ÇęÌ楣œ«ŃĐÄ„ÖÁÏž·ÛÄ©”ÄËź»ŹÊŻÇ°ÇęÌć500 ĄăCìŃÉŐ5 hŁŹČúÎïŽß»ŻŒÁ·Ö±đ±êŒÇÎȘNiFe-LDOŁŹNiMnFe-LDOșÍNiCuFe-LDOĄŁ
):n(ÄòËŰ)ÎȘ9:7ÏòÈÜÒșÖĐŒÓÈëÄòËŰŁŹœ«»ìșÏÈÜÒșÖĂÓÚŽĆÁŠœÁ°èÆśÉÏœÁ°è30 minșóŚȘÒÆÖÁžßŃč·ŽÓŠžȘŁŹÓÚ120 ĄăCËźÈÈ·ŽÓŠ24 hșóŸłéÂËĄąÏŽ”ÓșÍžÉÔï(80 ĄăCŁŹ12 h)ŁŹŒŽ”Ă”œNiFe-LDHșÍNi(Mn, Cu)Fe-LDHsÇ°ÇęÌ楣œ«ŃĐÄ„ÖÁÏž·ÛÄ©”ÄËź»ŹÊŻÇ°ÇęÌć500 ĄăCìŃÉŐ5 hŁŹČúÎïŽß»ŻŒÁ·Ö±đ±êŒÇÎȘNiFe-LDOŁŹNiMnFe-LDOșÍNiCuFe-LDOĄŁ
1.3ĄĄŽß»ŻŒÁ±íŐś
1) X-ÉäÏßŃÜÉä(XRD)ĄŁČÉÓĂRigaku D/max-2500XÉäÏß·ÛÄ©ŃÜÉäÒÇ(X-ray diffractionŁŹXRD)±íŐśŃùÆ·”ÄÎïÏàŚéłÉŒ°Ÿ§ĐÍœáč襣ČâÊԔķűÉäÔŽÎȘCu KŠÁÉäÏߣŹč€Śś”çŃčÎȘ40 kVŁŹ”çÁśÎȘ30 mAŁŹÉšĂèËÙ¶ÈÎȘ8(Ąă)/minŁŹÉšĂ跶ΧÎȘ5Ąă~85ĄăĄŁ
2) N2-ÎüžœÍŃžœĄŁČÉÓĂNova1 200(Quanta106 Chrome)ÒÇÆś¶ÔŽß»ŻŒÁŃùÆ·ČâÊÔN2-ÎüžœÍŃžœĐÔÄÜĄŁœ«0.1 gŽß»ŻŒÁÔÚ300 ĄăCŐæżŐÌőŒțÏÂÔ€ŽŠÀí4 hŁŹČąÔÚ-198 ĄăC(Òș”Ș)ÌőŒțÏÂČâÊÔN2-ÎüžœÍŃžœĐÔÄÜŁŹ»ńÈĄ¶ÔÓŠ”ÄÎüžœÍŃžœ”ÈÎÂÏߥŁČÉÓĂBET·šșÍBJH·š»ń”ñ»ČâŃùÆ·”ıȱíĂæ»ęșÍżŚÏ¶œáčč”ÈĐĆÏąĄŁ
3) ž”ÀïÒ¶±ä»»șìÍâčâÆŚ(FT-IR)ĄŁČÉÓĂBruker Vertex 70ž”ÀïÒ¶±ä»»șìÍâčâÆŚÒÇ(Fourier transform infrared spectrometerŁŹFT-IR spectrometer)ČâÊÔŽß»ŻŒÁŁŹÊčÓĂKBr·šÖÆÆŹĄŁłÆÈĄ1 mgŽß»ŻŒÁșÍ100 mg KBrŁŹœ«ÁœŐß»ìșÏłä·ÖŃĐÄ„ŸùÔÈșóŁŹœűĐĐŃčÆŹŽŠÀíĄŁÒÇÆś”Ä·Ö±æÂÊŃĄÔń4 cm-1ŁŹČ⶚ŃùÆ·”ÄșìÍâÍŒÏń(400~4 000 cm-1ČšÊęÄÚ)ĄŁ
4) NH-łÌĐòÉęÎÂÍŃžœ(NH3-TPD)ĄŁÊčÓĂłÌĐòÉęÎÂÍŃžœ»ŻŃ§ÎüžœÒÇFINESORB-3010C(Őăœ·șÌ©ÒÇÆśÓĐÏȚč«ËŸ)ÀŽÈ·¶šŽß»ŻŒÁ”ıíĂæËáĐÔĄŁłÆÈĄ0.08 gŽß»ŻŒÁŚ°ÈëÊŻÓą·ŽÓŠčÜŁŹÎȘÁËĆĆłęËźÒÔŒ°ÆäËûÆűÌć”ÄžÉÈĆŁŹÍšÈ뎿ș€ÆűÔÚ300 ĄăCÏÂÔ€ŽŠÀí1 hŁŹœ”ÎÂÖÁ50 ĄăCÍšÈëNH3Îüžœ30 minŁŹÔÙÓĂș€ÆűŽ”Éšl hÒÔłęÈ„ÆűÌŹșÍÎïÀíÎüžœ”ÄNH3ŁŹÒÔ10 ĄăC/min”ÄÉęÎÂËÙÂÊŽÓ50 ĄăCÉęÎÂÖÁ700 ĄăCŁŹÔÚÉęÎÂčęłÌÖĐŁŹÈÈ”ŒŒìČâÆśŒÇÂŒNH3łÌĐòÉęÎÂÍŃžœĐĆșĆĄŁ
5) H2-łÌĐòÉęλčÔ(H2-TPR)ĄŁÔÚłÌĐòÉęλŻŃ§ÎüžœÒÇ(FINESORB-3010CŁŹŐăœ·șÌ©ÒÇÆśÓĐÏȚč«ËŸ)ÉÏœűĐĐH2-TPRČâÊÔĄŁłÆÈĄ0.08 gŽß»ŻŒÁŚ°ÈëÊŻÓą·ŽÓŠčÜŁŹÍšÈ뎿ëČÆűÔÚ300 ĄăCÏÂÔ€ŽŠÀí1 hŁŹœ”ÎÂÖÁ50 ĄăCÍšÈëëČÆűŽ”Éš1 hŁŹÈ»șóÒÔ10 ĄăC/min”ÄÉęÎÂËÙÂÊŽÓ50 ĄăCÉęÎÂÖÁ700 ĄăCœűĐĐ»čÔÊ”Ń飏ČÉÓĂÈÈ”ŒŒìČâÆś¶ÔÏàčŰĐĆșĆœűĐĐŒìČ⥣
6) XÉäÏßčâ”çŚÓÄÜÆŚČâÊÔ(XPS)ĄŁœèÖúÓąčúKratosč«ËŸÉúČú”ÄAxis Ultra¶àčŠÄܱíĂæÄÜÆŚ·ÖÎöÒÇœűĐĐXÉäÏßčâ”çŚÓÄÜÆŚ(X-ray photoelectron spectroscopy)ČâÊÔŁŹ»ńÈĄŽß»ŻŒÁ±íĂæÔȘËŰșŹÁżșÍŒÛÌŹ·ÖČŒĐĆÏąĄŁČâÊÔÌőŒțÈçÏÂŁș·űŐŐčâÔŽČÉÓĂAl KŠÁŁŹÄÜÁżÎȘ1 486.6 eVŁŹČÙŚśčŠÂÊÎȘ150 WĄŁÍŒÆŚĐŁŐęČÉÓĂCls=284.6ĄŁÊčÓĂ·ÇÏßĐÔShirleyĐͱłŸ°·ÖÎöXPSĐĆșĆĄŁ
2 Ç°ÇęÌć±íŐś
ÍŒ1ËùÊŸÎȘÇ°ÇęÌćČúÎï”ÄXRDČâÊÔĄŁÓÉÍŒ1żÉŒûŁș3ÖÖÇ°ÇęÌćŸùłÊÏÖłöÏàËÆ”ÄŃÜÉä·ćŁŹÔÚ2ŠÈ ÎȘ11.44ĄăŁŹ22.97ĄăŁŹ35.39ĄăŁŹ38.68ĄăŁŹ46.29ĄăŁŹ59.91ĄășÍ62.70ĄăŽŠ·Ö±đłöÏÖÁËÀàËź»ŹÊŻ(003)ŁŹ(006)ŁŹ(012)ŁŹ(015)ŁŹ(018)ŁŹ(110)șÍ(113)Ÿ§Ăæ”ÄŃÜÉä·ćŁŹË”ĂśłÉčŠÖƱžNi(Mn, Cu)Fe-LDHsŁ»ÍŹÊ±ŁŹ°éËæŚĆčę¶ÉœđÊô”ÄČôÔÓŁŹÇ°ÇęÌć”Ĝ៧¶È·ąÉú±ä»ŻŁŹÏà±ÈÓÚNiFe-LDHŁŹMnșÍCuČôÔÓșó”Ă”œNiMnFe-LDHșÍNiCuFe-LDH·ćĐΞüŒâÈńŁŹœáŸ§¶ÈžüžßĄŁ
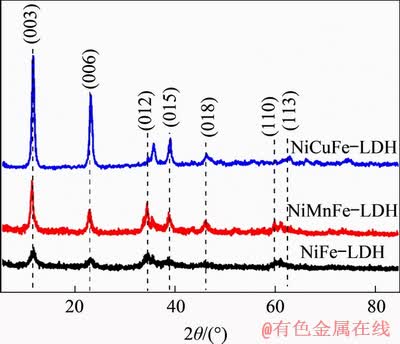
ÍŒ1ĄĄÇ°ÇęÌć”ÄXRDÍŒ
Fig. 1ĄĄXRD patterns of precursors
ÍŒ2ËùÊŸÎȘÖƱžËù”ĂÇ°ÇęÌć”ÄșìÍâÆŚÍŒĄŁÓÉÍŒ2żÉÖȘŁș3ÖÖÇ°ÇęÌćŸùÔÚ3 430ŁŹ1 630ŁŹ1 370șÍ722 cm-1ŽŠŽæÔÚÎüÊշ楣ÆäÖĐλÓÚ3 430 cm-1žœœü”ÄżíÎüÊŐ·ćÓëÇâŒüĄȘOHÒÔŒ°ČăŒäËź·ÖŚÓ”ÄĄȘOHÉìËőŐń¶ŻÓĐčŰŁŹ1 630 cm-1ŚóÓҔČâÈńÎüÊŐ·ćčéÒòÓÚœáŸ§ËźÖĐĄȘOH”ÄÍäÇúŐń¶ŻŁŹ1 370 cm-1ŽŠłöÏ֔Čâ·ćÎȘCO32-”ÄŐń¶ŻÎüÊշ棏¶űÔÚ722 cm-1ŽŠ”ÄÎüÊŐ·ćčéÒòÓÚMĄȘO (MĄȘOHŁŹMĄȘOĄȘM»òOĄȘMĄȘO)”ÄŐń¶Ż[13]ĄŁșìÍâ±íŐśœáčûœűÒ»ČœÖ€Ê”ÁËNiFe-LDHŁŹNiMnFe-LDHșÍNiCuFe-LDHÇ°ÇęÌć”ÄłÉčŠÖƱžĄŁ
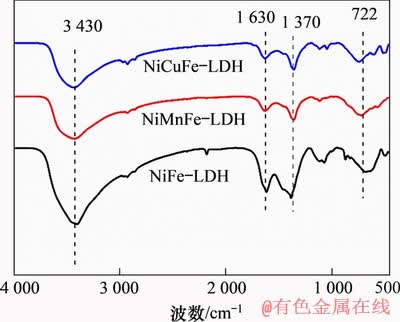
ÍŒ2ĄĄÇ°ÇęÌć”ÄșìÍâÆŚÍŒ
Fig. 2ĄĄFT-IR spectra of precursors
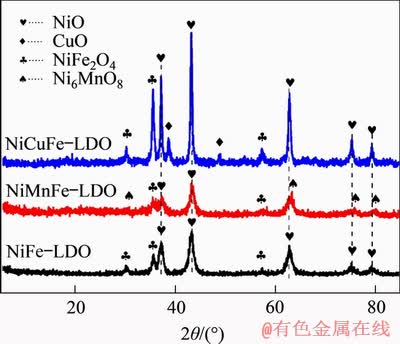
ÍŒ3ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄXRDÍŒ
Fig. 3ĄĄXRD patterns of Ni(Mn, Cu)Fe-LDO catalysts
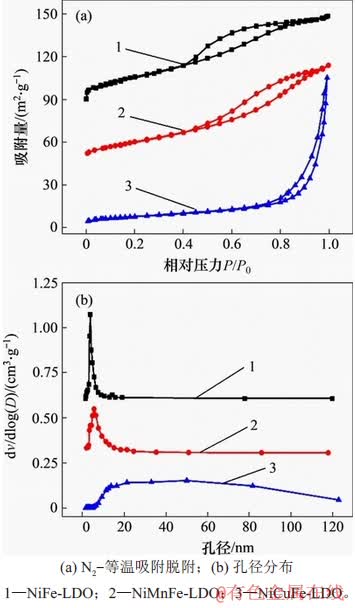
ÍŒ4ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄN2-ÎüžœÍŃžœ”ÈÎÂÏßșÍżŚŸ¶·ÖČŒÍŒ
Fig. 4ĄĄN2-adsorption desorption isotherms and pore size distribution of Ni(Mn, Cu)Fe-LDO catalysts
3 Ni(Mn, Cu)Fe-LDOŽß»ŻŒÁ±íŐś
3.1ĄĄXRDÍŒ·ÖÎö
ÍŒ3ËùÊŸÎȘœđÊôMnșÍCuČôÔÓÖƱž”ÄNi(Mn, Cu)Fe-LDHsÇ°ÇęÌćÔÚ500 Ąæ±șÉŐșó”Ă”œ”ÄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄXRDÍŒĄŁÓÉÍŒ3żÉŒûŁș3ÖÖŽß»ŻŒÁłÊÏÖÁËȻ͏”ÄÎïÏàŚéłÉŁ»NiFe-LDOŽß»ŻŒÁ”ÄÎïÏàŚéłÉÎȘNiOșÍNiFe2O4ŒâŸ§ÊŻŁ»ÔÚNiMnFe-LDOŽß»ŻŒÁÖĐŁŹMnČôÔÓŒőÉÙÁËNiFe2O4ŒâŸ§ÊŻÏàŁŹÆäÎïÏàŚéłÉÖśÒȘÎȘNiOșÍNi6MnO8Ł»¶űÔÚNiCuFe-LDOŽß»ŻŒÁÖĐŁŹČ»œöŽæÔÚNiOșÍNiFe2O4ŒâŸ§ÊŻÏàŁŹ¶űÇÒłöÏÖÁËĐ”ÄCuOÎïÏàĄŁ
±í1ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ıȱíĂæ»ęÓ뿌œáččČÎÊę
Table 1ĄĄSpecific surface area and pore structure parameters of Ni(Mn, Cu)Fe-LDO catalysts

3.2ĄĄN2-ÎüžœÍŃžœ·ÖÎö
ÍŒ4ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄN2-ÎüžœÍŃžœ”ÈÎÂÏßșÍżŚŸ¶·ÖČŒŁŹ±í1ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ıȱíĂæ»ęșÍżŚœáččČÎÊꥣÓÉÍŒ4(a)żÉÖȘŁșNiFe-LDOșÍNiMnFe-LDOŽß»ŻŒÁ”ÄÎüžœÍŃžœ”ÈÎÂÏßÎȘIVĐÍŁŹÖÍșó»·ÎȘH2ĐÍŁŹœáșÏÍŒ4(b)Œ°±í1żÉÖȘŐâ2ÖÖŽß»ŻŒÁŸùÎȘœéżŚČÄÁÏŁŹÇÒÆ俌Ÿ¶·ÖČŒœÏÎȘŸùÔÈŁ»¶űNiCuFe-LDOŽß»ŻŒÁ”ÄÎüžœÍŃžœ”ÈÎÂÏßÎȘIVĐÍŁŹÖÍșó»·ÎȘH3ĐÍŁŹžùŸĘÍŒ4(b)șͱí1ÍÆČâžĂŽß»ŻŒÁÓŠžĂŒÈÓĐœéżŚÒČÓЎ󿌥Ł
Óɱí1żÉÖȘŁșÏà±ÈÓÚNiFe-LDO”ıȱíĂæ»ęŁŹNi(Mn, Cu)Fe-LDO”ıȱíĂæ»ęŸùÓĐÒ»¶šłÌ¶ÈŒőĐĄŁŹÆäÖĐŁŹNiCuFe-LDOŽß»ŻŒÁ”ıȱíĂæ»ęžüĐĄŁ»Ïà±ÈÓÚNiCuFe-LDOŽß»ŻŒÁŁŹNiFe-LDOșÍNiMnFe-LDOŽß»ŻŒÁŸßÓĐœÏŽó”ıȱíĂæ»ęŁŹżÉÌáč©žü¶à”ÄÎüžœÎ»”㣏ŽÙœűŽß»Ż·ŽÓŠĄŁ
3.3ĄĄNH3-TPDșÍNO+O2-TPDÍŒ·ÖÎö
ÍŒ5(a)ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄNH3-TPDÍŒŁŹ±í2ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ¶ÔÓŠËáĐÔλ”ă±ÈÀę(œèÖúOriginÄâșÏ·ćĂæ»ęŒÆËăËáĐÔλ”ăÊęÁżČąÓĂčéÒ»»Ż·šŒÆËă)ĄŁÓÉÍŒ5(a)żÉŒûŁșÏà±ÈÓÚNiCuFe-LDOŽß»ŻŒÁŁŹNiFe-LDOșÍNiMnFe-LDOŽß»ŻŒÁ”ÄNH3ÍŃžœ·ćžüĂśÏÔĄŁÔÚ”ÍζÎ(100~300 Ąæ)”ÄÍŃžœ·ćÎȘÎüžœÔÚLewisËáĐÔλÉÏNH3”ÄÍŃžœÒÔŒ°ÎüžœÔÚBronstedËáĐÔλÉÏ”ÄNH4+”ÄÍŃžœ[14]ŁŹÔÚžßζÎ(300~600 Ąæ)”ÄÍŃžœ·ćÎȘÇżLewisșÍBronstedËáλÉϔĻŻŃ§Îüžœ°±[15]ĄŁ¶ÔÓÚNiFe-LDOșÍNiMnFe-LDOŽß»ŻŒÁŁŹ”ÍζΔÚ1žöÍŃžœ·ćλÖĂÏàČîČ»ŽóĄŁ¶űÔÚžßÎ¶ΣŹNiFe-LDOŽß»ŻŒÁÍŃžœ·ć”ÄλÖĂÎȘ471 ĄæŁŹNiMnFe-LDOŽß»ŻŒÁÍŃžœ·ć”ÄλÖĂÎȘ446 ĄæĄŁœáșϱí2żÉÖȘŁŹ3ÖÖŽß»ŻŒÁ”ıíĂæËáÁżÓÉžß”œ”ÍÒÀŽÎÎȘNiFe-LDOŁŹNiMnFe-LDOșÍNiCuFe-LDOŁŹËæŚĆMnșÍCuČôÔÓœűÈëNiFe-LDOŁŹÆäÈőËáÁżÓëÇżËáÁżŸùÓĐȻ͏łÌ¶È±ä»ŻĄŁÆäÖĐŁŹNiMnFe-LDOŽß»ŻŒÁ”ÄÈőËáλ±ÈÀęĂśÏÔÔöŽóŁŹŐâԀʟŚĆNiMnFe-LDOŽß»ŻŒÁżÉÄÜÓĐžüŒÓÓĆÒì”Ä”ÍλîĐÔĄŁ
ÍŒ5(b)ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄNO+O2-TPDÍŒŁŹ·ŽÓłÁËŽß»ŻŒÁ¶ÔNOx”ÄÎüžœÄÜÁŠĄŁ250ĄăC ÒÔÏ”ÄÍŃžœ·ć¶ÔÓŠÓÚÎüžœÔÚŽß»ŻŒÁ±íĂæ”Ä”„łĘÏőËáŃΔÄÍŃžœŁŹ¶ű250 ĄăCÒÔÉÏ”ÄÍŃžœ·ćÔò¶ÔÓŠÓÚÇĆÊœÏőËáŃÎŒ°Ë«łĘÏőËáŃÎ”Ä·ÖœâĄŁ”„łĘÏőËáŃΔÄČúÉú¶ÔSCRĐÔÄÜÓĐÀûŁŹ¶űÇÒÎüžœÁżÔœŽóŁŹÔœÓĐÀûÓÚ·ŽÓŠÎïČÎÓë·ŽÓŠ[16]ĄŁ
œáșÏNH3-TPD”ÄœáčûłőČœÍƶÏÀàËź»ŹÊŻŃÜÉúŽß»ŻŒÁ”ÄÍŃÏő»úÀíÈçÏÂŁș”ÍÎÂÏÂ(<350 ĄăC)ŁŹ3ÖÖŽß»ŻŒÁŒÈÄÜč»ÎüžœNH3ÒČÄÜč»ÎüžœNOxŁŹ2ÖÖ·ŽÓŠÎïčČÍŹÎüžœÔÚŽß»ŻŒÁ±íĂæ”Ä»îĐÔλ”ăÉÏČąŚȘ»ŻÎȘ»îĐÔÖĐŒäÌ棏ËæșóÏàÁÚœü”ÄÖĐŒäÌć·ąÉú·ŽÓŠŁŹÉúłÉN2șÍH2OŁŹÊôÓÚË«·ÖŚÓ·ŽÓŠ»úÀíŁŹŒŽL-H»úÀíĄŁžßÎÂÏÂ(>350 ĄăC)ŁŹNiFe-LDOŽß»ŻŒÁŒÈÄÜč»ÎüžœNH3ÒČÄÜč»ÎüžœNOxŁŹÊôÓÚË«·ÖŚÓ·ŽÓŠ»úÀíŁŹŒŽL-H»úÀíĄŁ¶űNiMnFe-LDOșÍNiCuFe-LDOŽß»ŻŒÁÖ»ÄÜÎüžœNH3ŁŹÊôÓÚ”„·ÖŚÓ·ŽÓŠ»úÀíŁŹŒŽE-R»úÀíĄŁ
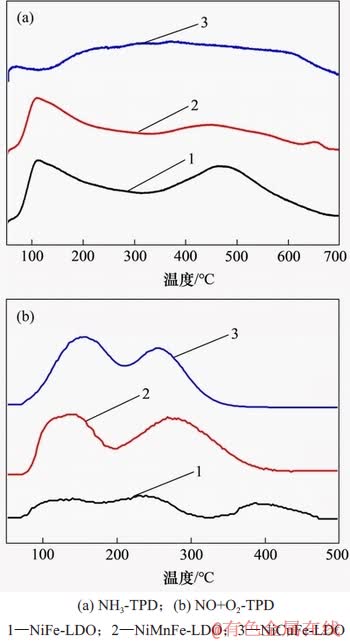
ÍŒ5ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄTPDÍŒ
Fig. 5ĄĄTPD profiles of Ni(Mn, Cu)Fe-LDO catalysts
±í2ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄNH3ÍŃžœÁżșÍËáĐÔλ±ÈÀę
Table 2ĄĄAmount of NH3 desorption and proportion of acid sites of the Ni(Mn, Cu)Fe-LDO catalysts

3.4ĄĄH2-TPRÍŒ·ÖÎö
ÍŒ6ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄH2-TPRÍŒĄŁÓÉÍŒ6żÉÖȘŁș¶ÔÓÚNiFe-LDOŽß»ŻŒÁŁŹÇúÏßłÊÏÖłö2žö»čԷ棏ÆäÖĐŁŹÎ»ÓÚ355 ĄæŚóÓҔĻčÔ·ćÎȘFe3+ĄúFe2+»òNi3+ĄúNi2+ŁŹ¶űλÓÚ436 Ąæžœœü”Ä»čÔ·ćÎȘNi2+ĄúNi0 [17-18]ĄŁčę¶ÉœđÊôMnșÍCuČôÔÓșóŁŹ»čÔ·ć”ÄžöÊęÔöŒÓĄŁNiMnFe-LDOŽß»ŻŒÁłÊÏÖłö3žö»čԷ棏»čÔ·ć”Äłö·ćλÖĂ·Ö±đÎȘ229ŁŹ387șÍ487 ĄæŚóÓÒŁŹÒÀŽÎżÉÒÔčéÊôÓÚMn4+ĄúMn3+ŁŹMn3+ĄúMn2+»òFe3+ĄúFe2+»òNi3+ĄúNi2+șÍNi2+ĄúNi0”Ä»čÔčęłÌ[6,19-20]ĄŁ¶űNiCuFe-LDOÇúÏßÖĐłöÏÖÁË4žö»čԷ棏·Ö±đλÓÚ300ŁŹ373ŁŹ466șÍ625 ĄæžœœüĄŁ»čÔ·ć”ÄłöÏÖÓëCu2+/Cu+ĄúCu0ŁŹFe3+ĄúFe2+»òNi3+ĄúNi2+ÒÔŒ°Ni2+ĄúNi0čęłÌÓĐčŰĄŁÖ””ĂŚąÒâ”ÄÊÇŁŹNiMnFe-LDOŽß»ŻŒÁ”ÄłőÊŒ»čÔ·ćζÈĂśÏÔ”ÍÓÚNiFe-LDOșÍNiCuFe-LDOŽß»ŻŒÁŁŹœÏ”͔ĻčÔζÈ˔ÜNiMnFe-LDOŽß»ŻŒÁ±íĂæÎïÖÖžüÒŚ±»»čÔŁŹŸßÓĐžüŒÓÓĆÒì”ÄŃő»Ż»čÔĐÔÄÜĄŁ
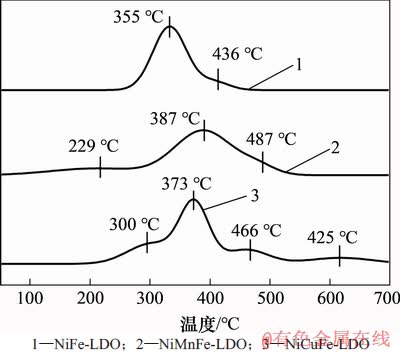
ÍŒ6ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄH2-TPRÍŒ
Fig. 6ĄĄH2-TPR profiles of the Ni(Mn, Cu)Fe-LDO catalysts
3.5ĄĄXPSÍŒ·ÖÎö
ÍŒ7ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄXPSÍŒĄŁÀûÓĂXPS Peak 4.1ÈíŒț¶ÔÆäÄÜÆŚÍŒœűĐĐ·Ö·ćÄâșÏŁŹÍŹÊ±žùŸĘÆä·ćĂæ»ęŒÆËăłöÆä±íĂæÀëŚÓÏà¶ÔșŹÁżŁŹËù”ĂŽß»ŻŒÁ±íĂæ»ŻŃ§ŒÛÌŹ·ÖČŒÈç±í3ËùÊŸĄŁÓÉÍŒ7(a)żÉŒûŁșNi 2p3/2ÆŚÍŒżÉčÛČ씜3žöÌŰŐś·ćŁŹ·Ö±đλÓÚ854.6ŁŹ856.0~856.2șÍ860.4~861.3 eVŁŹÒÀŽÎżÉčéÊôÓÚNi2+ŁŹNi3+ÌŰŐś·ćșÍÎÀĐÇ·ć[21]ĄŁČÉÓĂÍŹŃù”Ä·œ·š¶ÔFe 2p3/2ŁŹMn 2p3/2șÍCu 2p3/2œűĐĐ·Ö·ćÄâșÏŁŹœáčûÈçÍŒ7(b)~(d)ËùÊŸĄŁșÜĂśÏÔŁŹNiCuFe-LDOŽß»ŻŒÁ±íĂæCu2+șŹÁżÔ¶žßÓÚCu+șŹÁżŁŹNiFe-LDOșÍNiCuFe-LDOŽß»ŻŒÁ±íĂ涌șŹÓĐžü¶àNi3+ŁŹ¶űNiMnFe-LDOŽß»ŻŒÁÖĐNi3+șŹÁżÏà¶ÔœÏ”ÍŁŹ”«Æä±íĂæMn4+șŹÁżžßŽï48.7%ŁŹÍÆČâżÉÄÜÓëžĂŽß»ŻŒÁ±íĂæ·ąÉúMn3++Ni3+ Mn4++Ni2+·ŽÓŠÓĐčŰŁŹNiMnFe-LDOŽß»ŻŒÁ±íĂæŽóÁżžßŃő»ŻÌŹĂÌ(Mn4+)»á”ŒÖÂÆäŸßÓĐžüșĂ”ÄŃő»Ż»čÔĐÔÄÜ[22-23]ĄŁ
Mn4++Ni2+·ŽÓŠÓĐčŰŁŹNiMnFe-LDOŽß»ŻŒÁ±íĂæŽóÁżžßŃő»ŻÌŹĂÌ(Mn4+)»á”ŒÖÂÆäŸßÓĐžüșĂ”ÄŃő»Ż»čÔĐÔÄÜ[22-23]ĄŁ
Óɱí3żÉŒûŁșÏàœÏÓÚNiFe-LDOŽß»ŻŒÁŁŹŸMnșÍCuČôÔÓșóŃÜÉúËù”ĂŽß»ŻŒÁ±íĂæFe3+șŹÁżŸùłÊÏÖÉęžß”ÄÇśÊÆŁŹNiCuFe-LDOŽß»ŻŒÁÖĐșŹÓĐNiFe2O4ŒâŸ§ÊŻÏàŁŹCuČôÔÓșóÆä±íĂæNi3+șŹÁżŒőÉÙ¶űFe3+șŹÁżÉęžßżÉÄÜÓëNiFe2O4ŒâŸ§ÊŻÉÏŽæÔÚNișÍFeÔȘËŰŒä”ÄŃő»Ż»čÔ·ŽÓŠ(Ni3++Fe2+ Ni2++Fe3+)ÓĐčŰŁ»ÍščęÏàÓŠÌŰŐś·ćĂæ»ę±ÈÖ”ŒÆËă”ÄŽß»ŻŒÁ±íĂæOŠÁÓë(OŠÁ+OŠÂ)șŹÁżÖź±È˔ÜŁŹœđÊôČôÔÓșÏłÉ”ÄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁÏàœÏÓÚNiFe-LDOÆäOŠÁ(±íĂæŃő)șŹÁżĂśÏÔœ””ÍŁŹŐâżÉÄÜÊÇÓÉÓÚNiFe2O4ŒâŸ§ÊŻÖĐŃőÔŚÓĆĆÁĐ·œÊœÎȘÁą·œœôĂܶѻ꣏œđÊôÀëŚÓλÓÚČż·ÖËÄĂæÌćșÍ°ËĂæÌćżŐ϶ÖĐŁŹÒòŽËŁŹŽæÔÚžĂŃő»ŻÎïœÏ¶à”ıíĂæŃőżŐλÒÔŒ°œđÊôÀëŚÓœ»»»”ÄżÉÄÜĐÔ[24]ĄŁœáșÏXRD±íŐśŁŹMnșÍCuÀëŚÓ”ÄČôÔÓÒęÆđNi»ùŒâŸ§ÊŻÏàŒ°œáŸ§¶È·ąÉúÁ˱仯ŁŹŐâżÉÄÜ”ŒÖÂČż·Ö±íĂæÎüžœŃőÏòŸ§žńŃőŚȘÒƶűÒęÆđ±íĂæŃőșŹÁżœ””Í[25-26]ĄŁ
Ni2++Fe3+)ÓĐčŰŁ»ÍščęÏàÓŠÌŰŐś·ćĂæ»ę±ÈÖ”ŒÆËă”ÄŽß»ŻŒÁ±íĂæOŠÁÓë(OŠÁ+OŠÂ)șŹÁżÖź±È˔ÜŁŹœđÊôČôÔÓșÏłÉ”ÄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁÏàœÏÓÚNiFe-LDOÆäOŠÁ(±íĂæŃő)șŹÁżĂśÏÔœ””ÍŁŹŐâżÉÄÜÊÇÓÉÓÚNiFe2O4ŒâŸ§ÊŻÖĐŃőÔŚÓĆĆÁĐ·œÊœÎȘÁą·œœôĂܶѻ꣏œđÊôÀëŚÓλÓÚČż·ÖËÄĂæÌćșÍ°ËĂæÌćżŐ϶ÖĐŁŹÒòŽËŁŹŽæÔÚžĂŃő»ŻÎïœÏ¶à”ıíĂæŃőżŐλÒÔŒ°œđÊôÀëŚÓœ»»»”ÄżÉÄÜĐÔ[24]ĄŁœáșÏXRD±íŐśŁŹMnșÍCuÀëŚÓ”ÄČôÔÓÒęÆđNi»ùŒâŸ§ÊŻÏàŒ°œáŸ§¶È·ąÉúÁ˱仯ŁŹŐâżÉÄÜ”ŒÖÂČż·Ö±íĂæÎüžœŃőÏòŸ§žńŃőŚȘÒƶűÒęÆđ±íĂæŃőșŹÁżœ””Í[25-26]ĄŁ
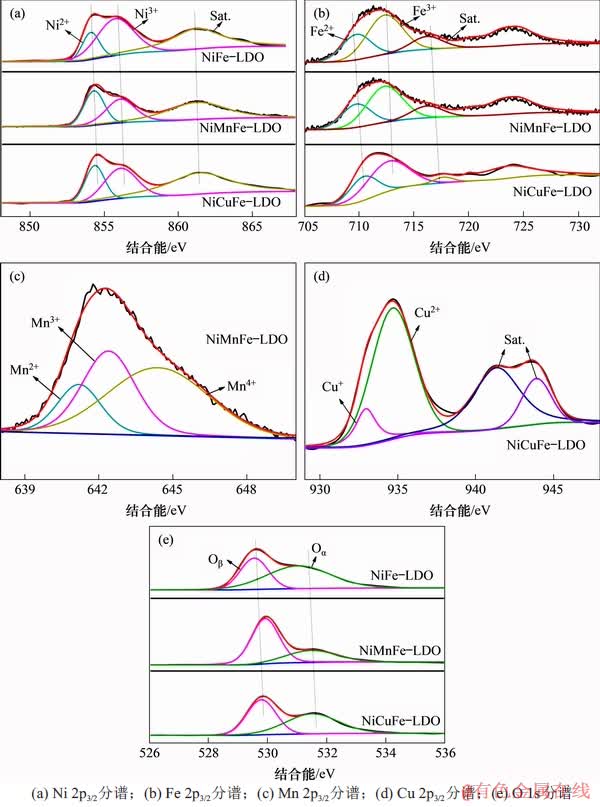
ÍŒ7ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄXPSÍŒ
Fig. 7ĄĄXPS spectra of the Ni(Mn, Cu)Fe-LDO catalysts
4 ÌÖÂÛ
4.1ĄĄŽß»ŻŒÁNH3-SCRŽß»ŻĐÔÄÜ
ËùÓĐŽß»ŻŒÁ”Ä»îĐÔČâÊÔŸùÔÚč̶šŽČÆűÌŹ·ŽÓŠŚ°ÖĂÉÏœűĐĐŁŹ·ŽÓŠ»ìșÏÆűŚéłÉÎȘÌć»ę·ÖÊęŠŐ(NO)=ŠŐ(NH3)=0.06%(ŠŐÎȘÌć»ę·ÖÊę)ŠŐ(O2)=5%(ŠŐ(H2O)=10%ŁŹŠŐ(SO2)=0.01%żčH2O/SO2ČâÊÔ)ŁŹN2ÎȘÆœșâÆűŁŹÊŻÓą·ŽÓŠčÜ”ÄÖ±Ÿ¶ÎȘ6 mmŁŹŽß»ŻŒÁÓĂÁżÎȘ0.35 g (250~380 ŠÌm)ŁŹÆűÌćżŐËÙ(gas hourly space velocityŁŹGHSV)ÎȘ45 000~75 000 h-1ŁŹłÌĐòÉęÎÂËÙÂÊÉèÖĂÎȘ3ĄăC/minŁŹČâÊÔζÈÎȘ120~420ĄăCĄŁĂżžô30ĄăCŒÇÂŒ1ŚéÊęŸĘŁŹŽęÆűÌćĆš¶ÈÎȶšșóŁŹÓÉșìÍâŃÌÆűŒìČâÒÇ(Thermofisher IS10)·ÖÎöč̶šŽČ·ŽÓŠÆśœűłöżÚÆűÌćŚé·ÖŒ°Ćš¶ÈĄŁ±ŸÎÄÖĐNO”ÄŚȘ»ŻÂÊŠÇ(NO)șÍN2ŃĄÔńĐÔŠÇ(N2)°ŽÏÂÊœŒÆËăŁș
 (1)
(1)

±í3ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ±íĂæÔȘËŰŒÛÌŹ·ÖČŒ
Table 3ĄĄValence distribution of elements on the surface of Ni(Mn, Cu)Fe-LDO catalysts %

 (2)
(2)
ÊœÖĐŁșcin(NO)șÍcin(NH3)·Ö±đÎȘ·ŽÓŠÆśÈëżÚŽŠ”ÄNOșÍNH3Ćš¶ÈŁ»cout(NO)ŁŹcout(NO2)șÍcout(N2O)·Ö±đÎȘ·ŽÓŠÆśłöżÚŽŠNOŁŹNO2șÍN2O”ÄĆš¶ÈĄŁ
ÍŒ8ËùÊŸÎȘœđÊôČôÔÓÖƱž”ÄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄŽß»ŻĐÔÄÜČâÊÔÍŒĄŁÓÉÍŒ8(a)żÉŒûŁșčę¶ÉœđÊôMnșÍCuČôÔÓNiFe-LDHŃÜÉúÖÆ”Ă”ÄNiMnFe-LDOșÍNiCuFe-LDOŽß»ŻŒÁ”Ä”ÍÎÂÍŃÏő»îĐÔÏàœÏÓÚNiFe-LDOŽß»ŻŒÁŸùÓĐÒ»¶š·ù¶ÈÌáÉ꣏¶űÇÒ»îĐÔζȎ°żÚŸù”Ă”œÍŰżíŁŹMnČôÔÓ¶ÔNiFe-LDOŽß»ŻŒÁ”Ä”ÍλîĐÔÌáÉę·ù¶ÈĂśÏÔ±ÈCuČôÔӔĞߥŁNiMnFe-LDOŽß»ŻŒÁÓ”ÓĐžüżí”Ä»îĐÔζȎ°żÚ(150~360 Ąæ)ŁŹÆäÔÚ·ŽÓŠÎ¶ÈÎȘ150 ĄæʱŁŹNOŚȘ»ŻÂÊÒŃŽï90%ŁŹ”±·ŽÓŠÎ¶ÈÎȘ180ĄæʱŁŹžĂŽß»ŻŒÁNOŚȘ»ŻÂʜӜü99%ĄŁNiMnFe-LDOŽß»ŻŒÁÓĆÒì”Ä”ÍÎÂÍŃÏőĐÔÄÜÓëNiMnFe-LDOŽß»ŻŒÁ±íĂæÎïÖÖžüÒŚ±»»čÔŁŹNi3+șÍMn3+Œä”Ä”çŚÓŚȘÒÆŒÓËÙÁËŃő»Ż»čÔŃ»·ÓĐčŰŁŹŽËÍ⣏NiMnFe-LDOŽß»ŻŒÁžüżí”ÄζȎ°żÚ(150~360 Ąæ)»čÓëŽß»ŻŒÁÖĐËáĐÔλ±ÈÀęœÏÎȘșÏÀíÇÒÈőËáλ±ÈÀęœÏŽóœôĂÜÏàčŰĄŁ
ÓÉÍŒ8(b)żÉŒûŁșÔÚ120~270 ĄæŁŹžśŽß»ŻŒÁ”ÄN2ŃĄÔńĐÔČî±đČ»ŽóŁ»”±·ŽÓŠÎÂ¶ÈłŹčę300 ĄæʱŁŹNiFe-LDOșÍNiMnFe-LDOŽß»ŻŒÁÈÔÈ»±ŁłÖœÏžß”ÄN2ŃĄÔńĐÔŁŹ¶űNiCuFe-LDOŽß»ŻŒÁ”ÄN2ŃĄÔńĐÔłöÏÖÇáÎąÏÂœ”ĄŁŐâÊÇÓÉÓÚNi3+șÍMn3+ÖźŒäŽæÔÚ”çŚÓŚȘÒÆŁŹÔÚÒ»¶šłÌ¶ÈÉÏ”śœÚÁËMnŃő»ŻÎïčęÇż”ÄŃő»ŻÄÜÁŠŁŹÒòŽËŁŹNiMnFe-LDOŽß»ŻŒÁ”ÄN2ŃĄÔńĐÔÒȘ±ÈNiCuFe-LDOŽß»ŻŒÁ”ÄÂԞߥŁ
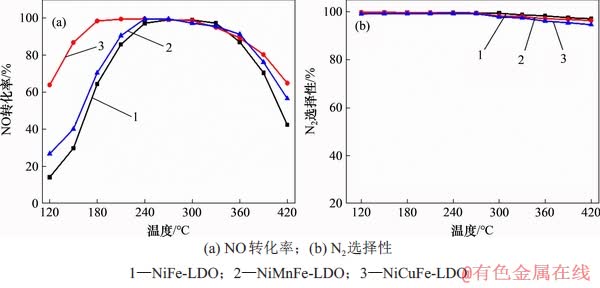
ÍŒ8ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ÄŽß»ŻĐÔÄÜ
Fig. 8ĄĄCatalytic performance of Ni(Mn, Cu)Fe-LDO catalysts
4.2ĄĄŽß»ŻŒÁ¶ŻÁŠŃ§ÆÀŒÛ
žùŸĘSCR·ŽÓŠÖĐNOxŚȘ»ŻÂÊÎȘ5%~20%ÖźŒäÊęŸĘČ⶚Žß»ŻŒÁ±íčÛ»î»ŻÄÜ(Ea)ŁŹŒÆËăËÙÂÊłŁÊęșͱíĂæ»î»ŻÄÜč«ÊœÈçÏÂŁș
 (3)
(3)
 (4)
(4)
ÊœÖĐŁșkÎȘ·ŽÓŠËÙÂÊłŁÊ꣏cm3/(gĄ€s)Ł»VÎȘÌć»ęÁśÁżŁŹcm3/sŁ»WÎȘŽß»ŻŒÁÖÊÁżŁŹgŁ»EaÎȘ±íčÛ»î»ŻÄÜŁŹkJ/molŁ»RÎȘÄŠ¶ûÆűÌ泣Ê꣏J/(molĄ€K)Ł»TÎȘÈÈÁŠŃ§ÎÂ¶ÈŁŹKŁ»AÎȘ֞ǰÒòŚÓŁŹcm3/(gĄ€s)ĄŁNH3-SCR·ŽÓŠÖĐNO”Ä·ŽÓŠŒ¶ÊęÎȘ1ŁŹNH3”Ä·ŽÓŠŒ¶ÊęÎȘ0ĄŁ
ŸĘ°ąÂŰÄáÎÚËčč«ÊœżÉÖȘŁșÈçÒÔlnk¶Ô1/TŚśÍŒŁŹÖ±Ïß”ÄбÂÊÎȘ-Ea/RŁŹŐâŃùÍščęŚśÍŒÇóœâȻ͏Žß»ŻŒÁÔÚSCR·ŽÓŠÖДıíčÛ»î»ŻÄÜ(Ea)ĄŁÍŒ9ËùÊŸÎȘNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ·ŽÓŠ»î»ŻÄÜÇóœâÍŒĄŁÓÉÍŒ9żÉŒûŁșÔÚČâÊÔ”Äζȷ¶Î§ÄÚ(120~240 Ąæ)ŁŹNiMnFe-LDO(53.85 kJ/mol)±íčÛ»î»ŻÄÜ(Ea)ŚîĐĄŁŹÆäŽÎÊÇNiCuFe-LDO(77.77 kJ/mol)șÍNiFe-LDO(89.96 kJ/mol)ŁŹŐâÓë3ÖÖŽß»ŻŒÁ”Ä”ÍÎÂÍŃÏőĐÔÄÜÏàÒ»ÖÂĄŁ
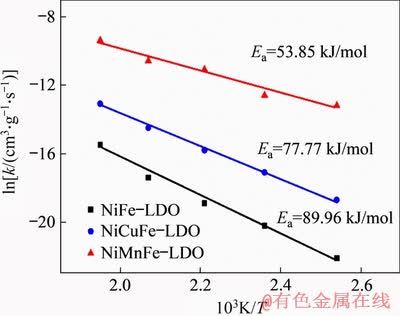
ÍŒ9ĄĄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ·ŽÓŠ»î»ŻÄÜÇóœâÍŒ
Fig. 9ĄĄCalculation chart of reaction activation energy of the Ni(Mn, Cu)Fe-LDO catalysts
4.3ĄĄÓĆŃĄŽß»ŻŒÁ”ÄĐÔÄÜ
4.3.1ĄĄČ»ÍŹżŐËÙÏ”Ď߻ŻĐÔÄÜĄĄ
ÍŒ10ËùÊŸÎȘÓĆŃĄłö”ÄNiMnFe-LDOŽß»ŻŒÁÔÚȻ͏żŐËÙÌőŒțÏÂËù¶ÔÓŠ”ÄNH3-SCR»îĐÔĄŁÓÉÍŒ10żÉŒûŁșËæŚĆżŐËÙÔöŒÓŁŹNiMnFe-LDOŽß»ŻŒÁ”ÄÍŃÏő»îĐÔÂÔÓĐœ””ÍŁŹ”«ŚÜÌćÇśÊÆ±ä»ŻČ»ŽóŁŹžĂŽß»ŻŒÁÔÚœÏžßżŐËÙÏÂÒÀÈ»±ŁłÖŚĆ±ÈœÏžß”ÄNOŚȘ»ŻÂÊșÍN2ŃĄÔńĐÔĄŁÔÚÊ”Ń鷶ΧÄÚŁŹżŐËÙ±ä»Ż¶ÔNiMnFe-LDOŽß»ŻŒÁ”ÄÍŃÏőĐÔÄÜÓ°ÏìČ»ŽóŁŹžĂŽß»ŻŒÁ±íÏÖłöœÏșÔĿŐËÙÊÊÓŠĐÔĄŁ
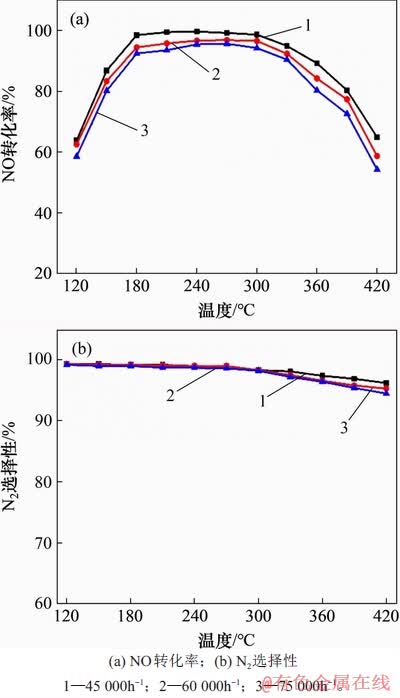
ÍŒ10ĄĄČ»ÍŹżŐËÙÏÂNiMnFe-LDOŽß»ŻŒÁ”ÄŽß»ŻĐÔÄÜ
Fig. 10ĄĄCatalytic performance of NiMnFe-LDO catalyst at different GHSV
4.3.2ĄĄÓĆŃĄŽß»ŻŒÁ”ÄżčËźżčÁòĐÔÄÜĄĄ
ÔÚÊ”ŒÊÉúČúÊ”ŒùÖĐŁŹŃÌÆűÖĐżÉÄÜ»áŽæÔÚÒ»¶šÌć»ę·ÖÊę”ÄSO2ŁŹÒòŽËŁŹ¶ÔÓĆŃĄłö”ÄNiMnFe-LDOŽß»ŻŒÁœűĐĐżčËźżčÁòĐÔÄÜČâÊÔÏÔ”ĂÓÈÎȘÖŰÒȘĄŁÍŒ11ËùÊŸÎȘÓĆŃĄŽß»ŻŒÁNiMnFe-LDOÔÚ210 ĄæŁŹ45 000 h-1żŐËÙÏÂœűĐĐ50 hżčH2O/SO2ČâÊԔĜáčûĄŁÊŚÏÈŁŹ”±ÍšÈëÌć»ę·ÖÊęÎȘ0.01%”ÄSO2șóŁŹČâÊÔÔÚ10 hÄÚNOŚȘ»ŻÂÊ±ä»ŻÇśÊÆŁŹ·ąÏÖŽß»ŻŒÁ”ÄÍŃÏő»îĐÔÈÔÈ»±ŁłÖÔڜϞßËźÆœŁ»È»șóŁŹ”±ÍšÈëÌć»ę·ÖÊęÎȘ10%”ÄH2OșóŁŹNOŚȘ»ŻÂÊłÊÏÖłöĂśÏÔÏÂœ”ÇśÊÆ(ŽÓ97%ÏÂœ””œ93%)Ł»œ«SO2ÆűÌćÇжÏșóŁŹNOŚȘ»ŻÂÊÂÔÓĐÌážßŁŹ”«ÈÔŽïČ»”œłőÊŒŚŽÌŹÊ±”ÄÖ”Ł»ŚîșóŁŹœ«ÍšÈë”ÄÌć»ę·ÖÊęÎȘ10% H2OÇĐ¶ÏŁŹŽß»Ż»îĐÔÏÔÖűÌáÉ꣏ŽóÖ¿ɻ֞Ž”œłőÊŒNOŚȘ»ŻÂÊĄŁÓÉŽËżÉŒûŁșNiMnFe-LDOŽß»ŻŒÁÔÚžĂÊ”ŃéÌőŒțϱíÏÖłöÁŒșÔĿčH2O/SO2ĐÔÄÜĄŁ

ÍŒ11ĄĄNiMnFe-LDOŽß»ŻŒÁ”ÄżčËźżčÁòĐÔÄÜČâÊÔ
Fig. 11ĄĄH2O and SO2 resistance test of NiMnFe-LDO catalyst
5 œáÂÛ
1) ÔÚNiFe-LDHČă°ćÉÏÔλÒęÈëĐÍŹčŠÄÜŚé·ÖMnșÍCușóŁŹŃÜÉúččÖț”ÄNi(Mn, Cu)Fe-LDOŽß»ŻŒÁ”ıȱíĂæ»ęĄąÎïÏàŚéłÉŒ°±íĂæŚé·ÖșŹÁż”È·ąÉúÁËÒ»¶šžÄ±äŁŹÆäŃő»Ż»čÔĐÔșÍËáŒîĐԔÔœÓĆ»ŻĄŁ
2) NiMnFe-LDOŽß»ŻŒÁŸßÓĐžüÓĆÒì”Ä”ÍÎÂÍŃÏőĐÔÄÜŁŹ150 ĄæʱNOŚȘ»ŻÂÊżÉŽï90%ŁŹ180 ĄæʱNOŚȘ»ŻÂʜӜü99%Ł»ÔÚ150~360 Ąæ»îĐÔÎÂŽ°·¶Î§ÄÚŁŹŽß»ŻŒÁ”ÄN2ŃĄÔńĐÔŸùżÉÒÔÎȶšÔÚ96%ÒÔÉÏĄŁÆäÓĆÒì”Ä”ÍÎÂÍŃÏő»îĐÔÓëNi3+șÍMn3+Œä”Ä”çŚÓŚȘÒÆŒÓËÙŃő»Ż»čÔŃ»·Ö±œÓÏàčŰĄŁ
3) ÓĆŃĄŽß»ŻŒÁNiMnFe-LDOÔÚÊ”Ń鷶ΧÄÚ¶ÔżŐËÙ±ä»ŻłÊÏÖłöœÏÇż”ÄÊÊÓŠĐÔŁŹÍŹÊ±ŸßÓĐœÏșÔĿčËźżčÁòĐÔÄÜĄŁ
ČÎżŒÎÄÏŚŁș
[1] LUO Shiping, ZHOU Wenting, XIE Aijuan, et al. Effect of MnO2 polymorphs structure on the selective catalytic reduction of NOx with NH3 over TiO2-Palygorskite[J]. Chemical Engineering Journal, 2016, 286: 291-299.
[2] PAN Weiguo, HONG Jienan, GUO Ruitang, et al. Effect of support on the performance of Mn-Cu oxides for low temperature selective catalytic reduction of NO with NH3[J]. Journal of Industrial and Engineering Chemistry, 2014, 20(4): 2224-2227.
[3] ŐĆłțÓš, ÍőÊéĐ€, ĐÏŒŃ, ”È. ÖĐčúÄÜÔŽÏàč۔ĔȘŃő»ŻÎïĆĆ·ĆÏÖŚŽÓë·ąŐčÇśÊÆ·ÖÎö[J]. »·ŸłżÆѧѧ±š, 2008, 28(12): 2470-2479.
ZHANG Chuying, WANG Shuxiao, XING Jia, et al. Current status and future projections of NOx emissions from energy related industries in China[J]. Acta Scientiae Circumstantiae, 2008, 28(12): 2470-2479.
[4] LI Junhua, CHANG Huazhen, MA Lei, et al. Low-temperature selective catalytic reduction of NOx with NH3 over metal oxide and zeolite catalysts: a review[J]. Catalysis Today, 2011, 175(1): 147-156.
[5] À»Ș, Ńîâț, łŁ»ŻŐń. ŃÌÆűŽß»ŻÍŃÏőčŰŒüŒŒÊőŃĐ·ąŒ°ÓŠÓĂ[M]. ±±Ÿ©: żÆѧłö°æÉç, 2015: 155-177.
LI Junhua, YANG Xun, CHANG Huazhen. Development and application of key technologies for selective catalytic reduction of NOx from flue gas[M]. Beijing: Science Press, 2015: 155-177.
[6] CHEN Liqiang, LI Rui, LI Zhibin, et al. Effect of Ni doping in NixMn1šCxTi10 (x = 0.1ĄȘ0.5) on activity and SO2 resistance for NH3-SCR of NO studied with in situ DRIFTS[J]. Catalysis Science & Technology, 2017, 7(15): 3243-3257.
[7] ÊŻÏțŃà, șŰăü, Đ»ÀûŸê. NH3-SCR·ŽÓŠÖĐFe-ZSM-5”ÄFeÎïÖÖ·ÖČŒșÍËáĐÔλ¶ÔÆäËźÈÈÎȶšĐÔŒ°żčÁòșÍżčÌŒÇâĐÔÄÜ”ÄÓ°Ïì[J]. Žß»ŻŃ§±š, 2015, 36(4): 649-656.
SHI Xiaoyan, HE Hong, XIE Lijuan. The effect of Fe species distribution and acidity of Fe-ZSM-5 on the hydrothermal stability and SO2 and hydrocarbons durability in NH3-SCR reaction[J]. Chinese Journal of Catalysis, 2015, 36(4): 649-656.
[8] WANG Ruonan, WU Xu, ZOU Chunlei, et al. NOx removal by selective catalytic reduction with ammonia over a hydrotalcite-derived NiFe mixed oxide[J]. Catalysts, 2018, 8(9): 384.
[9] LIU Fudong, HE Hong, DING Yun, et al. Effect of manganese substitution on the structure and activity of iron titanate catalyst for the selective catalytic reduction of NO with NH3[J]. Applied Catalysis B: Environmental, 2009, 93(1/2): 194-204.
[10] ÉòČźĐÛ, Ê·ŐčÁÁ, Ê©œšÎ°, ”È. »ùÓÚMn-CeOx/ACFN”Ä”ÍÎÂSCRÍŃÏő[J]. »Żč€œűŐč, 2008, 27(1): 87-91.
SHEN Boxiong, SHI Zhanliang, SHI Jianwei, et al. Research on de-NO by low-temperature SCR based on Mn-CeOx/ACFN[J]. Chemical Industry and Engineering Progress, 2008, 27(1): 87-91.
[11] QI Gongshin, YANG Ralph T. Performance and kinetics study for low-temperature SCR of NO with NH3 over MnOxšCCeO2 catalyst[J]. Journal of Catalysis, 2003, 217(2): 434-441.
[12] À¶, ÌÆÏțÁú, ÒŚșìșê, ”È. Mn»ù”ÍÎÂSCRŽß»ŻŒÁ”ÄżčH2OĄążčSO2ŃĐŸżœűŐč[J]. »Żč€œűŐč, 2017, 36(3): 934-943.
LI Chenlu, TANG Xiaolong, YI Honghong, et al. Review on manganese based catalysts resistant to H2O and SO2 for SCR reduction at low temperature[J]. Chemical Industry and Engineering Progress, 2017, 36(3): 934-943.
[13] YAN Qinghua, CHEN Sining, QIU Lei, et al. The synthesis of CuyMnzAl1šCzOx mixed oxide as a low-temperature NH3-SCR catalyst with enhanced catalytic performance[J]. Dalton Transactions, 2018, 47(9): 2992-3004.
[14] XU Haidi, WANG Yun, CAO Yi, et al. Catalytic performance of acidic zirconium-based composite oxides monolithic catalyst on selective catalytic reduction of NOx with NH3[J]. Chemical Engineering Journal, 2014, 240: 62-73.
[15] CHANG Huazhen, LI Junhua, SU Wenkang, et al. A novel mechanism for poisoning of metal oxide SCR catalysts: base-acid explanation correlated with redox properties[J]. Chemical Communications, 2014, 50(70): 10031-10034.
[16] LIU Fudong, HE Hong, DING Yun, et al. Effect of manganese substitution on the structure and activity of iron titanate catalyst for the selective catalytic reduction of NO with NH3[J]. Applied Catalysis B: Environmental, 2009, 93(1/2): 194-204.
[17] LI Xiansheng, LI Kezhi, PENG Yue, et al. Interaction of phosphorus with a FeTiOx catalyst for selective catalytic reduction of NOx with NH3: Influence on surface acidity and SCR mechanism[J]. Chemical Engineering Journal, 2018, 347: 173-183.
[18] JIANG Jianqing, PAN Hua, SUN Guojin, et al. Promotion of Ni/H-BEA by Fe for NOx Reduction with propane in a lean-burn condition[J]. Energy & Fuels, 2011, 25(10): 4377-4383.
[19] CHEN Zhihang, WANG Furong, LI Hua, et al. Low-temperature selective catalytic reduction of NOx with NH3 over FešCMn mixed-oxide catalysts containing Fe3Mn3O8 phase[J]. Industrial & Engineering Chemistry Research, 2012, 51(1): 202-212.
[20] TANG Xingfu, LI Yonggang, HUANG Xiumin, et al. MnOx-CeO2 mixed oxide catalysts for complete oxidation of formaldehyde: Effect of preparation method and calcination temperature[J]. Applied Catalysis B: Environmental, 2006, 62(3/4): 265-273.
[21] CAI Sixiang, ZHANG Dengsong, SHI Liyi, et al. Porous NišCMn oxide nanosheets in situ formed on nickel foam as 3D hierarchical monolith de-NOx catalysts[J]. Nanoscale, 2014, 6(13): 7346-7353.
[22] TANG Xingfu, LI Junhua, SUN Liang, et al. Origination of N2O from NO reduction by NH3 over ŠÂ-MnO2 and ŠÁ-Mn2O3[J]. Applied Catalysis B: Environmental, 2010, 99(1/2): 156-162.
[23] Ń, ÁőĐĄÇà, »Æ±ÌŽż, ”È. ZržÄĐÔMnOx/MWCNTsŽß»ŻŒÁ”ÄœáččÌŰŐśÓë”ÍÎÂSCR»îĐÔ[J]. ÎïÀí»ŻŃ§Ń§±š, 2014, 30(10): 1895-1902.
YANG Chao, LIU Xiaoqing, HUANG Bichun, et al. Structural properties and low-temperature SCR activity of zirconium-modified MnOx/MWCNTs catalysts[J]. Acta Physico-Chimica Sinica, 2014, 30(10): 1895-1902.
[24] FANG De, XIE Junlin, MEI Di, et al. Effect of CuMn2O4 spinel in CušCMn oxide catalysts on selective catalytic reduction of NOx with NH3 at low temperature[J]. RSC Advances, 2014, 4(49): 25540-25551.
[25] KONG Zhijian, WANG Cheng, DING Zhengnan, et al. Li-modified MnO2 catalyst and LiMn2O4 for selective catalytic reduction of NO with NH3[J]. Journal of Fuel Chemistry and Technology, 2014, 42(12): 1447-1454.
[26] DAMMA D, BONINGARI T, SMIRNIOTIS P G. High-temperature water-gas shift over Fe/Ce/Co spinel catalysts: Study of the promotional effect of Ce and Co[J]. Molecular Catalysis, 2018, 451: 20-32.
Łš±àŒ ÇŰĂśŃôŁ©
ÊŐžćÈŐÆÚŁș 2019 -06 -21; ĐȚ»ŰÈŐÆÚŁș 2019 -09 -10
»ùœđÏîÄż(Foundation item)ŁșčúŒÒŚÔÈ»żÆѧ»ùœđŚÊÖúÏîÄż(51978436); ÉœÎśÊĄžß”ÈѧУżÆŒŒŽŽĐÂÏîÄż(2019L0885) (Project(51978436) supported by the National Natural Science Foundation of China; Project(2019L0885) supported by Scientific and Technologial Innovation Program of Higher Education Institutions in Shanxi province)
ÍšĐĆŚśŐߣșÎâĐńŁŹČ©ÊżŁŹž±œÌÊÚŁŹŽÓÊÂŽóÆűÎÛÈŸżŰÖÆ»ŻŃ§ŃĐŸżŁ»E-mail: wuxu@tyut.edu.cn