固相法制备正交层状LiMnO2
石西昌,张志兵,陈白珍,杨喜云,徐徽,周定方,肖湘
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘要:以LiOH・H2O为锂源、Mn2O3(电解MnO2 680 ℃焙烧6 h)为锰源,采用一步固相法在氩气中制取正极材料o-LiMnO2。对Mn2O3和LiOH・H2O混合物进行热重分析,然后对影响LiMnO2合成的重要因素进行考察,最后对合成的样品进行Mn平均化合价的测定和SEM分析。研究结果表明:合成LiMnO2的温度应控制500 ℃以上。合成LiMnO2的最佳实验条件为:锂锰物质的量比1.03、焙烧温度600 ℃、焙烧时间8 h。合成的样品即为LiMnO2;样品的结构为正交层状结构。
关键词:正极材料;正交层状;LiMnO2;焙烧
中图分类号:TB34 文献标志码:A 文章编号:1672-7207(2011)12-3618-05
Layered orthorhombic LiMnO2 prepared by solid method
SHI Xi-chang, ZHANG Zhi-bing, CHEN Bai-zhen, YANG Xi-yun, XU Hui, ZHOU Ding-fang, XIAO Xiang
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: The cathode metarials o-LiMnO2 was prepared by a step solid-phase in an argon with LiOH・H2O as lithium source and Mn2O3 (roasting EMD at 680 ℃ for 6 h) as manganese source. The mixture of Mn2O3 and LiOH・H2O was analyzed by thermogravimetric analysis, and several important influence factors on the synthesis of LiMnO2 were studied. Finally, titration for average valence of Mn and SEM analysis were performed. The results show that the synthesis temperature of LiMnO2 should be controlled at above 500 ℃. The optimum condition for preparing LiMnO2 is as follows: mole ratio of lithium to manganese 1.03, roasting temperature 600 ℃, roasting time 8 h. Synthesis sample is LiMnO2 and its structure is a layered orthorhombic.
Key words: cathode materials; layered orthorhombic; LiMnO2; roasting
Li-M-O(M=Ni,Co,Mn)嵌入型复合氧化物作为锂离子电池正极材料已得到了广泛研究[1-4]。锂锰氧化物因锰资源丰富、成本低、安全性好、污染小等优势已经成为最有可能替代锂钴氧的正极材料。目前对于锂锰氧化物的研究主要集中在层状结构LiMnO2和尖晶石结构LiMn2O4上,但层状LiMnO2理论容量几乎是尖晶石型LiMn2O4的2倍[5-6],因此研究层状结构LiMnO2具有重要意义。层状结构LiMnO2用于正极材料研究较多的有单斜层状结构(m-LiMnO2)和正交扭曲层状结构(o-LiMnO2) 2种[7],前者为α-NaFeO2型结构,后者为岩盐结构[8]。由于Jahn-Teller畸变的影响,Mn3+之间的反铁磁相互作用及离子半径和电荷影 响[9],在热力学平衡条件下,m-LiMnO2不如o-LiMnO2稳定,故m-LiMnO2制备较困难、成本高,很难实现工业化生产,而o-LiMnO2制备简单,有望实现工业化生产。制备o-LiMnO2的方法有很多,固相法是实验室中制备粉体材料的一种常用方法,也是工业上生产锂离子电池正极材料的主要方法。固相法制备o-LiMnO2的研究一直受到重视。Gummow等[10]曾用H2还原LiMn2O4得到o-LiMnO2,但产物中往往含有没有电化学活性的MnO杂相,损害了材料的性能。Lee等[11]将MnOOH和LiOH・H2O混合,经过煅烧后,产品虽有较好的循环性能,然而MnOOH价格较高、且工艺繁琐。Reimers等[12]以Mn3O4和LiOH・H2O为原料,采用冷冻干燥技术,制备过程中对O2分压的控制要求较严格。在此,本文作者以较为廉价的LiOH・H2O为锂源和自制的Mn2O3(电解MnO2 680 ℃焙烧6 h)为锰源,采用一步固相法制取正极材料o-LiMnO2,通过热重、X线衍射和扫描电镜等探讨了o-LiMnO2的最佳合成条件,并通过测定所得样品的Mn平均化合价来进一步验证o-LiMnO2,为工业上开发优异性能的o-LiMnO2提供了一定参考。
1 实验
1.1 实验试剂及仪器
主要试剂:LiOH・H2O(AR),纯度≥90%,天津市科密欧化学试剂有限公司生产;EMD(AR),纯度为94.45%,湘潭电化厂生产;H2SO4(AR),衡阳市凯信化工试剂有限公司生产;Na2C2O4(AR),上海山浦化工有限公司生产。
实验仪器:程控管式电阻炉,型号SK2-4-10,长沙市远东电炉厂制造;程控箱式电炉,型号SXL-1302C,杭州卓驰仪器有限公司制造;X线衍射仪,型号Rigaku.max2550,日本理学公司生产;扫描电子显微镜,型号JMS-6360lv,日本电子株式会社生产;热重分析仪TGA,型号STA449c,德国莱茨公司生产。
1.2 实验原理
由文献[13-14]并通过实验验证和条件探索可知:电解MnO2在空气中高温灼烧(680 ℃)6 h能得到较纯的Mn2O3,其反应为:
4MnO2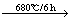 2Mn2O3 + O2↑
2Mn2O3 + O2↑
同时,Mn2O3 在隔绝空气通氩气防氧化加热环境下能与LiOH・H2O发生脱水反应生成目标产物LiMnO2:
Mn2O3+2LiOH・H2O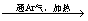 2LiMnO2+3H2O
2LiMnO2+3H2O
1.3 实验方法
首先,通过对Mn2O3 和LiOH・H2O的混合物做差热分析确定其合成反应的大致温度范围,然后,将按一定物质的量比配置的Mn2O3和LiOH・H2O研磨混合均匀置于密闭通氩气的程控管式炉中焙烧制取o-LiMnO2,通过XRD和扫描电镜等分析所制的样品物相和形貌,同时对样品进行Mn平均化合价的滴定,进一步验证所制得的样品。
2 结果与讨论
2.1 Mn2O3和LiOH・H2O混合物的热重分析
图1所示为Li与Mn物质的量比n(Li)/n(Mn)=1的Mn2O3和LiOH・H2O混合物在密闭通氩气的环境下34.4~509 ℃的TG-DSC曲线,其中,升温速率为 10 ℃/min。

图1 Mn2O3和LiOH・H2O混合物的TG-DSC曲线
Fig.1 TG-DSC curves of mixture of LiOH・H2O and Mn2O3
由图1可知:在初始阶段TG曲线上约100 ℃时质量损失率为15.45%,同时DSC曲线出现较大的吸热峰,这是样品LiOH・H2O中结晶水脱除而造成的质量损失。在150~400 ℃,TG曲线和DSC曲线基本是水平的,没有明显吸放热和质量损失,说明此段温度范围内没有发生合成反应。在410~500 ℃,TG曲线质量损失率较大,约为7.4%,同时DSC曲线分别在420 ℃左右和470 ℃左右都出现了放热峰,其中470 ℃左右的放热峰较为尖锐,说明这段温度范围内发生了合成反应,反应脱水造成质量的再次损失。到500 ℃以后,TG曲线和DSC曲线都未发生明显变化,这意味着500 ℃以后,层状LiMnO2已基本形成,即由Mn2O3和LiOH・H2O合成LiMnO2无氧焙烧温度应该维持在500 ℃以上。
2.2 LiMnO2合成的焙烧温度选择
将Mn2O3和LiOH・H2O按n(Li)/n(Mn)=1.08混合均匀,置于密闭通氩气管式炉中,分别在500,600,700和800 ℃焙烧12 h。所得样品的XRD分析结果如图2所示。
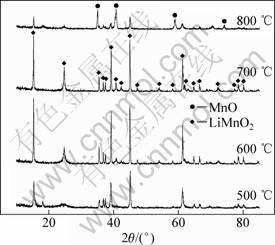
图2 不同焙烧温度下合成的LiMnO2 XRD图
Fig.2 XRD patterns of LiMnO2 at different roasting temperatures
由图2可知:800 ℃焙烧所得样品的主相是MnO,只有少量的LiMnO2,这可能是LiMnO2高温不稳定先分解生成Mn2O3,然后Mn2O3再分解生成MnO所致,同时高温时Li挥发也比较严重。500 ℃,600 ℃,700 ℃都能获得比较纯的LiMnO2,但是500 ℃的峰形较低,峰强较弱,晶体结构不够完整。600 ℃和700 ℃的峰形都较为尖锐,晶型结构较为规整,并且600 ℃的大多特征峰都比700 ℃的尖锐些,同时考虑到节能要求,所以合成LiMnO2的温度宜选择600 ℃。
2.3 LiMnO2合成的锂锰物质的量比的选择
将LiOH・H2O和Mn2O3分别以n(Li)/n(Mn)=0.97,1.00,1.03,1.05,1.08,1.10研磨混合均匀,置管式炉中,于600 ℃通氩气焙烧12 h,研究不同锂锰物质的量比对LiMnO2合成的影响,其XRD结果如图3 所示。
从图3可以看出:n(Li)/n(Mn)对合成LiMnO2的影响比较大。当n(Li)/n(Mn)=0.97时,出现了杂质峰Mn2O,这可能是因为配入的Li不足,Mn2O3高温分解造成的。当n(Li)/n(Mn)=1.10时,出现了杂质峰Li2O,这是因为配入的Li过多,LiOH分解导致的。当n(Li)/n(Mn)=1.00,1.03,1.05,1.08时,都能得到较纯的LiMnO2,但n(Li)/n(Mn)=1.03样品的峰比其他配比样品的峰都尖锐,结晶最为完全,这是因为Li在高温下会挥发损失,故合成LiMnO2的最佳n(Li)/n(Mn)为1.03。
2.4 LiMnO2合成的焙烧时间选择
将LiOH・H2O和Mn2O3按n(Li)/n(Mn)=1.03混合均匀,置于管式炉中,于600 ℃通氩气情况下分别焙烧2 h,4 h,6 h,8 h,12 h,考察焙烧时间对LiMnO2合成的影响,其结果如图4所示。
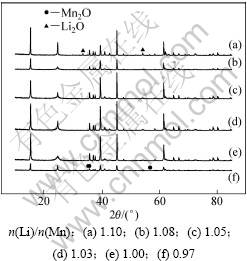
图3 不同锂锰物质的量比对LiMnO2合成的影响
Fig.3 Effect of mole ratio of lithium to manganese on LiMnO2 synthesis
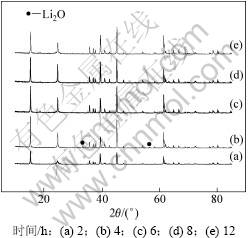
图4 不同焙烧时间对LiMnO2合成的影响
Fig.4 Effect of roasting time on LiMnO2 synthesis
从图4可知:焙烧2 h的样品峰强较弱,焙烧4 h的样品还出现微量的杂质峰Li2O,这可能是由于焙烧的时间过短,反应物还未充分反应完全所致。焙烧6 h,8 h,12 h的样品都能得到峰强较强的LiMnO2,其中,焙烧8 h所得样品峰强稍强,焙烧12 h样品峰强反而比焙烧8 h的样品的峰弱些,这说明焙烧的时间不能过长,否则会破坏LiMnO2的结构,故选择焙烧8 h较为合适。
2.5 LiMnO2中Mn平均化合价的测定
锰的平均化合价的测定采用氧化还原返滴定及络合滴定法[15],由参加反应的Mn得到的总电子数及总锰量来计算其平均化合价。
准确称取0.1 g左右的锂锰氧化物于250 mL锥形瓶中,分别加入15 mL 0.1 mol/L Na2C2O4标准液和10 mL H2SO4,然后加热至暗绿色锂锰氧化物完全溶解。趁热用已知浓度的KMnO4滴定反应剩余的Na2C2O4,滴定过程中以KMnO4自身作为滴定指示剂,溶液由无色变为粉红色为滴定终点。滴定反应为:MnO4-+C2O42-+H+→Mn2++CO2↑+ H2O,根据氧化-还原反应过程中得失电子数相等的原则计算合成样品中Mn平均化合价。其计算公式为:
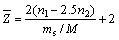
式中: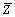 为样品中锰的平均化合价;ms为样品质量,g;M为LiMnO2的摩尔质量,g/mol;n1为加入的Na2C2O4物质的量,mol;n2为消耗的KMnO4物质的量,mol。
为样品中锰的平均化合价;ms为样品质量,g;M为LiMnO2的摩尔质量,g/mol;n1为加入的Na2C2O4物质的量,mol;n2为消耗的KMnO4物质的量,mol。
对n(Li)/n(Mn)=1.03,600 ℃通氩气焙烧8 h的样品进行了Mn平均化合价的测定,经测定其锰平均化合价为3,与LiMnO2的Mn平均化合价相吻合,这进一步验证了所制的样品为LiMnO2。
2.6 LiMnO2的电镜分析
将对n(Li)/n(Mn)=1.03,600 ℃通氩气焙烧8 h所得的样品进行电镜分析,其SEM形貌如图5所示。从图5可见:所制的LiMnO2层状结构明显,疏松多空隙,且粒度比较均匀,大多在1 μm以下,故其有较强的化学活性,性能比较优异。

图5 LiMnO2的SEM图
Fig.5 SEM images of LiMnO2
3 结论
(1) 通过对Mn2O3和LiOH・H2O混合物进行热重分析,初步确定了合成LiMnO2的温度应控制500 ℃以上。
(2) 合成LiMnO2的最佳实验条件:n(Li)/n(Mn)= 1.03、焙烧温度为600 ℃、焙烧时间为8 h。
(3) 合成的样品中Mn平均化合价为3价,与LiMnO2中Mn平均化合价相吻合,从而进一步断定合成的样品即为LiMnO2。
(4) 样品的结构为正交层状结构。
参考文献:
[1] 夏君旨, 纪海涛, 夏君磊. Li-Mn-O体系锂离子电池正极材料的结构与性能[J]. 陶瓷科学与艺术, 2003(1): 18-20.
XIA Jun-zhi, JI Hai-tao, XIA Jun-lei. The structure and performance of Li-Mn-O system cathode material for Li-ion battery[J]. Ceramics Science & Art, 2003(1): 18-20.
[2] 钟辉, 许惠. 层状Li0.7CoxMn1-xO2正极材料的合成与电性能研究[J]. 无机材料学报, 2004, 19(5): 1051-1057.
ZHONG Hui, XU Hui. Synthesis and electrochemical properties studies on layered Li0.7CoxMn1-xO2 cathode material for lithium-ion secondary batteries[J]. Inorg Mat, 2004, 19(5): 1051-1057.
[3] 舒东, 杨勇, 夏熙, 等. 尖晶石型LiMn2O4的电化学性质[J]. 电池, 2001, 31(5): 215-217.
SHU Dong, YANG Yong, XIA Xi, et al. Electrochemical property of spinel LiMn2O4 prepared by sol-gel method[J]. Battery Bimonthly, 2001, 31(5): 215-217.
[4] 阮艳莉, 韩恩山, 张西慧. 尖晶石型锂锰氧化物正极材料的研究进展[J]. 电源技术, 2003, 27(4): 400-403.
RUAN Yan-li, HAN En-shan, ZHANG Xi-hui. Development of research on spinel Li-Mn oxide as cathode material for lithium ion battery[J]. Power Sources, 2003, 27(4): 400-403.
[5] Kim J U, Jo Y J, Park G C, et al. Charge/discharge characteristics of LiMnO2 composite for lithium polymer battery[J]. J Power Sources, 2003, 119/120/121: 686-689.
[6] Wei Y J, Ehrenberg H, Bramnik N N, et al. In situ synchrotron diffraction study of high temperature prepared orthorhombic LiMnO2[J]. J Solid State Ionics, 2007, 178: 253-257.
[7] 许天军, 叶世海, 王永龙, 等. 单斜层状LiMnO2的球磨-离子交换法合成及其电化学性能研究[J]. 无机化学学报, 2005, 21(7): 993-998.
XU Tian-jun, YE Shi-hai, WANG Yong-long, et al. Synthesis and electrochemical properties of monoclinic layered LiMnO2 via ball-milling and ion exchange reaction[J]. Chinese Journal of Inorganic Chemistry, 2005, 21(7): 993-998.
[8] 钟辉, 周燕芳, 许惠, 等. 层状LiMnO2正极材料的研究进展[J]. 化学通报, 2003(7): 449-453.
ZHONG Hui, ZHOU Yan-fang, XU Hui, et al. Progress of layered LiMnO2 as cathode materials of lithium ion battery[J]. Chemistry Bulletin, 2003(7): 449-453.
[9] 赵世玺, 刘韩星, 李强, 等. 锂离子电池正极材料LiMnO2的结构稳定性及电化学过程中的相变[J]. 材料导报, 2002, 16(9): 40-43.
ZHAO Shi-xi, LIU Han-xing, LI Qiang, et al. Transition of LiMnO2 compounds as cathode materials for Li-ion batteries[J]. Materials Review, 2002, 16(9): 40-43.
[10] Gummow R J, Thackeray M M. An investigation of spinel-related and orthorhombic LiMnO2 cathodes for rechargeable lithium batteries[J]. J Electrochem Soc, 1994, 141: 1178-1182.
[11] Lee Y S, Sun Y K, Adachi K, et al. Synthesis and electrochemical characterization of orthorhombic LiMnO2 material[J]. Electrochimica Acta, 2003, 48: 1031-1039.
[12] Reimers J N, Fuller E W, Rossen E, et al. Synthesis and electrochemical studies of LiMnO2 prepared at low temperatures[J]. J Electrochem Soc, 1993, 140: 3396-3401.
[13] 张启蒙, 薛叙明, 马金花, 等. 三氧化二锰氧化法合成对氟苯甲醛的绿色工艺[J]. 精细化工中间体, 2010, 40(3): 47-51.
ZHANG Qi-meng, XUE Xu-ming, MA Jin-hua, et al. Green preparation of p-fluorobenzaldehyde by oxidation of p-fluorotoluene with Mn2O3[J]. Fine Chemical Intermediates, 2010, 40(3): 47-51.
[14] 朱晨燕, 朱宪. 苯甲醛绿色生产新工艺[J]. 高校化学工程学报, 2000, 14(5) : 448-452.
ZHU Chen-yan, ZHU Xian. Green chemical technology for benzaldehyde[J]. Journal of Chemical Engineering of Chinese Universities, 2000, 14(5) : 448-452.
[15] 陈永熙, 周丽娟, 郭丽萍, 等. 锂锰氧化物中锰的平均化合价的测定研究[J]. 武汉理工大学学报, 2001, 23(10): 1-3.
CHEN Yong-xi, ZHOU Li-juan, GUO Li-ping, et al. The research on the determination of average Mn valency in lithium manganese oxide[J]. Journal of Wuhan University of Technology, 2001, 23(10): 1-3.
(编辑 赵俊)
收稿日期:2011-01-11;修回日期:2011-04-20
基金项目:国家“十一五”科技支撑计划项目(2008BAB35B04);中央专项中南大学前沿研究计划重点项目(2010QZZD003)
通信作者:石西昌(1969-),男,甘肃西和人,博士,副教授,从事材料冶金和盐湖资源综合利用等研究;电话:0731-88877352;E-mail:xichang.shi@gmail.com