��������Է�ʯ��������ҵ������PH3
��ƽ1����С��1������1����ΰ��1����ӨӨ2��������1
(1. ����������ѧ ������ѧ�빤��ѧԺ������ ������650500��
2. ����������ѧ ��ѧԺ������ ������650500)
ժ Ҫ��
����ȡ�������Ʒ�Ӧβ���и�Ũ�ȵ�PH3���������Ը��Է�ʯΪ����������PH3���о���������������������ҺpH����Ӧ�¶ȡ�����������������������������������ռ�ת��Ч�ʵ�Ӱ�졣��������������������Ϊ20 mL/min; �ϼѵ�pHΪ13�������˵ķ�Ӧ�¶�Ϊ20 �棻��������������������Ϊ6%ʱ�����������Ч����ߣ�����������5 g/Lʱ�ɻ�ýϼѵ�ת��Ч��������������������������ά��73%���ϵ�ʱ��Ϊ120 min������ת����Ϊ40.4%���������������ڹ���������Һ���ܳ������´���ʧ��������ظ�����3�Ρ�
�ؼ��ʣ�
����������ʯ��������������������������
��ͼ����ţ�X701 ���ױ�־�룺A ���±�ţ�1672-7207(2013)11-4753-06
Catalytic oxidation PH3 in industrial waste gas with CeO2-modified zeolite catalyst
NING Ping1, HUANG Xiaofeng1, ZHOU Tao1, LIU Weiwen1, FAN Yingying2, QIN Yangsong1
(1. Faculty of Environmental Science and Engineering, Kunming University of Science and Technology, Kunming 650500, China;
2. Faculty of Science, Kunming University of Science and Technology, Kunming 650500, China)
Abstract: In order to realize the comprehensive utilization of PH3 produced by the preparation of sodium hypophosphite from phosphorous sludge, multiphase catalytic oxidation process of PH3 with mixed solution of model-Ce zeolite as catalyzer was studied. The influence laws of gas flow rate, pH value, temperature, H2O2 concentration and catalyst amount on the absorption and conversion efficiency of PH3 were investigated. The results show that optimal reaction conditions are: pH=13.0, gas flow rate of 20 mL/min, reaction temperature of 20 ��, H2O2 concentration of 6%, catalyst amount of 5 g/L. Under these conditions, the absorption efficiency of PH3 can reach 73% within 120 min, and the conversion efficiency reaches 40.4%. The active component dissolved in the hydrogen peroxide causes catalyst deactivation and the catalyst just could be reused three times.
Key words: cerium oxide; zeolite; catalytic oxidation; phosphine; sodium hypophosphite
�����ǻ����������̲�����һ�ֺ����к�������Ҫ��P4���۳����ʺ�ˮ���[1]�����������ķ�չ�����IJ����������ӣ��Ӷ������ĶѴ���������ͻ�������⣬�����к��д�������Ԫ�أ��粻���Ի��ջ��ۺ����ã�����ɼ������Դ�˷ѣ�ͬʱ��������һ��Σ�չ̷ϣ����и�ʴ�ԣ�����ڿ����л�ȼ�գ������ж���P2O5[2]����ˣ�������Ч�ش����������ֺ����к���ѳ�����ü�����⡣ǰ���о����֣��������ͼ���ȡ����������һ����Ч�������ۺ����÷���[3]���˷�Ӧ�����¶Ȳ��ߣ���Դ���ĵͣ����Ҵ���������Ϊһ�ֻ�ԭ�������㷺Ӧ���ڻ�ѧ��[4-6]���л��ϳ�[7]��ʳƷ�ӹ��ͱ���[5, 8]��ˮ����[9]����ҵ�����нϸߵľ��ø���ֵ�������ַ�����ʹ������Լ20%������ת��Ϊ������뵽β����[10]��������ӻ������ã���������������Ⱦ��Ŀǰ�������⾻������ķ����ܶ࣬��Ҫ��Ϊȼ�շ�[11-12]��������[13-14]�ͻ�ѧ���շ�[15-18]������������ѡ�����������������ʼ���Դ����������������Ũ�ȸߵij����û�ѧ���շ��������е�����Դ[19]��������ȡ�������Ʋ������������Ũ�Ƚϸߣ�Ϊ����Ч����β���е��ף����о����ö�������������շ����е����⣬���ù���������Һ������Һ����β���е����������ɾ��нϸ߸���ֵ�Ĵ������ƺ��������ƣ��Ӷ������˴������Ʋ��ʣ�ʹ��Դ�õ���Ч����[10, 20-21]�����ڹ������������ⷴӦ�ٶȽ�����������ƫ�ͣ���ˣ������������ô����Լӿ췴Ӧ�ٶȣ������������Ч�ʡ����ý��շ��Ʊ��˸���5.78%(��������)Ce�ĸ��Է�ʯ��������H2O2Ϊ�������������£����Դ�����PH3��̽�ָ���Ӱ�����ض������ռ�ת��Ч�ʵ�Ӱ�졣
1 ʵ��
1.1 �������Ʊ�
������4A��ʯ�����ϴ�Ӻ���110 ���¸��ȥ�����еĻ�е�����������ʡ�Ԥ�������4A��ʯ��������1:20���뵽���ƺõ�0.1 mol/L Ce(NO3)3��Һ�У������½���6 h������18 h�����˺��˱���ɣ���450~500 �決��3 h������ȴ��ɸ��125 ��m�����պ����������������������ʽ������������棬�õ�ʵ���ô�����
1.2 ���������ʵ��
���������ʵ��������ͼ1��ʾ��ʵ��������Ϊԭ����ȡ�������ƣ���Ӧβ���к��д�����Ũ��PH3����N2Ϊ���������ɸ�ƿѹ���ṩ������ ��һ����Ƚ����ס��������ơ��������Ƶȼ��뵽������������װ�õķ�Ӧ���У��õ���������һ���¶ȣ����д������Ƶ���ȡ��Ӧ����Ӧ���̲�����β���Ⱦ�����ƿ����������Ͼ��ȣ����Ž���װ��85%(��������)Ũ�����ϴ��ƿ����ȥ��β���е����ʡ�����β���¶ȵ����ã�Ȼ����װ�й���������Һ�ʹ���������ƿ�н��д�ת�������ú���ˮԡ�����Ʒ�Ӧ�¶ȣ�������������徭��Ũ�����β������ƿ��һ�����պ��ſա����ڽ���PH3Ũ�ȱ仯�ϴ�Ϊ��ȷ��Ч�ؼ����������Ч����������ƿǰ��ֱ�������㣬��������立ֹ��ȷ��ⶨPH3��Ũ�ȡ�
���������£�����ƿ�з�Ӧ����[9]��
2H2O2+PH3+OH-=H2PO2-+3H2O (1)
3H2O2+PH3+2OH-=HPO32-+5H2O (2)

ͼ1 ʵ��װ������ͼ
Fig.1 Flow sheet of experiment
1.3 ����ָ��
�Թ������������������ʡ���������Ԫ��ת��Ϊ����������Ƽ��������Ƶ�ת������Ϊ���۴������ܵ���Ҫָ�꣬���У�����������Ƽ����������õ��������з����ⶨ�����������ʼ����ʽ(1)������ת���ʼ����ʽ(2)��
�ģ�[(��0-��e)/��0]��100% (1)
��=(n1/n2)��100% (2)
ʽ�У���Ϊ����������ʣ���0Ϊ�����������Ũ�ȣ�mg/m3����eΪ�����������Ũ�ȣ�mg/m3����Ϊ�����ת���ʣ�n1Ϊ�������ƻ����������е���������g��n2Ϊ��������������g��
2 ���������
2.1 �������ٶԶ����������Ӧ��Ӱ��
����Ӧ�¶�Ϊ20 �棬��ͬ����������PH3���ռ�ת��Ч�ʵ�Ӱ��ֱ��ͼ2��ͼ3��
��ͼ2��ͼ3��֪������������Ϊ20 mL/minʱPH3���ռ�ת��Ч�ʽ���ߣ������������ٵ�����PH3���ռ�ת��Ч�ʽ��ͣ���������������40 mL/minʱ���ռ�ת��Ч��Ѹ���½���������Ϊ�����������������ӣ�����������Һ�е�ͣ��ʱ�����̣�PH3���ܽ��������Ӧ����ȫ�����������ռ�ת����Ч�ʡ�

ͼ2 ��ͬ�������������������ʵ�Ӱ��
Fig.2 Effect of different carrier gas flow rate on absorption rate of PH3
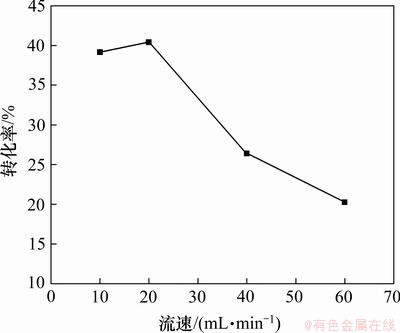
ͼ3 ��ͬ���������������ת����
Fig.3 Conversion rate of PH3 at different carrier gas flow rate
�����������ٵIJ��ϼ�С����Һ�Ӵ���ʱ�����ӳ���PH3������Ч����ߣ������������ٿ�����20 mL/minʱ������Һ��PH3����Ч�ʸ���85%�ҿ�ά��60 min��������Ϊ10 mL/minʱ��PH3���ռ�ת��Ч�ʽԵ���20 mL/minʱ���ݴ�ȷ�����˵���������Ϊ20 mL/min��
2.2 pH�Զ����������Ӧ��Ӱ��
������Ķ����������Ӧ�У���Һ��pH����Ҫ�Ŀ��Ʋ�����ʵ�鿼����pH�����������ʺ�ת���ʵ�Ӱ�죬�����ͼ4��5��
��ͼ4��5�ɿ���������Һ��pH��PH3�����ռ�ת��Ч���нϴ�Ӱ�죬 PH3������ת��Ч����pH�������д���ȵ���ߣ�������ҺpHΪ13ʱ��PH3�����ռ�ת��Ч����ߣ��ɼ�ǿ��������PH3�����ռ�ת������ΪOH-�ڷ�Ӧ�в�����H2O2 ������ġ�OH���ɻ�������Ӧ�������Լ����������£�H+Ũ�ȸߣ�����Ӧ�Լ�H2O2�Ľ�����ܵ����ƣ������ġ�OH�����٣�����PH3����Ч���ű��٣���ʹPH3ֱ����H2O2���ã���Ӧ���ʼ�����PH3�����ռ�ת��Ч�ʽϵ͡�pH���ߣ���ӦҺ�е�OH-�������࣬���뷴Ӧ���ٽ���OH�����ɣ�ʹ�õ�ѡ�����Ҹ������Եġ�OH�������࣬�ԡ�OH���������Ӧ��ռ��������Ӧ���ʼӿ죬���ռ�ת��Ч����������[22]�����⣬PH3�����������л�����������м��������Ի����������»��Է�����̬(��H3PO2��H3PO3)���ڡ��������ڲ������֮�����������ã���ɷ�Ӧ������Ӧ����С�����ڼ�����������Ҫ��������̬���ڣ���Ӧ����С����Ӧ���ʴ�[9]�����ȷ�����˵�����pHΪ13��
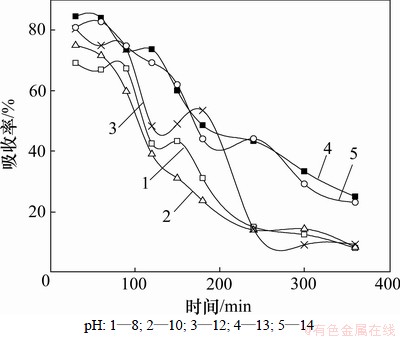
ͼ4 ��ͬpH�����������ʵ�Ӱ��
Fig.4 Effect of different pH on absorption rate of PH3
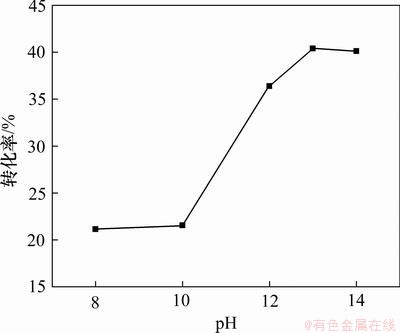
ͼ5 ��ͬpH�������ת����
Fig.5 Conversion rate of PH3 at different pH
2.3 �¶ȶԶ����������Ӧ��Ӱ��
�����¶ȣ����������ѧ��Ӧ���ʣ��������ڻ�ѧ���ʹ��̡��¶ȶ�PH3����ת��Ч�ʵ�Ӱ����ͼ6��7��ʾ����ͼ6��7���Կ��������¶ȴ�15 ������20 �������Һ��PH3������ת������������ǿ��˵���¶�������������߷�Ӧ���ʣ���ѧ��Ӧ����Ϊ��ʱ�Ŀ��Ʋ��裬���¶�Ϊ20~40 ��ʱ������Һ��PH3������Ч�ʼ�PH3��ת��Ч�����¶ȵ����߶����ͣ���ԭ���������Ϊ�������¶����ߣ�PH3�������ܽ���̻������PH3���ܽ�Ƚ��ͣ��Ӷ������������������Һ�ഫ�ʵ����ʣ���Һ�Ӵ�ʱ����٣�����ʹPH3������ת��Ч�ʽ��͡���˿��Կ�����ѧ�����Ǵ˷�Ӧ�Ŀ��Ʋ��裬����ѧ��Ӧ���ʶԴ˷�ӦӰ�첻���¶���������ս�Ϊ�������ʽϼѵķ�Ӧ�¶�Ϊ20 �档

ͼ6 ��ͬ�¶ȶ����������ʵ�Ӱ��
Fig.6 Effect of different temperatures on absorption rate of PH3

ͼ7 ��ͬ��Ӧ�¶��������ת����
Fig.7 Conversion rate of PH3 at different temperatures
2.4 ���������Զ����������Ӧ��Ӱ��
ʵ�鿼���˲�ͬ��������(��������Ϊ����������H2O2�������)�����������ʺ�ת���ʵ�Ӱ�죬�����ͼ8��ͼ9����ͼ8��9��֪��ʵ�鷶Χ����ѵĴ�������Ϊ5 g/L����������������Ͷ�������PH3�Ĵ�ת���������������ͣ�������������������Һ�Ӵ�������ޣ������ڴ����õIJ����������������ߣ��������ֽ�H2O2���ʹ��죬���Ĺ����H2O2��ʹ����ʵ����Ч��H2O2Ũ�ȼ�С�������ڴ����õĽ��У�����ʹPH3�����ռ�ת��Ч��Ҳ��Ӧ���٣������˵Ĵ���������Ϊ5 g/L��

ͼ8 ��ͬ�������������������ʵ�Ӱ��
Fig.8 Effect of different catalyst amounts on absorption rate of PH3

ͼ9 ��ͬ���������������ת����
Fig.9 Conversion rate of PH3 with different catalyst amounts
2.5 �����������������Ӱ��
H2O2��Ϊ�˷�Ӧ����������H2O2���������Ӱ�췴Ӧ�Ľ��С�ʵ�鿼���˲�ͬH2O2������PH3���ռ�ת��Ч�ʵ�Ӱ�죬�����ͼ10��ͼ11��

ͼ10 ��ͬ��������������������������ʵ�Ӱ��
Fig.10 Effect of different volume fraction of H2O2 on absorption rate of PH3
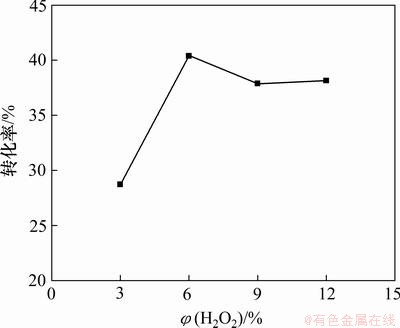
ͼ11 ��ͬ����������������������ת����
Fig.11 Conversion rate of PH3 with different volumes fraction of H2O2
��ͼ10��11��֪��ʵ�鷶Χ����ѵ�H2O2����(�������)Ϊ6%��H2O2����������Ͷ����ռ�ת����Ӧ����������H2O2����Ϊ3%ʱ��PH3�����ռ�ת��Ч��������H2O2�������ͻ�ʹ������PH3���ӵò���������������PH3��ת�������ա�H2O2�������ߣ�H2O2���ӻ�ռ�ݴ�����������λ����PH3���ӷ���������Ҳ�����ڴ�������PH3���������Ӷ�������PH3�����ռ�ת����Ӧ����ͼ10�У�120 min��H2O2����Ϊ6%ʱ��PH3�������½����ƽ�H2O2����Ϊ9%��12%ʱ�Ŀ죬�������H2O2�������йأ��ݴ�ȷ�����˵�H2O2����Ϊ6%�����⣬��ʵ��Ӧ��ʱӦ��ʱ����H2O2��ʹ�京��ά����6%��
2.6 �������ظ�ʹ�öԴ�������Ӱ��
�����ʹ�������Һ��ʹ�ã����л�������ܳ������⡣��������ܳ����������ܽ��ܵ��ܴ��Ӱ�졣ʵ�鿼���˴������ظ�ʹ������������ͼ12����ͼ12���Կ������ظ�ʹ�ô���3�κ�PH3��ת�����������40.4%�½���25.7%���Ѿ��ӽ��հ�4A��ʯ����ʱ��ת����23.7%��˵�������ظ�ʹ��3�κ�����ֽӽ�ȫ���ܳ���
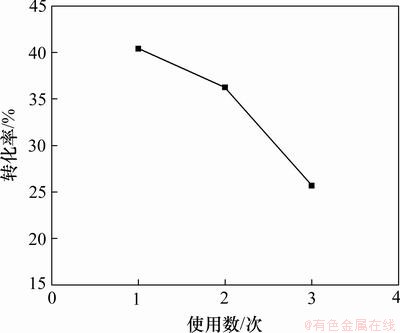
ͼ12 �����ظ�ʹ�ö�ת���ʵ�Ӱ��
Fig.12 Effect of repeat-used catalyst on conversion rate of PH3
3 ����
(1) ��������Է�ʯ(�渺����Ϊ5.78%)�������������ѷ�Ӧ����Ϊ����������20 mL/min�� pH 13����Ӧ�¶�20 �棬���������������6%����������5 g/L���ڴ�����������������ά����73%���ϵ�ʱ��Ϊ120 min������ת����Ϊ40.4%��
(2) �������ظ�����3�Σ����ڻ�����ֵ��ܳ������´��������Խ��͡�
�ο����ף�
[1] ������, ��С��, ��ƽ, ��. ��ɢ��ʮ������������ƶ�������ȡ�������Ƶ�Ӱ��[J]. ��Դ�������г�, 2008, 24(5): 388-389.
HU Ruopeng, HUANG Xiaofeng, NING Ping, et al. Effect of SDBS on producing sodium hypophosphite by phosphorous sludge[J]. Resource Development & Market, 2008, 24(5): 388-389.
[2] �⽭. һ�ִ������л��ջ��Ĺ���: �й�, CN95106266.2[P]. 1995-05-24.
WU Jiang. A process for yellow phosphoric recovery from phosphorous sludge: China, CN95106266.2[P]. 1995-05-24.
[3] ����, ��ƽ, ��С��, ��. ������ȡ��������ʵ���о�[J]. ���ϻ���, 2004, 31(5): 15-17.
GAO Huimin, NING Ping, HUANG Xiaofeng, et al. Experimental study on the preparation of sodium hypophosphite from phosphorus sludge[J]. Yunnan Chemical Technology, 2004, 31(5): 15-17.
[4] Mimani T, Mayanna S M. Study of the role of sodium hypophosphite in electroless nickel bath solution[J]. Journal of Chemical Sciences, 1997, 109(3): 203-209.
[5] �����, ����, ������. ��������������Ӧ��[C]// ��ʮ��ȫ����ѧ�ƻ���, ��ɳ, 2010: 74-80.
LI Deyu, LI Ning, DAI Changsong. Properties and application of sodium hypophosphite[C]// 10th National Conference on Electroless Plating. Changsha, 2010: 74-80.
[6] Hsu H F, Tsai C L, Lee C W, et al. Mechanism of immersion deposition of Ni-P films on Si(100) in an aqueous alkaline solution containing sodium hypophosphite[J]. Thin Solid Films, 2009, 517(17): 4786-4791.
[7] ������, ���㽨, ������, ��. һ�ָ��ϴ����������Ʊ�dzɫ�������е�Ӧ��: �й�, CN200810026951.0[P]. 2008-03-2l.
FAN Deming, ZENG Guangjian, XU Sheyang, et al. Application of composite catalyst in preparation of light-colored rosin ester: China, CN200810026951.0[P]. 2008-03-2l.
[8] ����. ʳ�þ������߱��ʴ���������ʹ��[J]. ����ũҵ, 2006(4): 31.
FU Sheng. Fabrication of storage bags and application in edible fungi, fruit and vegetable preservation[J]. Jilin Agricultural, 2006(4): 31.
[9] �����, �ڱ���, ʢ����. ���͵���ˮ�������ĺϳɼ������о�[J]. ��ҵˮ����, 2005, 25(7): 20-22.
WU Hongte, YU Bingchuan, SHENG Xijun. Study on the synthesis and performance of low phosphate content water treatment agent[J]. Industrial Water Treatment, 2005, 25(7): 20-22.
[10] ���ɿ�, ������, ������, ��. �������ƹ�ҵ����������PH3β����������[J]. ���, 2003, 17(5): 37-38.
WANG Chenjun, GUO Aihong, WANG Fusheng, et al. Treatmental technology of PH3 wastegas in the process of industrial sodium hypophosphite production[J]. Tianjin Chemical Industry, 2003, 17(5): 37-38.
[11] Elliant B, Balma F, Johnson F. Exhaust gas incineration and the combustion of arsine and phosphine[J]. Solid State Technology, 1990, 33(1): 89-92.
[12] ����ƽ, ������. �������������С����ϡ����ۺ�����[J]. ��ѧ����, 1999(3): 159-162.
WANG Huiping, TANG Zhongsong. Comprehensive management of waste materials in the production process of sodium hypophosphite[J]. Chemical World, 1999(3): 159-162.
[13] Juergen W. Absorbent mass for phosphine. WO 00/21644 A3[P]. 2000-04-02.
[14] ������, ������, κ��Ⱥ, ��. ���ºͱ�ѹ�������ӻ���β����������һ����̼[J]. ��Ȼ������, 2001, 26(4): 24-26, 39.
CHEN Zhongming, WU Lixin, WEI Xiqun, et a1. Purification and recovering of CO from yellow phosphorus tail gas by TSA and PSA[J]. Natural Gas Chemical Industry, 2001, 26(4): 24-26, 39.
[15] �̽���, ��Ӣ��, �ű���. ������������������β�������������о�[J]. �Ͽ���ѧѧ��: ��Ȼ��ѧ��, 2001, 34(2): 31-34
CHENG Jianzhong, ZHANG Yingzhe, ZHANG Baogui. Study on the treatment of PH3 in the process of making sodium hypophosphite[J]. Acta Scientiarum Naturalium Universitatis Nankaiensis, 2001, 34(2): 3l-34.
[16] �Ž���. ���⡢�����ѳ��¹���[J]. ���ϻ���, 1995(10): 21-22.
ZHANG Jianhua. A new technics wipe of PH3 and H2S[J]. Henan Chemical Industry, 1995(10): 2l-22.
[17] TimHerman, Soden S. Efficiently handing effluent gases through chemical scrubbing[J]. AIP ConfPro, 1988, l66: 99-108.
[18] �ܻ�, ������, �����. �������������ѳ�����β���е���������[J]. ��������, 2002, 22(3): 161-164.
XIONG Hui, YANG Xiaoli, LI Guangxing. Removal of sulfur and phosphorus from tail gas in yellow phosphorus production by sodium hypochlorite oxidation process[J]. Environmental Protection of Chemical Industry, 2002, 22(3): 161-164.
[19] ����. ����β������������ϵ�д��������о�[D]. ����: ����������ѧ������ѧ�빤��ѧԺ, 2006: 14.
ZHANG Yong. Explotation and research of series catalysts for purifying yellow phosphoric tail gas by catalytic oxidation[D]. Kunming: Kunming University of Science and Technology. School of Environmental Science and Engineering, 2006: 14.
[20] ����ȫ, ����, ����ҵ, ��. Ѭ��ɱ������PH3�����վ����о�[J]. ������Ⱦ�����������豸, 2003, 4(1): 29-32.
D1NG Baiquan, XU Zhou, FANG Dingye, et al. Study of absorbing purification for phosphine from fumigated disinfestation of pests[J]. Techniques and Equipment for Environmental Pollution Control, 2003, 4(1): 29-32.
[21] ����L��Լ˹. Matheson���������ֲ�[M]. ������, �ƽ���, ���, ��. ����: ��ѧ��ҵ������, 2003: 5-60.
Jos C L. Matheson gas date book[M]. TAO Pengwan, HUANG Jianbin, ZHU Dafang, Trans. Beijing: Chemical Industry Press, 2003: 5-60.
[22] ���. ����TiO2/��ʯ/UV������������ˮ�����������о�[D]. ����: ���ݿƼ�ѧԺ������ѧ�빤��ѧԺ, 2008: 43-44.
WANG Nan. Degradation of phenol by nano-TiO2/zeolite/UV catalyzed ozonation in aqueous solution[D]. Suzhou: Suzhou University of Science and Technology. Faculty of Environmental Science and Engineering, 2008: 43-44.
(�༭ �Կ�)
�ո����ڣ�2012-12-10�������ڣ�2013-03-01
������Ŀ������ʡ��������ѧ�о�����������Ŀ(2010Z011)������������ѧ�������Ի���������Ŀ(2010160��2011316)
ͨ�����ߣ���ƽ(1958-)���У�ɽ��̫ԭ�ˣ����ڣ���ʿ����ʦ�����»�����Ⱦ�����о����绰��13708409187��E-mail: hxfkm@sina.com��ningping58@sina.com
ժҪ��Ϊ���ۺ�����������ȡ�������Ʒ�Ӧβ���и�Ũ�ȵ�PH3���������Ը��Է�ʯΪ����������PH3���о���������������������ҺpH����Ӧ�¶ȡ�����������������������������������ռ�ת��Ч�ʵ�Ӱ�졣��������������������Ϊ20 mL/min; �ϼѵ�pHΪ13�������˵ķ�Ӧ�¶�Ϊ20 �棻��������������������Ϊ6%ʱ�����������Ч����ߣ�����������5 g/Lʱ�ɻ�ýϼѵ�ת��Ч��������������������������ά��73%���ϵ�ʱ��Ϊ120 min������ת����Ϊ40.4%���������������ڹ���������Һ���ܳ������´���ʧ��������ظ�����3�Ρ�
[2] �⽭. һ�ִ������л��ջ��Ĺ���: �й�, CN95106266.2[P]. 1995-05-24.
[3] ����, ��ƽ, ��С��, ��. ������ȡ��������ʵ���о�[J]. ���ϻ���, 2004, 31(5): 15-17.
[5] �����, ����, ������. ��������������Ӧ��[C]// ��ʮ��ȫ����ѧ�ƻ���, ��ɳ, 2010: 74-80.
[8] ����. ʳ�þ������߱��ʴ���������ʹ��[J]. ����ũҵ, 2006(4): 31.
[9] �����, �ڱ���, ʢ����. ���͵���ˮ�������ĺϳɼ������о�[J]. ��ҵˮ����, 2005, 25(7): 20-22.
[10] ���ɿ�, ������, ������, ��. �������ƹ�ҵ����������PH3β����������[J]. ���, 2003, 17(5): 37-38.
[12] ����ƽ, ������. �������������С����ϡ����ۺ�����[J]. ��ѧ����, 1999(3): 159-162.
[13] Juergen W. Absorbent mass for phosphine. WO 00/21644 A3[P]. 2000-04-02.
[16] �Ž���. ���⡢�����ѳ��¹���[J]. ���ϻ���, 1995(10): 21-22.
[18] �ܻ�, ������, �����. �������������ѳ�����β���е���������[J]. ��������, 2002, 22(3): 161-164.
[19] ����. ����β������������ϵ�д��������о�[D]. ����: ����������ѧ������ѧ�빤��ѧԺ, 2006: 14.
[20] ����ȫ, ����, ����ҵ, ��. Ѭ��ɱ������PH3�����վ����о�[J]. ������Ⱦ�����������豸, 2003, 4(1): 29-32.
[21] ����L��Լ˹. Matheson���������ֲ�[M]. ������, �ƽ���, ���, ��. ����: ��ѧ��ҵ������, 2003: 5-60.
[22] ���. ����TiO2/��ʯ/UV������������ˮ�����������о�[D]. ����: ���ݿƼ�ѧԺ������ѧ�빤��ѧԺ, 2008: 43-44.


