PEO������LiClO4������ϵ�ķǵ��½ᾧ����ѧ
����Ȫ1, �˴�Ծ2, ���ٻ�1
(1. ���ϿƼ���ѧ ��ѧ����ѧԺ ���Ͽ�ѧ�빤��ϵ, ��̶ 411201;
2. ���ϴ�ѧ ��ѧ����ѧԺ �л����ܸ߷����о���, ��ɳ 410083)
ժ Ҫ��
��ʾ��ɨ�����ȷ�(DSC)�о��˾�������ϩ(PEO)������������(LiClO4)������ϵ�ķǵ��½ᾧ���̡� ������Jeziorny ������ һ�ֽ��Avrami��Ozawa ���̵ķ���������������ϵ��PEO�ķǵ��½ᾧ����, �õ���PEO�ڲ�ͬ��ϵ�зǵ��½ᾧʱ�Ķ���ѧ������ ����ѧ��������LiClO4����������PEO�Ľᾧʱ��, ʹ������ϵ��PEO�Ľᾧ���ʴ���PEO��ϵ��, ��PEO��ϵ�γɸ����ƾ���; Ϊʹ���ߴﵽ��ͬ����Խᾧ��, PEO��ϵ��Ҫ�������ȴ���ʡ� �������, LiClO4�����ܹ���Ч�ؽ�PEO�Ľᾧ��ת��ɷǾ���, ��LiClO4����Ч������PEO�Ľᾧ���̡�
�ؼ���: ��������ϩ(PEO); �������; ������ϵ; �ǵ���; �ᾧ����ѧ
��ͼ�����: O793 ���ױ�ʶ��: A
Non-isothermal crystallization kinetics of poly(ethylene oxide) and its composite with lithium perchlorate
LIU Qing-quan1, PAN Chun-yue2, SHEN Shao-hua1
(1. School of Chemistry and Chemical Engineering,
Hunan University of Science and Technology, Xiangtan 411201, China;
2. Institute of Organic Chemistry and Functional Polymer,
School of Chemistry and Chemical Engineering,
Central South University, Changsha 410083, China)
Abstract: The non-isothermal crystallization kinetics of poly(ethylene oxide)(PEO) and its composite with lithium perchlorate(LiClO4) were investigated via differential scanning calorimetry(DSC).Non-isothermal crystallization process of PEO in the above system was described by Jeziorny method and a new method combined with the Avrami and Ozawa equation. The kinetics parameters of PEO in various system were obtained. The results show that grains of LiClO4 have curtailed crystalline time of PEO, and the overall crystallization rate of PEO in composite is higher than that of PEO system. However, more perfect crystal is formed in PEO system. A conclusion can be deduced that LiClO4 can be effective in producing and stabilizing the amorphous structure of PEO, that is to say, the addition of LiClO4 can availably hinder PEO crystallization.
Key words: poly(ethylene oxide); lithium perchlorate; composite; non-isothermal; crystallization kinetics
�ۺ����������������ӵ�ء� �������� ������ɫ�����ȷ������Ź㷺��Ӧ��ǰ��[1]�� ��������ϩ(PEO)�Ƿ������硢 �о�����һ�־ۺ���������ʻ���, ������������ɵĸ߷��Ӹ�����ϵ��һ�ֵ��͵����ӵ���[2]�� ����PEO���ᾧ, ʹ�����������˶������������ӵ��������ڲ��ֽᾧ��, �����谭PEOӦ�õ���Ҫ����, �������µ絼���ܴﵽ10-4 S/cm, PEO������ʵ������, ��Ŀǰ���о�������Ҫ�����ڽ���PEO�Ľᾧ����[3-5]�� �о����ֶ�������������Ч������PEO���εĹ������кͶ���, ������ᾧ����, �Ӷ���ߵ���ʵ����Ӵ�������[6-8]��
Matsuo��[9]�о���PEO/LiCF3SO3������ϵ�����ӵ絼��, �ڸ���ϵ�м�������SiO2�ɽ���PEO�Ľᾧ����, �Ҹ���ϵ�ĵ絼�������1~2���������� Kumar��[10]�����˸�����ζ�PEO�ۼ�̬�ṹ��Ӱ��, ����LiClO4������Ч�ؽ�PEO�Ľᾧ��ת��ɷǾ���, �������ȶ���Ǿ���ṹ�� ��ᾧ�Եľۺ���, ��PEO, ������̬���зǵ��½ᾧʱ���γɲ��־�̬�ṹ, ��ȴ������Ȼ��Ӱ��ۺ���Ľᾧ��Ϊ�����սᾧ�ȡ� ���ĵ�Ŀ�����о�PEO������ϵ��PEO�ķǵ��½ᾧ����ѧ, ͨ���Ƚ�����ϵ��PEO�Ľᾧ��Ϊ, ������LiClO4��PEO�ᾧ��Ϊ��Ӱ�졣
1 ʵ��ԭ��
�ڹ�ȥ20�����, �����һϵ�����ڴ����ۺ���ᾧ����ѧ��ģ�͡� ���ڶ�ģ����, Avrami���̱��ձ�����ڷ����ۺ���ĵ��½ᾧ��Ϊ, ��ǰ���Ǿۺ������Խᾧ����ʱ������Ӷ�����, Avrami���̿ɱ�ʾΪ[11]
![]()
ʽ(1)��ת����������ʽ:
![]()
ʽ�� X(t)�Ǿۺ������Խᾧ��, ����ʱ��t�ĺ���; Z �ǽᾧ���ʳ���; ��n��Avramiָ���� n����ۺ���ijɺ˻����;���������ʽ�йصij���, ���������Ŀռ�ά���ͳɺ˹��̵�ʱ��ά��֮��[11]�� ��lg[-ln(1-X(t))]��lgt��ͼ, ֱ�ߵ�б��Ϊn, ����ؾ�����Z��
Avrami����ֻ�����������ۺ���ĵ��½ᾧ����, Ϊ�˷�����ǵ��½ᾧ����, �Ⱥ�Ը÷������˸��ֲ�ͬ�������� ����[12] �����˼��ַǵ��½ᾧ����ѧģ�͡� ����, Jeziorny����ֱ�Ӱ�Avrami�����ƹ�Ӧ���ڽ������ٱ���DSC����, �����ǵ��ǵ��½ᾧ���̵��ص�, �Ի�õĽᾧ���ʳ�������ʽ����У��:
![]()
ʽ�� ZcΪ�ǵ��������µĽᾧ���ʳ���; ��Ϊ��ȴ���ʡ� ��ᾧ���50%��ʱ��Ϊ�ᾧ��ʱ��(t1/2), ���ǽᾧ����ѧ������Ҫ��һ�������� t1/2�붯��ѧ����Zc�� n�Ĺ�ϵΪ[13]
![]()
ͨ���ýᾧ��ʱ��ĵ���(��1/2=1/t1/2)��ֱ�������ۺ���Ľᾧ���ʡ�
��������[14, 15]���Avrami��Ozawa����, ����˽����ǵ��½ᾧ����ѧ�������·����� ʽ(1)��ʽ(2)������Avrami���̡� ��Ozawa������, ����ȴ���ʦ�ȡ��ʱ�����t, ������Խᾧ�Ⱦͱ�����Ϊ��ȴ���ʵĺ���[12]:
![]()
ʽ�� X(T)����Խᾧ��; m��Ozawaָ��; k(T)���¶�Tʱ�Ķ���ѧ������ m��nһ��, Ҳ�������κ˻����;���������ʽ�� �ۺ�ʽ(2)��ʽ(6), ��ijһ��Խᾧ����, �ɵõ����·���[14] :
![]()
ʽ�� F(T)=[k(T)/Z]1/m, a=n/m��ijһ��Խᾧ����, ��lgt��lg����ͼ, б��Ϊ-a, �ؾ�ΪlgF(T)�� F(T)����������Ϊ����ijһ�ۺ�����ϵ, �ڵ�λʱ���ڴﵽijһ��Խᾧ�ȱ���ѡȡ����ȴ����ֵ[15]��
2 ʵ��
2.1 ��Ʒ��
ʵ����PEOΪ�ձ�����, �Ϻ���ѧ�Լ���˾��װ����װ, ������1.8~2.0��, �۵�68������, ����������ո���24h��, ������ĥ�ɷ�״���ɡ� LiClO4�ɱ�����ѧ�Լ����ṩ, ��ո������PEO���, ������[O]��[Li]Ϊ8��2, Ȼ�������ȵ�180��, �ô����������������, ����30min����ȴ���ɡ� ���ڻ�Ϲ����ڸ���������С�
2.2 DSC����
��������Perkin-Elmer DSC-7��ʾ��ɨ���������Ͻ���, �Ե�������������, �������¶�У��, �²�Ϊ��0.1�档 ����Լ3mg��Ʒ����������̬, ����15min, ����������ʷ, Ȼ����20��/min����, ��¼DSC�������ߡ� �ظ����Ϲ���, �ı���ȴ����(10��/min�� 5��/min�� 2.5��/min), �ֱ��¼�������ߡ�
3 ���������
3.1 DSC���Խ��
ͼ1��ʾΪPEO������ϵ�ǵ��½ᾧ��DSC����, ��ᾧ���ȷ嶼����ȴ���ʵ���߶�����·����ƶ�, ��������ȴ���ʿ���Ч������PEO���临����ϵ�Ľᾧ[14]��
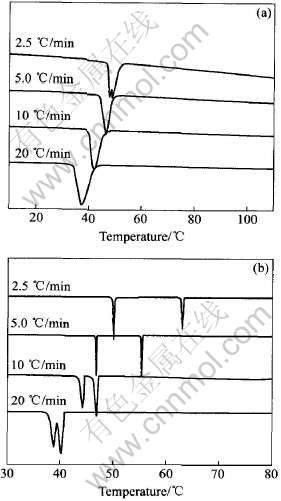
ͼ1 PEO��PEO/LiClO4������ϵ�ǵ��½ᾧʱ��DSC����
Fig.1 DSC curves of non-isothermal crystallization for PEO(a) and PEO/LiClO4 composite(b) at different cooling rates
��PEO��ϵ��DSC���߿�֪, ��ȴ����Ϊ2.5��/minʱ�ᾧ���ȷ���ֲַ�, �����������νᾧ�й�, ���νᾧ���ھۺ���Ľᾧ����, ������ĽӴ�������[13]; ������ȴ�����¶�ֻ�۲쵽��һ�Ľᾧ���ȷ塣 ������ϵ�г��������ᾧ���ȷ�, �������¶ȷ�Χ��֪, ��������PEO�Ľᾧ���ȷ�, ��������ΪLiClO4�ķ��ȷ塣 ������ȴ���ʵ�����, ���ᾧ���ȷ�֮��ľ������μ�С, �����ߵĽᾧ�¶Ȳ����μ�С�� ����ȴ����Ϊ20��/minʱ, �����ᾧ���ȷ��ѷ��������ص�, ������PEO�ᾧ֮ǰ, LiClO4����ȫ�ֽᾧ��
����, ��PEO�ᾧ���ȷ�Ŀ��ȿ�֪, ����ͬ����ȴ������, ������ϵ��PEO�Ľᾧʱ��϶̡�
��DSC���ߵõ���PEO������ϵ��PEO�ķ�ֵ�¶�(Tp)���ᾧ������(��Hc)���ڱ�1�� ����ͬ����ȴ������, PEO��ϵ�ķ�ֵ�¶��Ե��ڸ�����ϵ�е�PEO; ����ᾧ������ȴԶ���ں���, ����LiClO4����Ч��������PEO�Ľᾧ, ʹ��ᾧ�Ƚ���, ��������С��
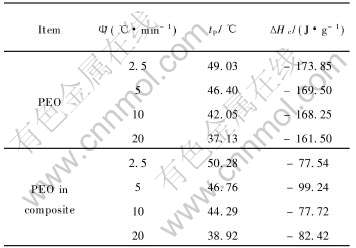
��1 ��ͬ��ȴ������PEO������ϵ��PEO��tp�ͦ�Hcֵ
Table 1 Values of tp and ��Hc for PEO and PEO in composite at various cooling rates
3.2 Jeziorny����
����ʽ(2), PEO������ϵ��PEO��Avrami������ͼ2��ʾ��
��ͼ2�п�֪, ����ȴ����Ϊ20��/minʱ, ʵ�����ֳ����õ����Թ�ϵ, �����ᾧ���̷���Avramiģ�͡� ��������¶��½��Ͽ�, PEO�����ܹ����й������кͶ�����ʱ�����, ���������������ɢ�����˵ı���, �¶Ⱦ��½����������¶�����, ʹPEO����ʧȥ�����, ����Ʒ����ɽᾧ�IJ��ֽ���, �γɵľ���ߴ粻��, û�дﵽ������Ӵ��ij̶�, Ҳ�����νᾧ������ ��������ȴ������, �ӽᾧ��ʼ����Խᾧ��Ϊ70%���һ��ܽϺõط���Avramiģ��, �������һ������, ������Ӵ�, ���ֶ��νᾧ��ƫ��Avramiģ�͡� �ӳ�ʼֱ�ߵ�б�ʺͽؾ�����Avramiָ��n�ͽᾧ���ʳ���Z; ����ʽ(3)�Խᾧ���ʳ�����������; ����ʽ(4)����ᾧ��ʱ��t1/2�ͽᾧ�����ʦ�1/2 , ������ѧ����ֵ���ڱ�2��
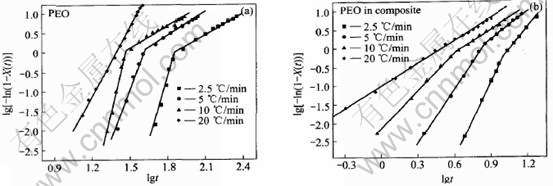
ͼ2 �ǵ��½ᾧʱPEO(a)������ϵ��PEO(b)��lg[-ln(1-X(t))]��lgt��ϵ
Fig.2 Plots of lg[-ln(1-X(t))] vs lgt for non-isothermal crystallization of PEO(a) and PEO in composite(b) at different cooling rates
��2 PEO������ϵ��PEO�ķǵ��½ᾧ����ѧ����ֵ
Table 2 Values of non-isothermal crystallization kinetics parameters for PEO and PEO in composite
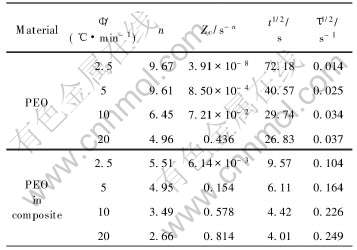
Xu��[16] �����ڷǵ���������, Avramiָ����ӳ�ۺ���һ�νᾧʱ�ľ�������ά��, ����nֵԽ��, ����Խ���ơ� �ӱ�2�п�֪, ����ȴ��������, nֵ���μ�С, ������������Ƴ̶����ν��͡� ����ͬ����ȴ������, ������ϵ��PEO��nֵ��С, ��������Ƴ̶Ƚϵ�, ����LiClO4��������Ч�ؽ�PEO�Ľᾧ��ת��ɷǾ���, ��Kumar��[10]�����Ľ��һ�¡�
�ɱ�2��֪, �ᾧ���ʳ���Zc�ͽᾧ���ʦ�1/2 ����ȴ���ʵ����Ӷ����ӡ� ������Ϊ��ȴ�ٶȴ���ζ�ŸߵĹ����, ���ߵĹ���ȸ�ϵͳ�ṩ���������, ������PEO����������ɢ���۵�, ���¸ߵĽᾧ���ʳ����ͽᾧ���ʡ� Ȼ��, ����ȴ���ʳ���10��/min ֮��, ��ȴ���ʶԽᾧ���ʳ����ͽᾧ���ʵ�Ӱ�����Լ����� �ᾧ��������ȴ���ʵı仯������ͼ3��ʾ��
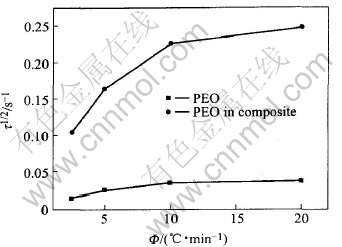
ͼ3 �ᾧ��������ȴ���ʱ仯��ϵͼ
Fig.3 Graph of crystallization rate varying with cooling rate
��ͼ3��֪, ������ϵ��PEO�Ľᾧ���ʽϴ�, ���ڽᾧ��ʱ��ͽᾧ���ʳʵ�����ϵ, ���ᾧ����Խ��; �ᾧ��ʱ��Խ��, ��������ͬ������, ������ϵ��PEO�Ľᾧʱ��϶̡� ǰ������, �ڸ�����ϵ�е�PEO��ʼ�ᾧ֮ǰ, LiClO4����ȫ�ֽᾧ�� ���, LiClO4���������˸�����ϵ������ճ��, �����¶ȵĽ���, PEO�������˶��ܿ촦�ڶ���״̬, ������PEO�ᾧʱ�䡣 ����, ���ݾۺ���Ľᾧ�κ˻���[12], LiClO4�������ܳ䵱PEO�ᾧʱ���κ˼�, ��Ҳ�Ǹ�����ϵ��PEO�Ľᾧ���ʽϴ��ԭ��֮һ��
3.3 һ�ֽ��Avrami��Ozawa ���̵ķ���
��һϵ����Խᾧ����, PEO������ϵ��PEO��lg����lgt֮��Ĺ�ϵ��ͼ4��ʾ��
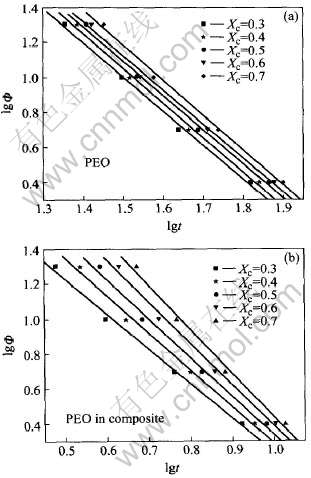
ͼ4 PEO(a)������ϵ��PEO(b)�ǵ��½ᾧʱ��lg����lgt֮��Ĺ�ϵͼ
Fig.4 Plots of lg�� vs lgt for PEO(a) and PEO in composite(b) under non-isothermal condition
��ͼ4�п�֪ , ʵ�������Թ�ϵ�Ϻ�, ˵����ѡ������ȴ���ʺ���Խᾧ����, �÷��������ڷ���PEO������ϵ��PEO�ķǵ��½ᾧ����ѧ�� ��Խᾧ����0.3��0.7֮��ʱ, ��ͼ��ֱ�ߵ�б�ʼ��ؾ�ɷֱ���õ�F(T)��aֵ, ���ڱ�3��
ǰ������, F(T)�����������ǵ�λʱ���ڴﵽijһ��Խᾧ�ȱ���ѡȡ����ȴ����ֵ, ����F(T)ֵ��ӳ�˽ᾧ���ʵĴ�С, ��F(T)ֵԽ��; �ᾧ����ԽС[14]�� �ӱ�3�п�֪, ������ϵ��PEO��F(T)ֵ��С, ��ᾧ���ʽϴ�, ��ǰ�����õ��Ľ��һ�¡� ����, ��˵��Ҫʹ�����ڵ�λʱ���ڴﵽ��ͬ����Խᾧ��, PEO��ϵ��Ҫ�������ȴ���ʡ�
�� 3 PEO������ϵ��PEO�ڲ�ͬ��Խᾧ���µĶ���ѧ����F(T)��aֵ
Table 3 Values of F(T) and a for PEO and PEO in composite under different relative crystallinity
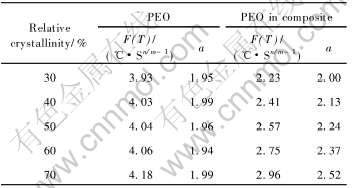
������Խᾧ�ȵ�����, ������ϵ��PEO��F(T)ֵ���ӵķ��Ƚϴ�, ������ȴ���ʶԸ�����ϵ��PEO�ĽᾧӰ������ԡ� ����ڿ��ƾۺ���������ʵ��ȴ���������һ����ָ�����á�
5 ����
��Jeziorny���������Ľ������, ����ȴ����Ϊ20��/min ��, PEO��������ȴ�����½ᾧʱ�������˶��νᾧ���� LiClO4����������PEO�Ľᾧʱ��, ʹ������ϵ��PEO�Ľᾧ���ʴ���PEO��ϵ; ��PEO��ϵ�ᾧʱ�γɵľ�������ơ� LiClO4������Ч�ؽ�PEO�Ľᾧ��ת��ɷǾ���, ��LiClO4����Ч������PEO�Ľᾧ���̡� ��һ�ֽ��Avrami��Ozawa���̵ķ��������������, Ϊʹ�����ڵ�λʱ���ڴﵽͬ������Խᾧ��, PEO��ϵ��Ҫ�������ȴ���ʡ�
REFERENCES
[1]������, ����ǿ, ��÷. ��̬�ۺ�������[J]. ����ѧѧ��, 1995, 28(4): 503-507.
YANG Lan-sheng, SHAN Zhong-qiang, ZHOU Jian-mei. Solid polymer electrolyte[J]. Journal of Tianjing University, 1995, 28(4): 503-507.
[2]Kwang S J, Hee S M, Jong W K. Role of functional nano-sized inorganic fillers in poly(ethylene) oxide-based polymer electrolytes[J]. Journal of Power Sources, 2003, 117(1): 124-130.
[3]����, �ܻ���, �½�ʤ. ��PEOΪ���ʵ����Ӽ�����ۺ�������[J]. ����ѧѧ��, 2002, 18(1): 63-66.
ZHAO Xu, XIONG Huan-ming, CHEN Jie-sheng. Proton-conducting and ionic-conducting polymer electrolytes based on polyethylene oxide(PEO)[J]. Chinese Journal of Inorganic Chemistry, 2002, 18(1): 63-68.
[4]Choi B K, Kim Y W. Thermal history effects on the ionic conductivity of PEO-salt electrolytes[J]. Mater Sci Eng B, 2004, B107(1): 244-250.
[5]Jong W K, Kwang S J, Jae P L, et al. Electrochemical characteristics of two types of PEO-based composite electrolyte with functional SiO2[J]. Journal of Power Sources, 2003, 119-121(2): 415-421.
[6]Chang H P, Dong W K, Jai P, et al. Electrochemical stability and conductivity enhancement of composite polymer electrolytes[J]. Solid State Ionics, 2003, 159(1): 111-119.
[7]Wesley A H, Stefano P. Ionic conductivity in crystalline-amorphous polymer electrolytes-P(EO)6: LiX phases[J]. Electrochemistry Communications, 2003, 5(2): 575-578.
[8]Joykumar S, Mimani T, Patil K C, et al. Enhanced lithium-ion transport in PEG-based composite polymer electrolyte with Mn0.03Zn0.97Al2O4 nanoparticles[J]. Solid State Ionics, 2002, 154-155(1): 21- 27.
[9]Matsuo Y, Kuwano J. Ionic conductivity of poly(ethylene glycol)-LiCF3SO3-ultrafine SiO2 composite electrolytes: effects of addition of the surfactant lithium dodecylsulfate[J]. Solid State Ionics, 1995, 79(1): 295-299.
[10]Kumar B, Rodrigues J, Koka S. The crystalline to amorphous transition in PEO-based composite electrolytes: role of lithium salts[J]. Electrochimica Acta, 2002, 47(11): 4125-4131.
[11]Avrami M. Kinetics of phase change(��)[J]. J Chem Phys, 1940, 8: 212-224.
[12]��, Ī־��. �ִ��߷�������ѧ[M]. ����: ��ѧ������, 2001. 102-120.
YING Jing-hua, MO Zhi-sheng. Modern Polymeric Physics[M]. Beijing: Science Press, 2001. 102-120.
[13]Supaphol P, Spruiell E. Isothermal melt and cold crystallization kinetics and subsequent melting behavior in syndiotactic polypropylene: a differential scanning calorimetry study[J]. Polymer, 1999, 42(2): 699-712.
[14]Liu T X, Mo Z S, Zhang H F. Nonisothermal crystallization behavior of a novel poly(aryl ether ketone): PEDEKmK[J]. Journal of Applied Polymer Science, 1998, 67(5): 815-821.
[15]Liu T X, Mo Z S, Zhang H F. Isothermal and nonisothermal melt crystallization kinetic behavior of poly(aryl ether biphenyl ether ketone ketone): PEDEKK[J]. Journal of Polymer Engineering, 1998, 18(4): 283-289.
[16]Xu G X, Lin S A. Study on the non-isothermal crystallization kinetics of syndiotactic polystyrene(SPS)[J]. Polymeric Materials Science and Engineering, 1999, 15(2): 65-68.
(�༭��ѧ��)
������Ŀ: ����ʡ������������Ŀ (03C499)
�ո�����: 2005-02-21; ������: 2005-07-19
�����: ����Ȫ(1974 -), ��, ��ʦ
ͨѶ����: ����Ȫ; �绰: 0732-8290045; E-mail: lqqlcm@126.com


