���±�ţ�1004-0609(2013)12-3394-07
���ȳ������Ʊ�����ǻ���ʯ��
�� Ƽ�������
(ɽ��������ѧ ���Ͽ�ѧ�빤��ѧԺ���Ͳ� 255091)
ժ Ҫ��
������̼�����Ϊ��Դ�����þ��ȳ��������Ʊ�����ǻ���ʯ(HA)������SEM��XRD��FT-IR��ѧ�����о�����ò���ߴ硢�ɷֺ�����ɡ��������������Ƭ״��̼��HA��������ɣ�ƽ��ֱ��Ϊ5~15 ��m����С���ȡ���ɢ�Ժá��ṹ���¡��Գ��Ժá�������ƫ�⾵�����ֺ�ʮ�����⣬�ò�ɫ������Ϊ��������
�ؼ��ʣ�
����̼������ǻ���ʯ�������ȳ�������ʮ��������
��ͼ����ţ�TB321 �� �� ���ױ�־�룺A
Preparation of porous hydroxyapatite spherulites by homogeneous precipitation method
WANG Ping, LI Guo-chang
(School of Materials Science and Engineering, Shandong University of Technology, Zibo 255091, China)
Abstract: Hydroxyapatite (HA) spherulites were prepared by homogeneous precipitation method using biological calcium carbonate as a raw material. The morphology, size, structure and phase of the HA spherulites were characterized by SEM, XRD, FT-IR and polarized light microscopy. The result show that the HA spherulites with delicate structure and supreme symmetry are formed by self-assembly of plate-shaped HA nanocrystals. The average diameter of HA spherulites with even sizes and better dispersibility is 5-15 ��m. The HA spherulites present a black cross extinction between the crossed polarizers microscopes, and they are optically positive spherulites by compensation principle.
Key words: biological calcium carbonate; hydroxyapatite spherulites; homogeneous precipitation method; cross extinction
��������ĩ������ȣ�������ĩ��������ܶȵ͡������Ժá������žۡ�ע��������������Ϊ�����ϲ�������Ӧ�����е��ŵ㣬�������Ѿ������о���Խ��Խ��Ĺ�ע[1-3]��
�ǻ���ʯ(Ca10(PO4)6(OH)2, HA)��һ���������������Ͷ����������Ҫ������ɷ֡���������HA��������ı���ͽṹ����[4]�����õ�������Ժ����������ԣ����㷺Ӧ��������ҽѧ[5-9]���к����ӵ����ӽ���[10-12]��ɫ����������[12]�ʹ�������[13]������
HA���˳ɷ���ṹ������������ܣ���һ�־�������Ӧ��ǰ���IJ��ϡ�Ŀǰ���Ʊ��ǻ���ʯ��ķ�����Ҫ��ģ�巨[14-15]���������[12]��﮸���(LCB)������ԭλת����[16]����Һ��[17]��ˮ�ȷ�[18]�;��ȳ�����[19]�ȡ�����Щ�����У�������ת��������Һ���ȹ��ձȽϸ��ӣ�Ӳģ�巨���Ʊ�ֱ���ϴ��HA��ͬʱ���ܽ�������������������γɵ�������С��2 ��m�Ŀ����϶࣬��С�����ȡ�
�����������Ƚϣ����ȳ��������ں����ľ�������Һ�У���������ҺpHֵ�ĸı��Է��γɾ��ˣ�ֱ�ӳ�����HA��������Ӧ���ڿ���ϵͳ�ͽϵ��¶�(85~95 ��)�½���[9, 19]��
�ڼ����ǵijɷ��У�����Լռ94%~97%���л���3%~6%(��������)����������ҪΪ̼���(Լ97%)������̼��þ(1%~2%)������������ء��ƺ����ȡ���������Դ�ḻ���ʵش�����������ֱ��Ӧ����ʳƷ�����ϵ���ҵ���ڲ��ϡ�ҽҩ��������������Ϊ���ø�Դ������ԭ�ϵĺϳɡ�
���������Լ�����Ϊ��Դ�����þ��ȳ��������Ʊ�����С���ȡ���ɢ�Ժá��ṹ���¡��߶ȶԳƵ�HA��������ò���ߴ硢���ࡢ�ɷֺͽṹ���������о��������Ĺ����������вⶨ��������ԭ�������á���ȫ��������ʵ����̲�������Ӧʱ��̡��ܺĵͣ���Ӧ�������ڿ��ƣ�������ظ��Ժá�
1 ʵ��
1.1 ʵ�鷽��
�����ǵ�Ԥ������Ca(OH)2ԭ�ϵ��Ʊ�������������[19]����ͬ�ķ������С����Ʊ��Ļ���ʵ��������£���Ca(OH)2�м�ȥ����ˮ�����γ�0.2 mol/L������Һ����H3PO4�м�ȥ����ˮ���Ƴ�0.12 mol/L����Һ�������½�H3PO4��Һ����Ca(OH)2����Һ��(n(Ca)/n(P)=1.67)������Һ�м��������������ܽ⣬��Һ���塣�ټ���0.5~1.0 mmol/L��EDTANa2��6 g���ء����ձ�����90 ���ˮԡ�У����¡���ѹ�·�Ӧ10 min�����������ˣ�������ˮ���Ҵ�����ϴ�ӣ�120 ����
1.2 ����
�������ò����ʹ�ú���Sirion200�ͳ�����ɨ���������(SEM)�����ٵ�ѹΪ5~10 kV���ֱ���Ϊ1.5 nm�������Ĥ���������ʹ�õ¹�D8-ADVANCE��X���߷�ĩ������(XRD)��������ΧΪ2��=2��~60�㣻����������Cu K������(��=0.154 nm)����ѹ40 kV������35 mA��ɨ���ٶ�2 (��)/min���������(FT-IR)����ʹ������Thermo Electron��˾������Nicolet 5700����Ҷ�任��������ǣ�KBrѹƬ��������ΧΪ400~4 000 cm-1���ֱ���Ϊ4 cm-1�������ѧ�����۲������˰µ�MOTIC POL-BA300��ƫ��������
2 ���������
2.1 ����
��ͬEDTANa2Ũ�������Ʊ���Ʒ����ò��ͼ1��ʾ����ͼ1��֪����EDTANa2Ũ��Ϊ0.3~1.0 mmol/Lʱ��������Ʒ��Ϊ���Σ�ֱ��Ϊ5~15 ��m����С���ȣ���ɢ�Ժá�����Ƭ״�������ɣ�Ƭ����ֱ���������У���֮����ڴ�����϶��EDTANa2Ũ�ȡ���Ӧ�¶ȡ���Ӧʱ�䡢�����ٶȺͽ���ʱ��ȶ���Ӱ��Ƭ״HA�����ľ��淢�����ᾧ�ȡ���ֱ�����׳ߴ�[19]��
EDTA ��һ�ְ������Ȼ���ϼ�����������������������4���Ȼ�����������������γ���λ������EDTA ���뵽Ca(OH)2��Һ��Ca2+Ѹ����EDTA ����γ�Ca2+-EDTA ����Ca2+-EDTA ����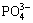 ��������HA��������Ӧʽ���£�
��������HA��������Ӧʽ���£�
Ca2++EDTA2-  Ca2+-EDTA (1)
Ca2+-EDTA (1)
Ca2+-EDTA+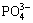
 HA+EDTA (2)
HA+EDTA (2)
����Ca-EDTA�����Ƚ��ȶ���������Ca2+���ͷ��ٶȡ�EDTANa2Ũ�����ӣ��Ӿ�����Һ��������Ca2+���٣�ʹ�ɺ˺;���������ٶȱ�������ˣ�������ʱ����ͬʱ����EDTANa2Ũ�ȵ����ӣ�Ƭ״���ijߴ����ֱ����С����һ���棬HA�е�Ca2+��¶��HAƬ״����(300)���棬ʹ(300)���������ɡ�EDTA2-��(300)�������������ƴ������������������ƽ��(002)�����Ƭ״������ͬƬ��ͨ��(300)��������ӣ��γɽṹ���¡��߶ȶԳƵ���
2.2 �������
��Ʒ��XRD���������ͼ2����ͼ2��֪����Ҫ�ᾧ��ΪHA����EDTANa2Ũ�ȵ����ӣ���������������������ԣ�HA�Ľᾧ�Ƚ��͡����ǣ�����EDTANa2Ũ�ȵ����ӣ�(300)���������ǿ�Ƚ��Ͳ�������ʧ��(002)���������ǿ�ȵı仯��С��I(002)/I(300)������(����1)���ɼ���EDTANa2��������HA(300)��������������(002)�����Ӱ���С����HA�⣬��������������˸�(OCP, Ca8(HPO4)2(PO4)4��5H2O)���������(DCPA, CaHPO4)���ࡣ����Ĵ�����ᾧ������Һ��pHֵ�ϵ��йء�

ͼ1 ��ͬEDTANa2Ũ����HA����Ʒ��SEM��
Fig. 1 SEM images of HA spherulite samples at different EDTANa2 concentrations
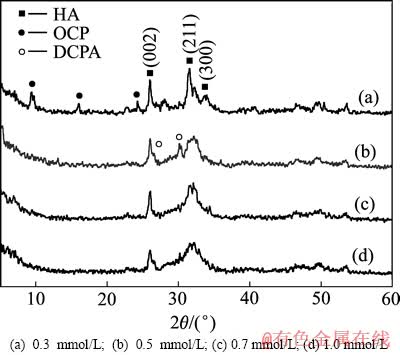
ͼ2 ��ͬEDTANa2Ũ����HA����Ʒ��XRD��
Fig. 2 XRD patterns of HA spherulite samples at different EDTANa2 concentrations
��1 EDTANa2Ũ������ƷI(002)/I(300)�Ĺ�ϵ
Table 1 Relationship between EDTANa2 concentration and I(002)/I(300) of samples

2.3 ���������
ͼ3��ʾΪEDTANa2Ũ��Ϊ0.5 mmol/Lʱ�Ʊ���Ʒ�ĺ�����ס���HA����Ʒ(Standard Reference MaterialR 2910)���жԱȣ�������Ĺ����Ǻ�̼���ǻ���ʯ�ĵ����ס���445��1 039 cm-1���ĵ����Լ�565~603 cm-1����˫�����������Ρ�1 650��3 450 cm-1�����Ŀ�������������ˮ���ǻ��屻����ˮ�Ŀ����ڸǡ�̼���������շ��λ��ȡ�������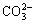 ������λ�á�
������λ�á�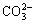 ��4����ģʽ��v1��v2��v3a��v3b��v1����
��4����ģʽ��v1��v2��v3a��v3b��v1����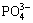 ��ǿ���ص�������Ʒ�ĺ��������û�й۲쵽����֪����ʯ�����У�
��ǿ���ص�������Ʒ�ĺ��������û�й۲쵽����֪����ʯ�����У�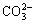 ���������λ�ã�A��ȡ��(
���������λ�ã�A��ȡ��(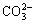 ���OH-)Ϊͨ�������滻������v2��v3a��v3b�ֱ��� 880��1 458��1 546 cm-1�����֡�����B����� (
���OH-)Ϊͨ�������滻������v2��v3a��v3b�ֱ��� 880��1 458��1 546 cm-1�����֡�����B����� (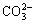 ���
���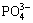 )��v2��v3a��v3b������871��1 420��1 475 cm-1λ��[20-21]�����ڱ��о��Ʊ������ĩ��̼����v2��v3a��v3b��������883��1 454��1 465 cm-1 �����֣�������Ʊ��ķ�ĩ��Ҫ��A���滻��̼��HA��
)��v2��v3a��v3b������871��1 420��1 475 cm-1λ��[20-21]�����ڱ��о��Ʊ������ĩ��̼����v2��v3a��v3b��������883��1 454��1 465 cm-1 �����֣�������Ʊ��ķ�ĩ��Ҫ��A���滻��̼��HA��
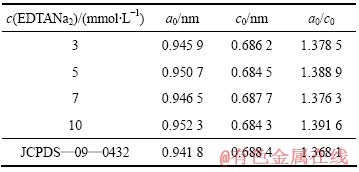
������Ʒ��XRD�������㾧��������������2���С��ɱ�2��֪���봿HA��ȣ����Ʊ���Ʒ��a0�������ӣ�c0���м�С�����ֳ����͵�ͨ�������滻(A���滻)����[21]���������������һ�¡������ϣ���HA�Ľṹ�У�OH-λ��ƽ��c��Ľϴ�ͨ���У�OH-��λ�ÿ��Ա�F-��Cl-��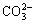 �������滻���γɸ����Ҿ�����ʯ�ṹ�Ĺ����塣��Щ������ľ�����������������ӵİ뾶�仯���仯��������Ӱ뾶���ӣ�a0���ӣ�c0������С[21]��
�������滻���γɸ����Ҿ�����ʯ�ṹ�Ĺ����塣��Щ������ľ�����������������ӵİ뾶�仯���仯��������Ӱ뾶���ӣ�a0���ӣ�c0������С[21]��
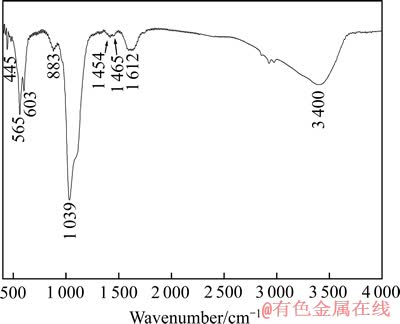
ͼ3 HA����Ʒ�ĺ������
Fig. 3 FT-IR spectrum of HA spherulite sample
��2 ����Ʒ�ľ�������
Table 2 Cell parameters of HA spherulite samples
�γ�A���滻̼���ǻ���ʯ��ԭ����Դ�����3�����������1) ��Ӧ���ڿ���ϵͳ�н��У���Ӧ��Һ�ij�ʼpHֵ�Ƚϵͣ���˻����е�CO2���Խ�����Һ�γ�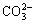 ��ͬʱ�����طֽ�Ҳ����
��ͬʱ�����طֽ�Ҳ����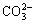 ��2) ��Ӧ��Һ�ij�ʼn(Ca)/n(P)=1.67��Ϊ��ѧ������ȡ��������ص��ֽ⣬��ҺpHֵ�����ߣ�HA�ᾧ����Ӧ��ʼ�Σ�����Ca2+�ܵ�EDTANa2��Լ�������ͷţ�ʹ��Һ�е�
��2) ��Ӧ��Һ�ij�ʼn(Ca)/n(P)=1.67��Ϊ��ѧ������ȡ��������ص��ֽ⣬��ҺpHֵ�����ߣ�HA�ᾧ����Ӧ��ʼ�Σ�����Ca2+�ܵ�EDTANa2��Լ�������ͷţ�ʹ��Һ�е�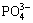 ������OH-�������㡣��ˣ��ڷ�Ӧ���ڣ���ϵ��û���㹻��OH-��
������OH-�������㡣��ˣ��ڷ�Ӧ���ڣ���ϵ��û���㹻��OH-��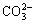 �γ�[CO3OH]�����壬
�γ�[CO3OH]�����壬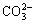 ��[CO3]��������λ���滻ͨ���е�OH-���γ�A�������3) [CO3]��������λ����OH-��ƥ���Խϵͣ�����ܽϴ���˽���ͨ����
��[CO3]��������λ���滻ͨ���е�OH-���γ�A�������3) [CO3]��������λ����OH-��ƥ���Խϵͣ�����ܽϴ���˽���ͨ����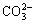 �������ޡ�����������Ҳ���Կ���������̼���ε����շ������
�������ޡ�����������Ҳ���Կ���������̼���ε����շ������
2.4 ���ṹ����������
ͼ4��ʾΪEDTANa2Ũ��Ϊ0.5 mmol/LʱHA����Ʒ�ĵ�ƫ������Ƭ����ͼ4��֪������£�������������Ӿ����пյ�ͬ�IJ�״���졣
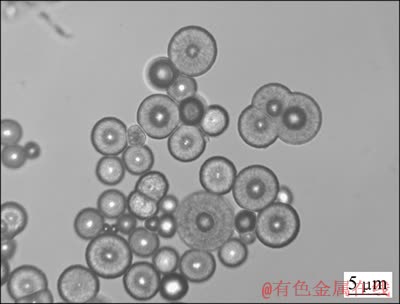
ͼ4 HA������Ƭ
Fig. 4 Micrograph of HA spheres
ͼ5��ʾΪHA����Ʒ������ƫ������Ƭ����ͼ5��֪������ƫ���£�����ֺ�ʮ������(��ͼ5(a))����ʮ�ֵ����۷ֱ�ƽ�����ϡ���ƫ��Ƭ������ʮ�ֵ�4��������һ���Ұ���ɫ����ʮ������ͼ��(Maltase cross, ������˹��ʮ��)����˫�������ʺ߶Գ��Եķ�ӳ[22]����ۺ��������ƣ�ʵ���õ������ɷ���״�ֲ����ǻ���ʯƬ״������ɵ���Ƭ״������������Գ������������������в����谭ʱ���γ������й�ѧ�������ԣ��Թ�����˫�������ã����������ƫ�������¹۲죬�ᾧ̬����ֳ����еĺ�ʮ����������
����ʯ�����ʮ�ֵĵ�1��3������ɫ���߱�Ϊ��ɫ����2��4������ɫ���ͱ�Ϊ��ɫ��Ϊ��������(��ͼ5(b))��
�ǻ���ʯΪ������ϵ���ռ�ȺC26h-P63/m������һ�ᾧ���塣���ڴ�ֱ���᷽���������No���ڹ��᷽���������N e����No��Ne��Ϊһ�ᾧ�����Ծ��塣���ǣ���С�ǻ���ʯƬ����ɵ���ȴ�������Ե�������Ƭ�����Ų���ʽ�йء�
Ƭ״HA��c��((002)����)��������[19](��ͼ6(a))�����й�����(��������ָ��������������Ⲩ�ķ���仯�Ĺ���ָʾ�壬���������Բ�뾶��ʾ��Ӧ�����������)��Բ�뾶No��Ne�ķֲ���ͼ6(b)��ʾ��ƽ��(002)����(���洹ֱ����)�Ĺ����������ǰ뾶ΪNo��Բ��ƽ��a��(����ƽ�й���)�Ĺ����������ǰ뾶ΪNo��Ne����Բ����Ƭ״����a����ṹ����ʱ������c�������洹ֱ(��ͼ6(c))����ʱ��No��Ҫ�����İ뾶����ֲ���Ne��Ҫ������ͬ��Բ�����߷���ֲ���������������ƫ�⾵֮��(��ͼ7(a))��ƽ��PP����ƫ�������������������ں�ʮ�ַ�Χ�ڣ��Ĺ�������Բ�뾶�ֱ���PP��AAƽ�У�ʹ����һ����������ֺ�ʮ�֡�����ʮ�ַָ��4�����ޣ���������Բ�뾶��PP��AAб��������ƽ��PP��ƫ������������ֽ⣬�γ���AA�������ķ������������棬��ˣ���4�������������ġ������뾶�����������(No)�ϴ�ͬ��Բ���߷����������(Ne)��С��������ƫ�⾵�����ʯ����(��ͼ7(b))������ʮ�ַָ��4�������У���1��3������ʯ����ͬ���뾶ƽ�У�����ɫ���߱�Ϊ��ɫ����2��4������ʯ���������뾶ƽ�У�����ɫ���ͱ�Ϊ��ɫ����Ϊ��������
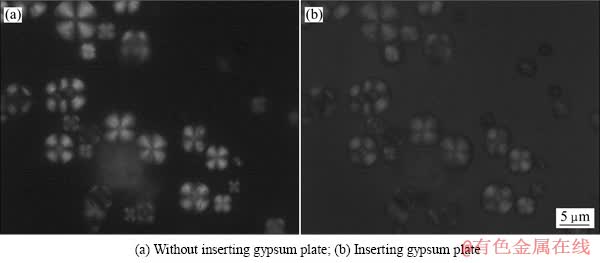
ͼ5 HA��������ƫ�⾵��ĺ�ʮ������
Fig. 5 Black cross of HA spherulites between crossed polarizers
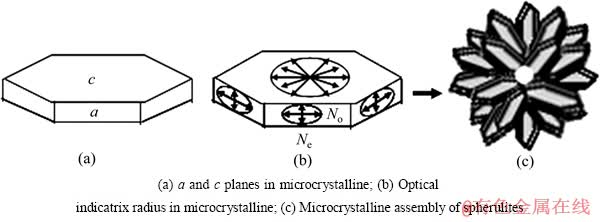
ͼ6 HAƬ״������ʾ��ͼ
Fig. 6 Schematic diagrams of lamellar microcrystalline and spherulites of HA
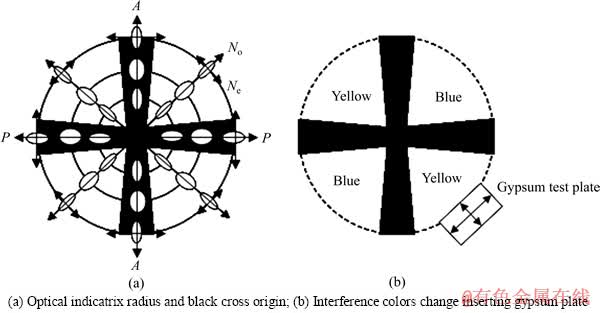
ͼ7 ����ƫ�⾵��HA��ʮ�ֳ�������Բⶨʾ��ͼ
Fig. 7 Schematic diagrams of black cross origin and optical sign determination of HA spherulites between crossed polarizers
��ˣ��ڱ��о������Ʊ���������Ƭ״HA��������ɵĽṹ���¡��߶ȶԳƵ���������
3 ����
1) ������̼�����Ϊ��Դ���ڿ���ϵͳ���ơ������ӵľ�����Һ��ͨ�����ȳ��������Ʊ����ǻ���ʯ(HA)��
2) ������HA����Ƭ����ɵĶ�ס��ṹ�� �¡��߶ȶԳƵ�����������ֱ��Ϊ5~15 ��m����С���ȡ���ɢ�Ժá�
3) EDTANa2Ũ��Ӱ��Ƭ״HA�����Ľᾧ�ȡ����淢������ֱ����
4) ���ڷ�Ӧ���ڿ���ϵͳ�н��У�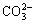 ���Խ���HA�����γ�A�������̼���ǻ���ʯ��
���Խ���HA�����γ�A�������̼���ǻ���ʯ��
REFERENCES
[1] NING Zhang-lei, LI Wen-jun, SUN Chang-yan, CHE Ping, CHANG Zhi-dong. Synthesis and optical properties of zinc phosphate microspheres[J]. Transactions of Nonferrous Metals Society of China, 2013, 23(3): 718-724.
[2] Ԭ�ﻪ, ���۱�, ������, ½����, ������, �Ŷ���. ����װĤ�յ��Ʊ�3D��״������þ[J]. �й���ɫ����ѧ��, 2013, 23(3): 735-741.
YUAN Qiu-hua, LUO Xiong-biao, ZHANG Pei-xin., LU Zheng-wu, REN Xiang-zhong, ZHANG Dong-yun. Preparation of 3D spherical Mg(OH)2 by self-assembled monolayers method[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(3): 735-741.
[3] LIU Chun, YIN Heng-bo, WANG Ai-li, WU Zhan-ao, WU Gang, JIANG Tao, SHEN Yu-tang, JIANG Ting-shun. Size-controlled preparation of hollow silica spheres and glyphosate release[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(5): 1161-1168.
[4] TANAKA H, YASUKAWA A, KANDORI K, ISHIKAWA T. Surface structure and properties of fluoridated calcium hydroxyapatite[J]. Colloids and Surfaces A: Physicochem Eng Aspects, 2002, 204(1/3): 251-259.
[5] SHEN Yu-hui, LIU Jin-hao, LIN Kai-li, ZHANG Wei-bin. Synthesis of strontium substituted hydroxyapatite whiskers used as bioactive and mechanical reinforcement material[J]. Materials Letters, 2012, 70(1): 76-79.
[6] HONG M H, SON J S, KIM K M, HAN M, OH D S, LEE Y K. Drug-loaded porous spherical hydroxyapatite granules for bone regeneration[J]. Mater Sci: Mater Med, 2011, 22(2): 349-355.
[7] ZHANG H Q, DARVELL BW. Synthesis and characterization of hydroxyapatite whiskers by hydrothermal homogeneous precipitation using acetamide[J]. Acta Biomaterialia, 2010, 6(8): 3216-3222.
[8] ������, ��ɹ��, ̷ ��, ������, ��־��, �ܿƳ�. �����ǻ���ʯ�ľ�����������μ��������Ľ������[J]. �й���ɫ����ѧ��, 2010, 20(6): 1203-1208.
ZHAO Yan-zhong, ZHU Shai-hong, TAN Juan, HUANG Yan-yan, LI Zhi-you, ZHOU Ke-chao. Arginine modification and gene binding property of hydroxyapatite nanoparticles[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(6): 1203-1208.
[9] TOMODA K, ARIIZUMI H, NAKAJI T, MAKINO K. Hydroxyapatite particles as drug carriers for proteins[J]. Colloids and Surfaces B, 2010, 76(1): 226-235.
[10] AIZAWA M, TREADO T, HOWELL FS, ITATANI K. Preparation of spherical apatite particles by the homogeneous precipitation method in the presence of magnesium ions and their ion-exchange properties[J]. Materials Research Bulletin, 1999, 34(8): 1215-1225.
[11] �� Ƽ, �����. �ǻ���ʯ���Ʊ������������о�[J]. ��������ѧ��, 2009, 3(3): 564-568.
WANG Ping, LI Guo-chang. Study on preparation and fluoride removal performance of hydroxyapatite[J]. Chinese Journal of Environmental Engineering, 2009, 3(3): 564-568.
[12] ������, ��С��, ������, ������, ����. �ǻ���ʯ����Ʊ���������ɫ������[J]. ������ѧ��, 2010, 38(3): 468-471.
WANG Ai-juan, MA Xiao-long,  Yu-peng, JIANG Bai-ling, ZHU Rui-fu. Preparation and characterization and chromatographic property of hydroxyapatite microspheres[J]. Journal of the Chinese Ceramic Society, 2010, 38(3): 468-471.
Yu-peng, JIANG Bai-ling, ZHU Rui-fu. Preparation and characterization and chromatographic property of hydroxyapatite microspheres[J]. Journal of the Chinese Ceramic Society, 2010, 38(3): 468-471.
[13] �Ŷ���, �Ի���, ����Ӣ, ������, �� ��, ���;�. �ǻ���ʯ�������ʹ��������Ӧ��[J]. ��ѧ��չ, 2011, 23(4): 687-694.
ZHANG Ding-lin, ZHAO Hua-wen, ZHAO Xian-ying, LIU Yi-min, CHEN Hua, LI Xian-jun. Application of hydroxyapatite as catalyst and catalyst carrier[J]. Progress in Chemistry, 2011, 23(4): 687-694.
[14] ��С��, �� ��, �����, ���Ӵ�. HA����װ��ļ��ϳɼ�������Ч����[J]. ������ѧѧ��, 2011, 27(12): 2939-2945.
YANG Xiao-hong, LIU Chang, LIU Jin-ku, ZHU Zi-chun. Facile synthesis of assembly HA nanoribbon spheres and the synergized action of its photocatalytic properties[J]. Acta Physico-Chimica Sinica, 2011, 27(12): 2939-2945.
[15] �¸�, �� ��, �� ��, ������. �ǻ���ʯ��������Ʊ�������ҩ����[J]. ������ͨ��, 2010, 29(3): 651-656.
LUO De-fu, ZHAO Kang, TANG Yu, MA Chu-fan. Fabrication and drug releasing property of hydroxyapatite hollow micro-spheres[J]. Bulletin of the Chinese Ceramic Society, 2010, 29(3): 651-656.
[16] �� Ϊ, Ҧ����, ������, ����ƽ, ���� . ����ǻ���ʯ���ҩ�ﻺ������[J]. �����о�ѧ��, 2011, 25(4): 439-443.
. ����ǻ���ʯ���ҩ�ﻺ������[J]. �����о�ѧ��, 2011, 25(4): 439-443.
XU Wei, YAOAi-hua, AI Fan-rong, WANG De-ping, HUANG Wen-hai. Drug release behavior of porous hydroxya-patite microspheres[J]. Journal of Materials Research, 2011, 25(4): 439-443.
[17] Ѧ ��, ������, Ҧ����. ��Һ���Ʊ�����п��ǻ���ʯ����о�[J]. �㽭������ѧѧ��, 2011, 28(3): 338-342.
XUE Hui, CAI Yu-rong, YAO Ju-ming. Study on porous hydroxyapatite microsphere with an internal cavity by emulsion method[J]. Journal of Zhejiang Institute of Science and Technology, 2011, 28(3): 338-342.
[18] �ν���, �� ӽ, �� Ө. ˮ�ȷ��ϳɲ�ͬ��ò�ǻ���ʯ[J]. ��ĩұ����Ͽ�ѧ�빤��, 2010, 15(5): 505-510.
SONG Jiang-feng, LIU Yong, ZHANG Ying. Hydroxyapatite particles with different morphologies synthesized by hydrothermal method[J]. Materials Science and Engineering of Powder Metallurgy, 2010, 15(5): 505-510.
[19] �� Ƽ, �����. �ǻ���ʯ���Ʊ�����������/���������о�[J]. �˹�����ѧ��, 2012, 41(3): 821-827.
WANG Ping, LI Guo-chang. Preparation and ion adsorption/exchange properties of hydroxyapatite (HA) microspheres[J]. Journal of Synthetic Crystals, 2012, 41(3): 821-827.
[20] YUSUFOGLU Y, AKINCW M. Effect of pH on the carbonate incorporation into the hydroxyapatite prepared by an oxidative decomposition of calcium�CEDTA chelate[J]. Am Ceram Soc, 2008, 91(1): 77�C82.
[21] ��־��, �� ��, �����, ʯ�ͱ�, �ݻ�. ��ʯ�������[M]. ����: ��ѧ��ҵ������, 2008: 103-109.
HUANG Zhi-liang, LIU Yu, XU Huan-yan, SHI He-bin, LUO Hui-hua. Hydroxyapatite mineral materials[M]. Beijing: Chemical Industry Press, 2008: 103-109.
[22] ������. �߷�������ʵ��[M]. ����: �㽭��ѧ������, 1996: 85-90.
LI Yun-ming. Polymer physics experiment[M]. Hangzhou: Zhejiang University Press, 1996: 85-90.
(�༭ ����Ƽ)
�ո����ڣ�2013-02-07�������ڣ�2013-07-23
ͨ�����ߣ��� Ƽ�����ڣ��绰��13220671386��E-mail: wangping-0616@sdut.edu.cn
ժ Ҫ��������̼�����Ϊ��Դ�����þ��ȳ��������Ʊ�����ǻ���ʯ(HA)������SEM��XRD��FT-IR��ѧ�����о�����ò���ߴ硢�ɷֺ�����ɡ��������������Ƭ״��̼��HA��������ɣ�ƽ��ֱ��Ϊ5~15 ��m����С���ȡ���ɢ�Ժá��ṹ���¡��Գ��Ժá�������ƫ�⾵�����ֺ�ʮ�����⣬�ò�ɫ������Ϊ��������
[11] �� Ƽ, �����. �ǻ���ʯ���Ʊ������������о�[J]. ��������ѧ��, 2009, 3(3): 564-568.
[15] �¸�, �� ��, �� ��, ������. �ǻ���ʯ��������Ʊ�������ҩ����[J]. ������ͨ��, 2010, 29(3): 651-656.
[16] �� Ϊ, Ҧ����, ������, ����ƽ, ����. ����ǻ���ʯ���ҩ�ﻺ������[J]. �����о�ѧ��, 2011, 25(4): 439-443.
[17] Ѧ ��, ������, Ҧ����. ��Һ���Ʊ�����п��ǻ���ʯ����о�[J]. �㽭������ѧѧ��, 2011, 28(3): 338-342.
[18] �ν���, �� ӽ, �� Ө. ˮ�ȷ��ϳɲ�ͬ��ò�ǻ���ʯ[J]. ��ĩұ����Ͽ�ѧ�빤��, 2010, 15(5): 505-510.
[19] �� Ƽ, �����. �ǻ���ʯ���Ʊ�����������/���������о�[J]. �˹�����ѧ��, 2012, 41(3): 821-827.
[21] ��־��, �� ��, �����, ʯ�ͱ�, �ݻ�. ��ʯ�������[M]. ����: ��ѧ��ҵ������, 2008: 103-109.
[22] ������. �߷�������ʵ��[M]. ����: �㽭��ѧ������, 1996: 85-90.
LI Yun-ming. Polymer physics experiment[M]. Hangzhou: Zhejiang University Press, 1996: 85-90.


