�й���ɫ����ѧ�� 2003,(04),1041-1045 DOI:10.19476/j.ysxb.1004.0609.2003.04.044
ˮ�ȷ��Ʊ���п�����������������ӷֲ���ȱ���������
���ϴ�ѧ��ѧ����ѧԺ,���ϴ�ѧ��ѧ����ѧԺ,���ϴ�ѧ��ѧ����ѧԺ ��ɳ410083 ,��ɳ410083 ,��ɳ410083
ժ Ҫ��
����XPS��������ԭ�ζ����ֶ�ȷ����һ��п�����������������ӷֲ�ʽ������XRD�ⶨ����Ʒ������(a��=0.8431nm)��ͨ�����ۼ���Ľ��(a=0.8393nm)ʮ�ֽӽ�����Ʒ��350,450��700�澭��4h�ȴ�����,���ӷֲ�����Ӧ�����˱仯:�����ӿ�λ��e��350��ʱ�ﵽ���ֵ0.05520;������a�澧�������ӿ�λ��e�����Ӷ�����,��e����0.05ʱ,������a�����ӱ仺���ȴ����¶Ȳ�ͬ,��Ʒ�ȱ��ʹŻ�ǿ�Ȧ�m��Ӧ�ı�,��350������Сֵ58.5Am2/kg�����ۼ�����ʵ��������,��Ʒ�ıȱ��ʹŻ�ǿ�Ȧ�m�뾧���������ӿ�λ��e�ʹξ����ϸ���̬�����ӷֲ���ʽ�йء�
�ؼ��ʣ�
п������������;���ӷֲ�;ȱ��;������;
��ͼ����ţ� TB383
����飺ɣ�̱�(1969),��,��ʿ�о���.�绰:07318836618,013873120519;Email:ss.ssb.ssb@263.net;
�ո����ڣ�2002-11-12
Ion distribution, defects and magnetic property of ZnMn ferrite nano particles prepared by hydrothermal method
Abstract��
The ion distribution model of ZnMn ferrite was determined by XPS and oxidimetry methods. The crystal lattice constant measured by XRD (0.8431 nm )is close to that of calculated(0.839 3 nm) by the ion distribution model. The number of ion distribution in the model changes after heat treatment at 350, 450 and 700 �� respectively, due to the different ability of occupying A and B sublattice of different metal ions. The metal ion vacancy ��e�� has a maximum value of 0.055 20 at 350 ��. The lattice constant ��a�� increases with the increase of metal ion vacancy ��e�� and at ��e��=0.05 the increasing tendency becomes slow. The specific saturation magnetization ���Ҫ���m alters with the heat treatment temperature and has a minimum value of 58.5 A��m��2/kg at 350 ��. Theoretical calculation and experimental results show that the specific saturation magnetization ���Ҫ���m is related with metal ion vacancy ��e�� and the crystal ion distribution model.
Keyword��
ZnMn ferrite nanoscale particles; ion distribution; defect; magnetic property;
Received�� 2002-11-12
�ṹ���ܲ�����Ƶ�ǰ��������ȷ�����ϵ��۽ṹ, �ر���ԭ���ڿռ�����з�ʽ�� �⾧ʯ������������������ӵķֲ�������ռ��A��Bλ���������Ƶ���Գ̶�������, ��һ��Գ̶ȿ������������б���
��������ռ��A�� Bλ�õ������Ǹ��������ۺϵĽ��, һ����Ϊ������4�������й�: ���Ӽ���; ���Ӱ뾶; ���ۼ��Ŀռ���λ��; ���峡��d���ӵ��ܼ��Ϳռ�ֲ���Ӱ�졣 ��п������⾧ʯ�ṹ��, �������������·ֲ�����
Zn2+ֻ��Aλ����, Fe2+ ����ռ��Bλ, Fe2+��ɳ�����Aλ, Mn2+ֻ��Aλ����, Mn3+, Mn4+ֻ��Bλ����, Fe3+���A��Bλ��ѡ����, ��������������ԭ��ɾ����ϳ��ֵĿ�λ����Bλ�ϳ��֡� ���, ���Ʊ�����п���������������������ӷֲ�ʽ:
(Zn2+x Fe2+yFe3+zMn2+k)-
[Fe2+aFe3+bMn3+cMn4+d��e]2O4 (1)
ʽ�� x, y, z, k, a, b, c, d, e��Ϊ��Ӧ��������Bλ�Ͻ��������ӿ�λ����
����ǰ���о���
1 ʵ�鷽��
�й��Ʊ�п�����������ϸ����μ�����
��Ʒ�ֱ���350�� 450��700 �����4 h�ȴ���, Ȼ�����ձ���ѧD/max-rA��X����������(XRD)ȷ�����ᄃ�ͼ��ⶨ������a; ��VBH- 55������Ʒ��ǿ�� (VSM)�ⶨ�ȱ��ʹŻ�ǿ����m; ���ظ����(K2Cr2O7)����Һ�ζ�Fe2+��������ԭ�ζ����ⶨ�������ӻ�ԭ��Mn2+�ĵõ���Ħ����, ���巽����: ��ȡ0.501 7 g����, ����100 mL������(700 mL H2O+150 mL H2SO4+150 mL H3PO4), 25.00 mL 0.103 2 mol��L-1����������隣���Һ, �Լ���, ������������ȫ�ܽ�, ��ȴ������, ����2�ζ�����������ָʾ��(0.5%ˮ��Һ), ��0.016 67 mol/L�ظ����(K2Cr2O7)����Һ�ζ���Һ�е�Fe2+, �����ĵ��ظ���ر���Һ�����ΪV�� ������ʽ���������и�Mn���ӵĵõ�����:
ʽ�� W����������, g; M��������Ħ������, g/mol, V0����������隣���Һ�����, mL; V�����ĵ��ظ���ر���Һ���, mL��
���ּ�̬�������Ӻ���֮����X���������(XPS)(VG ESCA-LAB MK-II��)�ⶨ��
2 ���������
2.1п���������������ӷֲ�ʽ��ȷ��
���ݼ⾧ʯ�;��������ӵķֲ�����, Aλ���ӷֲ���֮��Ϊ1, Bλ���ӷֲ���֮��Ϊ2, �������ӵ������Ӧ��ȡ� �����
2x+2y+3z+2k+4a+6b+6c+8d=8,
x+y+z+k=1,
a+b+c+d+e=1
�����������Ϊn(Zn2+)��n(Mn2+/3+/4+)��n(Fe2+/3+)=0.135 1��0.119 6��0.510 4=0.529 4��0.468 6��2��
�������ӷֲ�����ȷ����Ҫ�������m, ������������: ���ڴξ���Bλ�������ӿ�λ�Ĵ���, �����¸��ξ��������ӷֲ������ļ���, 0<m��1�� �������������ӵļ��ٳ̶�����ͬ��, ��ô��
ʽ�� n��ʾʵ�ʾ����еĽ�������������, N��ʾ���뾧���еĽ���������������
������п�����徧����Zn2+, Mn2+/3+/4+��Fe2+/3+�����ӷֲ����ֱ�Ϊ0.529 4m, 0.468 6m��2m, ��
x=0.529 4m, k+2c+2d=0.468 6m,
y+z+2a+2b=2m
���ּ�̬�������Ӻ���֮����X���������(XPS)�ⶨ, ����Ϊ
n(Mn2+)��n(Mn3+)��n(Mn4+)=k��2c��2d=39.23��23.54��37.23
���, k=0.183 8m, c=0.055 15m, d=0.087 23m��
��AλFe2+���ӵķֲ���Ϊy , �������ӷֲ�ʽ����дΪ
(Zn
[Fe
�ʾ��廯ѧʽΪZn0.529 4 mMn0.468 6 mFe2mO4�� ͨ���ⶨ��Mn3+/4+���ӻ�ԭ��Mn2+�ĵõ���Ħ�����ɼ��������m��ֵ��
ʵ���в��V=19.90 mL, �ɴ˿ɼ����m=0.966 2�� �����Ʊ�����п���������������ӷֲ�ʽΪ
(Zn
(0��y��0.175 1) (4)
2.2������a�������ӿ�λ��e�Ĺ�ϵ
���������ڴξ���A�� Bλ�ϵķֲ���ͬ, �ᵼ�¾�����a�ı仯�� ��������ͨ��ʵ��ⶨ, ����, ��XRD����, ���߾�����ó��� ����, ����ͨ������ʵ�ʲⶨ�ľ�����a��������õ��ľ�����a, ����֤���ӷֲ�ʽ�ĺ����ԡ� ���㷽������Laari
a=2.099 5dA+(5.818 2d
ʽ�� dA=��CAir(Mei��O)4, �����������徧λ; 2dB=��CBir(Mei��O)6, �����ڰ����徧λ�� CAi�� CBi�ǽ�������i��A�� Bλ�ϵ�Ũ��, r(Mei��O)��ʾ������ ��п�������������������ľ������1��ʾ
���ڷֲ�ʽ(4):
(Zn
[Fe
dA=0.194 8+0.011 6 y,
dB=0.203 0-0.007 91 y,
��1 A�� B�ξ����ϵ�Me��O����
Table 1 Bond length of Me��O inA, B sublattice
| Anion-cation bond | B site/nm | A site/nm |
| Mn2+��O | 0.222 0 | 0.204 1 |
| Mn3+��O | 0.204 5 | - |
| Mn4+��O | 0.184 3 | - |
| Fe3+��O | 0.202 0 | 0.185 8 |
| Fe2+��O | 0.214 8 | 0.197 8 |
| ����O | 0.224 0 | - |
| Zn2+��O | - | 0.197 0 |
����,
a=2.099 5��(0.194 8+0.011 6 y)+
[5.818 2��0.203 0-0.007 91 y)2-
1.410 7�� (0.194 8+0.011 6 y)2]1/2
��yֵ��0��0.175 1��Χ�ڱ仯ʱ, a=0.839 3��0.839 4 nm�� �ɼ�, ������a��ֵ�������ֲ��䡣 ����һ���dz�����˼�Ľ��, ��ij�̶ֳ���˵���������ӵ�����ֲ��Ծ���ṹ����Ӱ�졣
���ᄃ����a��XRD�ⶨ���a��Ϊ0.843 1 nm�� �ɼ�������(a=0.839 3 nm)�ӽ���XRD�ⶨ�����
�⾧ʯ�ṹ�������������, ���ڴξ���Bλ��϶��Aλ��һЩ, ��Fe2+, rB=0.214 8 nm, rA=0.197 8 nm, (rΪMe��O�ļ���), ���Bλ���ӻ����Ը�, ���ӵ�������ԭ����ͬ��Ԫ�صIJ�ͬ��̬���������ı��������仯, ���ڲ�ͬ��̬��������A�� Bλ�ķֲ�����һ����ѡ����, ��˱�Ȼ��ɾ����в�ͬ���ӵ����·ֲ��� Ϊ�˿����ȴ��������ӷֲ���Ӱ��, ������¯��, �����õ�����п������������350�� 450��700 �������4 h�ȴ���, �����ӷֲ�ʽ�ֱ�Ϊ
1) 350 ��ʱ
(Zn
[Fe
2) 450 ��ʱ
(Zn
[Fe
3) 700 ��ʱ
(Zn
[Fe
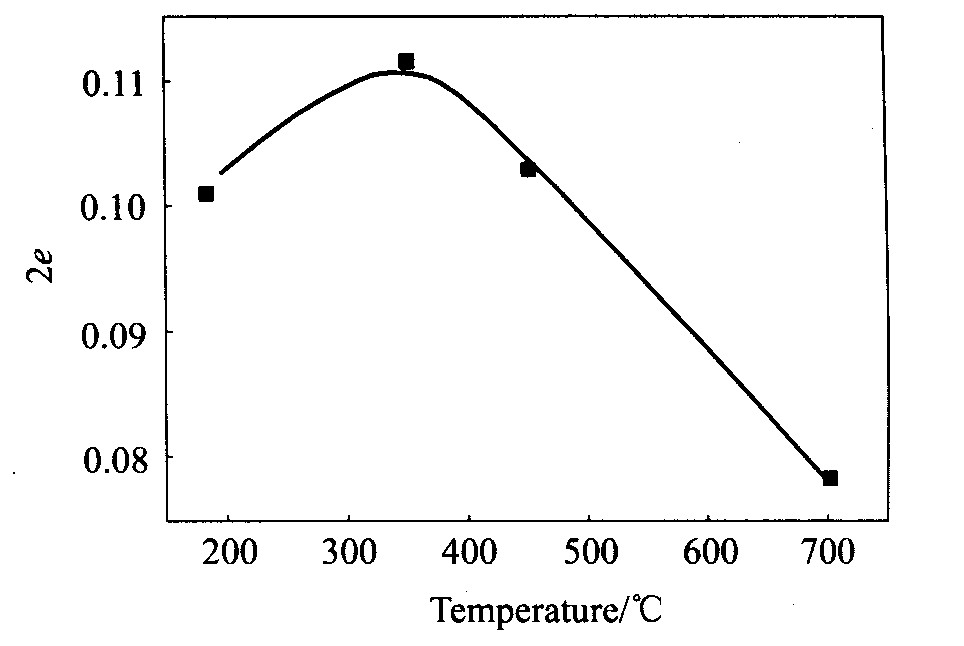
ͼ1��ʾ���ȴ����¶��������ӿ�λ��e�Ĺ�ϵ���ߡ� ��ͼ1���Կ���, ��λ��e��350 �������м���ֵ, ���߳���������, �����¶ȵ�����, ��λ��e��С�� ����Ҫ��������350 ��ʱ, �����ͼ۽��������ӱ������ɸ�����, ͬʱ���ִ�����λ����
200��300 �� 3Fe
320��480 �� 3Fe
250��400 �� 3Mn
250��400 �� 4Mn
���¶ȳ���400 ��, ���������ӿ�λ������, ������Ϊ�����·�Ӧ����:
400��500 �� 3Fe
600��700 �� 3Mn
400��700 �� 3Mn
ͼ1 ��λ��e���ȴ����¶ȵĹ�ϵ
Fig.1 Relationship between vacancy number eand heat treatment temperature
�����е�Mn
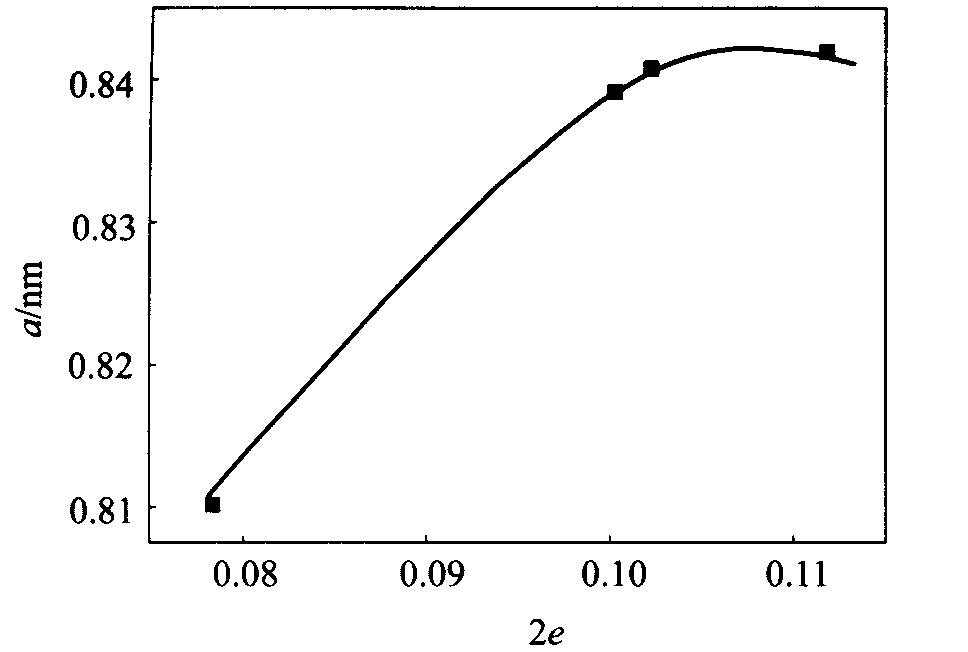
��ͼ2���Կ���, ������a�澧�������ӿ�λ��e�����Ӷ�����, ��e�ӽ�0.05ʱ, ������a�����ӱ仺��
2.3�ȴ�����п�������������ȱ��ʹŻ�ǿ�Ȧ�m��Ӱ��
��VBH-55������Ʒ��ǿ��(VSM)�ⶨ��п��������������ĩ�ı��ʹŻ�ǿ����m, �Լ���Ʒ�ڲ�ͬ�¶��´�����ı��ʹŻ�ǿ��, �����ݲ�ͬ���ӷֲ�ʽ������ȱ��ʹŻ�ǿ����m
ͼ2 ������a�Ϳ�λ��e�Ĺ�ϵ
Fig.2 Relationship between lattice constant a and vacancy number e
ʽ�� MΪ�����Ħ��������
�ⶨ������������ͼ3��
ͼ3 ��ͬ�¶��ȴ���4 h����Ʒ�ıȱ��ʹŻ�ǿ�Ȧ�m
Fig.3 Specific saturation magnetization ��m of sample treated at different temperature for 4 h
�������, ˮ�ȷ��Ʊ���п��������������ĩ�ıȱ��ʹŻ�ǿ����m=76.5 Am2/kg�� �����ڲ�ͬ�¶����ȴ���4 h��, ����350 ���ȴ�������Ʒ�ȱ��ʹŻ�ǿ����m��С, ��450 �� ��������Ʒ��ȱ��ʹŻ�ǿ����m��������, ����700 �洦������Ʒ��ȱ��ʹŻ�ǿ����m�ּ�С�� ��˵���ȱ��ʹŻ�ǿ����m�����������ӿ�λ��e�й���, �������������A�� B�ξ����ϵķֲ��йء� �����ӿ�λ������, ��Ʒ����ȱ�ݽ϶�, ��˱��ʹŻ�ǿ����m��С�� ʵ��ⶨֵ�ȼ���ֵ����ƫ��, �������������Ʊ�����п������������̫С, �����������, �ṹȱ�ݽ϶�, ����ṹ��������ԭ��
3 ����
1) ���ݼ⾧ʯ�ṹ�����������ӷֲ�����, ����XPS��������ԭ�ζ����ֶ�ȷ����һ����п�����������������ڴξ����ϵķֲ���ʽ�� ���ӷֲ�ʽ������ʽ����:
(Zn
[Fe
2) ����XRD�ⶨ����Ʒ������(a��=0.843 1 nm)��ͨ�����ۼ���Ľ��(a=0.839 3 nm)ʮ�ֽӽ�, �������Ʊ�����п�����������������ӿ�λ�͡�
3) ��Ʒ�ڲ�ͬ���¶����ȴ�����, ����������ԭ����, ���������Ӽ�̬�����仯, ����̬��������ռ�ݴξ����������ͬ, ���ӷֲ���ʽ��Ӧ�����仯�� �����ӿ�λ��e��350 ��ʱ�ﵽ���ֵ��
4) �о��˾������������ӿ�λ��e�ı仯�� ������a�澧�������ӿ�λ��e�����Ӷ�����, ��e����0.05ʱ, ������a�����ӱ仺�� �ȱ��ʹŻ�ǿ����m�����������ӿ�λ��e�й���, �������������A�� B�ξ����ϵķֲ���ʽ�йء�
�����