���±�ţ�1004-0609(2010)12-2351-06
���෨�ϳ�LiFePO4/C�������ϵĵ绯ѧ����
�������������ѣ���鲨����Ӣƽ����˳�㣬���������� ���������������췼��֣��Ƽ����Ȩ��
(��̶��ѧ ��ѧѧԺ �����Ѻû�ѧ��Ӧ�ý������ص�ʵ���ң���̶ 411105)
ժ Ҫ��
������ԭ����FeSO4��7H2OΪ��Դ��������Ϊ̼Դ�����ù��෨�ϳ�������ӵ���������ϡ���LiFePO4/C���ϲ��ϡ���X��������(XRD)��ɨ��羵(SEM)�͵绯ѧ���Լ����Բ�ͬ��Դ�ϳɵ�LiFePO4/C���ϲ��ϵĽṹ����ò�͵绯ѧ���ܽ����о�������������ϳɵ���Ʒ���о�һ�����ʯ�ͽṹ����FeSO4��7H2OΪ��Դ�ϳɵ�LiFePO4/C���ϲ��ϵ�ѭ�����ܺ߱��ʷŵ����ܾ�������FeC2O4��2H2OΪ��Դ�ϳɵ�LiFePO4/C���ϲ��ϵģ���FeSO4��7H2O�ϳɵ�LiFePO4/C���ϲ��ϵ�5C���ʷŵ������Ϊ105.9 mA?h/g����ѭ��30�κ������Ըߴ�105.2 mA?h/g��
�ؼ��ʣ�
LiFePO4/C���ϲ�������Դ������ӵ��������������
��ͼ����ţ�O646���� ���ױ�־�룺A
Electrochemical performance of LiFePO4/C cathode materials
synthesized by solid-state reaction
WANG Guo-bao, WANG Xian-you, SHU Hong-bo, WANG Ying-ping, YANG Shun-yi, LIU Xiu-ming,
PEI Fu, WANG Yan-sheng, AN Hong-fang, ZHENG Li-ping , CHEN Quan-qi
(Key Laboratory of Environmentally Friendly Chemistry and Applications,
Ministry of Education, School of Chemistry, Xiangtan University, Xiangtan 411105, China)
Abstract: The lithium ion battery cathode material LiFePO4/C composite was prepared by a solid-state method using the low cost FeSO4?7H2O as iron source and sucrose as carbon source. The structure, morphology and electrochemical performance of the LiFePO4/C samples prepared with different iron sources were investigated by X-ray diffraction (XRD), scanning electron microscopy (SEM) and electrochemistry techniques. The results show that the resultant LiFePO4/C has homogeneous olivine structure. And the capacity and cycle ability of LiFePO4/C prepared from FeSO4��7H2O are higher than that of LiFePO4/C composite synthesized by a traditional solid-state method using FeC2O4?2H2O as iron source. The capacity is 105.9 mA?h/g at 5C rate and remained 105.2 mA?h/g after 30 cycles.
Key words: LiFePO4/C composite; iron source; lithium ion battery; cathode material
����ӵ������߿����������ߵ�ѹ����ѭ�����ܺ������ܶȵ��������Զ�������������������Ϊ21���͵������ƶ���Դ����Ӧ����������������ӵ���У���������Լռ��������ɱ���40%���ң����������϶�����ӵ�صİ�ȫ��������Ҫ���ã����������ϼ�����Ϊ��Լ����ģ�ƹ�Ӧ�õ�ƿ��������Ƶ�������Խ���۸���˵������������������ҵ�������еĹؼ������ء��Ѿ���Ʒ����LiCoO2��Դ�ѷ����۸�ϸߣ������ж��ԣ�LiNiO2�ϳ����ѣ��ҵ绯ѧ���Բѭ������Ҳ�ϲ��LiMn2O4��ѭ�����ܺ��������д������������д���һ��������Դ�1997��PADHI��[1]�״���������ʯ�ṹ��LiFePO4��Ϊ����ӵ������������������θĽ������LiFePO4�����ܳ�Ϊ�о��ȵ㡣
LiFePO4����170 mA?h/g�����۱�������3.4 V (vs Li+/Li)�ĸ߷ŵ��ѹ�������ѭ�����ܺ����ȶ��ԣ�ԭ������Դ�ḻ�������ŵ㣬��Ϊ���������ӵ����������֮һ�������ʯ�ṹ��LiFePO4��������ͬʱҲ���ڵ��ӵ����ʺ��������ɢ���ʵ͵�ȱ�㣬���²����ڴ������/�ŵ�ʱ�����ͣ�ѭ�������½����谭��LiFePO4�������ϵ���ҵ�������ԣ�Ŀǰ��LiFePO4���о���Ҫ�������Щ������и����о�������������ĩ����[2-4]��̼����[5-8]�Ͳ��Ӹ��ֽ�������[9-13]�ȡ����У�̼�������������л���Ϊ̼Դ���л����ڶ������ո����£����ѽ�Ϊ����ϸС��̼�����ȷֲ���LiFePO4���棬������߲��ϵĵ��ӵ絼�ʡ�ͬʱ�����ȷֲ���̼������Ч����LiFePO4�����ij��Ӷ�����������LiFePO4�����е���ɢ���ʣ��Ľ����ϵĵ绯ѧ����[14]��������Ϊ̼Դ������̼�����ķ�ʽ���Ľ�LiFePO4�������ϵ����ܡ�LiFePO4�������ϵĺϳɷ�����Ҫ�й��� ��[15]���ܽ�-������[16]��ˮ�ȷ�[17]��Һ�������[18]�����ϳɷ�[19]�ȡ�Ŀǰ����ҵ�ϴ��ò����������ڿ��ƵĹ���ϳɷ�����ԭ�������FeC2O4?2H2OΪ��������FeSO4?7H2O��Ϊ��Դ���ϳ�LiFePO4�������ϵ���ع���[20-21]���б���������������ͨ����Һ�����ϳ�ǰ����FePO4����ֱ���Ʊ�LiFePO4��Ϊ�˸���LiFePO4�����ܣ����������ɱ������ڹ�ҵ�����������߲�������ԭ����FeSO4?7H2OΪ��Դ��ͨ�����෨�ϳɵ绯ѧ����������̼����LiFePO4/C���ϲ��ϣ����о�LiFePO4/C���ϲ��ϵĽṹ����ò�͵绯ѧ���ܡ�
1 ʵ��
��n(FeSO4��7H2O):n(NH4H2PO4):n(Li2CO3)=1:1:0.5��ԭ�ϻ�����м���ռ���ղ���5%̼���������ǣ��������������ĥ���У���ND2-1L�ͱ�Ƶ����ʽ��ĥ��(�Ͼ��ϴ������������˾)��ĥ3 h������ĥ��Ļ��������������������յĸ��¹�ʽ¯��350 ���±���8 h����ȴ�����£��ٽ�Ԥ���ղ�����ĥ3 h��������Ȼ��������Ar��H2�����Ϊ95:5��Ar��H2������յĸ��¹�ʽ¯�У���700 �決��15 h���������º���ĥ����37 ��mɸ���õ�LiFePO4/C���ϲ��ϣ���Ϊ��ƷA��
��Ϊ�Աȣ���FeC2O4��2H2OΪ��Դ�����ô�ͳ����ϳɷ�[14]�ϳ�LiFePO4/C���ϲ��ϣ���Ϊ��ƷB��
���ձ���ѧD/max-3C��X����������(XRD)����Ʒ�������������ʹ��Cu K���У���=0.154 056 nm��ʯī��ɫ�����ܵ���100 mA���ܵ�ѹ50 kV��ɨ��Ƕ�Ϊ10��~70��(2��)��ʹ���ձ�JEOL��˾JSM-5600LV��ɨ���������(SEM)�۲���Ʒ�Ŀ�����С�ͱ�����ò��
��NMPΪ�ܼ�����LiFePO4/C����Ȳ�ں�PVDF��������85:10:5��Ͼ��ȳ�������Һ��Ϳ����2025����ֿ�ʽ��ؿ��ϣ�120 ����ո���20 h����Celgard2400�۱�ϩ���ĤΪ��Ĥ�����ҺΪ1 mol/L LiPF6��̼����ϩ��(EC)�Ͷ��һ�̼����(DEC)�Ļ��Һ(V(EC):V(DEC)=1:1���������ǹ�˾)���Խ����ƬΪ�������ڳ������������������װ�ɿ�ʽ��ء�
��������������������˾������NEWARE��ز���ϵͳ���г�ŵ����ܲ��ԣ���ѹ���Է�ΧΪ2.3~4.2 V�����Ϻ�����������˾������CHI660�绯ѧ����վ����ѭ�������ͽ����迹���ԣ�ѭ���������Ե�ѹ��ΧΪ2.3~4.2 V��ɨ��Ϊ0.1 mV/s�������迹���Ե�Ƶ�ʷ�ΧΪ10 mHz~100 kHz���Ŷ���� ��5 mV��
2 ���������
ͼ1��ʾΪ��ͬ��Դ�ϳɵ�LiFePO4/C��Ʒ��XRD���Լ�LiFePO4�ı�XRD�ס���1����Ϊ��FeSO4��7H2O��Ϊ��Դ�ϳɵ�LiFePO4/C���ϲ�����ƷA����FeC2O4��2H2OΪ��Դ�ϳɵ�LiFePO4/C���ϲ�����ƷB�ľ��������;�������Աȣ���Ȼǰ�ߵľ��������С�ں��ߵģ��������LiFePO4��ֵ���������ͼ1�п��Կ�������ƷA��B�����������λ�þ���LiFePO4�ı�ͼ��(PDF��81-1173)���Ǻϣ�����������ϵ��Pnma�ռ�Ⱥ����ƷA��B������嶼�ܼ���˵�������ֲ��ϵĽᾧ�ȶ��ܸߡ����⣬Ԫ�ط����Dz����ƷA��B�ĺ�̼���ֱ�ԼΪ3.36%��3.74%��������ƷA��B��������о�û�г���̼����������壬����������̼������̼���ڻ���̼�����ϵ���ɵġ�
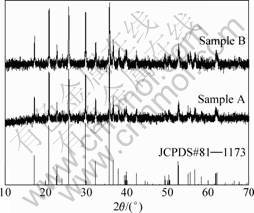
ͼ1 LiFePO4/C��Ʒ��XRD��
Fig.1 XRD patterns of LiFePO4/C samples
��1 LiFePO4/C��Ʒ�ľ�������
Table 1 Lattice parameters of LiFePO4/C samples
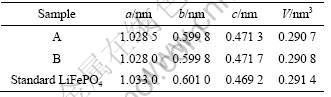
�����������϶��ԣ������һ�����ӺͶ������ӵĴ�С��������֮��Ľ�Ϸ�ʽ�Բ��ϵ�����Ӱ��ܴ�Ϊ�˱Ƚϸ���Ʒһ�����ӵĴ�С�����ݾ�����С����������֮��Ĺ�ϵ����Scherrer��ʽ�ɽ��м��㣺
D=Kl/(��1/2cos��) (1)
ʽ�У�D������ֱ�ڷ��侧��ľ���ƽ�����ȣ���1/2���������ֵ��߿��Ŀ����̶ȣ���Ϊ������ǣ���Ϊ����X���߲���(��=0.154 059 8 nm)��K����Scherrer�������뾧����״���¡�D�Ķ����йأ�Kȡ0.9��ѡȡ��������ǿ����������ľ���(311)���м��㣬�ɵø�����ƽ������DA=36 nm��DB=25 nm��
������Դ�ϳɵ�LiFePO4/C��Ʒ��SEM����ͼ2��ʾ����ͼ2�п��Կ�����������Դ�ϳɵIJ��ϵĿ���������������״�����Ե����ž۷�����������һ�����Ӿۼ���һ�������ϴ�Ķ������ӣ����������֮��ĽӴ��ȽϽ��ܣ�̼��ɢ��LiFePO4������Χ���γɵ���̼������Ч����߲��ϵĵ����ԡ���ƷA��һ�����ӳߴ�Ϊ40~50 nm���žۺ��γɵĶ������ӳߴ�Ϊ200 nm���ң�����ƷB������һ�����ӳߴ�Ϊ30~40 nm���žۺ��γɵĶ�����������100~150 nm����ˣ�һ�����ӵ�������Scherrer��ʽ����õ���ֵ�������Ǻϡ�

ͼ2 LiFePO4/C��Ʒ��SEM��
Fig.2 SEM images of LiFePO4/C samples: (a) Sample A; (b) Sample B
ͼ3��ʾΪ������Դ�ϳɵ�LiFePO4/C��ƷA��B��0.1C���������µij�ŵ����ߡ���ͼ3�п��Կ�����������Ʒ�ij�ŵ����߶�����һ�����Եij�ŵ�ƽ̨����Ӧ����LiFePO4��FePO4����֮���ת����Ӧ����
�����̣�
LiFePO4-xLi+-xe��xFePO4+(1-x)LiFePO4 (2)
�ŵ���̣�
FePO4+xLi++xe��xLiFePO4+(1-x)FePO4 (3)
��ƷA���״γ��������ͷŵ�������ֱ�Ϊ152.2 mA?h/g��151.1 mA?h/g�������Ч�ʸߴ�99.3%����ƷB���״γ��������ͷŵ�������ֱ�Ϊ156.8 mA?h/g��155.5 mA?h/g�������Ч��Ϊ99.2%����ƷA���״ηŵ�����������ƷB���Եͣ�����ƷA�ķŵ����߸�Ϊƽ̹���ŵ��λƽ̨���Ա���ƷB�ĸߣ��ɼ���ƷA������ƷB���и��ߵı���������ƷA�ij��ƽ̨������ƷB�ģ�����ƷA�ķŵ�ƽ̨������ƷB�ģ�˵����ƷA�ĵ缫��������ƷB��С����ƷA����ƷB���и��õķ�Ӧ�����ԣ�������ƷA���ܾ��и��õ�ѭ�����ܡ�

ͼ3 ��ƷA��B���״γ�ŵ�����
Fig.3 Initial charge-discharge curves of samples A and B
��ƷA��B��0.1Cѭ������������ͼ4��ʾ����ͼ4�ɿ�������0.1C���ʷŵ������£���ƷA���״ηŵ������Ϊ151.1 mA?h/g��ѭ��100�κ�����Ϊ148.9 mA?h/g������������Ϊ98.5%����ƷB���״ηŵ������Ϊ155.5 mA?h/g��ѭ��100�κ�����Ϊ149.6 mA?h/g������������Ϊ96.2%��ͬʱ���Ӳ�ͬ�ŵ籶���µ�ѭ����������(��ͼ5)�Ͽ��Կ�������Ȼ��0.1C��0.5 C��1C�ķŵ籶���£���ƷA�ķŵ����������ƷB���Եͣ�������ѭ���ȶ���������ƷB�ġ���5C�߱��ʷŵ�ʱ����ƷA�ķŵ��������ѭ���ȶ��Ծ�������ƷB�ġ���ƷA��5C�״ηŵ�����Ϊ105.9 mA?h/g��ѭ��30�κ������Ըߴ�105.2 mA?h/g������ƷB��5C�״ηŵ�����Ϊ101.2 mA?h/g��ѭ��30�κ�������Ϊ95.7 mA?h/g��
ͼ6��ʾΪ��ƷA��B��0.1 mV/sɨ���µ�ѭ���������ߡ���ͼ6�п��Կ�����������Ʒ������״���Ƶ�ѭ���������ߣ�˵������������ͬ��FeԴ�Ʊ�LiFePO4/C����������Ʒ������ͬ�ĵ缫��Ӧ������������Ʒ��ѭ�����������϶�����һ�ԱȽ϶ԳƵ�������ԭ�壬���ֳ����͵����෴Ӧ�����������������Ӧ��������LiFePO4����﮹��̣���ԭ���Ӧ��������LiFePO4��Ƕ﮹��̡�����ƷA��������ͻ�ԭ����λ��С����ƷB�ģ���˵����ƷA�ķ�Ӧ�����Ը�����ƷB�ģ���ѭ�������У���ƷA��ѭ���ȶ��Խ�������ƷB�ģ�����ͼ5���ڲ�ͬ�ŵ籶���µ�ѭ�����ܲ��Խ��һ�¡�
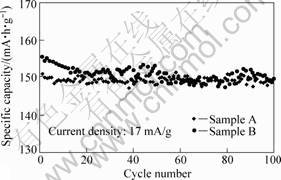
ͼ4 ��ƷA��B��0.1Cʱ��ѭ����������
Fig.4 Cycle performance curves of samples A and B at 0.1C
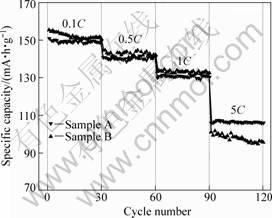
ͼ5 ��ƷA��B�ڲ�ͬ�ŵ籶���µ�ѭ����������
Fig.5 Cycle performance curves of samples A and B at different discharge rates
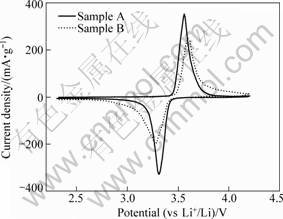
ͼ6 ��ƷA��B��ɨ������Ϊ0.1 mV/sʱ��ѭ����������
Fig.6 Cyclic voltammograms of samples A and B at scan rate of 0.1 mV/s
Ϊ�˽�һ���о����ϵĵ绯ѧ���ܣ�����ƷA��B�������˵绯ѧ�迹���ԡ�ͼ7��ʾΪ��ƷA��B�ĵ绯ѧ�迹��ͼ����2����Ϊͨ��ͼ8�ĵ�Ч��·��Ϻ�ó�����ز�������ͼ7�У�������ͼ�����ɸ�Ƶ���İ�Բ�͵�Ƶ����ֱ����ɡ���Ƶ���İ�Բ�Ƿ����ڵ����/������缫����ĵ�ɴ��䷴Ӧ��������迹Rct����Ƶ����ֱ�������������������缫������ɢ�������Warburg�迹(Rw)������Ƶ������ʵ��Ľ���һ����Է�ӳ����Һ����Rs�������弰����������������֮���ŷķ����(R��)���ܺ�[22]��
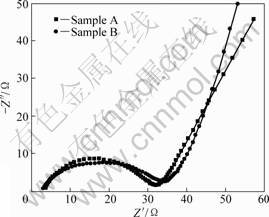
ͼ7 ��ƷA��B�Ľ����迹��
Fig.7 AC impedance spectra of samples A and B
![]()
ͼ8 ��ϵ绯ѧ�����迹ʵ�����ݵĵ�Ч��·
Fig.8 Equivalent circuit used for fitting experimental AC impedance date
��2 ��ϵó��ĵ�Ч��·��Ԫ������ֵ
Table 2 Values of elements in equivalent circuit

�ӱ�2�и���ͼ8�ĵ�Ч��·��Ϻ�����ݷ��֣���ƷA��B���ֲ��ϵĵ��ת���迹Rct�ֱ�Ϊ27.81 ?��31.77 ?����ƷA���и�С�ĵ��ת���迹���������ڿ˷���ŵ�����еĶ���ѧ���ƣ�ʹLiFePO4�Ļ��Կ�������Ƕ���ȵõ���ߣ��Ӷ�ʹ����ֳ����õĵ绯ѧ���ܡ�ͬʱ����ƷA��ŷķ����R���Դ�����ƷB�ģ���ԭ���������ƷA��̼�����Ե�����ƷB�������Դ�����ƷB�����¡�
3 ����
1) �����۵���������Ϊ��Դ�ϳɵ�LiFePO4/C�����������Լ۸�Ϲ�IJ�������Ϊ��Դ�ô�ͳ���෨�ϳɵ�LiFePO4/C�������Ͼ����е�һ�����ʯ�ͽṹ������Ϊ��������״���ᾧ�ȸߣ�̼������LiFePO4�����γɾ��ȵĵ�������
2)����������Ϊ��Դ�ϳɵ�LiFePO4/C�Ŀ����ߴ��Դ��ڲ�������Ϊ��Դ�ϳɵ�LiFePO4/C�ģ���ǰ�ߵķŵ�ƽ̨�ϸߣ��缫��ŵ缫��С�����ת���迹С��
3) �����£�����������Ϊ��Դ�ϳɵ�LiFePO4/C��0.1C��0.5C��1C���ʵķŵ�������ֱ��ȶ���150��140��130 mA?h/g���ң��������������Ϊ��Դ�ϳɵ�LiFePO4/C���൱����ǰ����5C���ʷŵ�ʱ��30��ѭ���������Ըߴ�105.2 mA?h/g��������30��ѭ����������Ϊ95.7 mA?h/g����ǰ�ߵ�ѭ�����ܺʹ��ʷŵ����ܾ����ں��ߵġ�
REFERENCES
[1] PADHI A K, NANJUNDASWAMY K S, GOODENOUGH J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. Journal of the Electrochemical Society, 1997, 144(4): 1188-1194.
[2] CHUNG S Y, BLOKING J T, CHIANG Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nature Materials, 2002, 1(2): 123-128.
[3] MI C H, CAO Y X, ZHANG X G, ZHAO X B, LI H L. Synthesis and characterization of LiFePO4/(Ag+C) composite cathodes with nano-carbon webs[J]. Power Technology, 2008, 181(3): 301-306.
[4] ������, ������. LiFePO4/Cu�����������ϵ��Ʊ����绯ѧ����[J]. ��ɫ����(ұ������), 2008(3): 48-50.
[5] ZHANG Ya-li, GAO Li-jun. Preparation and electrochemical performance of LiFePO4/Cu composite cathode material[J]. Nonferrous Metals(Extractive Metallurgy), 2008(3): 48-50.
[6] HSU K F, TSAY S Y, HWANG B J. Physical and electrochemical properties of LiFePO4/carbon composite synthesized at various pyrolysis periods[J]. Journal of Power Sources, 2005, 146(1/2): 529-533.
[7] ZHENG Jun-chao, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun, ZHOU Shao-yun. LiFePO4 with enhanced performance synthesized by a novel synthetic route[J]. Journal of Power Sources, 2008, 184(2): 574-577.
[8] KIM J K, CHERUVALLY G, AHN J H. Electrochemical properties of LiFePO4/C synthesized by mechanical activation using sucrose as carbon source[J]. Journal of Solid State Electrochemistry, 2008, 12(7/8): 799-805.
[9] ������, ��־��, ������. ������Դ��̼�Ȼ�ԭ���Ʊ�LiFePO4/C�ṹ�����ܵ�Ӱ��[J]. �й���ɫ����ѧ��, 2009, 19(8): 1462-1467.
[10] ZHONG Mei-e, ZHOU Zhi-hui, ZHOU Zhen-tao. Effects of Fe3+ sources on structure and properties of LiFePO4/C prepared by carbothermal reduction method[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(8): 1462-1467.
[11] WANG De-yu, LI Hong, SHI Si-qi, HUANG Xue-jie, CHEN Li-quan. Improving the rate performance of LiFePO4 by Fe-site doping[J]. Electrochimica Acta, 2005, 50(14): 2955-2958.
[12] LIU H, CAO Q, FU L J, LI C, WU Y P, WU H Q. Doping effects of zinc on LiFePO4 cathode material for lithium ion batteries[J]. Electrochemistry Communications, 2006, 8(10): 1553-1557.
[13] WANG G X, NEEDHAM S, YAO J, WANG J Z, LIU R S. A study on LiFePO4 and its doped derivatives as cathode materials for lithium-ion batteries[J]. Journal of Power Sources, 2006, 159(1): 282-286.
[14] HU Guo-rong, GAO Xu-guang, PENG Zhong-dong, DU Ke, TAN Xian-yan, Liu Yan-jun. Influence of Ti4+ doping on electrochemical properties of LiFePO4/C cathode material for lithium-ion batteries[J]. Transactions of Nonferrous Metals Society of China, 2007, 17(2): 296-300.
[15] SHIN H C, PARK S B, JANG H, CHUNG K Y, CHO W I, KIM C S, CHO B W. Rate performance and structural change of Cr-doped LiFePO4/C during cycling[J]. Electrochimica Acta, 2008, 53(27): 7946-7951.
[16] ������, �� ��, ���춫, ������, �� ��. ����ӵ����������LiFePO4/C���о���չ[J]. �����Ƽ�, 2008, 16(4): 56-59.
[17] ZHAO Lian-hai, LI Qi, QIAO Qing-dong, LIANG Zi-lei, SONG Yang. Research progress of LiFePO4/C cathode material for Li-ion batteries[J]. Science & Technology in Chemical Industry, 2008, 16(4): 56-59.
[18] DONG Y Z, ZHAO Y M, CHEN Y H, HE Z F, KUANG Q. Optimized carbon-coated LiFePO4 cathode material for lithium-ion batteries[J]. Materials Chemistry and Physics, 2009, 115(1): 245-250.
[19] �� ��, ����ϼ, �����, �˺��, ����Ȩ. ��Դ���ܽ�-�������Ʊ�LiFePO4/C�Ľṹ�͵绯ѧ���ܵ�Ӱ��[J]. �й���ɫ����ѧ��, 2008, 18(3): 546-550.
[20] LIN Yan, GAO Ming-xia, LI Yu-feng, PAN Hong-ge, LI Shou-quan. Effects of iron sources on structure and electrochemical properties of LiFePO4/C prepared by sol-gel method[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(3): 546-550.
[21] DOKKO K, KOIZUMI S, SHARAISHI K, KANAMURA K. Electrochemical properties of LiFePO4 prepared via hydrothermal route[J]. Journal of Power Sources, 2007, 165(2): 656-659.
[22] YANG Mu-rong, KE Wei-hsin, WU She-huang. Preparation of LiFePO4 powders by co-precipitation[J]. Journal of Power Sources, 2005, 146(1/2): 539-543.
[23] ZHANG Yong, FENG Hui, WU Xing-bing, WANG Li-zhen, ZHANG Ai-qin, XIA Tong-chi, DONG Hui-chao, LIU Ming-hao. One-step microwave synthesis and characterization of carbon-modified nanocrystalline LiFePO4[J]. Electrochimica Acta, 2009, 54(11): 3206-3210.
[24] ZHOU Bin-quan, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun. Novel synthesis of LiFePO4 by aqueous precipitation and carbothermal reduction[J]. Materials Chemistry and Physics, 2006, 98(2/3): 373-376.
[25] KUWAHARA A, SUZUKI S, MIYAYAMA M. High-rate properties of LiFePO4/carbon composites as cathode materials for lithium-ion batteries[J]. Ceramics International, 2008, 34(4): 863-866.
[26] SHIN H C, CHO W I, JANG H. Electrochemical properties of the carbon-coated LiFePO4 as a cathode material for lithium-ion secondary batteries[J]. Journal of Power Sources, 2006, 159(2): 1383-1388.
(�༭ ����)
������Ŀ��������Ȼ��ѧ����������Ŀ(20871101)���Ƽ������ƻ�������Ŀ(2009GJD20021)������ʡ�Ƽ����ص㹥��������Ŀ(2009WK2007)������ʡ��Ȼ��ѧ�������ϻ����ص�������Ŀ(09JJ8001)
�ո����ڣ�2009-11-01�������ڣ�2010-01-15
ͨ�����ߣ������ѣ����ڣ���ʿ���绰��0731-58293043��E-mail��wxianyou@yahoo.com


