��ʯ����ƺ�EDTA��2Na�λ�ѧ��ͭ��ϵ
֣�Ž�1, ��ΰ��1, ����2, ������1, ���º�1
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ, ���� ��ɳ, 410083;
2. ���ϴ�ѧ ���Ͽ�ѧ�빤��ѧԺ, ���� ��ɳ, 410083)
ժ Ҫ��
����(TART)��EDTA��2Na��˫��ϻ�ѧ��ͭ��ϵ�и����ضԳ�ͭ�ٶ��ȶ��Լ��Ʋ㸽������Ӱ�졣 ʵ��������: ��ѧ��ͭ�ٶ�������ϼ���ʯ����ƺ�EDTA��2Na��Ũ���Լ�ʩ��ʱ������Ӷ���С, ��������ͭŨ�ȡ� ��ȩŨ�ȡ� ��ҺpHֵ�ͷ�Ӧ�¶ȵ����Ӷ�����; ���Ӽ���, ����-����ड� �����軯�غ�PEG-1000�Զ�ͭ�ٶȵ�Ӱ���С, ����ͭ�Ʋ��������Ӱ��ϴ� �仯ѧ��ͭ�������Ϊ: CuSO4��5H2O����Ũ��Ϊ16 g/L, EDTA��2Na��Ϊ21 g/L, ��ʯ�����Ϊ16 g/L, ��ȩΪ5.0 g/L, �����軯��Ϊ70 mg/L, ��, ����-�����Ϊ8 mg/L, PEG-1000Ϊ1 g/L, pHֵΪ12.75, ��Һ�¶�Ϊ50 �档 �����������, ��ѧ��ͭ30 min�����öƲ㸽�������á� ��ۺ����Ҷ��ٴﵽ3.4 ��m/h�� ��ɨ��羵��Ƭ�ɼ�: �Ʋ����ƽ���� �⻬�� ����ϸ�¡�
�ؼ���: ��ѧ��ͭ; ��ͭ�ٶ�; �ȶ���; ABS����
��ͼ�����:TQ153.14 ���ױ�ʶ��:A ���±��: 1672-7207(2005)06-0971-06
Electroless copper plating system of potassium sodium tartrate and EDTA��2Na
ZHENG Ya-jie1, ZOU Wei-hong1, YI Dan-qing2, GONG Zhu-qing1, LI Xin-hai1
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. School of Materials Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Electroless copper plating system of potassium sodium tartrate and EDTA��2Na was investigated comprehensively. The results indicate that the copper deposition rate decreases with the increase of the concentration of potassium sodium tartrate and EDTA��2Na and plating time, and increases with the increase of the concentration of CuSO4��5H2O and HCHO, pH value and reaction temperature. Although the influences of ��, ����-Dipyridyl, K4[Fe(CN)6]��3H2O and PEG-1000 additives on the deposition rate are small, those of these additives on the surface qualities of copper film are great. The optimal conditions of the electroless copper plating system are as follows: CuSO4��5H2O is 5.0 g/L, EDTA��2Na is 21 g/L, potassium sodium tartrate is 5.0 g, HCHO is 16 ml/L, ��, ����-Dipyridyl is 8 mg/L, K4[Fe(CN)6]��3H2O is 70 mg/L, PEG-1000 is 1 g/L, pH value is 12.75, reaction temperature is 50 ��. Plating for 30 min in the bath, the copper deposition rate reaches 3.4 ��m/h. The SEM image demonstrates that the surface of copper film is smooth and fine.
Key words: electroless copper plating; deposition rate; stability; ABS substrate
��ѧ��ͭ�ѳ�Ϊ���洦������Ҫ����֮һ, �������ǽ�������������ķ�����Ƚ�, ��ѧ��ͭ����á� ��ķ���[1]�� ���ſ�ѧ���������õķ�չ, �����ԡ� �ͳɱ��Լ�����Ⱦ��ѧ��ͭ�ѳ�Ϊ�о����ȵ㡣 Ŀǰ, �г��Ϲ㷺Ӧ�õĻ�ѧ��ͭ��ϵΪ��ʯ����ƺ�EDTA��2Na��˫�����ϵ, �������ͭ�ٶȽ�Ϊ1.2~2.5 ��m/h, �Ʋ�ԼΪ1 ��m, ����ϵ�������ڻ�ѧ�Ʊ�ͭ�� ���ڹ����Ի�ѧ��ͭ, ���ٶ�Ҫ��ﵽ6~9 ��m/h, 30 min�ڶƲ�ﵽ2~3 ��m, �ü�����Ϊ��ѧ�ƺ�ͭ�� ��ѧ�ƺ�ͭ�ﵽ���Ϲ��ܻ�Ҫ����������, ���������ڶƲ���״��������ɶƲ���治���ȵ����ȱ�ݡ� ���, ���ٻ�ѧ��ͭһֱ�Dz��ϻ�ѧ���о��ص�[2, 3]�� F. J. Nuzzl[4]�о���һϵ�м��ټ�, ʹ��Һ���ֽϺ��ȶ���ͬʱ�����нϸ߳�ͭ�ٶ�; D.Vitkavage[5]������һ�����Ӽ�������߳�ͭ�ٶȺͶƲ�����; Kondo��[6]�о������Ҵ�������ϼ��Ļ�ѧ��ͭ; ��˨�õ�[7]�ô�����������ԭ��, ���Һ��ͭ�ٶȡ� ͭ����ɼ�������̬�ȷ�����������ص㡣 �ڴ�, ������EDTA��2Na�κ;�ʯ�����˫��ϼ���ѧ��ͭ��ϵΪ�о�����, �����˸������ضԸ���ϵ��ͭ�ٶȡ� �ȶ��Լ��Ʋ㸽������Ӱ��, ����������¸û�ѧ��ͭ��ϵ��ͭ�ٶȴﵽ3.4 ��m/h��
1 ʵ�鲿��
1.1 ʵ���������Լ�
����: ����ˮ��; ����pH��(pHS-25); ���Ϳ���ѹ����(WM-2H); �����
�Լ�: ��ˮ����ͭ; EDTA��2Na; ��ʯ�����; ��ȩ; ��������; �����軯��; PEG-1000; ��, ����-����ड�
1.2 ��������
��������Ϊ: ����(ABS)��ˮϴ�����Գ��͡�ˮϴ���ֻ���ˮϴ���к͡�ˮϴ��Ԥ��������⽺��ˮϴ����ѧ��ͭ��
1.3 �����������䷽
a. ������: ������ϴ���������Ϊ8%, �¶�Ϊ65 ��, ʱ��Ϊ5 min��
b. �ֻ�����: CrO3����Ũ��Ϊ400 g/L, H2SO4����Ũ��Ϊ350 g/L, �¶�Ϊ65 ��, ʱ��Ϊ10 min��
c. �к���: Na2SO3��������Ϊ10%, �¶�Ϊ30 ��, ʱ��Ϊ2 min��
d. Ԥ������: Ԥ��Һ��������Ϊ100%, �¶�Ϊ30 ��, ʱ��Ϊ3 min��
e. �����: Ԥ��Һ��������Ϊ95%, �λ���������������Ϊ5%, �¶�Ϊ30 ��, ʱ��Ϊ5 min��
f. �⽺����: �⽺Һ��������Ϊ10%, �¶�Ϊ30 ��, ʱ��Ϊ5 min��
1.4 ���ټ��������IJⶨ
a. ���ٵIJ��Է���: �ԶƼ��ߴ�Ϊ4 cm��4 cm(������)��ABS���Ͻ��л�ѧ��ͭ, ��ͭ30 min���������ⶨ����[8], ���㹫ʽ����:
��=(��m��104)/(�ѡ�A��t)��
����: ��Ϊ����, ��m/h; ��mΪ�ƺ�����, g; ��Ϊ��ͭ���ܶ�, g/cm3; AΪ�Ʋ����, cm2; tΪʩ��ʱ��, h��
b. ����������: ���չ���GB 5270��85���л��ߡ� �������顣
2 ���������
2.1 ��ʯ����ƺ�EDTA��2Na��Ũ�ȶԳ�ͭ�ٶȵ�Ӱ��
Ӱ�컯ѧ��ͭ��Һ�ȶ��Ժͳ�ͭ�ٶȵ�����Ҫ��������ϼ��ĺ����� ��K��ʾ��ʯ�������EDTA��2Na�ε���֮��������ͭ����֮�ȡ� ��Һ�е�CuSO4��5H2O ����Ũ��Ϊ12 g/L, ��ȩΪ5.0g/L, �����軯��Ϊ20 mg/L, ��, ����-����Ϊ10 mg/L, PEG-1000Ϊ1 g/L, pHֵΪ12.5����Һ�¶�Ϊ40 ��ʱ, ��ʯ�����(TART)��EDTA��2Na�ζԶ��ٵ�Ӱ����ͼ1��ʾ��
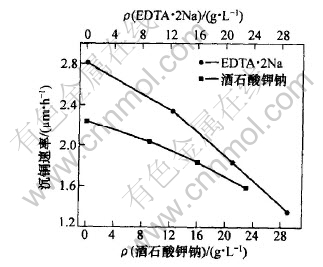
ͼ 1 ��ʯ����ƺ�EDTA��2Na������Ũ�ȶԶ��ٵ�Ӱ��
Fig. 1 Influence of TART and EDTA��2Na on deposition rate
��ͼ1��֪, ��EDTA��2Na������Ũ��Ϊ21 g/L, ��ʯ����Ƶ�����Ũ�ȷֱ�Ϊ0, 9.1, 16.0, 23.0 g/Lʱ, ��ͭ�ٶȷֱ�Ϊ2.23, 2.03, 1.83, 1.58 ��m/h�� ����ʯ���������Ũ��Ϊ0(K=1.18)ʱ, ��ͭ�ٶȿ�, ����Һ�ȶ��Բ�; ��ʯ�����Ũ��Ϊ16 g/L(K=2.35)ʱ, ���ٽϿ�, ͭ�����, ��������; ����ʯ�����Ũ��Ϊ23 g/L(K=2.85)ʱ, ��Һ�ȶ��Ժ�, ����ͭ�ٶȽ����� ���, ��ʯ����Ƶ���������Ũ��Ϊ16 g/L��
����ʯ���������Ũ��Ϊ16 g/L, EDTA��2Na�ε�����Ũ�ȷֱ�Ϊ0, 12.4, 21.0, 29.0 g/Lʱ, ��ͭ�ٶȷֱ�Ϊ2.81, 2.23, 1.83, 1.35 ��m/h�� ��EDTA��2Na�ε�����Ũ��Ϊ0(K=1.18)ʱ, ��ͭ�ٶȿ�, ����Һ�ȶ��Բ�; EDTA��2Na������Ũ��Ϊ29 g/L(K=2.85)ʱ, ��Һ�ȶ��Ժ�, ����ͭ�ٶ����� ����, EDTA��2Na�ε���������Ũ��Ϊ21 g/L(K=2.35)��
ʵ��������: KֵԽ��, ��ͭ�ٶ�Խ��, KֵԽС, ��ͭ�ٶ�Խ��; K=2.35ʱ, ��Һ�ȶ�, ���ٽϿ�, �Ʋ����, ������ǿ, ��������[9]�б�����K�����˷�Χ����һ�¡� EDTA��2Na�ζԶ��ٵ�Ӱ��Ⱦ�ʯ����Ƶ�Ӱ���, ��ΪlgKCu -EDTA��2Na��lgKCu �CTART��ֵ�ֱ�Ϊ18.8��6.51, EDTA��2Na�����Cu2+�������Ⱦ�ʯ����Ƶ�����ǿ, ����, ����EDTA��2Na������Ũ�ȼ���, ��Һ������Cu2+����Ũ������, Cu2+���ȩ��Ӧ�ٶȼӿ�, ��ʹ��ͭ�ٶ�����[9]��
2.2 ����ͭ�ͼ�ȩŨ�ȶԳ�ͭ�ٶȵ�Ӱ��
����������ͬ, ��ʯ���������Ũ��Ϊ16 g/L, EDTA��2Na������Ũ��Ϊ21 g/Lʱ, ����ͭ�ͼ�ȩŨ�ȶԳ�ͭ�ٶȵ�Ӱ����ͼ2��ʾ��
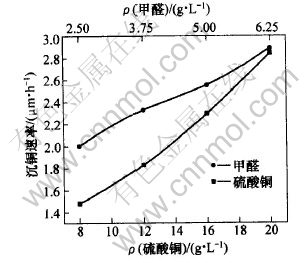
ͼ 2 ��ȩ������ͭ����Ũ�ȶԶ��ٵ�Ӱ��
Fig. 2 Influence of HCHO and CuSO4��5H2O on deposition rate
��ͼ2��֪, ��ȩ����Ũ��Ϊ3.75 g/L, ������ͭ����Ũ�ȷֱ�Ϊ8, 12, 16, 20 g/Lʱ, ��ͭ�ٶȷֱ�Ϊ1.48, 1.83, 2.33, 2.84 ��m/h�� ����ͭ����Ũ��Ϊ8 g/Lʱ, ��ͭ�ٶ����� �Ʋ㷢��; ����ͭ����Ũ��Ϊ16 g/Lʱ, ��ͭ�ٶȿ�, �Ʋ���۹���, ������ǿ; ����ͭ����Ũ��Ϊ20 g/Lʱ, ��Ƭ�����Ŷơ� ��Һ�ȶ��Բ�, �Ʋ�ᾧ�ֲ�, ���������� CuSO4��5H2O��������Ũ��Ϊ16 g/L��
��CuSO4��5H2O����Ũ��Ϊ16 g/L, ��ȩ����Ũ�ȷֱ�Ϊ2.5, 3.75, 5.0, 6.25 g/Lʱ, ��ͭ�ٶȷֱ�Ϊ2.0, 2.33, 2.55, 2.89 ��m/h�� ��ȩ����Ũ��Ϊ2.5 g/Lʱ, ���ٽ���, �Ʋ�����а���; ��ȩ����Ũ��Ϊ5.0 g/Lʱ, ��ͭ�ٶȽϿ�, ��Һ�ȶ�, �Ʋ���۽Ϻ�, ������ǿ; ��ȩΪ6.25 g/Lʱ, ��ͭ�ٶȿ�, ���Ʋ㸽������, ��۲�, �Ʋ�ᾧ�ֲ�, ��Һ���ȶ���
2.3 pHֵ�Գ�ͭ�ٶȵ�Ӱ��
����ʵ��������ͬ, ��ȩ����Ũ��Ϊ5.0 g/Lʱ, ��������Ũ��Ϊ150 g/L��NaOH��Һ�ı���ҺpHֵ�� pHֵ�Գ�ͭ�ٶȵ�Ӱ����ͼ3��ʾ��
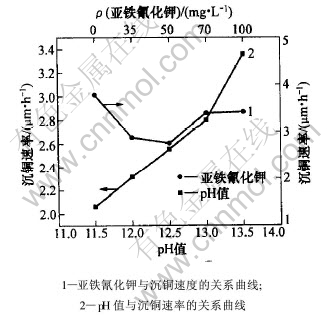
ͼ 3 pHֵ�������軯������Ũ�ȶԶ��ٵ�Ӱ��
Fig. 3 Influence of pH value and K4[Fe(CN)6]��3H2O content on deposition rate
��ʵ���֪, pH��12ʱ, ������, �Ʋ㷢��; pH=12.5~13.0ʱ, ��Һ�ȶ�, ��ͭ�ٶȽϿ�, �Ʋ���۹���, ������ǿ; pH=13.5ʱ, ��Һ���к�ɫCu2O����, �Ʋ����ֲڡ�
���ݻ�ѧԭ����֪, ��Һ��pHֵԽ��, ��Ӧ�ٶ�Խ��, ��pH>11ʱ��ȩ�缫��λE������ҺpHֵ�������¹�ϵ:
E��=+0.32-0.12pH��
��ȩֻ����pH>11.9ʱ�ž��л�ԭ����, ���ܷ�ӦΪ:
Cu2++2HCHO+4OH-��
Cu+2HCOO-+2H2O+H2��+2e��
����������Ӧ��, ��ȩ�ڻ�ѧ��ͭ�����л��������¸���Ӧ��
�������绯��Ӧ:
2HCHO+NaOH��HCOONa+CH3OH��
Cu+������:
Cu2++e��Cu+;
Cu++OH-��CuOH;
2CuOH��Cu2O+H2O��
Cu+���绯��Ӧ:
Cu2O+H2O��2Cu++2OH-;
Cu2O+H2O��Cu+Cu2++2OH-;
2Cu+��Cu+Cu2+��
pH>13.5ʱ��Һ�ȶ��������½�, ������Cu2O����Ӱ��Ʋ�����, ����ʹ��ȩ�����绯��Ӧ�� ��ѧ��ͭҺpHֵһ�������12~13[9]��
2.4 �����軯��Ũ�ȶԳ�ͭ�ٶȵ�Ӱ��
����������ͬ, ��ҺpHֵΪ12.75ʱ, �����軯������Ũ�ȶԳ�ͭ�ٶȵ�Ӱ����ͼ3��ʾ��
��ʵ���֪, ���������軯��ʱ, ��ͭ�ٶȿ�, ��Һ�ȶ��Բ�, �Ʋ����ֲڲ������; �����軯������Ũ��Ϊ35~50 mg/Lʱ, �Ʋ�������Ը���, ����������, ����ͭ�ٶȼ���; �����軯������Ũ��Ϊ50~70 mg/Lʱ, ��ͭ�ٶ������ӿ�, �Ʋ���۹����� ƽ��; �������������軯��Ũ�ȶԶ���������Ӱ���ҶƲ������� ��۱� �����軯����������Ũ��Ϊ70 mg/L��
ʵ��������: �����軯�ز������ȶ�����, ����������Ũ�ȵı仯�Գ�ͭ�ٶ������Ե�Ӱ�졣 ����Ҫԭ���������軯����ʹCu2+�Ļ�ԭ���λ���Ʋ�ʹ�伫�����ߵļ���������, �Ӷ��谭Cu2+�Ļ�ԭ����, ��ͭ�ٶȼ����������Ʋ�����[10]��
2.5 ��, ����-�����Ũ�ȶԳ�ͭ�ٶȵ�Ӱ��
�������軯������Ũ��Ϊ70 mg/L������ʵ��������ͬʱ, ��, ����-���������Ũ�ȶԳ�ͭ�ٶȵ�Ӱ����ͼ4��ʾ��
��ʵ���֪, ���Ӧ�, ����-�����ʱ, ��ͭ�ٶȿ�, ����Һ�ȶ��Բ�, �Ʋ�ɫ��, ����ֲ�; ��, ����-���������Ũ��Ϊ8 mg/Lʱ, �Ʋ������ ƽ��, ������ǿ, ��Һ�ȶ�; ��, ����-���������Ũ��Ϊ20 mg/Lʱ, �Ʋ�����к�ɫ�İߺۡ� ���, ��, ����-��������˵�����Ũ��Ϊ8 mg/L��
ʵ��������: ��, ����-�������ʹ��Һ���ȶ��Ժ�ͭ�������õ����Ը���[10, 11]�� ��Ϊ, �ڻ�ѧ��ͭ������, ��ȩ�������ǿ��Ʋ���, ��, ����-������ܹ����Ƽ�ȩ������, �Ӷ�����ͭ�ij������ʶ������Ʋ�����[12]��
2.6 ������Լ�PEG-1000����Ũ�ȶԳ�ͭ�ٶȵ�Ӱ��
��, ����-���������Ũ��Ϊ8 mg/L������ʵ����������ʱ, ������Լ�PEG-1000����Ũ�ȶԳ�ͭ�ٶȵ�Ӱ����ͼ4��ʾ��
ʵ��������: PEG-1000����Ũ�ȶԳ�ͭ�ٶ�����������, ����Ҫ�����Ǹ��ƶƲ���������С����ࡱ���á� ��Ϊ��ѧ��ͭ�ķ�Ӧ����������������, �Ʋ�������������, ��������Ե��¶Ʋ������½�, ��������Լ�PEG-1000�ܰ�����ͭ����Ӧ������Cu�۶����ƶƲ������[9, 13]�� �ӶƲ���������ж�PEG-1000��������Ũ��Ϊ1 g/L��
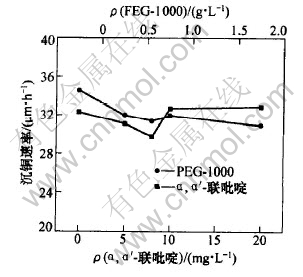
ͼ 4 ��, ����-����ऺ�PEG-1000����Ũ�ȶԶ��ٵ�Ӱ��
Fig. 4 Influence of ��, ����-Dipyridyl and PEG-1000 content on deposition rate
2.7 ��Ӧ�¶ȶԳ�ͭ�ٶȵ�Ӱ��
��������ʵ��õ���Ѷ�ͭҺ�����: CuSO4��5H2O����ΪΪ5.0 g/L, ��ȩΪ5.0 g/L, �����軯��Ϊ70 mg/L, ��, ����-����Ϊ8 mg/L, PEG-1000Ϊ1 g/L, pHֵΪ12.75�� �ڴ˶�Һ�н���ʵ��, ��Ӧ�¶ȶԳ�ͭ�ٶȵ�Ӱ����ͼ5��ʾ��
��ͼ5��֪, ��Ӧ�¶ȷֱ�Ϊ30, 40, 50, 60 ��ʱ, ��ͭ�ٶȷֱ�Ϊ2.27, 2.55, 3.43, 4.05 ��m/h�� ʵ��������: ��Ӧ�¶�Ϊ30 ��ʱ, ���ڳ�ͭ�ٶȽ��������¶Ʋ㷢��; ��Ӧ�¶�Ϊ60��ʱ, ��Һ�в���������ɫCu2O��ĩ, ��Һ�����ȶ�; ��Ӧ�¶�Ϊ40~50 ��ʱ, ��ͭ�ٶȽϿ�, �Ʋ���ۺ���, ��Һ�ȶ���
2.8 ʩ��ʱ��Գ�ͭ�ٶȵ�Ӱ��
��Һ��ɲ���, ����Ӧ�¶�Ϊ50 ��ʱ, ʩ��ʱ��Գ�ͭ�ٶȵ�Ӱ����ͼ6��ʾ��
��ͼ6��֪, ʩ��ʱ��ֱ�Ϊ5, 15, 30, 60 minʱ, ��ͭ�ٶȷֱ�Ϊ12.10, 5.56, 3.40, 2.33 ��m/h�� ʩ��ʱ��Ϊ5~15 minʱ, �Ʋ����ֲ�, ɫ������
ʵ��������: ��ͭ�ٶ�����ʩ��ʱ�����Ӷ����͡� ��Ϊ����ʩ��ʱ�������, ��Һ��Cu2+�ͼ�ȩŨ�Ƚ���, �����½�; ͬʱ, ���ڶƲ�Cu������, Cuԭ�Ӵ�����Ҳ��֮����, ���ټ���[14, 15]�� ���, �Ƚ϶���ʱҪ����ʩ��ʱ�䡣
���������������, ��ѧ��ͭ30 min��ԶƲ����SEM����, �����ͼ7��ʾ�� ��ͼ7��֪, �Ʋ����ƽ��, �ᾧ���ȡ� ϸ�¡�
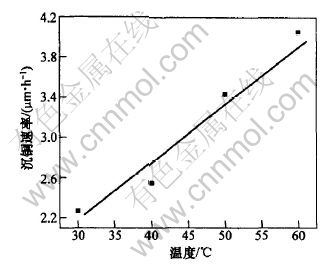
ͼ 5 ��Ӧ�¶ȶԶ��ٵ�Ӱ��
Fig. 5 Influence of reaction temperature on deposition rate
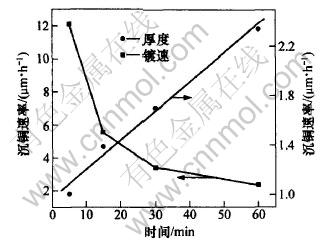
ͼ 6 ʩ��ʱ��Զ��ٺͺ�ȵ�Ӱ��
Fig. 6 Influence of time on deposition rate and thickness

ͼ 7 ���������ͭ�Ʋ��SEM��Ƭ
Fig. 7 SEM images of copper film under the best conditions
3 �� ��
a. ��ѧ��ͭ�ٶ����ž�ʯ������������Ӷ�����, ��EDTA��2Na������Ũ��Ϊ21 g/Lʱ, ��ʯ����ƴ�0���ӵ�23 g/L, ����ٴ�2.23 ��m/h����1.58 ��m/h; ��ѧ��ͭ�ٶ�����EDTA��2Na���������Ӷ�����, ����ʯ���������Ũ��Ϊ16 g/Lʱ, EDTA��2Na������Ũ�ȴ�0���ӵ�29 g/L, ����ٴ�2.81 ��m/h����1.35 ��m/h; EDTA��2Na�ζԶ��ٵ�Ӱ����ھ�ʯ����Ƶ�Ӱ��; ��ѧ��ͭ�ٶ���������ͭ�� ��ȩ�� ��ҺpHֵ�ͷ�Ӧ�¶ȵ����Ӷ�����, ����ʩ��ʱ������Ӷ����͡�
b. ���Ӽ���, ����-����ड� �����軯�ء� PEG-1000�Զ��ٵ�Ӱ�첻��, ���ԶƲ������������нϴ�Ӱ�졣
c. ��ʯ����ƺ�EDTA��2Na��˫�����ϵ��ͭҺ���������: CuSO4��5H2O����Ũ��Ϊ16 g/L, EDTA��2Na��Ϊ21 g/L, ��ʯ�����Ϊ5.0 g/L, ��ȩΪ5.0 g/L, �����軯Ϊ70 mg/L, ��, ����-�����Ϊ8 mg/L, PEG-1000Ϊ1 g/L, pHֵΪ12.75, ʩ���¶�Ϊ50 �档
d. ����������»�õĶƲ���ۺ���, ����ƽ��, ����ϸ��, ��ѧ��ͭҺ�ȶ�, �������ﵽGB 5270��85��, ���ٴﵽ3.4 ��m/h��
�����:
[1]Deckert C A. Electroless copper plating a review: part ��[J]. Plating and Surface Finishing, 1995, 82(2): 48-50.
[2]�ܺ�ƽ, ���Ե�, �齨��, ��. ��ѧ��ͭ�Ľ�չ[J]. ���漼��, 2002, 31(2): 5-6.
XIONG Hai-ping, XIAO Yi-de, WU Jian-hua, et al. Development of electroless copper plating[J]. Surface Technology, 2002, 31(2): 5-6.
[3]Mandich N V, Krulik G A. The evolution of process: fifty years of electroless nickel[J]. Metal Finishing, 1992, (5): 25-27.
[4]Nuzzi F J. Accelerating the rate of electroless copper plating[J]. Plating and Surface Finishing, 1998, 73(1): 52-54.
[5]Vitkavage D, Paunovic M. Maximum rate of the cathodic reaction in electroless copper deposition[J]. Metal Finishing, 1983, 73(4): 48-50.
[6]Kondo K, Shikawa J I. Electroless copper plating in the presence of excess triethanol amine[J]. Electrochem Soc, 1990, 137(6): 1859-1860.
[7]��˩��, �����. ��ѧ��ͭ�¹��ռ����ڵ��ӹ�ҵ�е�Ӧ��[J]. ���漼��, 2000, 29(6): 41-46.
BAI Shuan-tang, WANG Yu-ping. A new electroless copper plating technique and the application in electronic industry[J]. Surface Technology, 2000, 29(6): 41-46.
[8]��ѧ��, ������. ��ѧ�Ƽ���[M]. �ɶ�: �Ĵ���ѧ����������, 1985.
WU Xue-gao, LI Ming-hua. Electroless Plating Techonology[M]. Chengdu: Sichuan Science and Technology Press, 1985.
[9]����. ��ѧ��ʵ�ü���[M]. ����: ��ѧ��ҵ������, 2004.
LI Ning. Practical Electroless Plating Techonology[M]. Beijing: Chemical Industry Press, 2004.
[10]����, ������, ������, ��. ���Ӽ��Ի�ѧ��ͭ��Ӱ��[J]. ���ϱ���, 1997, 30(1): 91-93.
DONG Chao, DONG Gen-ling, ZHOU Wan-zhen, et al. The effect of additives on electroless copper plating[J]. Materials Protection, 1997, 30(1): 91-93.
[11]Yuri L, Roger P, Karen M. New plating bath for electroless copper deposition on sputtered barrier layers[J]. Microelectronic Engineering, 2000, 50: 441-447.
[12]Oita M, Matsuoka M. Deposition rate and morphology of electroless copper film from solutions containing ��, ����-Bipyridyl[J]. Electrochimica Acta, 1997, 42(9): 1435-1440.
[13]LIN Yi-mao, YEN Shi-chern. Effects of additives and chelating agents on electroless copper plating[J]. Applied Surface Science, 2001, 178(1-4): 116-126.
[14]Hanna F, Hamid Z A, Aal A A. Controlling factors affecting the stability and rate of electroless copper plating[J]. Materials Letters, 2004, 58(1-2): 104-109.
[15]�Ű�ά, ������, ������, ��. ʩ�ƹ��ղ����Ի�ѧ�Ƴ������ʵ�Ӱ��[J]. ����뻷��, 1999, 19(5): 15-22.
ZHANG Bang-wei, HU Wang-yu, WANG Ling-ling, et al. Effects of plating process parameters on electroless deposition rate[J]. Electroplating and Pollution Control, 1999, 19(5): 15-22.
�ո�����:2005-01-15
�����: ֣�Ž�(1959-), ��, ���ϳ�����, ��ʿ, ����, ����ʪ��ұ�� ��ѧ�ơ� �����������о�
������ϵ��: ֣�Ž�, ��, ����, ��ʿ; �绰: 0731-8876621(O); E-mail: ZZYYJJ01@yahoo.com.cn
ժҪ: �о��˾�ʯ�����(TART)��EDTA��2Na��˫��ϻ�ѧ��ͭ��ϵ�и����ضԳ�ͭ�ٶ��ȶ��Լ��Ʋ㸽������Ӱ�졣 ʵ��������: ��ѧ��ͭ�ٶ�������ϼ���ʯ����ƺ�EDTA��2Na��Ũ���Լ�ʩ��ʱ������Ӷ���С, ��������ͭŨ�ȡ� ��ȩŨ�ȡ� ��ҺpHֵ�ͷ�Ӧ�¶ȵ����Ӷ�����; ���Ӽ���, ����-����ड� �����軯�غ�PEG-1000�Զ�ͭ�ٶȵ�Ӱ���С, ����ͭ�Ʋ��������Ӱ��ϴ� �仯ѧ��ͭ�������Ϊ: CuSO4��5H2O����Ũ��Ϊ16 g/L, EDTA��2Na��Ϊ21 g/L, ��ʯ�����Ϊ16 g/L, ��ȩΪ5.0 g/L, �����軯��Ϊ70 mg/L, ��, ����-�����Ϊ8 mg/L, PEG-1000Ϊ1 g/L, pHֵΪ12.75, ��Һ�¶�Ϊ50 �档 �����������, ��ѧ��ͭ30 min�����öƲ㸽�������á� ��ۺ����Ҷ��ٴﵽ3.4 ��m/h�� ��ɨ��羵��Ƭ�ɼ�: �Ʋ����ƽ���� �⻬�� ����ϸ�¡�
[2]�ܺ�ƽ, ���Ե�, �齨��, ��. ��ѧ��ͭ�Ľ�չ[J]. ���漼��, 2002, 31(2): 5-6.
[7]��˩��, �����. ��ѧ��ͭ�¹��ռ����ڵ��ӹ�ҵ�е�Ӧ��[J]. ���漼��, 2000, 29(6): 41-46.
[8]��ѧ��, ������. ��ѧ�Ƽ���[M]. �ɶ�: �Ĵ���ѧ����������, 1985.
[9]����. ��ѧ��ʵ�ü���[M]. ����: ��ѧ��ҵ������, 2004.
[10]����, ������, ������, ��. ���Ӽ��Ի�ѧ��ͭ��Ӱ��[J]. ���ϱ���, 1997, 30(1): 91-93.
[15]�Ű�ά, ������, ������, ��. ʩ�ƹ��ղ����Ի�ѧ�Ƴ������ʵ�Ӱ��[J]. ����뻷��, 1999, 19(5): 15-22.


