���±�ţ�1004-0609(2009)04-0744-05
��ϸ�������������������б�����Լ������û���
����1��������2������1
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083��
2. ���ϴ�ѧ ��ѧ����ѧԺ����ɳ 410083)
ժ Ҫ��
���ڳ�ϸ�����������ȷֲ����ߺͺ�����ף�ͨ�������������3 700~3 000 cm-1�������ַ���ϣ��о��˸�������б�����Լ��Գ�ϸ�������ȵ�Ӱ����ɡ�������������������Լ������ϸ�����������������ļ��ٲ�����6%�������ӱ�����Լ�ʱ��������������99.98%��ͬʱ��������������С��0.1 ��m�������������ڱ�����Լ���ԭ��������е��ž۳̶Ƚ�С��������Ϊ0.5~10 ��m�������ž۽����ԡ����������������������������Լ�A��B����1 310 cm-1����������O��H�����壬ͬʱ�����O��H��32.3%(��������)�ֱ�������39.88%��35.95%������Ӽ�ϵ�O��H�������36.65%�ֱ������29.78%��27.79%����˵��������Լ��ļ�������������Ʒ��Ӽ�O��H���γɣ��Ӷ��ɽ������ӵ��ž۳̶ȡ�
�ؼ��ʣ�
������Լ�����ϸ����������������
��ͼ����ţ�TF 821 ���ױ�ʶ�룺 A
Agglomeration mechanism of surfactant of ultra-fine Al(OH)3 in drying process
LIU Gui-hua1, ZHANG Yu-min2, LI Xiao-bin1
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: The influence of surfactant on the particle size and agglomeration mechanism was studied in term of the particle numbers calculated from particle size distribution and multi-peak fitting of IR spectra. The results show that the particle number reduces less than 6% with addition of surfactant, while that reduces 99.98% without adding surfactant. The coarse particle (0.5-10 ��m) is much easier to be agglomerated than the ultra-fine particle(less than 0.1 ��m), which maybe due to the easy absorption of surfactant for the ultra-fine particle. The results from IR show that the characteristic peak appears at 1 310 cm-1 accounting for free O��H when surfactant is added, and then free O��H increases from 32.30% (mass fraction) to 39.88% and 35.95%, respectively, and O��H in association molecular reduces from 36.65% to 29.78% and 27.79%, respectively. This shows that the agglomeration is inhibited by reducing the amount of O��H in association molecules with addition of surfactant in the drying process.
Key words: surfactant; ultra-fine Al(OH)3 powder; agglomeration mechanism
ʪ��ѧ���Ʊ���ϸ�����Ƿ����Ʊ�����Ҫ��������Ҫ�ŵ�Ϊ��Ӧ�������ơ��ɱ��͡��ײ�ҵ���ȣ�����Ҫȱ�������Ӻ��������ž�[1-4]��Ŀǰ�������ž۵Ļ����������֣���ëϸ���������ۡ�������ۡ���ѧ�����ۺ;������۵�[1-2, 5-9]����Һ���м��������Լ����Կ�����������ʱ��������������ʪ������˺��˱���ˮ�ʸ�(������С��2 ��mʱʪ�����������庬ˮ�ʴ���70%)������ڳ����������������ž۷dz����ء�Ŀǰ�����÷dz�����������(������䶳����ͳ��ٽ����ȷ���[10-11])ʵ�ֳ�ϸ����ĸ����ʪ�����������м��������ı�����Լ���Ҳ�����ڳ�����������¿������ӵ��ž۳̶ȡ�������Լ�������һ�㶨�Եع���ڱ�����Լ��������ı������ӵı�������(��������)���γɿռ�λ��[12-14]�������ִ���⼼��(��ⶨ�ȵ�㡢Zeta��λ��IR��DRIFRS��)Ҳ֤��������Լ������ӷ�����������ѧ�� ��[15-18]������Щ�о������û������ؽ��ͱ�����Լ���������������ӷ�����Щ����ã������������ò��������ž۵Ĺؼ����������߽�ϳ�ϸ�����ڸ���������������ı仯��ͨ���ȽϷ���������Լ�����������ı仯���ɣ��Ա�����Լ�Ӱ�������ž۵Ļ��������˳���������
1 ʵ��
������������������������ˮ�У����Ƴ�c(Al3+)Ϊ0.5~1.0 mol/L����������Һ����ȡһ���������������Һ���ڽ������������60 �����һ����ؼ���ϡ��ˮ(Լ3 mol/L)��pHֵԼΪ5.5ʱֹͣ����Һ�����˺�õ���ϸ���������˱���������ȡһ�ݽ��и���ⶨ�˱��ĺ�ˮ����Ȼ������ȡһ���˱������������Լ���Ϻ���101A-1E�ķ��������(�Ϻ�ʵ������������˾)���и�����ⶨ���������Լ��벻�ӱ�����Լ�������������ȷֲ���
��ˮΪ��ɢ���ʣ�������SB2200�ͳ�����������(�Ϻ������ų�������˾��75 W)�з�ɢ15 min��Ȼ�����Mastersizer2000�������ȷ�����(Ӣ��������)�������ȷֲ���
����Nicolet��˾FT-IR��������ǡ���KBrѹƬ������16��ɨ�裬Ȼ����origion75�����Ժ�������зַ���ϣ�����3 700~3 000 cm-1����O��H�ı仯���ɡ�
2 ��������
2.1 ������Լ��Ը������������������Ӱ��
������Լ����ڽ����Ͼۼ����ܽ��ͽ����������Ӷ��ı��������ʡ�����������ʪ������ѡ���Եؼ����˱�����Լ�A��B������A�ĽṹΪHO�� R��SO3Na RΪ�����BΪ������ˮ�ĸ߷��ӻ����ƽ����Է�������ԼΪ10 000����Ҫ������Ϊ�Ȼ����ǻ���������Լ�������Ϊʪ�˱�������0.05%)����50���º��¸��������Լ��Է������ȷֲ����ߵ�Ӱ����ͼ1��ʾ��������Ʒ1Ϊԭʼ��Ʒ(ϴ�Ӻ���˱���û�и���)����Ʒ2��3��4Ϊ������Ʒ��
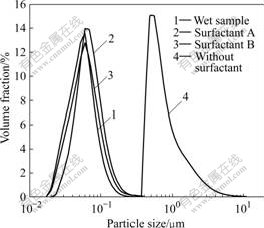
ͼ1 �����������б�����Լ�������������Ӱ��
Fig.1 Effect of surfactant on particle size in drying process
��ͼ1��֪������ͬ�IJ��������£����������Լ�A��Bʱ����������ȷֲ�������δ����ԭ�������ȷֲ���������һ�µġ�ԭ���ͼ���A��B������Լ����d0.5�ֱ�Ϊ58��63��72 nm��˵��������Լ��ļ�������ֹ���ӵ��žۡ�������ͬ�����£������������Լ�ʱ��������������ȷֲ�����������������ķ��������ƶ���d0.5=650 nm��˵�������ڸ�������з��������ص��žۡ�
Ϊ�˽�һ��������������������ž۵Ĺ��ɣ�������ԭʼ��������(Primary particle)�žۣ��������ȷֲ����ߣ��������������������ı仯���ɡ�������������������Ϊ�����Բ��ijһ����(Di)����ni�����ӣ���������µ����ӵ������Ϊ��
![]()
��ij����������ΪV�������������ӵ��������Ϊ��i(���ȷ�����Ϊ��֪)����
![]()
![]()
���豻�������������Ϊ1 g�����ܶ�Ϊ�ѣ�V��=1��
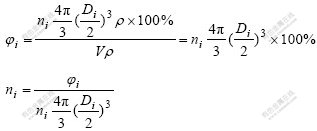
���������������м��㣬������Լ�������������Ӱ�����1���С�
��1 ������Լ��ڸ�������ж�����������Ӱ��
Table 1 Effect of surfactant on particle number in drying process
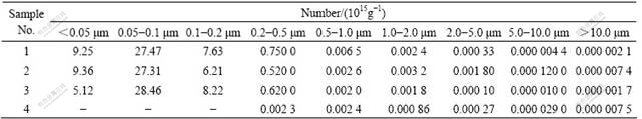
��1�еĽ���������������Ʒ1�����������Լ�(A��B)�����Ʒ2��3������������������ٷ��Ƚ�С�������������A����Ʒ2��������������Ʒ1����������������3.77%��������ϸ���ӱ����ܸߣ���������������Լ���ԭ��С��0.1 ��m���������仯���٣�0.5~10 ��m���Ӽ��ٷ�����Խϴ���10 ��m���������������ӣ�������������B����Ʒ3����������������5.99%��С��0.2 ��m���������仯���٣�1.0~2.0 ��m�������������ӣ������ӱ�����Լ�ʱ����Ʒ4��������������Ʒ1����������������99.98%��ͬʱС��0.2 ��m������ȫ����ʧ(���ž�)��0.2~1.0 ��m����������Ҳ�������٣�����1.0 ��m���������������ӵġ�
2.2 ���������O��H������ı仯����
��0~4 000 cm-1�ĺ������(��ͼ2)���з�����֪�����۱�����Լ��Ƿ���룬��4 000~3 000 cm-1��1 650 cm-1��740 cm-1��625 cm-1�������������塣��Щ��ֱ���O��H������O��H��������(��Ҫ�ǽᾧˮ�����)��O��H�������������������塣ͬʱ��������Լ��ļ������Ըı����ĺ�����ף�һ������ּ��������Ժ���ֵ���1 310 cm-1�壬�˷������Ϊ������O��H���������������塣��һ���棬��4 000~3 000 cm-1�䣬���ӱ�����Լ�ʱ����һ������ǿ�Ƚ����������ϴ�ķ塣��֮�Ա��Ǽ��������Լ�A��B�������ǿ�ȸߣ�������С��������[19-21]��֪������O��H�������������ʸߣ����μ���ǿ�ȵͣ��ϵ�O��H�������������ʵͣ����νϿ���ǿ�ȸߣ������Ŷ���Ӽ�ϳ̶ȵ����ӣ�O��H�������������С�ķ����ƶ������ڴ˿�����Ϊ�����ӱ�����Լ�ʱ�˱��ڸ�������д��ڽ϶�ĵ�O��H�������������Լ����������ӱ���ʣ��ۼ��������Լ�����øı���ԭ��������ˮ���Ӽ������ã��������ָ��������O��H�����µϵ�O��H�����仯��
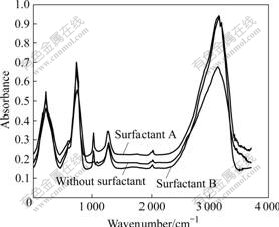
ͼ2 ������Լ��Ը�������������Ӱ��
Fig.2 Effect of surfactant on IR spectra of powder
�����������ۣ�ͨ����3 700~3 000 cm-1���� O��H��������зַ���ϣ��Ƚ��˸���O��H�ڸ�������еı仯���ɡ�������O��H��Ҫ�У�����������O��H�������O��H�����Ӽ�����������γɵ�O��H (������)������ӵ��γɵ�O��H (�ɽ�ǿ�������������������[20])��һ����ԣ�����O��H��������λ�ô���3 560 cm-1�����������O��H�����崦��3 420 cm-1����������ӵ�ʱO��H������λ����ɴ���3 220 cm-1��[19-20]���������߲���Origin75������3 700~3 000 cm-1�ĺ����������ϣ��ַ���ϵĽ����ͼ3��ʾ����������Ϊ3 700~3 000 cm-1���������Ͻ����ȫ���µ�ʵ���Ƿַ���ϵĽ����ͬʱ�����û��ּ������������Ĵ�С���ɰ붨���رȽϲ�ͬO��H�ı仯����(����2)��
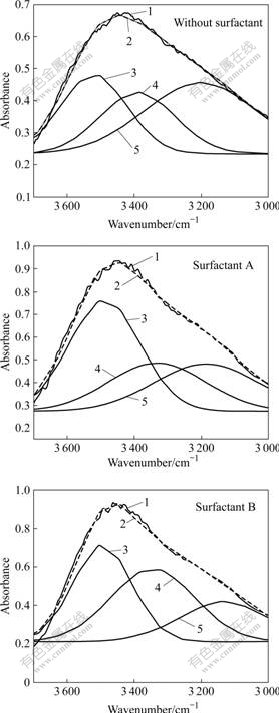
ͼ3 ��������ĺ�����ַ���ϵĽ��
Fig.3 Multi-peak fitting of IR spectra with or without surfactant: 1-Original IR spectrum; 2-Simulated IR spectrum; 3-Free O��H; 4-O��H in dimmer; 5-O��H in molecular association
��2 ������Լ���O��H����(�����)��Ӱ��
Table 2 Effect of surfactant on O��H peaks proportion
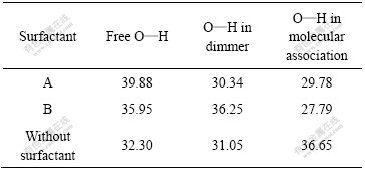
�ַ���ϵĽ��������һ���棬��3 700~3 000 cm-1�������������ϣ������������ԭ�����������һ�£����ϵ��R2������0.99��˵����������ǿɿ��ģ���һ���棬����ϵõ��������Ͻ��зַ���ϣ�����Ĵ�С��ͬ(����2)��û�м��������Լ�ʱ������O��H����������ռ������Խ���(32.30%)�����ڽ϶�ĵͲ�����������(36.65%)�������Ӽ���ڽ϶�ķ��Ӽ����(���ǻ���ˮ�γɹ��ۼ�)����Щ����ڸ�����������¶ȸߡ�ëϸ��̮���ȶ����������ӵ��žۣ�ʹ���������������١������������Լ�������O��H����������(39.88%��35.95%)��������ӵ��γɵ�O��H���Լ���(29.78%��27.79%)��˵������Ӽ���ڵ�������Լ������ڸ������������������ν��Ӳ�žۡ��ɴ˿�����Ϊ�����������Լ����������ı��˷��Ӽ���������ʽ��ʹ�÷��Ӽ�ϵ�������Լ��٣��Ӷ����������Ӽ���ž۳̶ȡ�
3 ����
1) ���������Լ������ϸ�����������������ļ��ٲ�����6%�������ӱ�����Լ�ʱ��������������99.98%�������������ϸ�����������л������С��0.1 ��m�����ž۳̶Ƚ�С��������Ϊ0.5~10 ��m�������ž۽����ԡ���˵�����������Լ��������������ڸ�������е��žۡ�
2) ������ޱ�����Լ�����ʱ�����������Լ�A��B����1 310 cm-1����������O��H�����壬ͬʱ�����O��H��32.3%�ֱ�������39.88%��35.95%������Ӽ�ϵ�O��H��36.65%�ֱ������29.78%��27.79%����˵��������Լ���Ҫ��ͨ�����ٷ��Ӽ�������������O��H���ﵽ���������ž۵�Ŀ�ġ�
REFERENCES
[1] ��־ǿ, ��С��, ��־��, ͯ ��, ����. ʪ��ѧ���Ʊ���ϸ��ĩ�����е��žۻ�������������[J]. ��ѧͨ��, 1999(7): 54-57.
LIU Zhi-qiang, LI Xiao-bin, PENG Zhi-hong, TONG Bin, LIU Gui-hua. The mechanism of agglomeration and control in the process of ultrafine powder prepared by wet chemical method[J]. Chemistry, 1999(7): 54-57.
[2] �����, �� ΰ, �� ��. �������ӵĸ��﷽���뼼����չ[J]. ������չ, 2006, 25(1): 20-24.
SONG Xi-jin, GONG Wei, WANG Jie. Progress of drying methods of nanoparticles[J]. Chemical Industry and Engineering Progress, 2006, 25(1): 20-24.
[3] ISHIZAKI C, RAHARJO P, SATO K, ISHIZAKA K. Mechanism of hard agglomerate formation in a high purity sub-micron ��-alumina powder[J]. Journal of Ceramic Society of Japan, 2001, 109(1265): 16-22.
[4] �� ��, �� �, �� ǿ. ����TiO2��������ı����������ž�״̬[J]. ������ѧ��, 1997, 12(3): 445-448.
SONG Zhe, GAO Lian, LI Qiang. Study on the surface status and agglomeration of TiO2 nano-powder[J]. Journal of Inorganic Materials, 1997, 12(3): 445-448.
[5] ALOK M, DOUGLAS M S, Agglomeration during the drying of fine silica powders, Part II: The role of particle solubility[J]. J Am Ceram Soc, 1997, 80(7): 1715-1722.
[6] SHI J L, GAO J H, LIN Z X, YAN D S. Effect of agglomerates in ZrO2 powder compacts on the microstructure development[J]. J Mater Sci, 1993, 28(2): 342-348.
[7] HENCH L, WEST J K. The sol-gel process[J]. Chem Rev, 1990, 90: 33-59.
[8] KALISZEWSKI M S, HEUER A H. Alcohol interaction with zirconia powder[J]. J Am Ceram Soc, 1990, 73(6): 1504-1509.
[9] SCHERER G W. Drying gels (I): general theory[J]. Journal of Non-crystalline Solids, 1986, 87(1/2): 199-225.
[10] ATSUSHI N, TOSHIHIRO M, SHIN-ICHI T, MASAHIKO T, TORU S, CHOA Y H, KOICHI N. Effect of supercritical drying method on microstructure and properties of Al2O3 composites reinforced with ultrafine SiC particulate[J]. Journal of the Ceramic Society of Japan, 1999, 107(5): 460-464.
[11] FUKASAWA T, DENG Z Y, ANDO M, OHJI T, GOTO Y. Pore structure of porous ceramics synthesized from water-based slurry by freeze-dry process[J]. Journal of Materials Science, 2001, 36(10): 2523-2527.
[12] �ƽ���, �� Կ, ��㤳�, ����ƽ, �� ��, �����. ���ž���������ﯵ��Ʊ���Ӧ��[J]. ������ѧ��, 2001, 5: 867-871.
JIU Jin-ting, GE Yue, ZHANG Shu-rong, LI Li-ping, TU Fan, ZHU He-sun. Preparation and application of agglomeration- free and nanoparticles zirconia[J]. Journal of Inorganic Materials, 2001, 5: 867-871.
[13] ��֥��, ŷ����, ��ϲ��, ���½�, ������. ������Լ�PEG�ڲ�������SnO2��ĩ�������Ʊ��е�����[J]. ���̹���ѧ��, 2005, 5(3): 305-308.
WEI Zhi-xian, OU Hai-feng, GONG Xi-jun, SUN Xin-jian, ZHU Zhen-xiao. Study on the function of additive-PEG in the preparation of Sb-doped SnO2 nano-powder via oxidative- coprecipitation[J]. The Chinese Journal of Process Engineering, 2005, 5(3): 305-308.
[14] FROST R, ZHU Huai-yong, WU P, BOSTROM T. Synthesis of acicular goethite with surfactant[J]. Materials Letters, 2005, 59(17): 2238-2241.
[15] ��õ��, �׳���, ��ʢ��, �� ��, �� ��. �ɿ�����TiO2���Ʊ�[J]. ������ѧѧ��, 2008, 24(12): 2287-2292.
HU Mei-long, BAI Chen-guang, XU Sheng-ming, XU Gang, LIANG Dong. Preparation of the size-controlled TiO2 with spherical morphology[J]. Acta Phys-Chim Sin, 2008, 24(12): 2287-2292.
[16] HU Y, DAI J. Hydrophobic aggregation of alumina in surfactant solution[J]. Minerals Engineering, 2003, 16: 1167-1172.
[17] UNWIN P J, RUSNACIK M E, KRESTA S M, NELSON A E. Effect of amine and thiod addition on the surface chemistry and agglomeration of fine Cu powders[J]. Colloids and Surface A: Physicochem Eng Aspects, 2008, 325(1/2): 72-80.
[18] TSANTILIS S, PRATSINIS S. Soft and hard agglomerate aerosols made at high temperature[J]. Langmuir, 2004, 20: 5933-5939.
[19] ������, ������. ʵ�ú������ѧ[M]. ����: �й�ʯ����ҵ������, 1982: 284.
WANG Zong-ming, HE Xin-xiang. Practical infrared spectra[M]. Beijing: China Petrolic Industry Press, 1982: 284.
[20] BELLAMY L J. ���ӷ��ӵĺ������[M]. ��άԫ, ����ʵ, ��. ����: ��ѧ������, 1976: 115.
BELLAMY L J. The infra-red spectra of complex molecular[M]. HUANG Wei-heng, NIE Cong-shi, transl. Beijing: Science Press, 1976: 115.
[21] �� ��. ����������ĺ����������[J]. ����ѧ�������, 2001, 24(3): 506-507.
ZHAO Hong. IR characteristics of oxide[J]. Spectroscopy and Spectral Analysis, 2001, 24(3): 506-507.
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2005CB623702)
�ո����ڣ�2008-06-11�������ڣ�2009-01-09
ͨѶ���ߣ�����������ʵ��ʦ���绰��0731-8830453��E-mail: Zhangym@mail.csu.edu.cn
ժ Ҫ�����ڳ�ϸ�����������ȷֲ����ߺͺ�����ף�ͨ�������������3 700~3 000 cm-1�������ַ���ϣ��о��˸�������б�����Լ��Գ�ϸ�������ȵ�Ӱ����ɡ�������������������Լ������ϸ�����������������ļ��ٲ�����6%�������ӱ�����Լ�ʱ��������������99.98%��ͬʱ��������������С��0.1 ��m�������������ڱ�����Լ���ԭ��������е��ž۳̶Ƚ�С��������Ϊ0.5~10 ��m�������ž۽����ԡ����������������������������Լ�A��B����1 310 cm-1����������O��H�����壬ͬʱ�����O��H��32.3%(��������)�ֱ�������39.88%��35.95%������Ӽ�ϵ�O��H�������36.65%�ֱ������29.78%��27.79%����˵��������Լ��ļ�������������Ʒ��Ӽ�O��H���γɣ��Ӷ��ɽ������ӵ��ž۳̶ȡ�


