�ӷ�������Һ����ȳ����Ʊ��ߴ�V2O5���о�
���ϴ�ѧұ���ѧ�빤��ѧԺ
ժ Ҫ��
���ſƼ��ķ�չ, ��Ӧ�����ϵ�����, �Է���Ʒ���ȵ�Ҫ��ҲԽ��Խ��, ���ԶԸߴ��Ⱦ����Ʊ��������о��Ǻ��б�Ҫ�ġ�����Ӱ�쾫��������һ����Ҫ����, ��ʯú�ᷰ������, ��������Һ�е�����李����γɸ��ӵ������ (�Ӷ���) , ���ﵽһ����ʱ, Ӱ������������������, ��ɷ���Ʒ���������ꡣ��ʯú�ᷰ���̵����ӽ�������ҺΪ��Һ, ��Ҫ���ʯú�ᷰ���ӽ�������������Ϊ, �����þ�γ������ӷ�������Һ����ȳ���, �Ʊ��ߴ�V2O5���о��������˳������еĻ���, �о���þ�μ�������pH���¶ȡ�ʱ������ضԳ���Ч����Ӱ�졣ʵ��������:��������������, þ�η�����Ч��ȥ��������Һ�е���, �����ʴﵽ96%����, ͬʱ�����Ч��ȥ��������Һ�е�Si, Fe, As������Ԫ��, ���V2O5�Ļ����ʴﵽ94%���ϡ���ѳ���������Ϊ:�¶�45��, ����ʱ��50 min, þ�μ�����Ϊԭ��Һ12%, pH=10.0��������Һ��50�������γ���, �õ���ƫ�������500����������¯������2 h, ���յõ���������������Ʒ�����ﵽ99.9%���ϡ�
�ؼ��ʣ�
��ͼ����ţ� TF841.3
�ո����ڣ�2010-10-30
�������ҿƼ�֧�żƻ���Ŀ (863) (2007AA06Z129) ����;
Removing Phosphorus from Sodium Vanadate Solution for Production of High-Purity V2O5
Abstract��
P was the main impurity in vanadium production since the formation of complexes with V and ammonium in the sodium vanadate solution during the process of extracting vanadium from stone coal, which resulted in unqualified V2O5 product.The complete removal of phosphorous from sodium vanadate solution obtained from the strip liquor of ion exchange in the extraction of vanadium from stone coal by magnesium salt precipitation was studied.The effects of addition amount of magnesium salt, pH, temperature and time on the removal of P were investigated, and the mechanism for the removal of P was also proposed.The results showed that the removal of P reached 96% under weak base condition.Other impurities, such as Si, Fe and As were also effectively removed.The optimum conditions for P removal were as follows: 12% feed solution of magnesium salt addition amount at 45 �� and pH 10.0 for 50 min.The ammonium salt was then added into filtrate at 50 �� after filtration, and the obtained ammonium vanadate was calcined in Muffle furnace at 500 �� for 2 h.The purity of final product V2O5 reached 99.9%.
Keyword��
dephorsphorization;high-purity;vanadium;stone coal;
Received�� 2010-10-30
�ҹ�ʯú�ᷰ�������о��Ǵ�20������60�������ʼ�ġ� ���ں���ʯú��������ɱȽϸ���, ���ĸ���״̬�ͼ�̬���ֶ���, ʯú�ᷰ���շ���Ҳ������ͬ�� ��ͳ���ƻ����շ�������Ի�����ɵľ��ƻ�������̭, �µ��ᷰ����Ӧ�˶����� �ܽ�Ŀǰʯú�ᷰ����, �������ɱ��ա� ������ ���ӽ�������ȡ�� ��ƫ����李� ������ȡ�����ȹ������, ����һ��Ʒ��Ϊ97%��99%�� �����ŷ�Ӧ�÷�Χ���ϵ��ؿ�, һЩ��ҵ���캽�ա� ���ӹ�ҵ�� �绯ѧ��ҵ�Է���Ʒ�Ĵ���Ҫ��Խ��Խ��, ���ԶԸߴ��Ⱦ����Ʊ��������о��Ǻ��б�Ҫ�ġ� P�Ǵ���Ȼ��һ�ֳ���Ԫ��, Ҳ��Ӱ�쾫��������һ����Ҫ����, ��ʯú�ᷰ������, ��������Һ�е�����李� ���γɸ��ӵ������ (�Ӷ���) , ���ﵽһ����ʱ, ����Ӱ������ʡ� ����, ����Ӱ������������������, ��ɷ���Ʒ����������
1 ʵ ��
1.1 ԭ ��
��������Һ: ���Ժ��ϻ���ij����, �ó���ʯú��Ϊԭ��, ���հױ��պ���3���������
����Һ����ɺ�ȡ����Xӫ��붨������, ��ѧ�ɷּ���1��
��1 ���ϻ�������Һ����Ҫ��ѧ�ɷַ������
Table 1Main chemical composition analysis results of strip liquor from Huaihua in Hunan
Analyte |
V2O5 | Na | Si | P | S | Al |
Concentration/ (g��L-1) |
117.76 | 53.86 | 1.16 | 1.02 | 6.50 | 0.22 |
Analyte |
K | Ca | Fe | As | Cu | Cl |
Concentration/ (g��L-1) |
0.06 | 0.04 | 0.078 | 0.06 | 0.007 | 3.41 |
1.2 ԭ ��
���ڼ��Է�������Һ����Ҫ��PO
Mg2++PO
��25 ��ʱ����þ���ܶȻ�Ϊ1.04��10-24
ͬʱ, �����Ҳ�������ܽ�ȼ�С�������ζ���ȥ:
Mg2++SiO
3Mg2++2AsO
þ�ķ������������ķ���������, ��������ˮ
1.3 �� ��
1.3.1 þ�ξ���
ÿ����ȡ��������ƷҺ100 ml���ձ������ڵ��Ⱥ���ˮԡ���м���, ����һ������þ�β�����, ������һ����ʱ���, ����һ��ʱ���ٽ��й���, ������ƷҺ������Һ�еķ��� ��Ũ��, ���㷰��ʧ�ʼ������ʡ�
����ʧ�ʼ��㹫ʽ:
�����ʼ��㹫ʽ:
ʽ��: C1Ϊ��������Һ��V2O5��Ũ��, g��L-1; C0Ϊԭ��Һ��V2O5��Ũ��, g��L-1; D1Ϊ��������Һ��PO
1.3.2 ����
���Ӻ�õ��ĺ�������Һ��50 �����������¼����Ȼ��, ��NH4VO3����������, ����һ��ʱ���ٹ��ˡ� ϴ�ӡ� ���, Ȼ��NH4VO3�����������¯����500 �����������Ƚ��V2O5��
1.4 ��������
������������������: ���������������; �IJⶨ: ����ɫ���ⶨ�����Ũ��; ��������IJⶨ: ICP (�����ϵ������巢�����) ��
2 ���������
2.1 þ�μ������Գ����ʼ�����ʧ�ʵ�Ӱ��
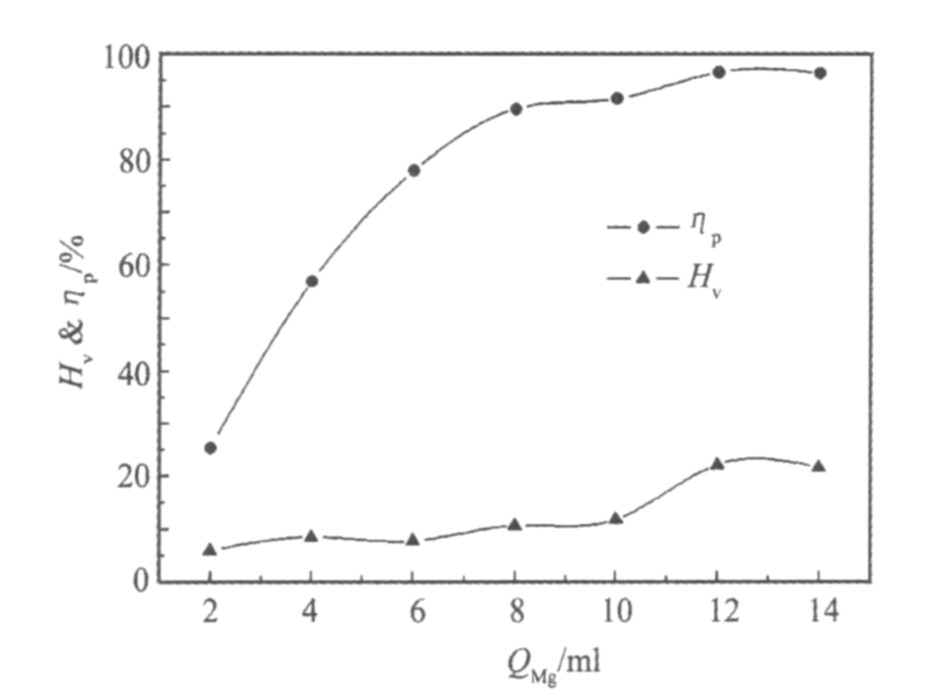
ʵ������: �¶�, 85 ��; �����ٶ�, 300 r��min-1; ����ʱ��, 1 h�� ����þ�μ�����QMg�Գ�������P������ʧHv��Ӱ��, �����ͼ1��
��ͼ1�п��Կ���, ����þ�εļ���������, ����������������, ����þ�εļ������ﵽ12 ml�Ժ�, þ�εļ��������ڳ����ʵ�Ӱ�첻������, �����������ȶ��� ��������ʧ���ڼ����þ�δﵽһ������֮��ʼ���ż��������������������, һ��������ǹ�����þ����������������ˮ�����ɽ���Mg (OH) 2, ˮ�����������������������ʹ��������
ͼ1 þ�μ������Գ����ʼ�����ʧ�ʵ�Ӱ��
Fig.1 Voltage collapses and loss rate of V2O5 influenced by addtion amount of magnesium salt
2.2 pHֵ�Գ����ʼ�����ʧ�ʵ�Ӱ��
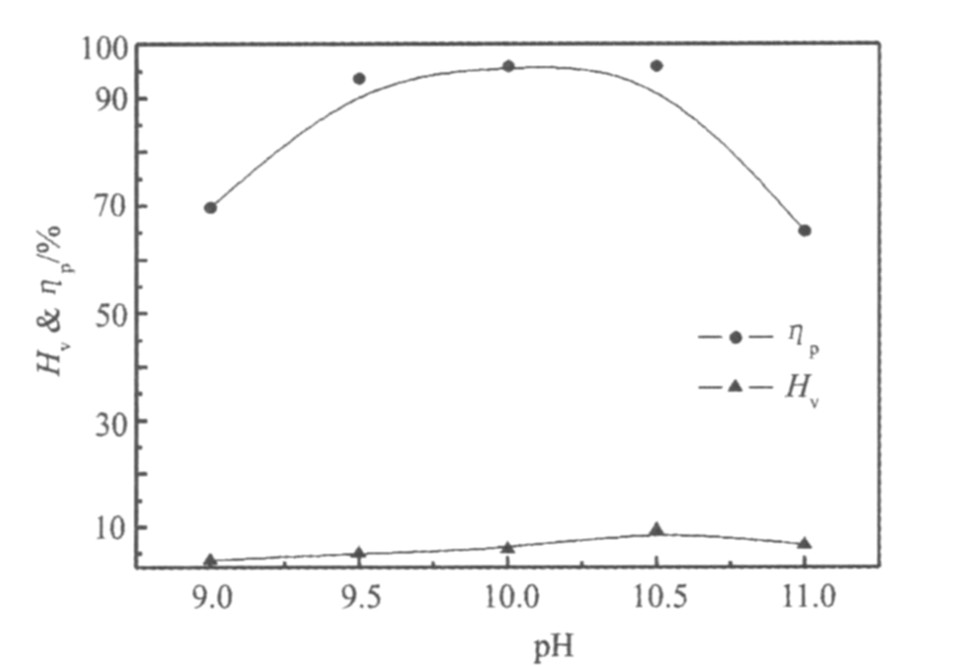
ʵ������: �¶�, 85 ��; þ��, 12 ml; �����ٶ� , 300 r��min-1; ����ʱ��, 1 h�� ������ҺpH�Գ�������P������ʧHv��Ӱ��, �����ͼ2��
��ͼ2���Կ���, pHֵ�Գ�����Ӱ�������� ��pH=9.0��10.0ʱ, pH�������ʹ������Ҳ���� ������������, pH������ʹ������PO
ͼ2 pH�Գ����ʼ�����ʧ�ʵ�Ӱ��
Fig.2 Voltage collapses and loss rate of V2O5 influenced by pH
��ͼ, ����pH�ı仯, ������Һ�еĴ�����̬�;ۺ�״̬�ı仯�Ƚ϶�, �����Կ�������pH�ϸ�ʱ, ����ƫ��, ��pH>10ʱ, Mg2+���OH-�������Mg (OH) 2, ����������ɷ���ʧ�ʵ����ߡ� ��pH��С��9.5ʱ, ���ܷ���ʧ�ʽϵ�, ��������˵õ�����Һ�ھ���һ��ʱ�����������, ��Ҫ���ι��ˡ� �Һ�����������Ҫ����ҺpHֵ��9��10֮�䡣 ���ѡ��ԭҺ��pH������10.0����Ϊ��ѵ�ʵ��������
2.3 �¶ȶԳ����ʼ�����ʧ�ʵ�Ӱ��
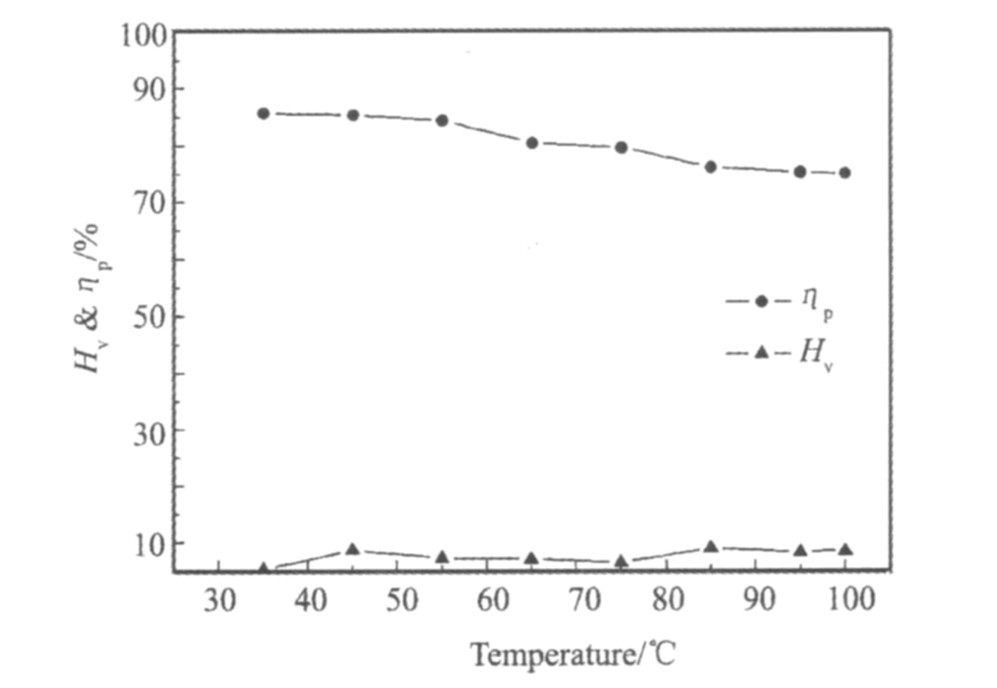
ʵ������: þ��, 6 ml; �����ٶ�, 300 r��min-1; ����ʱ��, 1 h�� �����¶�TEMP�Գ�������P������ʧHv��Ӱ��, �����ͼ3��
�����¶ȶԹ����и���Ӧ�ķ�Ӧ����, ������������ܶȻ�����Ӱ�졣 �������¶ȵ���35 ��ʱ, ��������˻�õ���Һ�ڷ���һ��ʱ���, ���������, �������Ͽ�������豸�ĽṸ�����, ������Ҫ���ж��ι���, ʹ�ù��̱�ø���, �������¶ȸ���35 ��ʱ, ��������, ��˲����ǵ���35 ����¶ȡ�
��Ӧ�¶�̫��, ��������þ�ķ�Ӧ�ٶ���Խ���, ��������þ������̬� �¶�����, �������ܽ�Ⱦͻ�����, ʹ�ó������½��� ��һ�������´ٽ�Mg2+ˮ�����Mg (OH) 2����, ���³����ʽ��͡�
ͼ3 �¶ȶԳ����ʼ�����ʧ�ʵ�Ӱ��
Fig.3 Voltage collapses and loss rate of V2O5 influenced by temperature
����ͼ3���Կ���, ����ʧ�������¶ȵ�����ֻ����һ����Χ�ڲ���, �ɼ��¶ȶԷ����Ӱ�첢���� �¶ȶԳ����Ĺ�������Ӱ��Ҳ����, �����Ǹ��»��ǵ����ھ�������˶�������, ����Ҳ����Ҫѡ��ϸߵ��¶������ƹ������ܡ� ���������������ѡ��45 ��Ϊ��Ѿ����¶ȡ�
2.4 ����ʱ��Գ����ʼ�����ʧ�ʵ�Ӱ��
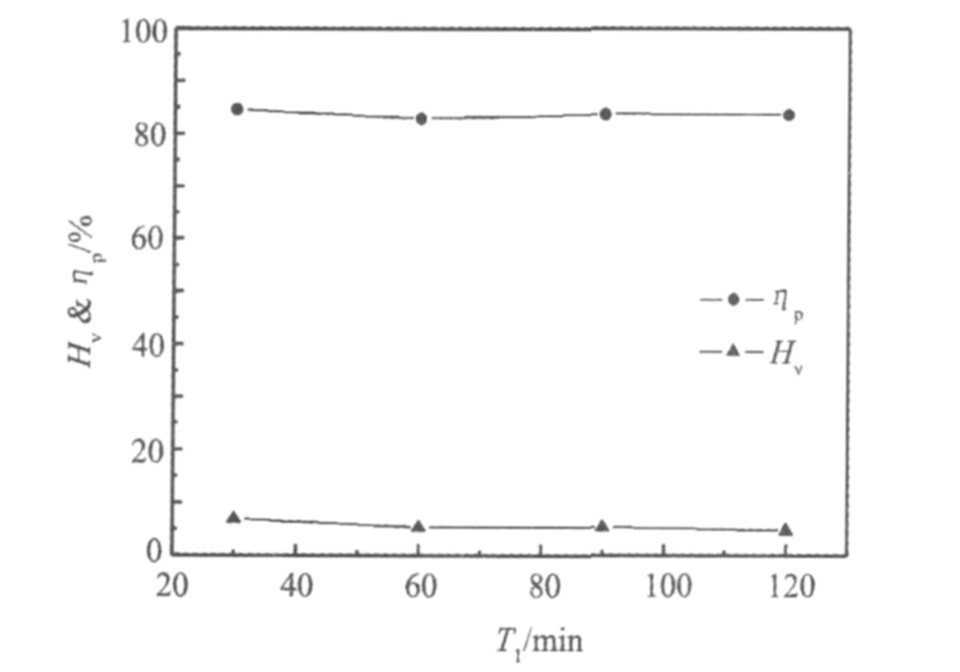
ʵ������: �¶�, 35 ��; þ��, 8 ml; �����ٶ�, 300 r��min-1�� �������ʱ��T1�Գ�������P������ʧHv��Ӱ��, �����ͼ4��
��ͼ4��ʾ, ����ʱ����ӳ��Գ����ʵ�Ӱ�첢������, ˵��þ�γ���Ӧƽ��ʱ��ܶ�, ����ʱ��Գ����ʵ�Ӱ�첻�� ������ʧ�����ž���ʱ��������������½�, �������Ҫ���ͷ�������ʵ����ӳ�����ʱ��, ���ڱ���ʵ����Ҫ̽�����dz�����, ������Ժ��ʵ���н�����ʱ�䶨Ϊ50 min��
2.5 ����ʱ��Գ����ʼ�����ʧ�ʵ�Ӱ��
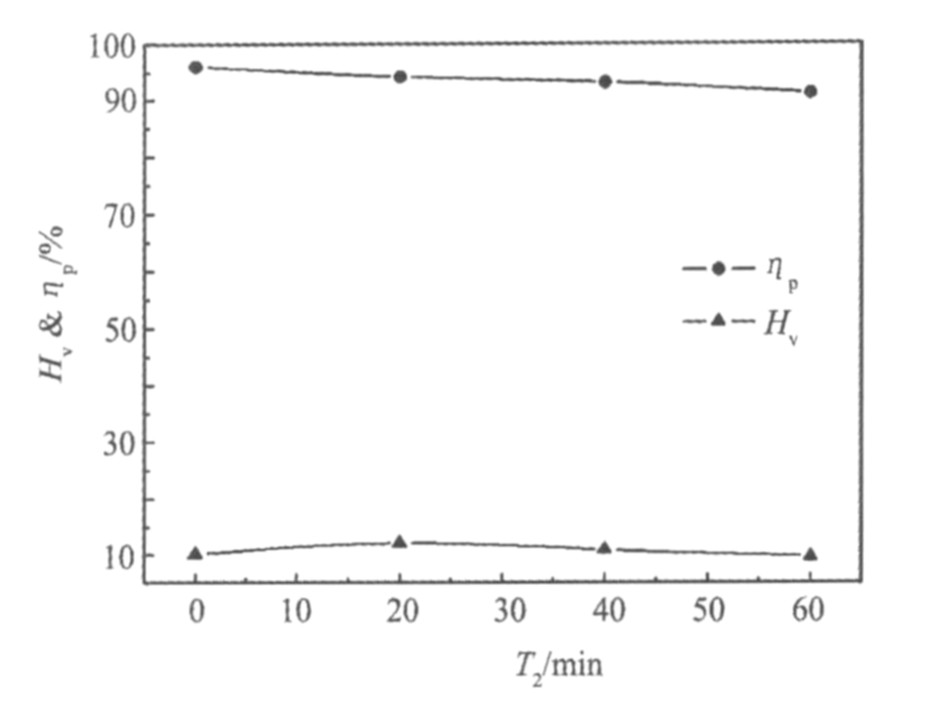
ʵ������: �¶�, 35 ��; þ��, 8 ml; �����ٶ�, 300 r��min-1; ����ʱ��, 50 min, ����һ����ʱ�����˵õ���Һ���з����� ���쾲��ʱ��T2�Գ�������P������ʧHv��Ӱ��, �����ͼ5��
ͼ4 ����ʱ��Գ����ʼ�����ʧ�ʵ�Ӱ��
Fig.4 Voltage collapses and loss rate of V2O5 influenced by stirring time
ͼ5 ����ʱ��Գ����ʼ�����ʧ�ʵ�Ӱ��
Fig.5 Voltage collapses and loss rate of V2O5 influenced by standing time
����ʱ����Ҫ��Ӱ����Һ������е����ȶ���, ��Һ������е����ȶ����ھ�����һ����ʱ����ת��Ϊ�ȶ���, ��Ծ������̿��ܻ���һ����Ӱ�졣
��ͼ5���Կ���, ����ʱ����ӳ���ʹ�ó������½�, �ɼ��ӳ�����ʱ��Ծ�����Ӧ�Dz�����, ���Է���ʧ�ʵ�Ӱ�첻�Ǻܴ�, ������ѵľ����������ھ�����ֱ�ӹ��ˡ�
2.6 �ߴ�V2O5���Ʊ�
��ҵ�������ӽ�������Һ�Լ�����ѵľ��������� (�����¶�45 ��, ����ʱ��50 min, þ�μ�����Ϊԭ��Һ12%, pH=10.0, ������Ҫ����ֱ�ӹ���) �� ���Ӻ�õ��ĺ�������Һ�ֱ��� 50 ��ʱ�����Ȼ��, ��NH4VO3����������, ����һ��ʱ���ٹ��ˡ� ϴ�ӡ� ���
�������������2��
��2 V2O5��Ʒ���� (%, ��������)
Table 2 Product quality of V2O5 (%, mass fraction)
| Component | V2O5 | P | Si | Fe | As | S | Na2O+K2O |
Unpurity |
99.120 | 0.114 | 0.2000 | 0.0220 | 0.001 | 0.036 | 0.445 |
Purity |
99.917 | 0.017 | 0.0005 | 0.0003 | - | 0.012 | 0.049 |
�ӱ�2���Կ���, ����������ȡ��V2O5��δ�����ķ�������Һ����ȡ��V2O5���, PԪ�ش�0.114%������0.017%�� ����, Si, Fe, As��Ԫ�غ���Ҳ�½�
3 �� ��
��������������, þ�η�����Ч��ȥ��������Һ�е�PԪ��, ͬʱҲ��Ч��ȥ��������Һ�е�Si, Fe, As������Ԫ�ء� �������Ϊ: �¶�45 ��, ����ʱ��50 min, þ�μ�����Ϊԭ��Һ12%, pH=10.0, ������Ҫ����ֱ�ӹ��ˡ� ������Һ��50�������γ���, �õ���ɫ�����ɫ��ƫ����李� ƫ�������500 ����������¯������2 h, �ƵõIJ�Ʒ����>99.9%, V2O5�Ļ�����>94%��
�����
[6] David R.Lide, Handbook of Chemistry and Physics[M].Florida:CRC Press, 1997-1998.
[9] Cheresnowsky et al.Purificationo fm olybdate[P].US4702895, 1987.
[11] Dean J A, Ed.Lange��s Handbook of Chemistry[M].Florida:CRC Press, 1985.