DOI: 10.11817/j.ysxb.1004.0609.2021-37631
Ln-MOFs���Ʊ�������������ӵ������ͼ��
��ӳ÷1, 2��������1, 2��������1, 2���� ��1, 2��������1, 2���� ��1, 2���� ��1, 2������Ȼ1
(1. �ϻ���ѧ �˿�ұ���\�������ص�ѧ��ʵ���ң����� 421001��
2. �ϻ���ѧ ��������ѧԺ������ 421001)
ժ Ҫ��
����ˮ�Ⱥϳɷ��Ʊ�һ��ϡ�����ӵĽ����л��Ǽܲ���(MOFs) Tb3+-UiO-66-(COOH)2(Ln-MOFs)������ɨ��羵(SEM)���������(IR)��ӫ�����(FL)�Բ��Ͻ��б���������������������������������ΪpH=7������ʱ��Ϊ10 h���¶�Ϊ313 K��U�ij�ʼŨ��60 mg/L�����£����������������ӵ�������Ϊ333.13 mg/g���ò���Ҳ������ӫ����U(��)����Ѽ��������ͷ��䲨���ֱ�Ϊ300 nm��540 nm����200 ��g/L��10 mg/L 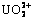 Ũ�ȷ�Χ�ھ������õ����Թ�ϵ���������ϵ��r=0.9924�������(LOD)Ϊ232.7 ��g/L���÷���������㡢ѡ����ǿ�������Ƚϸߡ�
Ũ�ȷ�Χ�ھ������õ����Թ�ϵ���������ϵ��r=0.9924�������(LOD)Ϊ232.7 ��g/L���÷���������㡢ѡ����ǿ�������Ƚϸߡ�
�ؼ��ʣ�
���������л��Ǽܲ�����������ӫ��ʶ����
���±�ţ�1004-0609(2021)-05-1405-08���� ��ͼ����ţ�O615��X131��X591�� ���ױ�־�룺A
���ĸ�ʽ����ӳ÷, ������, ������, ��. Ln-MOFs���Ʊ�������������ӵ������ͼ��[J]. �й���ɫ����ѧ��, 2021, 31(5): 1405-1412. DOI: 10.11817/j.ysxb.1004.0609.2021-37812
LI Ying-mei, ZHOU Xia-yu, XIA Yu-xin, et al. Synthesis of Ln-MOFs and its adsorption and fluorescence recognition of uranyl ions[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(5): 1405-1412. DOI: 10.11817/j.ysxb.1004.0609.2021-37812
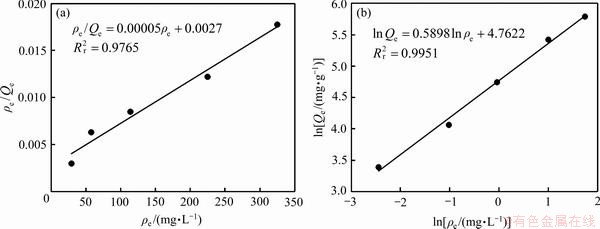
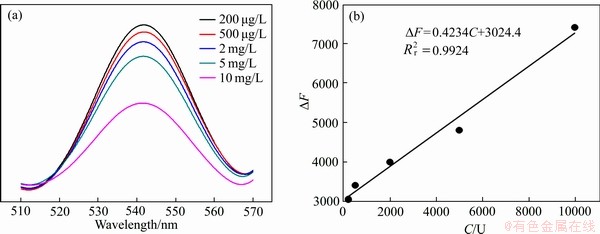
���ź˹�ҵ�Ŀ��ٷ�չ������Ϊһ����Ҫ�ĺ�ȼ�ϵõ��˹㷺Ӧ��[1-3]��ˮ��Һ�е�����Ҫ����������(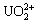 )��̬���ڡ����ڼ��ѧ�ͷ��䶾�ԣ��˽�����������߰�֢��������ļ���[4-5]����������������(USEPA)�涨����ˮ��
)��̬���ڡ����ڼ��ѧ�ͷ��䶾�ԣ��˽�����������߰�֢��������ļ���[4-5]����������������(USEPA)�涨����ˮ��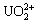 �ĺ���Ӧ����30��10-9����ˣ���Чȥ�����������ˮ���е��������Ӷ��ڻ�����ȫ����ʮ����Ҫ���塣
�ĺ���Ӧ����30��10-9����ˣ���Чȥ�����������ˮ���е��������Ӷ��ڻ�����ȫ����ʮ����Ҫ���塣
Ŀǰ��������ƾ�������������Ч��Ч�ʸߵ��ŵ��Ϊ���Ƿ��븻���ؽ������Ӻͷ����Ժ�����õķ���֮һ[6-10]�������л��Ǽܲ���(MOFs)���ھ��п׳ߴ�ɵ������˽ṹ�ḻ�����ܻ����������ǿ���ϳɹ��ռ���������մ��������ƶ���Ϊ�о����ȵ�[11-13]��ӫ���⼼��������Ӧʱ��̡������ȸߡ��ȶ��Ժá��ɱ��͵��ŵ㣬���������������ǵĹ㷺��ע[14-15]������ MOFs��������������Ľṹ��DZ�ڵ�Ӧ�ü�ֵ�����о��������𡣵�ĿǰΪֹ���о��ȵ���Ҫ�����ںϳ���ӱ��MOFs���������������������Ǽ��Լ��ڹǼ���������ֻ�ѧ���ţ���չ��Ӧ�������[16-17]��
Ŀǰ����������ˮ�����������ӵ�������ӫ���������Ѿ���չ�˴�����ص��о�����[18-19]�����ǣ�ͬʱ�߱���Ч������ѡ���ԡ����������ˮ�����������ӵ�����о�����Ϊ�ټ�����ˣ�������ƺϳ���ϡ�����ӵ�MOFs����Tb3+-UiO-66- (COOH)2������������ӫ��ʶ��U(��)����Ϊ�ͻ����������о���
1 ʵ��
1.1 �Լ�������
1,2,4,5-���ļ���(BTEC)(CAS��89-05-4)����ˮ�����(��)[Tb(NO3)3��6H2O]���Ȼ��(ZrCl4)����ͪ����ˮ�Ҵ���ż���Ϣ��������ᡢ�����ơ�Ũ���ᡢ�������ƾ�Ϊ��������
RF 4500��ӫ��ֹ��ȼƣ�CenPoreUv/UF�ͳ���ˮϵͳ��Research����Һǹ��KQ2200DE�����س�������ϴ����AL104�͵�����ƽ��PHSJ-3F��pH�ƣ�Z36H K��̨ʽ�����䶳���Ļ���DJS-2012R�͵���ʽ��������������ҡ����RET basic�ʹ������Ƚ�������DZF-6030A����ո����䣻����IR Prestige-21����Ҷ�任��������ǣ�Zeiss Merlin microscope��T6������������ɼ��ֹ��ȼơ�
1.2 ���������ϵ��Ʊ������
1.2.1 UiO-66-(COOH)2���Ʊ�
��ȡ2.15 g 1,2,4,5-���ļ���(BTEC)��1.15 g�Ȼ��(ZrCl4)����������ƿ�У�����25 mL����ˮ��õ�����Һ��373 K�½���9 h����Ӧ������õ��İ�ɫ��״���ó���ˮ��ϴ����ϴ��õ��Ĺ����ܽ��ڳ���ˮ�м�����100 ���½���16 h���õ��IJ����ñ�ͪϴ��3�Σ�10000 r/min���ķ���5 min���õ����²������60 ����ո���24 h���ɵõ�UiO-66-(COOH)2��
1.2.2 Tb3+-UiO-66-(COOH)2���Ʊ�
��ȡ0.5 g UiO-66-(COOH)2��0.5 g Tb(NO3)3�� 6H2O������ƿ�У�����10 mL����ˮ��60 ���½���24 h���õ��IJ�������ˮ�Ҵ�ϴ��3�Σ�10000 r/min ���ķ���5 min��ȡ�²������60 ����ո���20 h���ɵõ�Tb3+-UiO-66-(COOH)2��
1.2.3 ���������ϵı���
���ú������(IR)��ɨ��羵(SEM)��ӫ�����(FL)���Ʊ��õ���UiO-66-(COOH)2��Tb3+-UiO-66- (COOH)2���б���������
UiO-66-(COOH)2�ĺ�����ײ���KBrѹƬ���ڵ���IR Prestige-21����Ҷ�任����������ϲⶨ��ã�UiO-66-(COOH)2��ɨ��羵ͼ��ͨ��Zeiss Merlin microscope ɨ���ã�UiO-66-(COOH)2��ӫ�⼤���ͷ��������RF 4500��ӫ��ֹ��ȼ��ϻ�ã������õ���Ʒ��Һ����1 cmʯӢ��ɫ���У���϶��������Ϊ10 nm����Ʒ��300 nm������������540 nm���۲�����ѷ�����ס�
1.3 ����ʵ��
����1.0 g/L�˱���Һ��ʵ����������õ�����Ũ�ȵ�����Һ�����Ѿ��Ʊ����˱���Һ��ϡ�ͻ�á��ھ�̬���������£��о���ͬ��pHֵ������ʱ�䡢��Һ���˳�ʼŨ�Ⱥ��¶ȶ�����������Ч�ʵ�Ӱ�졣���岽�����£�ȡ����������Һ����ƿ��,�ٳ�ȡ���������������뵽����Һ�У�����Ʒ������������Ϊ303 K��180 r/min�ĺ���ҡ���У�����һ��ʱ���ȡ����ȡ����Һ��0.22 ��m��ͷ���˺�ȡ1 mL����5.0 mL pH 2.5����������-�����ƻ�����Һ��1.0 mL 0.5 g/L��ż���Ϣ���Һ������ɫ�����ó���ˮ���ݣ�ҡ�ȣ���ɫ10 min��������/�ɼ��ֹ��ȼ��ڲ���650 nm���ⶨ����ȣ�ͨ������������������Ũ�ȡ�
pHֵ��Tb3+-UiO-66-(COOH)2������Ӱ��ʵ�飺ȡ���ɷ�30 mL��ʼŨ��Ϊ10 mg/L������Һ��������Һ��pHֵ�ֱ��Ϊ3��4��5��6��7��Ȼ�����5 mg Tb3+-UiO-66-(COOH)2�ں���ҡ��������������������Ϊ303 K��180 r/min������22 h��ȡ����Һ����������ȣ��ݱ�����������������
Tb3+-UiO-66-(COOH)2��������ʱ��仯ʵ�飺��pHΪ7��10 mg/L������Һ�У�����5 mg Tb3+-UiO-66-(COOH)2����303 K��180 r/min����ҡ�������������ֱ��ڲ�ͬʱ���ȡ����Һ����������ȣ����������ʺ���������
�¶ȶ�Tb3+-UiO-66-(COOH)2������Ӱ��ʵ�飺��pHΪ7��10 mg/L������Һ�У�����5 mg Tb3+-UiO-66-(COOH)2����ͬ�¶�����180 r/min����ҡ����������10 h����ȴ��ȡ����Һ���˲�������ȣ������������ʺ���������
��ͬ�˳�ʼŨ�ȶ�Tb3+-UiO-66-(COOH)2������Ӱ��ʵ�飺����5��10��20��40��60 mg/L������Һ������pH=7���ֱ����5 mg Tb3+-UiO-66- (COOH)2����313 K��180 r/min����ҡ����������10 h��ȡ����Һ������ȣ������������ʺ���������
1.4 ��Ũ�ȵķ���
��ʵ�����ż���Ϣ�ֹ��ȷ�������Һ�е���Ũ�ȡ�
����5 mg/L ���˱���Һ���ֱ�ȡ1��2��3��4 mL��25 mL����ƿ�У�Ȼ�����μ���5.0 mL pH 2.5����������-�����ƻ�����Һ��1.0 mL 0.5 g/L��ż���Ϣ���Һ������ó���ˮ�������̶ȣ�����10 min ���������ȣ����Ʊ����ߡ�Ȼ���������������ֵ���������Һ�е��˺�����
��ƷŨ�Ȳⶨ��ȡ������Ʒ����Һ��25 mL����ƿ�У���������ͬ�ϡ�
Tb3+-UiO-66-(COOH)2���˵��������������������й�ʽ���㣺
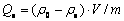 (1)
(1)
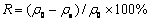 (2)
(2)
ʽ�У�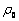 Ϊ��ʼ��Ũ�ȣ�mg/L��
Ϊ��ʼ��Ũ�ȣ�mg/L��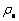 Ϊ�����ﵽƽ��ʱ����Ũ�ȣ�mg/L��QeΪ��������mg/g��RΪ�����ʣ�%��VΪ����Һ�������L��mΪ��������Ͷ������mg��
Ϊ�����ﵽƽ��ʱ����Ũ�ȣ�mg/L��QeΪ��������mg/g��RΪ�����ʣ�%��VΪ����Һ�������L��mΪ��������Ͷ������mg��
1.5 ����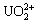 ��ӫ���ȷ���ʵ��
��ӫ���ȷ���ʵ��
��2 mL PE���У�����1 mg Tb3+-UiO-66- (COOH)2(������ƽ��С�ֶ�ֵΪ0.0001 g)�Ͳ�ͬŨ�ȵ��˱���Һ(���չܼ�����ͬ����ij���ˮ)�������³���3 minʹ��Һ�ʾ��Ȼ���Һ��ⶨ(��������Ϊ300 nm)���ֱ�ⶨ��Һ�Ϳհ���Һ��540 nm����ӫ��ǿ��F��F0��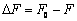 ��
��
2 ���������
2.1 �������ı���
2.1.1 SEM��EDS����
UiO-66-(COOH)2��Tb3+-UiO-66-(COOH)2��ɨ��羵���������ͼ1��ʾ����ͼ1���Կ�������������ӵ�Tb3+-UiO-66-(COOH)2�ı����UiO-66-(COOH)2���Ӵֲڣ�����״̬�������������̵Ľ��У�Ϊ�������ṩ�˽ϴ�ı�������������λ�㡣�����UiO-66-(COOH)2��Tb3+-UiO-66- (COOH)2������ͼ�ϳ��������Ե�����Tb��������(��ͼ2)��˵������ӳɹ����ӵ���UiO-66- (COOH)2�С�

ͼ1 UiO-66-(COOH)2��Tb3+-UiO-66-(COOH)2��SEM��
Fig. 1 SEM images of UiO-66-(COOH)2(a) and Tb3+- UiO-66-(COOH)2(b)
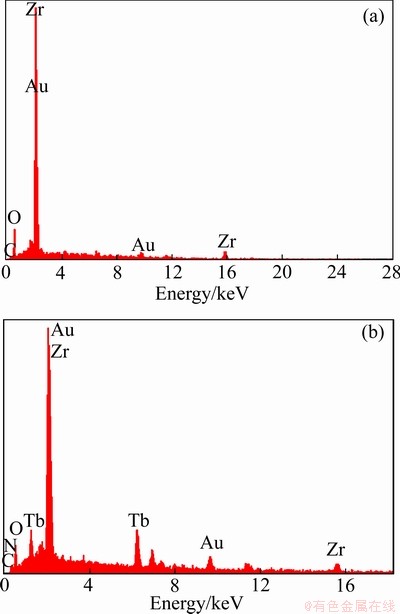
ͼ2 UiO-66-(COOH)2��Tb3+-UiO-66-(COOH)2��EDS��
Fig. 2 EDS spectra of UiO-66-(COOH)2(a) and Tb3+-UiO- 66-(COOH)2(b)
2.1.2 FT-IR����
UiO-66-(COOH)2��Tb3+-UiO-66-(COOH)2�ĺ�����ױ�����ͼ3��ʾ��UiO-66-(COOH)2�ĺ��������֮ǰ���������������[20]��˵���ɹ��ϳ���UiO-66-(COOH)2�����У�3369.57 cm-1������һ��ǿ�����ķ壬�ô�ΪO��H��Ӧ�����������շ壬1712.57 cm-1��C=O���������շ壬1496.99 cm-1��C��O���������塣��������UiO-66-(COOH)2��������Ӻ��FT-IR����ͼ���Կ�����O��H��C=O��C��O������û�����Ա仯��˵������ӵ�����û���ƻ�UiO-66- (COOH)2�Ľṹ��
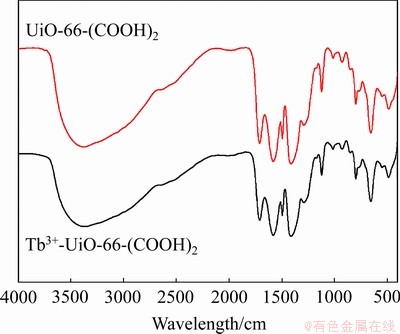
ͼ3 UiO-66-(COOH)2��Tb3+-UiO-66-(COOH)2�ĺ������
Fig. 3 FT-IR spectra ofUiO-66-(COOH)2 and Tb3+-UiO- 66-(COOH)2
2.1.3 ӫ���������
Tb3+-UiO-66-(COOH)2��ӫ�������ͼ4��ʾ������Ѽ���������(��������Ϊ300 nm)��Tb3+-UiO-66-(COOH)2���ֳ�Tb3+������ӫ�ⷢ��壬��5D4��7FJ (J=6��5��4)�ĵ���ԾǨ���ڲ���Ϊ486��540��590 nm���ֱ���5D4��7F6��5D4��7F5��5D4��7F4����ԾǨ�������Բ���540nm��5D4��7F5����ԾǨ������ӫ����ǿ������Tb3+������ӫ����ʾ��ɫ��
2.2 ���������ӵ���������
2.2.1 ����ʵ�������Ż�
��ͼ5(a)��֪��Tb3+-UiO-66-(COOH)2��U(��) ��������pH���Ӷ������ߣ�pH=7ʱ�������ʴﵽ���ֵ97.26 %����ʱ������Ϊ58.36 mg/g����ͼ5(b)��֪����������ʼ��ǰ30 min��Tb3+-UiO- 66-(COOH)2���˵�������Ѹ��������8 h�������ʱ仯���Ƽ����������10 h�ﵽ����ƽ�⣬��ʱ����������Ϊ94.34%�����������Ϊ56.6 mg/g����ͼ5(c)��֪��Tb3+-UiO-66-(COOH)2���˵������������¶����߶����ߡ�313 Kʱ�ﵽ���������96.32%����������57.79 mg/g����ͼ5(d)��֪�����ʼ��Ũ�ȵ����ӣ�Tb3+-UiO-66-(COOH)2���˵����������½��������������ӡ����¶�313 K���˳�ʼŨ��60 mg/Lʱ������ʽ(1)��(2)����ã����������������ӵ�������Ϊ333.12 mg/g��
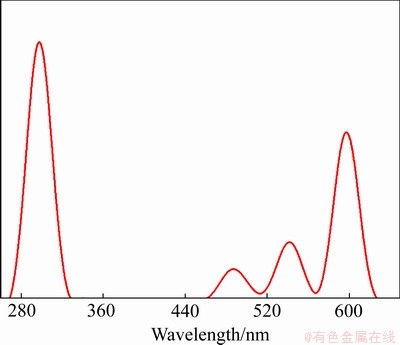
ͼ4 Tb3+-UiO-66-(COOH)2��ӫ�����
Fig. 4 Fuorescent spectra of Tb3+-UiO-66-(COOH)2
2.2.2 ��������ѧ����ģ��
��������ѧ��Ҫ�����о������ضԷ�Ӧ���ʵ�Ӱ����ɣ��Ӷ��������������������ӵĻ��������о������о���������ʱ���������ʵĶ�Ӧ��ϵ������һ������ѧģ�ͺ���������ѧģ�ͽ�����ϣ���Ͻ�����1��ͼ6��ʾ����Ͻ�����1��ͼ6��ʾ��Qt��ʱ��Ϊtʱ����������k1��һ������ѧģ�͵��������ʳ�����k2����������ѧģ�͵��������ʳ�����
�ɱ�1��֪��Tb3+-UiO-66-(COOH)2�����˵Ĺ��̸�������������ѧģ�ͣ��������ϵ���ߴ�0.9999���Ҹ�����Ϸ��̼�������QeֵΪ59.17 mg/g���ӽ�ʵ��ֵ59.28 mg/g����������һ������ѧģ�͡���ˣ���������ѧģ������������Tb3+-UiO-66-(COOH)2���˵��������̣�˵��Tb3+-UiO-66-(COOH)2��U�����������Ի�ѧ����Ϊ����
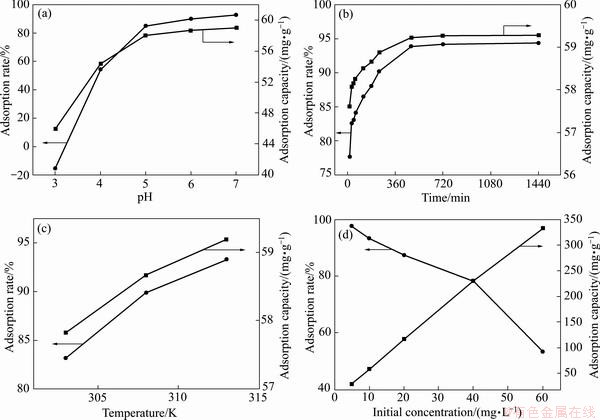
ͼ5 pHֵ������ʱ�䡢�¶��Լ��˳�ʼŨ�ȶ�Tb3+-UiO-66-(COOH)2�����˵�Ӱ��
Fig. 5 Effect of pH(a), contact time(b), temperature(c) and concentration(d) on adsorption of U(��) by Tb3+-UiO-66-(COOH)2
��1 Tb3+-UiO-66-(COOH)2����U(��)�Ķ���ѧ����
Table 1 Kinetic constants for adsorption of U(��) on Tb3+-UiO-66-(COOH)2
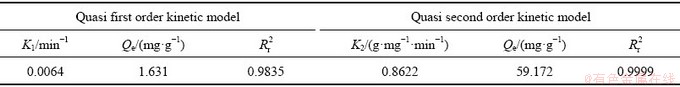
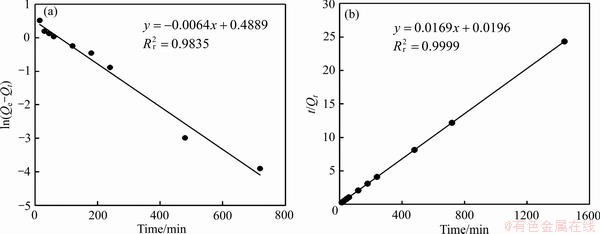
ͼ6 һ������ѧ���ߺ���������ѧ����
Fig. 6 Pseudo-first-order(a) and pseudo-second-order(b) kinetic curves
2.2.3 ������������ģ��
��������ģ���Ƿ�ӳ��һ���¶��£�������ƽ��ʱ����������Һ������е�Ũ�ȹ�ϵ����ʵ�齫��ͬ�¶��²�ͬŨ������Һ��������������Ӧ���ƽ��Ũ��ֵ��e���Ӧ������Qe�������ݴ�����ֱ����Langmuir��Freundlich�����ߣ���Ͻ�����2��ͼ7��ʾ����Ͻ�����2��ͼ7��ʾ��Qm�������������KL��Langmuir���������߳�����Kf��Freundlich ���������߳�����
�ɱ�2��֪��Freundlich��������ģ���ܸ��õض�������Tb3+-UiO-66-(COOH)2�����˵Ĺ��̽�����ϣ�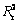 =0.9951��˵��Tb3+-UiO-66-(COOH)2��U(��)�������Զ������Ϊ����
=0.9951��˵��Tb3+-UiO-66-(COOH)2��U(��)�������Զ������Ϊ����
2.3 MOFs���ϵķ���Ӧ�á�������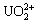 ��ӫ���ȷ���
��ӫ���ȷ���
MOFs���Ͼ��п��ŵĽ���λ�㣬�������л������ĵ���ת��Ѹ�٣����Կ�������ؽ���ӫ����Ӧ����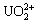 ���Խ�Tb-MOFs�е�Tb3+�û�������ʹ�����ӫ�����������һ����Ũ�ȷ�Χ�ڣ�������Ũ�ȵ����ӣ�ӫ�����Խ���ԡ���ͨ���ⶨ��ϵ��540 nm��ӫ��ǿ�ȵı仯���������Ũ�ȣ�ӫ������ǿ������Ũ��֮���������ع�ϵ��
���Խ�Tb-MOFs�е�Tb3+�û�������ʹ�����ӫ�����������һ����Ũ�ȷ�Χ�ڣ�������Ũ�ȵ����ӣ�ӫ�����Խ���ԡ���ͨ���ⶨ��ϵ��540 nm��ӫ��ǿ�ȵı仯���������Ũ�ȣ�ӫ������ǿ������Ũ��֮���������ع�ϵ��
��2 Tb3+-UiO-66-(COOH)2����U(��)�ĵ�������ģ��
Table 2 Adsorption isotherm constants of uranium by Tb3+-UiO-66-(COOH)2

ͼ7 Tb3+-UiO-66-(COOH)2�����˵�Langmuir��Freundlich��������ģ���������
Fig. 7 Langmuir(a) and Freundlich(b) isotherms for adsorption of U(��) by Tb3+-UiO-66-(COOH)2
ͼ8 Tb3+-UiO-66-(COOH)2�Բ�ͬU(��)Ũ�ȱ�����ӫ�ⷢ����ͱ�����
Fig. 8 Fluorescent emission spectra of Tb3+-UiO-66-(COOH)2 toward U(��) with different concentrations(a) and standard curve of U(��)recognition by Tb3+-UiO-66-(COOH)2(b)
��ͼ8��֪������Ѽ����ͷ��䲨���ֱ�Ϊ300 nm��540 nm�£�������Ũ�ȵ�������ϵ����ӫ�������������Ż��������ʵ�������£���������Ũ�ȷ�ΧΪ200 ��g/L~10 mg/Lʱ����ϵ��ӫ��仯ֵ���ֽϺõ����Թ�ϵ�����Իع鷽��Ϊ��F=0.4234C+3024.4�����ϵ��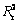 =0.9924�����ݿհܵı�ƫ��Sb�ͱ����ߵ�б��k���LODΪ232.72 ��g/L��
=0.9924�����ݿհܵı�ƫ��Sb�ͱ����ߵ�б��k���LODΪ232.72 ��g/L��
3 ����
1) �ϳɵõ���Tb3+-UiO-66-(COOH)2��U(��)��������������ӫ��ʶ�����ܡ�Tb3+-UiO- 66-(COOH)2��10 mg/L����Һ�������ʿɴﵽ97.26%������ѵ���������ΪpHΪ7���¶�313 K������ʱ��10 h��
2) Tb3+-UiO-66-(COOH)2��������ʶ���������ӣ��ݴ˽����˻���ˮ�������˵ļ���·������½��������ʵ�ã������Ⱥ�ѡ���Խϸߣ�Ϊ����Һ���˵ĸ�Чȥ���ͼ���ṩ��һ���µķ�����˼·��
REFERENCES
[1] YANG Q Y, VAESEN S, RAGON F, et al. A water stable metal-organic framework with optimal features for CO2 capture[J]. Agewandte Chemie-International Edition, 2013, 52(39): 10316-10320.
[2] ABNEY C W, MAYES R T, SAITO T, et al. Materials for the recovery of uranium from seawater[J]. Chemical Reviews, 2017, 117(23): 13935-14013.
[3] WU Yi-han, PANG Hong-wei, YAO Wen, et al. Synthesis of rod-like metal-organic framework (MOF-5) nanomaterial for efficient removal of U(��): Batch experiments and spectroscopy study[J]. Science Bulletin, 2018, 63(13): 831-839.
[4] �� ��, ����ܰ, ��ǿ�, ��. �̶�������ù����̿�����˵Ļ���[J]. �й���ɫ����ѧ��, 2016, 26(4): 937-945.
YU Qing, DING De-xin, LI Deng-ke, et al. Adsorption mechanism of uranium of immobilizing Aspergillus niger activated carbon[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(4): 937-945.
[5] GORUR F K, CAMGOZ H. Natural radioactivity in various water samples and radiation dose estimations in Bolu province, Turkey[J]. Chemosphere, 2014, 112: 134-140.
[6] �� ��, �� ��, ����ܰ, ��. ����ù���������������Ʊ�����������Ũ���������о�[J]. Ӧ�û���, 2018, 47(2): 219-223.
CHENG Bin, LI Le, DING De-xin, et al. Preparation of nano-Fe3O4 modified Aspergillus niger and its properties for adsorption of low concentration uranium(��)[J]. Applied Chemical Industry, 2018, 47(2): 219-223.
[7] �� ��, �� ��, �� ��, ��. ��������ȡ��Ũ���˵��о���չ[J]. Ӧ�û���, 2017, 46(3): 537-541.
LI Le, CHENG Bin, LIAO Qi, et al. Research advance in adsorption of low concentration uranium-bearing wastewater[J]. Applied Chemical Industry, 2017, 46(3): 537-541.
[8] LI Le, LU Wei, DING De-xin, et al. Adsorption properties of pyrene-functionalized nano-Fe3O4 mesoporous materials for uranium[J]. Journal of Solid State Chemistry, 2019, 270: 666-673.
[9] ZHANG Hui, DAI Zhong-ran, SUI Yang, et al. Adsorption of U(��) from aqueous solution by magnetic core dual shell Fe3O4@PDA@TiO2[J]. Journal of Radioanalytical and Nuclear Chemistry, 2018, 317(1): 613-624.
[10] TAN Yan, LI Le, ZHANG Hui, et al. Adsorption and recovery of U(��) from actual acid radioactive wastewater with low uranium concentration using thioacetamide modified activated carbon from liquorice residue[J]. Journal of Radioanalytical and Nuclear Chemistry, 2018, 317(2): 811-824.
[11] MELINDA S, NOBUHIRO Y, AH-YOUNG J, et al. Colloidal-sized metal-organic frameworks: Synthesis and applications[J]. Accounts of Chemical Research, 2014, 47(2): 459-469.
[12] WEN Jia, FANG Ying, ZENG Guang-ming. Progress and prospect of adsorptive removal of heavy metal ions from aqueous solution using metal�Corganic frameworks: A review of studies from the last decade[J]. Chemosphere, 2018, 201: 627-643.
[13] �� ��, �����, �ſɸ�, ��. �����л��Ǽܲ��������������о��е�Ӧ�ý�չ[J]. ��ѧѧ��, 2017 , 75(9): 841-859.
ZHANG He, LI Guo-liang, ZHANG Ke-gang, et al. Advances of metal-organic frameworks in adsorption and separation applications[J]. Acta Chimica Sinica, 2017, 75(9): 841-859.
[14] DUEDU K O, FRENCH C E. Two-colour fluorescence fluorimetric analysis for direct quantification of bacteria and its application in monitoring bacterial growth in cellulose degradation systems[J]. Journal of Microbiological Methods, 2017, 135: 85-92.
[15] LAGOS M, PAREDES R, RETAMAL C. High precision energy measurements from the analysis of wide spectral features. Application to the fluorescence of YAG:Ce3+[J]. Journal of Photochemistry and Photobiology A-Chemistry, 2017, 344: 163-167.
[16] LIU Di, WAN Jia-wei, PANG Guang-sheng, et al. Hollow metal-organic-framework micro/nanostructures and their derivatives:emerging multifunctional materials[J]. Advanced Materials, 2019, 31(38): 1803291.
[17] STASSEN I, BURTCH N, TALIN A, et al. An updated roadmap for the integration of metal-organic frameworks with electronic devices and chemical sensors[J]. Chemical Society Reviews, 2017, 46(11): 3185-3241.
[18] LIU J, HOU J X, GAO J P, et al. Stable Cd(��)-MOF as a fluorescent sensor for efficient detection of uranyl ions[J]. Materials Letters, 2019, 241: 184-186.
[19] LIU J, HOU J X, GAO J P, et al. Highly selective and sensitive detection of Pb2+ and 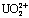 ions based on a carboxyl-functionalized Zn(II)-MOF platform[J]. Dyes and Pigments, 2019, 160: 159-164.
ions based on a carboxyl-functionalized Zn(II)-MOF platform[J]. Dyes and Pigments, 2019, 160: 159-164.
[20] HAO Ji-na, YAN Bing. A water-stable lanthanide- functionalized MOF as a highly selective and sensitive fluorescent probe for Cd2+[J]. Chemical Communications, 2015, 51(36): 7737-7740.
Synthesis of Ln-MOFs and its adsorption and fluorescence recognition of uranyl ions
LI Ying-mei1, 2, ZHOU Xia-yu1, 2, XIA Yu-xin1, 2, HU Dan1, 2, LI Zhe-yi1, 2, ZHANG Xu1, 2, LI Le1, 2, DAI Zhong-ran1
(1. Key Discipline Laboratory for National Defense for Biotechnology in Uranium Mining and Hydrometallurgy, University of South China, Hengyang 421001, China;
2. College of Public Health, University of South China, Hengyang 421001, China)
Abstract: A luminescent MOFs material Tb3+-UiO-66-(COOH)2(Ln-MOFs) was prepared by hydrothermal synthesis. The structure of Tb3+-UiO-66-(COOH)2 was characterized by Fourier transform infrared (FT-IR), scanning electron microscopy (SEM) and fluorescence spectrum (FL). The results show that the best conditions of uranium adsorption are as follows: pH is 7, adsorption time is 10 h, temperature is 313 K, the initial U(��) concentration is 60 mg /L, the maximum adsorption capacity of U(��) is 333.13 mg/g. The material can also be used to detect U(��) with fluorescence at the same time. The optimal excitation and emission wavelengths are 300 and 540 nm, respectively. There is a good linear relationship in the concentration range of 200 ��g/L to 10 mg/L 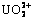 with a correlation coefficient of 0.9924. Limit of detection (LOD) is 232.7 ��g/L. The proposed method is simple, selective and sensitive.
with a correlation coefficient of 0.9924. Limit of detection (LOD) is 232.7 ��g/L. The proposed method is simple, selective and sensitive.
Key words: uranyl ions; MOFs; adsorption; fluorescence recognition
Foundation item: Project(51704170) supported by the National Natural Science Foundation of China; Project (2020JJ3028) supported by the Natural Science Foundation for Outstanding Young Scientists of Hunan Province, China; Project(2018SK2029) supported by the Key Program of Research and Development of Hunan Province, China; Project(S201910555148) supported by the Hunan College Students Innovation and Entrepreneurship Training Program, China
Received date: 2019-11-07; Accepted date: 2021-05-06
Corresponding author: DAI Zhong-ran; Tel: +86-15675479402; E-mail: dzr1122@126.com
(�༭ �� ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51704170)������ʡ���������ѧ����������Ŀ(2020JJ3028)������ʡ�ص��з��ƻ���Ŀ(2018SK2029)������ʡ��ѧ�����´�ҵѵ���ƻ���Ŀ(S201910555148)
�ո����ڣ�2019-11-07�������ڣ�2021-05-06
ͨ�����ߣ�����Ȼ����ʵ��ʦ����ʿ���绰��15675479402��E-mail��dzr1122@126.com
ժ Ҫ������ˮ�Ⱥϳɷ��Ʊ�һ��ϡ�����ӵĽ����л��Ǽܲ���(MOFs) Tb3+-UiO-66-(COOH)2(Ln-MOFs)������ɨ��羵(SEM)���������(IR)��ӫ�����(FL)�Բ��Ͻ��б���������������������������������ΪpH=7������ʱ��Ϊ10 h���¶�Ϊ313 K��U�ij�ʼŨ��60 mg/L�����£����������������ӵ�������Ϊ333.13 mg/g���ò���Ҳ������ӫ����U(��)����Ѽ��������ͷ��䲨���ֱ�Ϊ300 nm��540 nm����200 ��g/L��10 mg/L 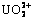 Ũ�ȷ�Χ�ھ������õ����Թ�ϵ���������ϵ��r=0.9924�������(LOD)Ϊ232.7 ��g/L���÷���������㡢ѡ����ǿ�������Ƚϸߡ�
Ũ�ȷ�Χ�ھ������õ����Թ�ϵ���������ϵ��r=0.9924�������(LOD)Ϊ232.7 ��g/L���÷���������㡢ѡ����ǿ�������Ƚϸߡ�


