���±�ţ�1004-0609(2008)08-1560-06
��������������Һ��Al(OH)3����ɺ˻���
������������Ԫ��������
(���ϴ�ѧ ��ѧ����ѧԺ����ɳ 410083)
ժ Ҫ��
�����������ƿ�������������Һ�絼���߸����ǣ��ڹ�������������Һ����ɺ˹����У�������¶�Ϊ323��328��333 K�����Ա�Ϊ1.337�������Ƴ�ʼŨ��Ϊ50~110 g/L����Һ�絼����ʱ��ı仯���ɣ�ȷ����Ӧ�յ��ڡ������������������������Һ����ɺ˹����еı��۷�Ӧ����Ϊ6~8���ٽ��?Һ������Ϊ34~35 mJ/m2���ٽ�ɺ˰뾶Ϊ1.5~2.0 ��m�� ���۷�Ӧ���Ϊ50.2 kJ/mol���������������Һ�ɺ˹���Ϊ�����ľ��෴Ӧ���ƣ��ҳɺ���������Һ��Թ����Ͷȴ��ڽ�ǿ��������ϵ�������ɺ˹�������ѧ���ƹ��̡�
�ؼ��ʣ�
��������Һ������ɺ����絼�������������
��ͼ����ţ�O643.12 ���ױ�ʶ�룺A
Mechanism of homogeneous nucleation in supersaturated sodium aliminate solutions
ZHANG Li-chuan, CHEN Qi-yuan, YIN Zhou-lan
(College of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: The homogeneous nucleation induction period of synthetic, optically clear caustic aluminate solution were investigated with the application of a self-made online conductivity analyzer. The experiments were performed at 323, 328 and 333 K and solution ratio of 1.337 with Na2Ok concentration in the range of 50?110 g/L. The results show that the nucleation kinetics are 6~8 orders dependence upon Al2O3 relative supersaturation and strong temperature effect, the critical interfacial energy is of 34?35 mJ/m2, the critical nucleus size is of 1.5?2.0 ��m and the activation energy is of 50.2 kJ/mol. The mechanism of sodium aluminate solution nucleation is homogeneous and chemical reaction controlled.
Key words: sodium aluminate solution; homogeneous nucleation; conductivity analyzer; online detection
��������Һ�ɺ˹�����Ϊ�ֽⷴӦ�ĵ�һ�����Ժ����������źܴ��Ӱ�졣��Ȼ������������������������Һ�ķֽ��ǼӾ��ַֽ���̣�Ȼ�����۶���ѧ�ĽǶ��������Բ��Ӿ��ֵľ���ɺ˹��̶���ѧ���ɵ��о�����Ϊ����������������Һ�ֽ�����ṩ��Ϊ��Ҫ����Ϊֱ�ӵ�ʵ������[1?2]��Ŀǰ���ڵ�������Ҫ�ǹ�������������Һ�ֽ��յ��ڽ綨����ȷ������ļ�ⷽ�������˹���ʱ������������������(��15��min)��������ʵ�龫��Ҫ��[2]��ROSSITER��[3]����MALLS��TEM��XRD��IFESEM���Ϸ���ʵ��������ӣ�������Ҫ��ߡ�
�������߲����������Ƶ���������Һ�絼�����߸����ǣ�ͨ���ⶨ��Һ�絼����ʱ��ı仯���ɣ�ȷ����������������Һ����ɺ˹����յ��ڣ�����Ͼ���ɺ����ۣ��о���������������Һ��Al(OH)3����ɺ˶���ѧ���̡�
1 ����ɺ�����
��������Һ�ֽⱾ�����Ǵ���������Һ������������������Ļ�ѧ��Ӧ���̣�����ľ���ɺ�����[4]��Ϊ���˹��̵�����������Һ�����Ͷȣ�����ɺ�����J(��λΪm?3s?1)�İ�������˹��Ӧ����ʽΪ

��Ϊ��Һ����Թ����Ͷȡ�Ce����Misra���鹫ʽ[8]����
![]()
��Һ��Ӧ�յ��ڦ���ɺ�����J�Ĺ�ϵ���Լ�ʾΪ
![]()
KΪ����ϵ��������ʽ(1)��(3)���ɵ�
![]()
ʽ�� B=K/A��ʽ(4)��������һ���¶��£�ln ����(ln S)?2�����Թ�ϵ������б��Ϊm���ɴ˿ɵ�

�����?Һ�����ܦã��������Gibbs-Thomson��ϵʽ[4]����ٽ�ɺ�����rc����Һ�����ͶȵĹ�ϵΪ

����ѧ�б�ʾ�ɺ����ʵķ���ʽΪ[4]
![]()
ʽ�� knΪ�ɺ����ʳ�����nΪ���۷�Ӧ����������ʽ(3)��(7)���õ��յ��ڼ���ʽ

2 ʵ��
�����������Ƶ���������Һ�絼�����߸����Dzⶨ��Һ�絼����ʱ��仯���̡���������LRC��Ƶ���ֵ����Ǹ�װ���ɣ�����Ƶ��Ϊ3��/s���������������������¼���������ݣ��Զ������յ���ֵ������ʹ�õĴ�����ʽ�絼�缫Ϊ���Ƶ�����Ƕ��ʯӢ���ڵ�Բϸ��˿(��=0.5 mm)���������ɣ����d=0.1~0.5 mm������������������Ϊ0.1%��ƽ����Ӧʱ�䣼0.1 s��
ʵ���о����ԱȦ�k=1.337�������Ƴ�ʼŨ��N0=50~110 g/L�Ĺ�������������Һ��323��328��333 K�µľ���ɺ˹��̣�ÿһ���¶���������7~10��ϵ��Ũ��ʵ�顣��k=1.645N/CΪ��Һ���Աȣ�N��C�ֱ�Ϊ��Һ���Լ��������������Ũ�ȡ�ʵ��ʱȡһ����Ԥ�����Ƶġ��ɳ����ȶ������Ũ��Һ(N0��254 g/L)��У� ��һ�������ڵ�ȥ����ˮϡ�ͣ����Ƴ���������Һ������0.2 ��m�ͼ�����Ĥ��ճ������Σ�ȥ��ϸ���ӣ�ʹ��Һ�����ȥ����ˮ������Ϊ100%��Ȼ�������Ч�ݻ�Ϊ600 mL���ܱ�ʽ�����ײ���ַ�Ӧ���У�����JHS?1/90�͵��Ӻ��ٽ�����ٽ���Һ��־��Ȼ�ϣ������ٶ�Ϊ300 r/min������LH586?2�ͳ�������ˮԡѭ�����ֺ��¡�ͬʱ���絼�缫������������Һ�в���ͨ�����ǿ�ʼʵʱ�����Һ�絼����ʱ��仯���̡�
���о����������Ƶ���Һ�ﵽ�ȶ��¶ȵ�ʱ��Ϊ��ʱ�̣�����ʱ��������Һ�絼�ʳ���ת������ʱ��Ϊ�յ��ڣ�Ҫ�������Ƶ���Һ����ճ��˵�װ�뷴Ӧ���в������¿�ʼ�������ʱ�䲻����5 min����Է�Ӧ�յ��ڿɺ��Բ��ơ�
3 ���������
ͼ1��ʾΪ��Ӧ��������Һ�絼����ʱ��ı仯���ɣ���ͬʵ�������»�����ƵĽ������ͼ1��֪�������ɺ˷�Ӧ�������Է�Ϊ3���Σ���һ��(A��)Ϊ�յ��ڣ��ڶ���(B��)Ϊ�����ڣ�������(C��)Ϊ���ٷ�Ӧ�ڡ������յ��ڼ���Һ���ֳ��壬���ȥ����ˮ�ڿɼ������������Ϊ�㣬��Al(OH)3�ᾧ��Ⱥ���������������ٽ�������Al(OH)3����㿪ʼ���ɣ���ҺҲ�ɾ����Ϊ�Ǿ��࣬��Һ�ֽⷴӦ����Ѹ������[8]�������Һ�ĵ絼��ͻȻ��������ζ���յ��ڵĽ��������ڵ絼�ʵIJ����½�������Ϊ���ŷ�Ӧ�IJ��Ͻ��У�Al(OH)3��������������࣬��Һ�������Ի��ǣ����ŵ絼�ز���������ȵ�ͬ���ⶨӡ֤����һ���̡�
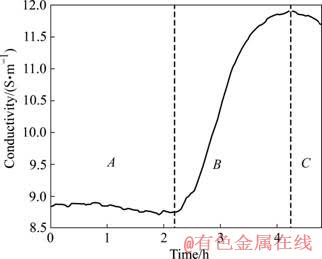
ͼ1 ��������������Һ����ɺ˹��̵絼����ʱ��ı仯����
Fig.1 Conductivity of homogeneous nucleation in sodium aluminate solution as a function of time (��k=1.337, N0=82.60 g/L, T=323 K)
��������Һ����ɺ���һϵ�п���Ļ�Ԫ��Ӧ����[2]���ӵ绯ѧ�Ƕȷ�������������������Һ�ɺ˹��������Ϊ�����ԱȽϲ�ĺ����������١�������ǿ��OH?������Ĺ��̣���Һ�ĵ�������˷����仯������ʵ�ʵ��յ��ں;���ɺ˹���ʮ�ָ��ӣ���ͼ1���Կ�������ʵ�����ݽ���С���˲��۳��������ź絼����һ���������Դ������ԵIJ��������������ƵķֽⷴӦ���̿��ܰ�����������Ӳ����ع����ת����
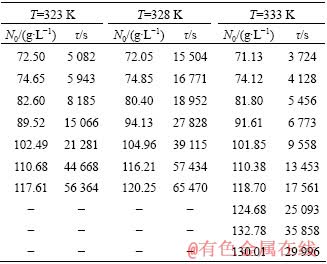
ʵ��ⶨ��ͬ�����¹�������������Һ����ɺ˹��̵��յ������1���С�
�� 1 ��ͬʵ�������¹�������������Һ����ɺ˹����յ���
Table 1 Induction periods of homogeneous nucleation in supersaturated sodium aluminate solutions (��k=1.337, N0= 50?110 g/L)
һ����Ϊ��������������Һ������Al(OH)3������������Һ�����Ͷ�S��S������Misra���鹫ʽ����ó�������S����Һ�����Ƴ�ʼŨ��N0��ϵ��ͼ2��ʾ��
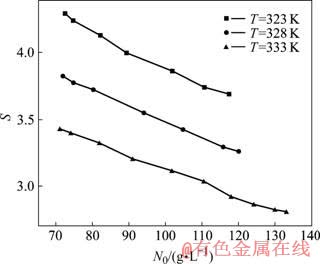
ͼ2 ��������Һ�����Ͷ�S������Ƴ�ʼŨ��N0�Ĺ�ϵ
Fig.2 Relationships between S and N0 diagram for supersaturated sodium aluminate solutions(��k=1.337)
��ͼ2��֪�����ڦ�k��ͬ�Ĺ�������������Һ��ͬһ�¶��£�����Һ�����Ͷ�����Һ�����Ƴ�ʼŨ�����Ӷ����ͣ�ͬһ�����Ƴ�ʼŨ���£���Һ�����Ͷ����¶ȵ����߶����͡�
ͼ3��ʾΪ��323��328��333 K�£���k=1.337ʱ��������Һ�����Ͷ������ɺ��յ��ڹ�ϵ����������ع鴦����ϵ����ͼ3��֪��ͬһ�¶��£���������Һ����ɺ��յ��ڶ���Һ��ʼ�����Ͷȴ��ں�ǿ��������ϵ����ͬ���Աȵ���������Һ�Ĺ����Ͷ�Խ�ͣ���Ӧ�ľ���ɺ��յ���Խ����������Һ�����Ͷ�һ���Ĺ�������������Һ�������ɺ˹��̵��յ����淴Ӧ�¶ȵ����߶����̡��������[2]���о���һ���������ڿ��Ա���ͬʱ����Һ�Ĺ����Ͷ���Ũ����������Ͻ��ͣ���һ����������ڵ�Ũ����Һ�У��ܼ�ˮ���㣬������Ԫ���ɶ�����ˮ�����Ӷ�ʹ������Ԫ�������ȶ�����Һ�к�������ת����������Ԫ���ٶȼӿ죬��ʹ��Һ���ڷֽ⣬�յ������̡�
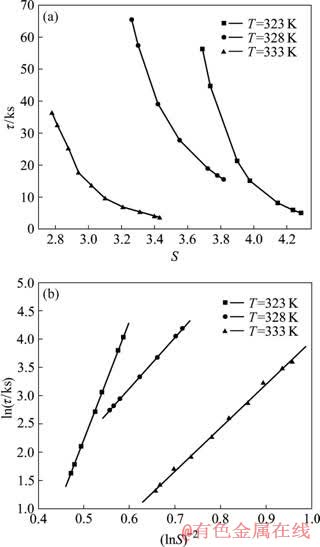
ͼ3 ��������������Һ����ɺ˹���S���ӡ�(lnS)?2��ln�ӹ�ϵͼ
Fig.3 S���� and (lnS)?2��ln�� diagrams for homogeneous nucleation of sodium aluminate solutions(��k=1.337)
����ROSSITER��[9?10]���о�����Һ�����Ͷ�S��2.51ʱ�ķ�ӦΪ���෴Ӧ�����ٶ���=2���ó��á�45��6 mJ/m2�����о��е���������Һ�����Ͷ�S������2.51��(lnS)?2��ln�ӹ�ϵ����û�г��ֶַ�����֤����Ӧ����Ϊ�����ľ��෴Ӧ���ơ���ʽ(5)��֪������?Һ�����ܵĹؼ�����ȷ��Ħ�������ܽ����ܼ��в����� �������͡�һ����Ϊ��������ҺŨ�ȡ����Աȵ������IJ�ͬ����ˮ��ʯ�ܽ���NaOH�еķ�Ӧ����3�ֿ��ܵ����[3]��
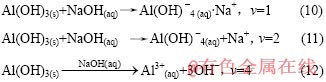
���ݻ�ѧƽ��ԭ������ǿ����£�Al(OH)3������ȫ����ΪAl+��OH?��ʽ(12)����ʾ�Ĺ����Dz����ܳ��ֵġ�
Ϊ�˼����������Ŀɿ��ԣ�ͨ������Mersmann����ľ��鹫ʽ[12]���ٽ��?Һ�����ܦý��й���

ͬʱ����1=1����2=2�ֱ����ʽ(5)������(lnS)?2��ln�ӻع�����mֵ������ٽ��?Һ�����ܦã����У���=16��/3��k=1.38��10?23 J/K��Mw=78��10?3 kg/mol����=2 420 kg/m3��N=6.02��1023/mol����=Mw/��N=5.35��10?29/m3��������2���С�
��2 ��ͬ�¶�����������Һ����ɺ˹����ٽ��-Һ�����ܹ���ֵ
Table 2 Critical interfacial energy of homogeneous nucleation in sodium aluminate solution(��k=1.337)
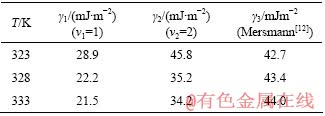
�ɼ�������֪���ڱ��о����о������£�Al(OH)3��NaOH��Һ�е��ܽ���̸�������ʽ(11)�������е�Ũ�ȹ�������������Һ�У��е�Ũ�ȹ�������������Һ�������������Ҫ��S4�ԳƵ�Al(OH)?4��ʽ���ڣ��ɴ˽�һ������ʽ(6)����ٽ�ɺ˰뾶rc=1.5~2.0 ��m��ֻ�����ɵľ��˰뾶����rc�ſ����ȶ����ڲ�������������ʵ�������¶���������Һ����ɺ˹����ٽ��Һ�����ܡ��ٽ�ɺ˰뾶�ļ������Ŀǰ���о�����[9?12]��һ�µġ�
���ڸ��ӷ�Ӧ���ԣ����۷�Ӧ������ӳij�ַ�Ӧ���Ũ�Ȼ���Թ����ͶȶԷ�Ӧ���ʵ����ô�С�������о����ӷ�Ӧ����Ҫָ�ꡣ���þ���ɺ����ۣ�����ͬ�¶��µĦҡ��ӹ�ϵ����������ع鴦����ϵ��ͼ4��ʾ��lg�ӡ�lg��ֱ��б�ʵľ���ֵ��Ϊ�ɺ˷�Ӧ���̵ı��۷�Ӧ����n�����о��У�T=323 Kʱ����������������Һ����ɺ˹��̵ı��۷�Ӧ����n=11��T=328 Kʱ��n=7��T=333 Kʱ��n=6�����ݱ��۷�Ӧ�����Ĵ�С�������ۣ���ʵ����������������Һ�ijɺ�����ǿ����������Һ����Թ����Ͷȣ��ɺ˹����Ǿ�����ƻ������ǻ�ѧ��Ӧ���̡�T=328��333 Kʱ�ķ�Ӧ������Ϊ�ӽ�������323 K�µķ�Ӧ��������Զ������������������¶ȵĽ��ͣ���Һ�ṹ�����仯���ɺ˹��̵Ŀ��ƻ���Ҳ�����˱仯����[9]�������о�һ�㼯����T=328 K���ϣ�һ���������������Һ����ɺ˹��̵ı��۷�Ӧ������5~8����[2, 9?13]�����о������֮�Ǻϡ�
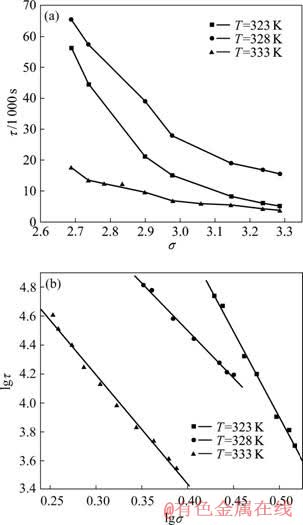
ͼ4 ��������������Һ����ɺ˹��̦ҡ��ӡ�lg�ҡ�lg�ӹ�ϵͼ
Fig.4 �ҡ��� and lg�ҡ�lg �� diagrams for homogeneous nucleation of sodium aluminate solutions(��k=1.337)
Ϊ�˽�һ�������¶ȶ���������Һ����ɺ˹��̵�Ӱ�죬���ð�������˹���ʳ�������ʽ[13]����ɺ˷�Ӧ���̵Ļ�ܡ�

ͼ4��lg�ӡ�lg��ֱ�߽ؾ�Ϊlg(K/kn)������3���¶���lg�ӡ�lg��ֱ�߽ؾ࣬������ɺ˷�Ӧ���Ea��50.2 kJ/mol��DAMIEN��[14]�����������»�õĽ��ΪEa��55 kJ/mol��van STRATEN��[15]��VEESLER��[16]�ֱ�ó��ɺ˹��̵Ļ����40~70 kJ/mol֮��Ľ������ʵ������֮���ơ��ϸߵĻ�ܽ�һ��֤����������������Һ����ɺ˹������ڻ�ѧ���� ���̡�
4 ����
1) ��������������Һ����ɺ˹����յ��ڶ���Һ��ʼ�����Ͷȴ��ں�ǿ��������ϵ����ͬ���Աȵ���������Һ�Ĺ����Ͷ���Ũ����������Ͻ��ͣ���Ӧ�ľ���ɺ��յ��ڲ�����������ͬ���ԱȺ����Ͷ���������Һ����ɺ��յ������¶����������̡�
2) �о��õ�ʵ�������£���������������Һ����ɺ˹����еĹ�?Һ�����ܦá�34~35 mJ��m2���ٽ�ɺ˰뾶rc��1.5~2.0 ��m�����۷�Ӧ����n��6~8�����۷�Ӧ���Ea=50.2 kJ/mol��������������������Һ�ɺ˹���Ϊ�����ľ��෴Ӧ���ƣ��ҳɺ���������Һ��Թ����Ͷȴ��ڽ�ǿ��������ϵ�������ɺ˹�������ѧ���ƹ��̡�
3) �о������������������Ǻϣ���������������������������Һ����ɺ��о�������Ҫ��ľ��Ⱥ�ȷ�ȣ��ֱ����˳����ⷽ�����Ȳ����������Ͷ����������÷��豸Ҫ��ߡ��������ߵ�ȱ�㣬��ˣ�������������Һ����ɺ˶���ѧ�о�������кܺõ�Ӧ�ü�ֵ��
[1] �� ��, ����Ԫ, ������, ��ƽ��. ��������������Һ�ṹ������ֽ�����о���״[J]. ��ѧ��չ, 2003, 15(3): 170?177.
LI Jie, CHEN Qi-yuan, YIN Zhou-lan, ZHANG Ping-min. Development and prospect in the fundamental research on the decomposition of supersaturated sodium aluminate solution[J]. Progress in Chemistry, 2003, 15(3): 170?177.
[2] �� ��, ����Ԫ, ������. ��������������Һ�����������Է��ɺ˶���ѧ���ɵ��о�[J]. �ߵ�ѧУ��ѧѧ��, 2003, 24(9): 1652?1656.
LI Jie, CHEN Qi-yuan, YIN Zhou-lan. Studies on the kinetics of unseeded nucleation of aluminum trihydroxide from supersaturated sodium aluminate solutions[J]. Chemical Research in Chinese Universities, 2003, 24(9): 1652?1656.
[3] ROSSITER D S, FAWELL P D, ILIEVSKI D. Investigation of unseeded nucleation of gibbsite, Al(OH)3, from synthetic Bayer liqours[J]. Journal of Crystal Growth, 1998, 191(3): 525?536.
[4] MULLIN J W. Crystallization[M]. London: Butterworth- Heinemann Ltd. 1993: 304?315.
[5] ZHANG Yi-fei, LI Ying-hui, ZHANG Yi. Supersolubility and induction of aluminosilicate nucleation from clear solution[J]. Journal of Crystal Growth, 2003, 254(1/2): 156?163.
[6] SMITH P, WOODS G. Measurement of very slow growth rates during the induction period in aluminum trihydroxide growth from Bayer liquors[J]. Light Metals, 1993: 113?117.
[7] MISRA C, WHITE E T. Kinetics of Crystallization of aluminium trihydroxide from seeded caustic aluminate solution[J]. Chem Eng Progr Sympos Ser, 1970, 110(2): 53?64.
[8] SAWSAN J F, GORDON M P, MANIJEH M R. Atomic force microscopy study of the growth mechanism of gibbsite crystals[J]. Journal of Chemical Physics, 2004, 6(1/4): 1049?1055.
[9] LI Hui-xin, ADDAI-MENSAH J, JOHN C T. The crystallization mechanism of Al(OH)3 from sodium aluminate solutions[J]. Journal of Crystal Growth, 2005, 279(3/4): 508?520.
[10] MERSMANN A. Calculation of interfacial tensions[J]. Journal of Crystal Growth, 1990, 102(2): 841?847.
[11] ����Ⱥ, ������, ����Ԫ, �� ��, ����Ƽ, ��ƽ��. ��������Һ�������ܼ�������[J]. �й���ɫ����ѧ��, 2004, 14(2): 311?316.
ZHANG Mu-qun, YIN Zhou-lan, CHEN Qi-yuan, LI Jie, HU Hui-ping, ZHANG Ping-min. Solvent effect of species in sodium aluminate solution[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(2): 311?316.
[12] LI Hui-xin, ADDAI-MENSAH J, JOHN C T. The influence of Al(��) supersaturation and NaOH concentration on the rate of crystallization of Al(OH)3 precursor particles from sodium aluminate solutions[J]. Journal of Colloid and Interface Science, 2005, 286(2): 511?519.
[13] LI Jun, CLIVE A P, ADDAI-MENSAH J. The influence of alkali metal ions on homogeneous nucleation of Al(OH)3 crystals from supersaturated caustic aluminate solutions[J]. Journal of Colloid and Interface Science, 2000, 224(2): 317?324.
[14] DAMIEN R H, ROLAND I K, CLIVE A P. A dynamic light scattering investigation of nucleation and growth in supersaturated alkaline sodium aluminate solutions (synthetic Bayer liquors)[J]. Colloids and Surfaces A, 1999, 154(3): 343?352.
[15] VAN STRATEN, DE BRUYN P L. Precipitation from supersaturated aluminate solutions 2. Influence of alkali ions with special reference to Li2+ plus[J]. Journal of Colloid Interface Science, 1985, 103(2): 493?507.
[16] VEESLER S, BOISTELLE R. Growth kinetics of hydrargillite Al(OH)3 from caustic soda solutions[J]. Journal of Crystal Growth, 1994, 142(1/2): 177?183.
������Ŀ��������Ȼ��ѧ�����ص�������Ŀ(520476107)
�ո����ڣ�2007-11-23�������ڣ�2008-05-08
ͨѶ���ߣ�����Ԫ�����ڣ���ʿ���绰��0731-8877364��E-mail: cqy@mail.csu.edu.cn


