���ӽ�������ȳ����Ʊ��ߴ��ܵ��о�
������ɫ�����о���Ժ�����ڽ��²��Ϲɷ�����˾
ժ Ҫ��
ѡ����������������֬201��D301��ȳ��Ӿ������Һ,��������֬�Ե��Һ�����ӵ��������,�Լ����ܵ�⾫��������,�¶ȡ������ܶȡ�pH�ȵ��ղ����Դ�CoCl2��6H2O��ϵ���Һ����Ҫ����Fe,Ni,Cu,Zn,Pb��ȥ��Ӱ��,������ܾ����Թ�ŵ�����(GD-MS)ȫԪ��(73��Ԫ��)����,�õ�����Ϊ99.9995%�ĸߴ��ܡ�ֻͨ�����ӽ�����֬�͵�⾫�������ᴿ,�Ϳ����ȶ��Ʊ��ߴ���,ʵ�ָߴ��ܵĹ�ҵ��������
�ؼ��ʣ�
���ӽ���;�ߴ���;��⾫��;��������������֬;�Թ�ŵ�����;
��ͼ����ţ� TF816
����飺����(1984-),Ů,����������,˶ʿ,��������ʦ;�о�����:�ܡ����ȵĸߴ������ᴿ(E-mail:liudan@grikin.com);
�ո����ڣ�2012-04-18
�������ҿƼ����Ƽ�֧�żƻ�����(2006BAF07B02);
Preparation of High Purity Cobalt with Deep Purification by Ion Exchange
Abstract��
The electrolyte was deeply purified through a weak alkaline anion resin 201 and D301.The resin for the adsorption of ions in the electrolyte,and the influence of the electrolytic parameters in cobalt electrolytic refining process,such as temperature,current density and pH,on removing the main impurities Fe,Ni,Cu,Zn and Pb in the pure system CoCl2 �� 6H2O,were studied.The cobalt electrodeposition was analyzed by GD-MS(for 73 elements),and the high purity cobalt of 99.9995% was prepared.Only using the ion exchange resin and electrolytic refining for purification,high purity cobalt could be prepared steadily to achieve high-purity cobalt industrialization.
Keyword��
Received�� 2012-04-18
�����Ʊ��ż�¼���ʡ� �ż�¼��ͷ�� ��������ͼ��ɵ�·��Ԫ��������Ҫ����, 99.999%�������ߴ��ȵ�����������Ϊ�Ƚ�����Ԫ���İвġ� �ܰв��е����ʻ�Ӱ�����������ʹ������, �ߴ�������Ҫ������Ԫ��ΪFe, Ni, Cu, Fe�ᵼ�µ������������ܵIJ�һ��, Ni��Ӱ��뵼��Ľ�������, Cu��Ӱ��뵼��Ԫ���ĵ�������
�������ӽ������ķ�չ, ����Һ�ᴿ�����õ��Ͽ�ķ�չ�� ������ ���ô� ������ �ձ��ȹ������ᴿ�����Ͻ����˴������о�����, �ձ�JMC��˾����99.998%�ߴ��ܲ�Ʒ, Nikko��˾���ձ���ʽ���绯ѧ�о�������99.999%�ߴ���, ���ڽ���ɫ������˾���ø�Ĥ��ⷨ���������ȴ���99.99%��1#�����
1 ����ԭ��
�����ӽ�����֬��д��R��N+Cl-(ǿ����), R-NH+3OH-(������)��
R-NH+3OH-+H++FeCl-4?R-NH+3FeCl-4+H2O (1)
R-NH+3OH-+H++NiCl-4?R-NH+3NiCl-4+H2O (2)
R-NH+3OH-+H++CuCl-4?R-NH+3CuCl-4+H2O (3)
2 ʵ ��
2.1 ���ӽ�����֬ʵ��
��֬Ԥ����: ��֬����30 �洿ˮ��ϴ3�γ�ȥ�л���, ����5%��NaOH��Һ����12 h, ϴ������, ����5%��HCl��Һ����12 h, ϴ�����Ա���
��֬����: ����10%��HCl��ϴ��֬ϴ��, ��ϴҺ�в�������ɫΪֹ; ����5%�������ϴȥ��Cu, Fe, ��ˮ���γ�ϴȥ��Zn, ����
��ʵ��ѡ�÷�����CoCl2��6H2O, �ô�ˮ���Ƴ��Ȼ��ܵ��Һ, ͨ�����ӽ��������е��Һ�ľ������ӡ� ÿ�����ӽ������ijߴ�Ϊ: ��10 cm��100 cm, �����������ּ�����, ��������оѭ���ý��е��Һ��ѭ��, ά�ֵ��Һ����֬�е�����Ϊ15 L��h-1�� ��1��2�ֱ�Ϊ��֬����ǰ����Ҫ���ʵ�ICP-MS���������
������֬201, D301, 201+D301, �ֱ�������ӽ�������, ���Һ����ICP-MS�������ʺ���, ����2��
��1 CoCl2��6H2O(AR)�������(��g��ml-1)
Table 1 Results of CoCl2��6H2O(AR)(��g��ml-1)
| Elements | Fe | Ni | Cu | Zn | Pb |
| Content | <5.0 | <1.0 | 6.0 | <1.0 | <1.0 |
��2 ��֬�������Һ�����ʺ���(��g��ml-1)
Table 2Impurities content in electrolyte by resin adsorption (��g��ml-1)
| Types | Fe | Ni | Cu | Zn | Pb |
| 201 | 2.9 | 1.0 | 4.0 | <1.0 | 0.8 |
| D301 | 1.0 | 1.0 | <1.0 | <1.0 | <1.0 |
| 201+D301 | <1.0 | <1.0 | <1.0 | <1.0 | <1.0 |
�Ա���֬����ǰ��, 201���Ȼ�����ϵ�ж�Fe, Pb������Ч��������, D301����Ҫ����Fe, Cu���ӵĽ���, ���������������ܽ�ʹ���������ۻ�, �Ȼ��ܵ��Һ����201��D301���Ͻ�������ʵ���, ���ʺ�����С��1.0 ��g��ml-1, ʼ��ά���ڸߴ����Ʊ����Һ����Ҫ��Χ֮��, ��֤�����ܵĴ���, �÷��������ɱ���, ������
2.2 ��⾫��ʵ��
2.2.1 �¶ȵ�Ӱ��
�¶Ȼ�������Һ�����ӷŵ��λ�ı�, ���������������ij���λ�����͡� ����һ�������, ��ɢ�ٶ����¶����߶��ӿ�, �����������ײ���ƶ����; �����¶�̫��, ������ܵ���Ӧ��̫��, �ܴ���̫��, Ϊ�¸������ܰ���и�����ܴ�IJ���
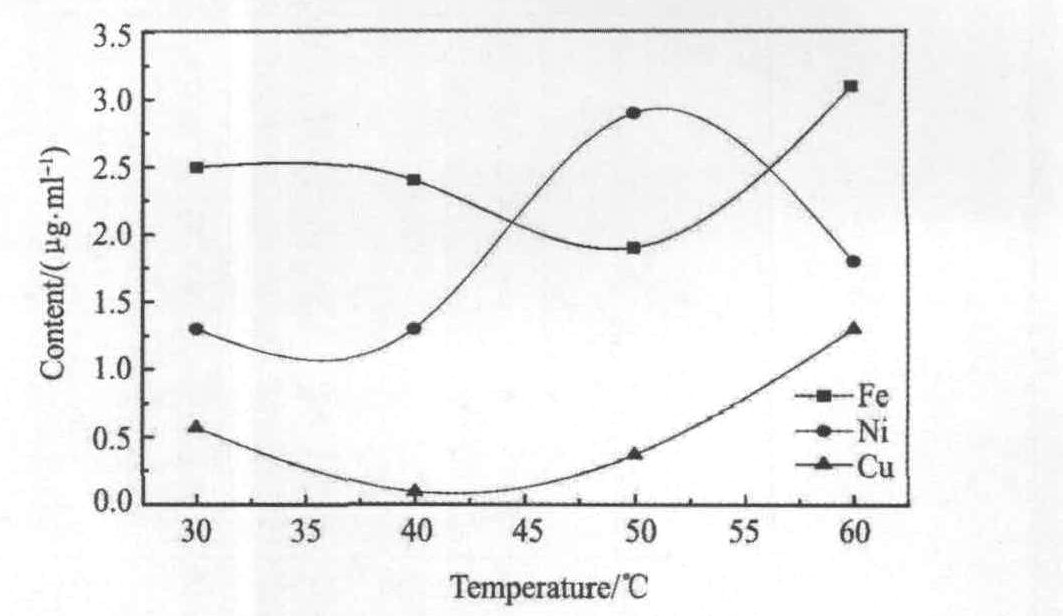
��ͼ1���Կ���: ���¶ȵ�����, Fe, Cu�����ȼ��ٺ�����, Ni�����Ӻ͡� ���ܵ�ԭ����
2.2.2 �����ܶȵ�Ӱ��
ͼ1 ��ͬ�¶����������ʺ����仯
Fig.1 Impurities of cobalt at different temperatures
��ߵ����ܶ�, ������ߵ��۵���������, �ʵ���ߵ����ܶȿ��Խ��������ɱ��� ��֤��Ʒ����, ��ά�����������dz���Ҫ�� ���ǵ����ܶȹ���, ����������������ǿ�ҷŵ�, �Ӷ�Ӱ����������Ʒ������
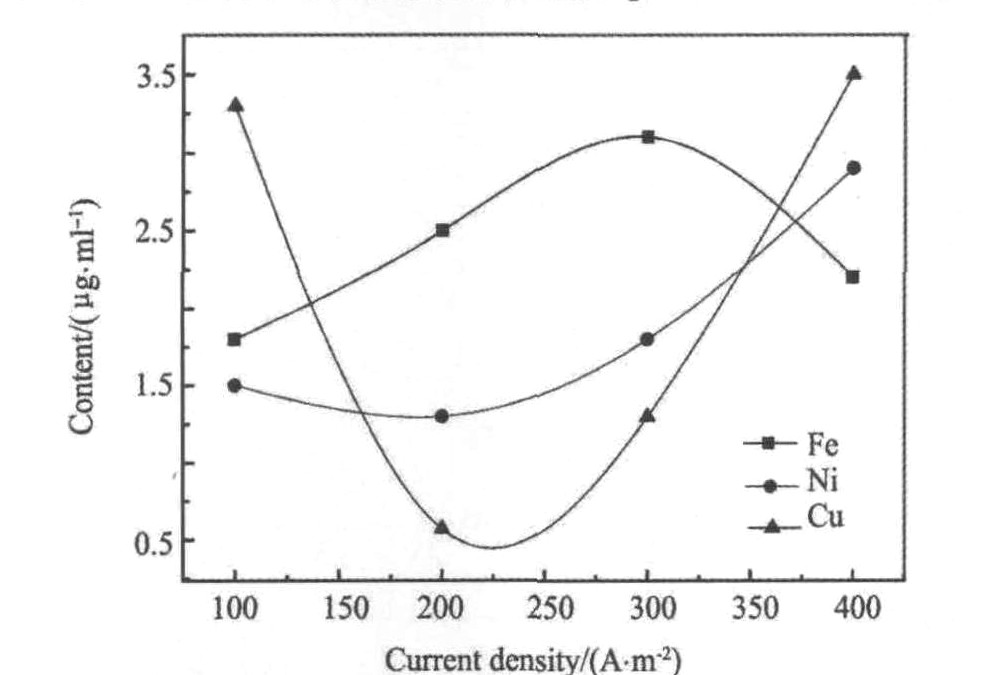
��ͼ2���Կ���: Cu������ܶȵ����Ӷ�����, Fe����ı仯����Ҳ�Ǽ��ٵ�(�����ܶ�>250 A��m-2)�� ���ʽ��������������е����÷���ʽ(4)��ʾ
ʽ��KiΪ������ɢ�ٶȳ���; CiΪ�����ڲ���Ũ��; iΪ��ͬ����; ��Ϊ��������Ч��; IΪ���������ܶȡ�
��ʽ(4)�ɿ��������������������к������ŵ����ܶȵ����Ӷ�����, ���Ƕ�Ni����, ���ݧ����֧ߧ֧��ӧ觪��
2.2.3 pH��Ӱ��
���Һ��ȶԵ����̵�Ӱ�����Ϊ��pHֵ����������ѹ��Ӱ��, �Ӷ�Ӱ�쵽�������ӵ�ƽ���λ
ͼ2 ��ͬ�����ܶ������������ʺ����仯
Fig.2 Impurities of cobalt at different current density
2.2.4 ��Ĥѭ�����
���ÿ������������ܵĵ����, �����ϵĸ��ֽ����ؽ������������ܽ��������Һ��, �������������������ϳ�����Ӱ���ܵĴ��ȡ� ��ʵ���в��ø�Ĥ���, ʹ�����������Һ��������Ⱦ, ��֤���ܵĴ���, ��3�Ǹ�Ĥ����Ĥ������ܲ�Ʒ��GD-MS����������ձ�, ��Ĥ�����Fe, Ni, Cu�������Խ��͡�
��Ĥ�����Ŀǰ�ߴ����������ձ�ʹ�õĵ�ⷽ��
��3 GD-MS�������(��g��ml-1)
Table 3 Results by GD-MS (��g��ml-1)
| Element | Fe | Ni | Cu |
| Non-diaphragm electrolysis | 2.2 | 2.6 | 4.00 |
| Diaphragm electrolysis | 1.9 | 1.3 | 0.37 |
��4 �����GD-MS������� (��g��ml-1)
Table 4 Results of electrolytic cobalt by GD-MS (��g��ml-1)
| Elements | Content | Elements | Content | Elements | Content |
| Na | 0.200 | Ni | 1.100 | Cd | 0.037 |
| Si | 0.058 | Cu | 0.066 | Sn | 0.007 |
| Cl | 0.570 | Zn | 0.065 | Sb | 0.005 |
| K | 0.016 | Pb | 0.590 | W | <0.005 |
| Cr | 0.013 | Ge | <0.050 | Cd | 0.037 |
| Mn | <0.005 | Zr | <0.005 | Bi | <0.005 |
| Fe | 2.000 | Ag | 0.150 | Purity | 99.9995% |
3 �� ��
ͨ�������������ӽ�����֬201��D301, ��Ⱦ����Ȼ�����ϵ�е�Fe, Ni, Cu, Zn, Pb������, ��֤�����Ĥ�����еĵ��Һ�����ʺ�����<1.0 ��g��ml-1, �ٽ��е�⾫��, ͨ�����Ƶ������������ܶ�200 A��m-2, �¶�35��45 ��, pHֵ1��2, �Ʊ��õ�����Ϊ99.9995%�ĸߴ��ܡ� ��Դ�ͳ�ߴ��ܵ��Ʊ�����, ��ʵ�鷽�����ռ� �ɲ�����ǿ�� �ɱ���, �����ȶ����иߴ��ܵĹ�ҵ��������
�����