���±�ţ�1004-0609(2016)-06-1339-11
���ȶ��ķ�������ﯷ�ĩ��ˮ��ˮ�ⷨ�Ʊ�
��־�꣬�����ǣ������£�����������
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ��
����ˮ��ˮ�ⷨ�Ʊ������ɿص����ȶ��ķ��������(Y-TZP)��ĩ������ˮ��ʱ�䡢�¶Ⱥ�H+Ũ�ȶ�Y-TZPǰ�����ĩ������������ֲ���Ӱ�졣���������ˮ��ˮ�ⷨ�Ʊ���Y-TZPǰ�����ĩΪ��б�࣬��ɢ�Ժã���������Ϊ50~300 nm��ˮ��ˮ�ȷ�Ӧ����Խ��֣�ǰ�������ƽ������Խ�»������������ֲ��������ʵ���Ũ��(0.485 mol/L ZrOCl2��0.03 mol/L YCl3)���¶�(130~150 ��)��Χ�ڣ������¶ȣ�ǰ�������ƽ��������186.2 nm����Ϊ94.1 nm������ֲ���խ��H+Ũ�ȶ�ǰ�������ƽ������Ӱ�����ԣ����H+Ũ�ȣ�ǰ���������ƽ��������������С��ˮ��ˮ�ⷨ�Ʊ���Y-TZPǰ����ΰ����ƺ���1000 ������1 h�õ����ȶ��ķ��������(Y-TZP)��ĩ������ԼΪ120 nm������ֲ���խ��
�ؼ��ʣ�
�������Y-TZPǰ������ˮ��ˮ�����������ֲ���
��ͼ����ţ�TG146.2���� ���ױ�־�룺A
�������һ����;�㷺���մɲ��ϣ������������ķ��͵�б3�־���ṹ�����Ƿֱ���2643 K���ϡ�1443~2643 K֮���С��1443 K�¶ȷ�Χ���ȶ���������ķ���ת��Ϊ��б�����䣬������5%�ļ���Ӧ��������8%���������[1]����ˣ���������մ����սή���У�������һ������������ͣ�������������Խϲ�[1]���о����֣���������Y3+��Mg2+��Ce4+�������ӣ���ʹ��������������Ա����ķ���������࣬�Ӷ����������մ��ս���ȴ��������͵�����[2]�����ȶ������(YSZ)�մ���ѧ������Խ���������������Ʊ�����һֱ���о����ȵ�[2-8]��
Ŀǰ��ʪ��ѧ���Ʊ����ȶ�����ﯷ�ĩ�ķ����г�����[3-5]���ܽ�-������[6]������-ˮ�ȷ�[8-10]��ˮ�ⷨ[11-15]�ȶ��֣����У������ַ����ѵõ��Ϲ㷺����ҵӦ��[12]���������Ʊ���ˮ�������������С�����������ֲ��������ޣ���ˮ���ͱȱ����ܽϸߣ���ϴ�ӡ����P���չ��������γ�Ӳ�žۡ��ܽ�-�������ܺĵͣ����ﻯѧ�ɷ־�һ�������ո�����ԭ�ϳɱ��ߣ�����ʵ�ֹ�ҵ��������-ˮ�ȷ��ǽ��������Ʊ���ˮ��������پ�ˮ�ȴ�������߷�ĩ�ķ�ɢ�Ժͽᾧ�ȣ�����ĩ��ò�仯�����Ծ��нϸߵıȱ����ܣ����žۡ�ˮ�ⷨ�ַ�Ϊ��ѹˮ�ⷨ[13-15]��ˮ��ˮ�ⷨ[11-12]����ѹˮ�ⷨ���ڳ�ѹ���¶ȵ���100 ��������£�ͨ���������Һˮ������Ʊ�����ﯷ�ĩ���÷���ĩ��ò���ڿ��ƣ�����Ӧ��ʱ��������������70 h�������ڹ�ҵ����[13]������¶ȿ���������ˮ��ʱ��[13]��ˮ��ˮ�ⷨ�����¶ȴ���100 ���ˮ�������£�ʹ�������Һ�Է�ˮ�⣬�Ʊ�����ﯷ�ĩ�ķ������÷��ȿ˷���ѹˮ�ⷨ��Ӧ��ʱ�����IJ��㣬�ֱ�������ò���ڿ��Ƶ��ŵ㡣
Ŀǰ������ﯷ�ĩ�ij�ѹˮ�ⷨ�Ʊ������������ƣ��������б���[13]��������ˮ��ˮ�ⷨ�ı�������[11-12]���ر��ǶԷ�ĩ��������ֲ���ˮ��ˮ������֮��Ĺ�ϵ����ȱ��������о����⼫����Լ�����ȶ�����ﯷ�ĩ�Ʊ�����ˮƽ��������
����������ZrOCl2��YCl3Ϊԭ�ϣ�����ˮ��ˮ�ⷨ���ֱ�������Ͱ�ˮΪ��ҺpHֵ���ڼ�����ˮΪ����������130~150 ��ˮ���������Ʊ�Y-TZPǰ�����ĩ��ϵͳ�о�ˮ��ʱ�䡢�¶ȡ�H+Ũ�ȵȶ�Y-TZPǰ�������������ֲ���Ӱ�죬�о�����Ը��������ȶ�����ﯷ�ĩ�Ĺ�ҵ����������ָ�����塣
1 ʵ��
1.1 ʵ��ԭ��
ʵ��ԭ��Ϊ�������(ZrOCl2��8H2O���Ͳ����ػ�������˾����)���Ȼ���(YCl3��6H2O���Ϻ������������Ƽ��ɷ�����˾����)������(HCl���������Ż����Լ�����˾����)����ˮ(NH3����ҩ���Ż�ѧ�Լ�����˾����)��������(AgNO3����ҩ���Ż�ѧ�Լ�����˾����)�����������Ϊ��ѧ���⣬�����Ϊ�������Լ���ʵ����ˮΪ����ȥ����ˮ��
1.2 ��Ʒ�Ʊ�
1) ��ZrOCl2��8H2O��YCl3��6H2O��Ħ����97:6�ı����ܽ⣬����ZrOCl2Ũ��Ϊ0.97 mol/L��YCl3Ũ��Ϊ0.06 mol/L����Һϡ��һ������130~150 ���¶ȷ�Χ��ˮ��6~18 h����Ȼ��ȴ���õ���ɫ�ȶ�����Һ������ˮϴ3~5�飬ֱ����0.1 mol/L��AgNO3��Һ��ⲻ�������ӣ������Ҵ�ϴ�����Σ����ĺ���ں����о�60 �����8 h���õ���ɫ��ĩ����ĥ��������
2) ȡ����������Һ50 mL���ֱ���벻ͬŨ�ȵİ�ˮ��HCl��Һ50 mL����130 ��ˮ��18 h����Ȼ��ȴ��ͬ����1ϴ�Ӹ����ĥ��������
3) ȡ����130 ��ˮ��12 h��İ�ɫ�ȶ�����Һ����30����½�������1mL/min����10%��ˮ(��������)��pH=9�����ó»�һ��ҹ��ͬ����1ϴ�Ӹ����1000��������1h����ĥ��������
ˮ��ˮ�ⷨ�Ʊ�Y-TZP������ͼ1��ʾ��
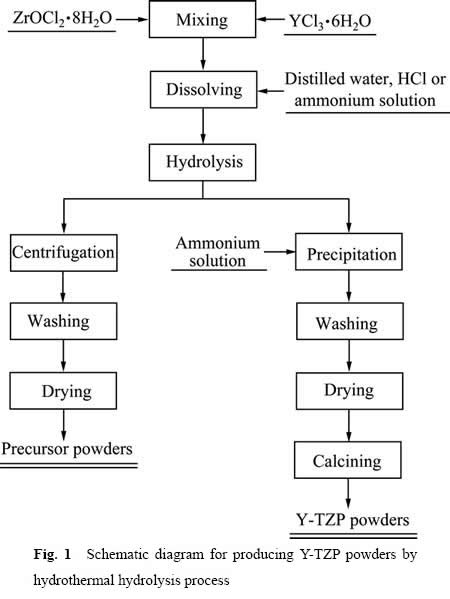
ͼ1 ˮ��ˮ�ⷨ�Ʊ�Y-TZP����ͼ
1.3 ��ĩ����
���ó�����ɨ��羵(JSM-2100F)�۲������ò����������ɢ״̬������XRD(Rigaku-TTR����X���������ǣ�Cu�У�K������=0.154 06 nm)������Ʒ���ࣻ����ICP-AES��ﯺ��Ƶij����ʽ��з������㣻����BET�����Dzⶨ����ǰ����Ʒ��N2�������Ѹ����߲����з�����
2 ���������
2.1 ˮ��������Ʊ�������κ�����������
���Ȼ������Һ��ˮ�ⷽ��ʽΪ
![]() ��
��![]() (1)
(1)
һ����ΪZrOCl2����ˮ��ZrO2+������ˮ��Һ�����������[Zr(OH)2��4H2O]48+��ʽ���ڣ���ÿ��[Zr(OH)2��4H2O]48+���ԭ�Ӱ����������У�ÿ���ԭ��ͨ��4�����ǻ���4��ˮ���ӳ�ͬ����λ�������¶ȣ�[Zr(OH)2��4H2O]48+ͨ�������ӻ����̴����ˮ���ͷ�H+�����ɾ������ǻ����������[13][Zr(OH)2+x��(4-x)H2O]4(8-4x)+������һ���Ͽ�Ĺ���[14]����Ӧ���£�
![]() ��
��![]() (2)
(2)
�������ǻ���![]() ֮���ͨ���ۺ��γɾۺ������ˮ��Ľ��У��ۺ���Ũ�ȴﵽ�ٽ�ֵ����౬���κˣ�
֮���ͨ���ۺ��γɾۺ������ˮ��Ľ��У��ۺ���Ũ�ȴﵽ�ٽ�ֵ����౬���κˣ�![]() ���ھ��˱��渽�����������˳����γ���ʼ��������ʼ������ͨ���ۺ����ã��γɱ��ۿ���[15]������HOGG��[16]��Homocoagulation��Heterocoagulationģ�ͼ��㣬��ʼ�����ľۼ��־���ۼ��ͷǾ���ۼ����ַ�ʽ����BLEIER��[17]�о����֣��ڽϸߵ�ZrOCl2Ũ���£�ͨ��ˮ�ⷴӦ�Ʊ��������ǰ������ۿ�����Ҫ�ɷǾ���ۼ��γɵġ�ͼ2��ʾΪͨ��ˮ��ˮ��������Ʊ���Y-TZPǰ�����SEM����ͼ2���Կ�����Y-TZPΪϸС�����ž��塣
���ھ��˱��渽�����������˳����γ���ʼ��������ʼ������ͨ���ۺ����ã��γɱ��ۿ���[15]������HOGG��[16]��Homocoagulation��Heterocoagulationģ�ͼ��㣬��ʼ�����ľۼ��־���ۼ��ͷǾ���ۼ����ַ�ʽ����BLEIER��[17]�о����֣��ڽϸߵ�ZrOCl2Ũ���£�ͨ��ˮ�ⷴӦ�Ʊ��������ǰ������ۿ�����Ҫ�ɷǾ���ۼ��γɵġ�ͼ2��ʾΪͨ��ˮ��ˮ��������Ʊ���Y-TZPǰ�����SEM����ͼ2���Կ�����Y-TZPΪϸС�����ž��塣
2.2 ˮ��ʱ���Ӱ��
����0.485 mol/L ZrOCl2+0.03 mol/L YCl3��Һ100 mL��װ���ܱյĸ�ѹ���У��ֱ���130 ��ˮ��6��9��12��18 h������ˮ��ʱ���Zr��Y�ij����ʼ�Y-TZPǰ������ò��Ӱ�죬��1����Ϊ��ͬˮ��ˮ����������Һ��Zr��Y�ij����ʡ�ͼ3��ʾΪ�����SEM�������ֲ�ͼ��

ͼ2 ˮ��ˮ��������Ʊ�������ﯸ߱���SEM��
ͼ3������Ϊˮ�Ȳ�ͬʱ�����Ʒ��SEM������Ϊ���ͳ��ͼƬ��150~200������(��˵����Ϊ���ۿ�������ͬ)������õ��������ֲ�ͼ������dΪƽ����������ϱ�1��ͼ3���Կ�����ͨ��ˮ��ˮ��������Ʊ���Y-TZPǰ�������Ϊ���������Σ���ɢ�Ժã���Ӧ6 h��9 h��Zr�ij����ʴ�76.1%����Ϊ94.2%����ĩ��ƽ��������131.4 nm��Ϊ185.2 nm��˵��ˮ��ˮ�ⷴӦ���е�����֣������ߴ�����[14]��ˮ��9 h��12 h��18 h��Zr�ij�������94%���ϣ��������仯�����ԣ��������ֲ�������������ڷ�Ӧ����������ˮ��ʱ����ӳ�����0.96 mol�������У�Y-TZPǰ���巢����Ostwald�»������´���������ͬʱ��һ�Ա���1��ˮ�Ⱥ�Y�ij����ʺ�С�����ǵ�����ﯵ�����������130 ��ˮ��ʱ��Y3+��0.96 mol/L��������Һ�л������ᷢ��ˮ�������Ӧ��
2.3 ˮ���¶ȵ�Ӱ��
����0.485 mol/L ZrOCl2+0.03 mol/L YCl3��Һ100 mL��װ���ܱյĸ�ѹ���У��ֱ���130��140��150 ��ˮ��12 h������ˮ���¶ȶ�Y-TZPǰ������ò�������ߴ��Ӱ�졣ͼ4��ʾΪ�����XRD�ס�ͼ5��ʾΪ�����SEM�������ֲ���
ͼ4��XRD��ɨ�跶ΧΪ22��~28�㣬ɨ������ 1 (��)/s������0.01�㡣ͼ����ʾ����ͬ�¶����Ʊ�����Ʒ��Ϊ��б�࣬�������¶ȵĸı䣬���β�û�����Ա仯���ʵ�б�ࡣ��ͼ3��[111]����������ϲ���л�ֹ�ʽ���м��㣺
![]() (3)
(3)
ʽ�У�KΪScherrer������DΪ������ֱ�ھ��淽���ƽ����ȣ�BΪʵ����Ʒ�������ְ�߿��ȣ���Ϊ����ǣ���ΪX���߲�����
ͨ��л�ֹ�ʽ�����130~150 ���¶���ˮ��12 h������ﯵľ����ߴ�ֱ�Ϊ2.53��2.51��2.49 nm��ǰ������ۿ���Ϊ��ʼ����ͨ���ۼ��γɵģ���ˣ�ͨ��л�ֹ�ʽ��![]() ����������ϼ���õ��ľ����ߴ練Ӧ����ʼ�����ijߴ��С[18]���Ӽ�������������ͬ�¶���ˮ��12 h����ʼ�����ߴ�������䣬����������ʼ�������κ˻��EI�;����������EG������ȣ���Ȼ�¶����ߣ�����ʼ�������κ��볤�����ʱ�ֵ���䣬����������Ϊ��ʼ�����ߴ粻��[19]��
����������ϼ���õ��ľ����ߴ練Ӧ����ʼ�����ijߴ��С[18]���Ӽ�������������ͬ�¶���ˮ��12 h����ʼ�����ߴ�������䣬����������ʼ�������κ˻��EI�;����������EG������ȣ���Ȼ�¶����ߣ�����ʼ�������κ��볤�����ʱ�ֵ���䣬����������Ϊ��ʼ�����ߴ粻��[19]��
��1 ��ͬˮ��ˮ��������Zr��Y�ij�����

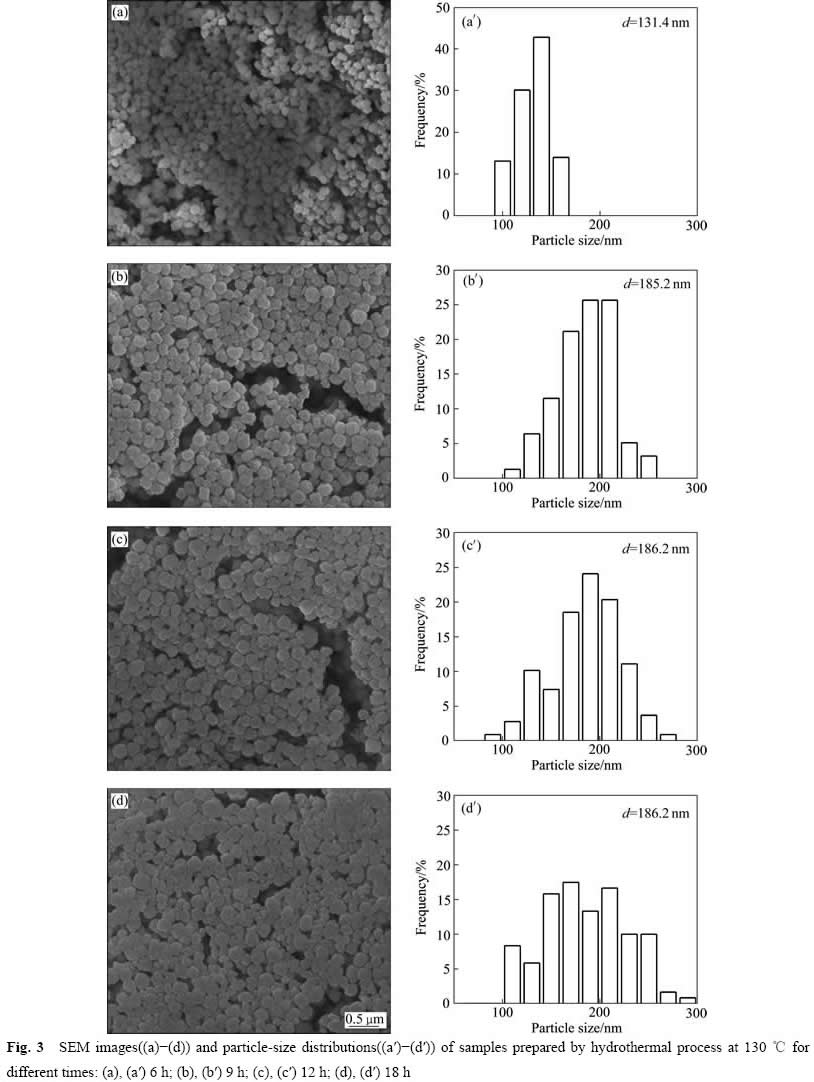
ͼ3 130 ����ˮ�Ȳ�ͬʱ�����ƷSEM�������ֲ�
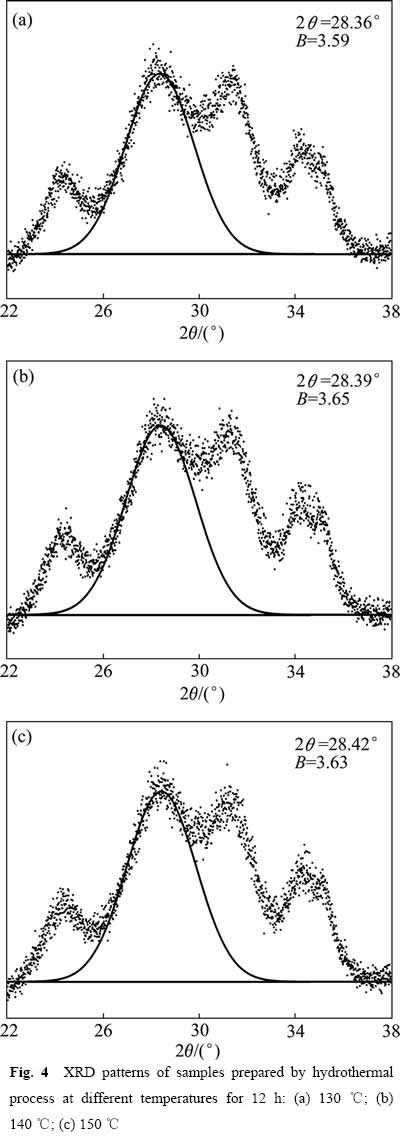
ͼ4 ��ͬ�¶�ˮ��12h����Ʒ��XRD��
ͼ5�У������¶ȵ����ߣ�Y-TZPǰ������ۿ���ƽ��������186.2 nm��СΪ94.1 nm��ͬʱ�����ֲ���խ���������������¶ȵ����ߣ�ǰ������ʼ���������˶��������ų�����֮�ı䣬ʹ�䷢���ۼ������ܱ��ݷ����仯���Ӷ�Ӱ����ۿ�������������3.4�л�����һ��������ͬʱ��ǰ�����ڵ����½ᾧ�Ƚϲ���������ܽ��ٽᾧ��Ϊ[8]�������ŷ�Ӧ�¶ȵ����ߣ������ɵ�Y-TZPǰ����ᾧ�Ƚϸߣ��������ٷ����ܽ��ٽᾧ��Ϊ����˻�Ϻõر�����������Ʊ���ĩ�ľ�һ�ԡ�ͬʱ��1��ʾ�������¶����������ˮ��ˮ�������Y�ij����ʡ�
2.4 H+Ũ�ȵ�Ӱ��
ȡ4��0.97 mol/L ZrOCl2+0.06 mol/L YCl3��Һ50 mL���ֱ����0.48 mol/L��0.24 mol/L�İ�ˮ��0.24 mol/L��0.48 mol/L��HCl��Һ��50 mL����130 ��ˮ��18 h����Ӧ��������Һ�е�H+Ũ�ȷֱ�Ϊ0.73��0.85��1.09��1.21 mol/L���Ա�����������Ͱ�ˮ����Ʒ(c(H+) =0.97 mol/L)������H+Ũ�ȶ�Y-TZPǰ������ò�������ߴ��Ӱ�졣��2����Ϊ�Ը���ƷXRD����![]() ��2.2������Ϻ�õ��ľ����ߴ磬ͼ6��ʾΪ�����SEM�������ֲ�ͼ��
��2.2������Ϻ�õ��ľ����ߴ磬ͼ6��ʾΪ�����SEM�������ֲ�ͼ��
��2 ��ͬH+Ũ�����Ʊ���ƷXRD��![]() �����Ͻ��
�����Ͻ��
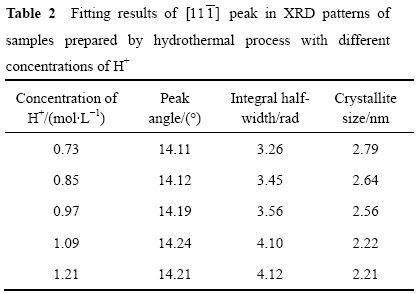
��ZrOCl2ˮ������У����������ж�Y-TZPǰ��������Ӱ�����Ҫ������H+������Cl-[13]����Һ��pHֵ������ʼ�ο��ٽ��͵����ֵ����һֱ���ֵ�ˮ�����[14]����HCl����Ũ�������ʽ(1)��ȫˮ��������ɵ�����Ũ��һ��[13]����ˣ���ˮ���κ˼����������У���Һ��H+Ũ����һ���ġ���ϱ�2��ͼ5��֪������H+Ũ�ȵ����ӣ�Y-TZPǰ�������ʼ�����ߴ���С�������ۿ����ߴ����������С�����ơ�ͬʱ�����ۿ���ƽ���ߴ�ԽС�������ֲ�Խխ����������Ũ�Ƚϸ�ʱ�������ߴ�仯����1�У���H+Ũ����0.85 mol/L����ʱ��Y�ij����ʻ��������Һ�С������Ũ�Ƚ���Ϊ0.73 mol/Lʱ�������ߵ�5%��˵��pH�ı仯��Y�ij�������һ����Ӱ�졣
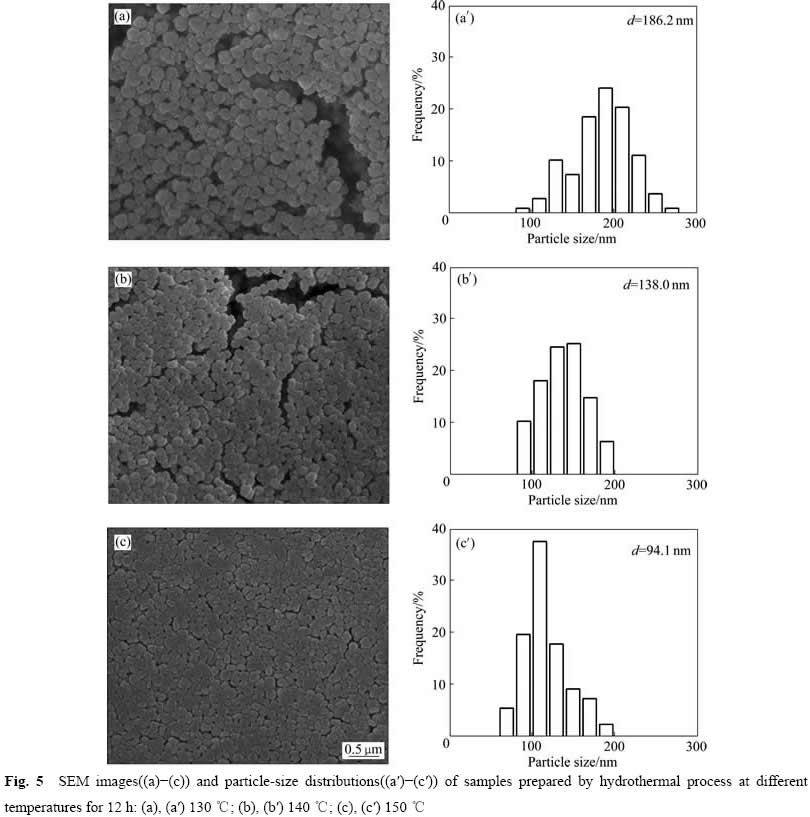
ͼ5 ��ͬ�¶���ˮ��12 h����Ʒ��SEM�������ֲ�
Ϊ�˶��Եط���H+Ũ�ȶ�Y-TZPǰ�����κ˼��������̼�Ӱ�����أ�����HOGG��[16]�Ƶ���Homocoagulation��Heterocoagulationģ�͡����ȣ��������ο�����ķ��»���Fa��˫��㾲���ų���Fr�ֱ���ʽ(4)��(5)��ʾ��
![]() (4)
(4)
ʽ�У�AΪHamaker������D1��D2Ϊ����������ֱ����H0Ϊ����������������̾��롣
![]()
![]() (5)
(5)
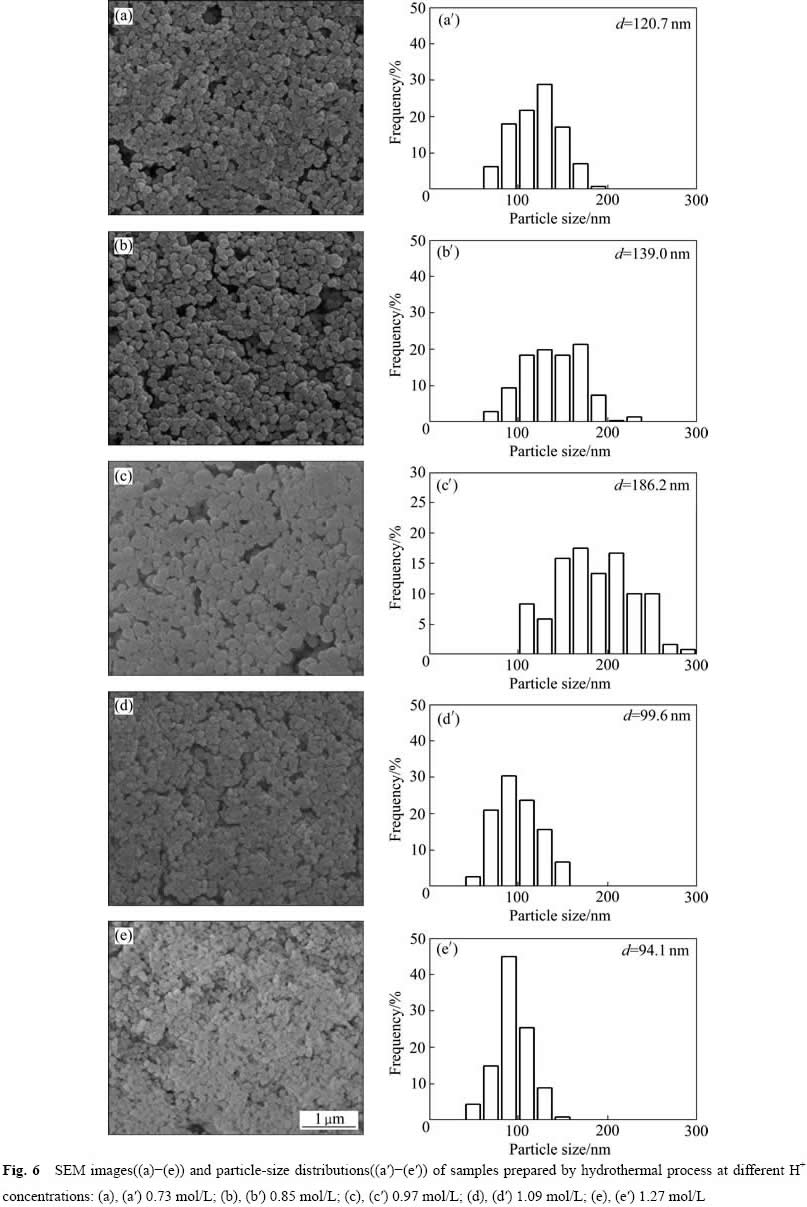
ͼ6 ��ͬH+Ũ�����Ʊ���Ʒ��SEM�������ֲ�
ʽ�У���Ϊ�������ʵĽ�糣������Ϊ�°�-�ݿ˶�����Ȳ�������1�ͦ�2�ֱ�Ϊ���������ı������(����)��
![]() (6)
(6)
ʽ�У�e��T��k�ֱ����������ɡ������¶ȺͲ�������������c��z�ֱ�Ϊ���ܶȺ͵������
ͨ������������������������������Ҫ����������ܡ������ı�����������Һ�о�����λ���ӵ�Ũ���������������������У�H+��OH-���Ǿ�����λ���ӣ��������(![]() )��������˹�ط�������ʾ��
)��������˹�ط�������ʾ��
![]() (7)
(7)
ʽ�У�pH0iΪ����i�ĵȵ��(PSC)��pHֵ���������������������(Ft)�����þ������(Fr)�ͷ��»���(Fa)�ĺ������㣬��ʽ(8)��ʾ��
![]() (8)
(8)
BLEIR��[17]�����������ǰ������ۿ������γɻ��ƣ����Ƿ��ֱ��ۿ�����Ҫ��ͨ����ʼ����������֮��ķǾ���ۼ�(Heterocoagulation)�γɵģ��ɴ��ƶ�Ӱ����ۿ����ߴ������ʼ���������ձ��ۿ���֮������ܱ��ݡ�����D1��D2�ֱ�Ϊ��ʼ�����ͱ��ۿ����ߴ磬��ʵ������֪D2>>D1����D1+D2��D2������ʽ(8)��֪�����ı������������ߴ��أ�����1=��2����ˣ���ʽ(4)��(5)��(8)���Ƴ�ʽ(9)��
![]() (9)
(9)
��ʽ(9)��֪���ڷǾ���ۼ�ģ���У���������������һ�µ�����£���ʼ�����ߴ�ԽС�����������������FtԽС��Խ����ͨ���ۼ��γɽϴ���������ߴ�ЧӦ(Factor of size effects)��ͬʱ����ʽ(7)��֪������������Ʀ�������pH�Ľ��Ͷ�������ˣ��������������������£�Ft������H+Ũ�ȵ����߶����ͣ����������ЧӦ(Factor of electrical repulsion force)[13]����ͼ7��ʾ�����ŷ�Ӧ��H+Ũ�ȵ���ߣ���ʼ�����ߴ���С����ǿ�˿����ľۼ����ƣ�ͬʱ��H+Ũ�ȵ����������ǿǰ���������ĵ���������Ft�����Ʊ��ۿ����ij�����ˣ����������Ӱ�죬��ͬһ�¶������£����ۿ����ߴ�����H+Ũ�ȵ����߳���������С�����ơ�
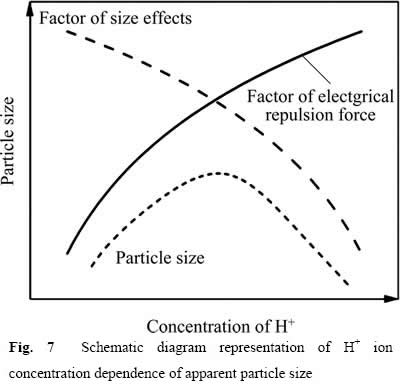
ͼ7 H+Ũ�ȶԱ��ۿ����ߴ�Ӱ��ʾ��ͼ
2.5 ���յ�Ӱ��
ȡ130 ��ˮ��12 h�Ʊ�����Ʒ���ζ���Y����1000 ��������1h��ͨ��XRD�����ǡ�������ɨ��羵��BET�����Ƕ�����ǰ����Ʒ��ò�����ࡢ�ȱ���Ϳ�϶���з������������Ȼ����������Ʊ���Ʒ���պ��XRD���жԱȡ�ͼ8��9��10��ʾ�ֱ�Ϊ��Ʒ��XRD�ס�SEM���N2�������Ѹ��������ֲ�ͼ��
��ͼ8��֪������ǰ��Y-TZPǰ����ʵ�б�࣬ͨ����ˮ�ζ�����Y����1000 ������1 h����Ʒ���ķ��࣬��û��Y���ӵ���Ʒ�����պ���Ϊ��б�࣬˵��ͨ����ˮ�ζ�ʹY(OH)3�����ڱ��ۿ������棬��ͨ�����տ��Եõ�Y-TZP��ĩ��

ͼ8 ����ǰ����Ʒ��XRD��

ͼ9 ����ǰ������ƷSEM��
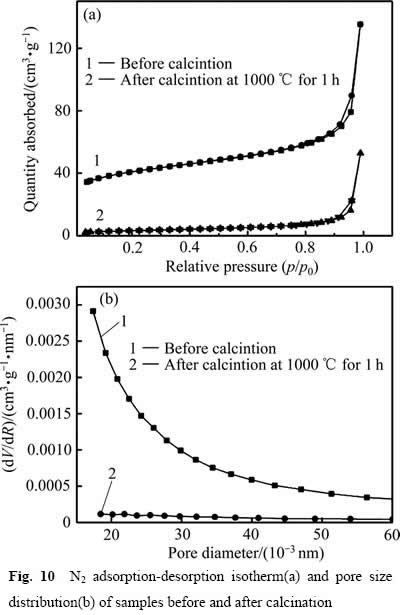
ͼ10 ����ǰ������Ʒ��N2�������Ѹ����ߺͿ��ֲ�
��ͼ9��֪��1000 �����պ�ĩ�Ա��ֽϺõķ�ɢ״̬��ͬʱ��ĩ����������С����120 nm���ҷֲ�����ͼ10�ɿ�����BETģ�ʹ�������ǰ�����Ʒ���õ��ıȱ�����ֱ�Ϊ145 m2/g��11 m2/g������ǰ����Ʒ��N2�������Ѹ����߾�����IV�����ߣ��Ҵ���H3�ͺ�[20]��������Ʒ����һЩ�ѻ������Ľ�ʹ�ף�����Ʒ�ڸ�������յĹ����в�����һ�����žۡ�ͬʱ������ǰ��Ʒ�ڵ�ѹ�����нϸߵĵ�����������������ֲ������п�ԽС��������ʿ����������ƣ�˵������ǰ��Y-TZPǰ���������ž�������ʽ����˽϶�Ľ���ף���1000 ������1 h�������û�н���״��ڣ����¶����ߺ�ԭ����ɢ�Ӿ磬����֮��Ϊ�˽��������ܶ������γ����ܵĿ���������ͽ����ʧ��ͬʱ��������С��
3 ����
1) 130 ��ˮ��ʱ��ˮ�����ǰ������ˮ��ʱ����ӳ���Y-TZPǰ�������������ˮ������»���ᵼ�·�ĩ�����ֲ��������ƽ�������仯����
2) ��ʵ�����������ҺŨ�Ⱥ�ˮ���¶ȷ�Χ��(130~150 ��)�������¶ȵ����ߣ�Y-TZPǰ�����ĩƽ�������ߴ���С����һ������ߡ�
3) ������Һ��H+Ũ�ȵ���ߣ�Y-TZPǰ����ƽ�������ߴ���������С���ҳߴ�ԽС����ĩ�����ֲ�Խխ��
4) �ζ���Y��1000 �����յõ�Y-TZP��ĩ��ɢ�Ժá��ס��ȱ����С��
REFERENCES
[1] �ܱ���, ����, ������, ������, ����, ������. ��������Ʊ�������Ӧ��[M]. ����: ұ��ҵ������, 2008: 3-7.
XIONG Bing-kun, LIN Zhen-han, YANG Xin-min, JIANG Dong-min, LUO Fang-cheng, ZHANG Ling-xiu. Preparation technology and application of zirconium oxide[M]. Beijing: MetallurgicalIndustryPress, 2008: 3-7.
[2] ��ΰУ, ������, �� ��, ������, �����, �� ��. ��/������������ﯷ���ˮ�ȷ��Ʊ��о���չ[J]. ���ϵ���, 2013, 27(19): 146-149.
PENG Wei-xiao, WANG Kai-jun, HU Jin, WANG Yu-tian, SUN Hong-peng, YI Feng. Research progress on preparation of pure/doped nano-zirconia powders by hydrothermal[J]. Materials Review, 2013, 27(19): 146-149.
[3] ������, ����ƽ, ����ϲ, ������,������,������.��ѧ���������Ʊ�Sc2O3-Y2O3-ZrO2�����մɷ�ĩ����������ȶ���[J]. ��ĩұ����Ͽ�ѧ�빤��, 2014, 19(1): 154-158.
HE Tie-lun, LONG An-ping, ZHOU Wu-xi, LIU Huai-fei, LI Yu-xi, LI Song-lin. Sc2O3-Y2O3-ZrO2 ceramic nanopowder fabricated by chemical co-precipitation and its high temperature phase stability[J]. Materials Science and Engineering of Powder Metallurgy, 2014, 19(1): 154-158.
[4] ������, ������, ������. ����ZrO2-8%Y2O3��ĩ����ת�估������������ѧ[J]. �й���ɫ����ѧ��, 2011, 21(12): 3120-3128.
LIU Chun-bo, YU Lian-sheng, JIANG Xian-liang. Phase transition and grain growth kinetics of nanocrystalline 8% yttria stabilized zirconia powder[J]. The Chinese Journal Nonferrous Metals, 2011, 21(12): 3120-3128.
[5] HSU Y W, YANG K H, CHANG K M, YEH S W, WANG M C. Synthesis and crystallization behavior of 3mol% yttria stabilized tetragonal zirconia polycrystals (3Y-TZP) nanosized powders prepared using a simple co-precipitation process[J]. Journal of Alloys and Compounds, 2011, 509(24): 6864-6870.
[6] DAVAR F, HASSANKHANI A, LOGHMAN-ESTARKI M R. Controllable synthesis of metastable tetragonal zirconia nanocrystals using citric acid assisted sol-gel method[J]. Ceramics International, 2013, 39(3): 2933-2941.
[7] �� ӥ, ��Ϫ��, ����ǿ, �Ը���. ����Һ�;��ȳ�����Ϸ��Ʊ���������ZrO2(Y2O3)��ĩ[J]. �й���ɫ����ѧ��, 2006, 16(1): 73-78.
CHANG Ying, LI Xi-bin, MENG Zhen-qiang, ZHAO Fu-an. Preparation of ZrO2(Y2O3)spherical nanometer powders via coupling route of water-oil emulsion with homogenous precipitation[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(1): 73-78.
[8] ����, ������, �º���, �� ��, Ф����. ����ˮ�ȷ��Ʊ���ϸ���������ȶ������[J]. ��ĩұ����Ͽ�ѧ�빤��, 2012, 17(3): 395-400.
SU Yu-chang, LIU Sai-nan, CHEN Hong-yan, JIANG Min, XIAO Li-hua. Preparation of ultra-fine yttria-stabilized zirconia nanoparticles by two-step hydrothermal process[J]. Materials Science and Engineering of Powder Metallurgy, 2012, 17(3): 395-400.
[9] ESMAEILIFAR A, ROWSHANZAMIR S, BEHBAHANI A. Hydrothermal synthesis of nano-size zirconia using commercial zirconia powder: Process optimization through response surface methodology[J]. Iranian Journal of Hydrogen & Fuel Cell, 2014, 1(3): 163-173.
[10] ���, ����ƽ, ������, ������, Ҧ ��, ����Ȼ, ֣ ��. ���ȶ��ֲ�������ﯵ�ˮ�Ⱥϳ���ṹ����[J]. ��ĩұ����Ͽ�ѧ�빤��, 2014, 19(5): 715-720.
LIU Yu-chen, CHEN Wei-ping, NIE Dong-hong, CHEN Xiao-yu, YAO Rui, JIANG Zi-ran, ZHENG Feng. Hydrothermal synthesis and characterization of cerium-stabilized scandium-doped zirconia[J]. Materials Science and Engineering of Powder Metallurgy, 2014, 19(5): 715-720.
[11] MACHMUDAH S, WIDIYASTUTI W, PRASTUTI O P, NURTONO T, WINARDI S, WAHYUDIONO, KANDA H, GOTO M. Synthesis of ZrO2 nanoparticles by hydrothermal treatment[J]. AIP Conference Proceedings, 2014, 1586(2): 166-172.
[12] ���½�, ��Խ��, ������, �Ӣ, �¶���, �ǿ, л����. ˮ��-ˮ��������Ʊ�����ﯷ�ĩ�������[J]. ���ϵ���, 2015, 29(1): 43-46.
LIANG Xin-jie, QIU Yue-xiu, WANG Hong-you, YANG Jun-ying, CHEN Dong-dong, LI Qiang, XIE Yan-jun. Preparation of zirconia powder through hydrothermal-hydrolysis and its characterization[J]. Materials Review, 2015, 29(1): 43-46.
[13] MATSUI K, OHGAI M. Formation mechanism of hydrous-zirconia particles produced by hydrolysis of ZrOCl2 solutions[J]. Journal of the American Ceramic Society, 1997, 80(8): 1949-1956.
[14] ������, �����, л�ݷ�. �ྦྷ��б����ﯿ�����ˮ��������ϳ�[J]. ������ѧ��, 1993, 21(5): 461-465.
HUANG Yue-xiang, GUO Cun-ji, XIE Yi-fen. Synthesis of polycrystalline monoclinic zirconia particles by hydrolysis precipitation[J]. Journal of the Chinese Ceramic Society, 1993, 21(5): 461-465.
[15] MATSUI K, OHGAI M. Formation mechanism of hydrous-zirconia particles produced by hydrolysis of ZrOCl2 solutions: ��[J]. Journal of the American Ceramic Society, 2001, 84(10): 2303-2312.
[16] HOGG R, HEALY T W, FUERSTENAU D W. Mutual coagulation of colloidal dispersions[J]. Trans Faraday Society, 1966, 62: 1638-1651.
[17] BLEIER A,CANNON R M. Nucleation and growth of uniform m-ZrO2[J]. MRS proceedings, 1986, 73: 71-78.
[18] MATSUI K, SUZUKI H, OHGAI M. Raman spectroscopic studies on the formation mechanism of hydrous-zirconia fine particles[J]. Journal of the American Ceramic Society, 1995, 78(1): 146-152.
[19] MATSUI K, OHGAI M. Formation mechanism of hydrous-zirconia particles produced by hydrolysis of ZrOCl2 solutions: ��[J]. Journal of the American Ceramic Society, 2002, 85(3): 545-553.
[20] SEIICHI K, TATSUO I, IKUO A. ������ѧ[M]. ����: ��ѧ��ҵ������, 2006: 31-103.
SEIICHI K, TATSUO I, IKUO A. Adsorption science[M]. Beijing: ChemicalIndustryPress, 2006: 31-103.
Preparation of yttria-stabilized tetragonal zirconia powders by hydrothermal hydrolysis
LIU Zhi-hong, ZHAO Li-xing, LIU Zhi-yong, LI Yu-hu, LI Qi-hou
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Yttria-stabilized tetragonal zirconia polycrystal(Y-TZP) powders of controllable sizes were prepared by hydrothermal hydrolysis process. The effects of hydrothermal time, temperature and H+ions concentration on the particle sizes and their distributions of the Y-TZP precursor powders were investigated experimentally. The results show that the Y-TZP precursor powders prepared by hydrothermal hydrolysis are monoclinic with good dispersion, and the particle sizes are 50-300 nm. The average particle size of the Y-TZP precursor increases as the reaction progresses more fully, while aging will broaden the particle-size distribution of the Y-TZP precursor. At the range of experimental concentrate (0.485 mol/L ZrOCl2, 0.03 mol/L YCl3) and temperature (130-150 ��), when the temperature increases from 130�� to 150 ��, the average particle sizes of the Y-TZP precursor decrease from 186.2 nm to 94.1 nm, and the particle-size distributions become narrow. The concentrations of H+ ions affect the average particle sizes of the Y-TZP precursor significantly, and the average particle sizes of the Y-TZP precursor increase at first, and then decrease with the increase of H+ ions concentration. Yttria-stabilized tetragonal zirconia powders (Y-TZP) are obtained by doping the precursor powders with yttria through ammonia titration and then calcining them at 1000 �� for 1 h. The average particle size is 120 nm, and the size distributions become narrow.
Key word: zirconia; Y-TZP precursor; hydrothermal hydrolysis; particle size; distribution
Received date: 2015-08-11; Accepted date: 2015-12-30
Corresponding author: LIU Zhi-hong; Tel: +86-731-88830478; E-mail: zhliu@mail.csu.edu.cn
(�༭ ����)
�ո����ڣ�2015-08-11�������ڣ�2015-12-30
ͨ�����ߣ���־�꣬���ڣ���ʿ���绰��0731-88830478��E-mail: zhliu@mail.csu.edu.cn
ժ Ҫ������ˮ��ˮ�ⷨ�Ʊ������ɿص����ȶ��ķ��������(Y-TZP)��ĩ������ˮ��ʱ�䡢�¶Ⱥ�H+Ũ�ȶ�Y-TZPǰ�����ĩ������������ֲ���Ӱ�졣���������ˮ��ˮ�ⷨ�Ʊ���Y-TZPǰ�����ĩΪ��б�࣬��ɢ�Ժã���������Ϊ50~300 nm��ˮ��ˮ�ȷ�Ӧ����Խ��֣�ǰ�������ƽ������Խ�»������������ֲ��������ʵ���Ũ��(0.485 mol/L ZrOCl2��0.03 mol/L YCl3)���¶�(130~150 ��)��Χ�ڣ������¶ȣ�ǰ�������ƽ��������186.2 nm����Ϊ94.1 nm������ֲ���խ��H+Ũ�ȶ�ǰ�������ƽ������Ӱ�����ԣ����H+Ũ�ȣ�ǰ���������ƽ��������������С��ˮ��ˮ�ⷨ�Ʊ���Y-TZPǰ����ΰ����ƺ���1000 ������1 h�õ����ȶ��ķ��������(Y-TZP)��ĩ������ԼΪ120 nm������ֲ���խ��
[1] �ܱ���, ����, ������, ������, ����, ������. ��������Ʊ�������Ӧ��[M]. ����: ұ��ҵ������, 2008: 3-7.
[14] ������, �����, л�ݷ�. �ྦྷ��б����ﯿ�����ˮ��������ϳ�[J]. ������ѧ��, 1993, 21(5): 461-465.
[20] SEIICHI K, TATSUO I, IKUO A. ������ѧ[M]. ����: ��ѧ��ҵ������, 2006: 31-103.
SEIICHI K, TATSUO I, IKUO A. Adsorption science[M]. Beijing: ChemicalIndustryPress, 2006: 31-103.


