���±�ţ�1004-0609(2015)-07-1987-06
����ͬʱƽ��ԭ����Au-I--H2Oϵ����ѧ����
����Ӣ1, 2, 3��������3���ﴺ��3��Ԭϲ��3��������3��������3���� ��4
(1. ����������ѧ ��ҵ����ѧԺ����ɽ 063009��
2. �ӱ�ʡ��ҵ�����밲ȫ�����ص�ʵ���ң���ɽ 063009��
3. �����Ƽ���ѧ ������ɽ��Ч�����밲ȫ�������ص�ʵ���ң����� 100083��
4. ��ұ��ұ(����) ����ó������˾������ 100029)
ժ Ҫ��
����ͬʱƽ��ԭ����Au-I--H2Oϵ�Ľ�������ѧ���з������ֱ��о���Һ�����Au�Լ�AuI���������Auƽ��ʱ�Ħ�-pH��ϵ��AuI������������Һ�к�����ֵı仯���ɡ����������������Һ�к�����ֵ���Ũ��cT(Au)�Ľ��ͻ���ֵ���Ũ��cT(I-)�����ӣ���ԭ��λ��sol/AuѸ�ٽ��ͣ�Au3+/Au2O3��ƽ��pHֵ���dz������ڽ�ĵ⻯������������Һ��cT(I-)�����ӣ�����AuI�����������������������С�����ƣ���cT(Au)Ϊ1��10-4 mol/L�������£�����Һ��cT(I-)Ũ�ȴ���0.0021 mol/Lʱ���ɱ���AuI���������ɣ�����Ҫ��AuI2-���������ʽ���ڡ�Au-I--H2Oϵ�Ľ�������ѧ����Ϊ��ĸ�Ч�⻯�����ṩ���������ݡ�
�ؼ��ʣ�
Au-I--H2Oϵ��ͬʱƽ��ԭ������-pHͼ��AuI����������ѧ������
��ͼ����ţ�TF111���� ���ױ�־�룺A
Thermodynamic analysis for Au-I--H2O system based on principle of simultaneous equilibrium
LI Shao-ying1, 2, 3, ZHAO Liu-cheng3, SUN Chun-bao3, YUAN Xi-zhen3,
WANG Pei-long3, DENG Xiang-yi3, LIU Ke4
(1. College of Mining Engineering, North China University of Science and Technology, Tangshan 063009, China;
2. Hebei Province Mining Industry Develops with Safe Technology Priority Laboratory, Tangshan 063009, China;
3. Key Laboratory of the Ministry of Education of China for High-Efficient Mining and Safety of Metal Mines,
University of Science and Technology Beijing, Beijing 100083, China;
4. MCC Huaye (Beijing) International Trade Co., Ltd., Beijing 100029, China)
Abstract: Thermodynamic analysis of Au-I--H2O system was carried out based on the principle of simultaneous equilibrium. The ��-pH programs of balance with solution and Au, solid AuI and Au were investigated. Also, the existence condition of AuI precipitation and change-rule of gold-bearing components were studied. The results show that with decreasing cT(Au) or increasing cT(I-) in the solution, ��sol/Au reduces rapidly compared to the standard potential of Au, and the balance pH value of Au3+/Au2O3 increases. This is beneficial to gold leaching with iodine-iodide. As the cT(I-) increases gradually in the solution, AuI precipitation appears and the trend of AuI precipitation amount increases firstly and then reduces. When the cT(Au) is 1��10-4 mol/L, if the cT(I-) is more than 0.0021 mol/L, AuI precipitation will not occur, meanwhile, the main complex ion is AuI2-. The thermodynamic analysis of Au-I--H2O system provides theoretical basis for the efficient gold leaching with iodine-iodide.
Key words: Au-I--H2O system; simultaneous equilibrium principle; ��-pH diagram; AuI precipitation; thermodynamic analysis
Ŀǰ����������Ҫ��������軯�����軯���ռ�������ʸߣ��������������ƣ��Կ�ʯ������ǿ[1]��������Ҳ������һЩ���ݺ��ӵ�ȱ�㣺�軯���о綾��������Ⱦ�����ٶ�������ϸ�������𡢸��顢�����л�̼���Ѵ������ʯ����Ч���������������ͭ������Ǧ��п��������ʵ�Ӱ���[2-3]����ˣ�������Աһֱ�����ڷ�����������о������������еķ��������Ҫ�����巨����������η���ʯ��ϼ�����±����������淨(�л��淨)�����軯����������[4-7]��
�⻯����һ�ַ������������20����90���������һЩ�о���Ա�Ϳ�ʼ�Ե⻯��������о�����ȡ����һ���ijɹ���QI��[8-9]�о��˽��ڵ�-�⻯����Һ�еĶ���ѧ���绯ѧ��Ϊ�������������ܽ���ѭһ����Ӧ����ѧ��һ����Ӧ������Բ����ת�ٶȵĶ��η������ȣ����ڵ⻯����Һ����Ҫ��AuI2-��AuI4-����ʽ���ڡ�ANGELIDIS��[10]������תԲ�̼����Խ��ڵ�-�⻯����ϵ�е��ܽ�������о��������ʵ�������Һ�е�͵⻯���Ũ�ȣ�����ܽ⼴���Է����У��ҽ���ܽ�����Զ���軯�������Ŀ졣����˹Ī˹�ƹ����������̽�о�Ժ�о�֤������-���������ȶ��Խ����ڽ�-�������ģ�������������������ȶ���[11]����Ժ�̼��ʯ(�л�̼����Ϊ1.6%)��������ʯ[12]���������̼ԭ����[13]����ѡ��[14]����ͭ�Ѵ������[15]�Ƚ��еĵ⻯�����������������⻯���������õĽ���Ч���������������ڿ�����[16]ͨ���⻯��Խ����Ч����Ӱ���о����֣��⻯�صĽ���Ч�����������͵⻯泥�����Ը�ѡ������˶���ѧ�о������ֽ�����Ӧ������Ҫ�ܽ��滯ѧ��Ӧ����[17]��
MARUN��[18]�����[19]����Pourbaix���ֱ���Ƴ��˵⻯������ϵ�Ħ�-pHͼ��Pourbaix���Ǹ�������������ɷ�Ӧ��ƽ�⣬ȷ������������������Ӹ��Ե�����ѧ�ȶ��������ж����������ڵĸ��ӽ�����ϵ�У��ȴ��ڼ������ִ���������ӣ����Ҽ��������������֮���ת�������ڶ�̬ƽ�⡣����Pourbaix�������ж����������ڵĸ��ӽ�����ϵ�Dz�����ʵ������ġ�Ϊ�˸�Ϊȷ�ػ��Ƶ⻯������ϵ�Ħ�-pHͼ�ͷ����⻯��������ѧ�仯���ɣ��������߸����о���Ա[20-22]�����ͬʱƽ��ԭ������Au-I--H2Oϵ�Ľ�������ѧ�����˷�������Ҫ�о�����Һ�����Au��AuI���������Auƽ��ʱ�Ħ�-pH��ϵ��AuI������������Һ�к�����ֵı仯���ɡ�Ϊ��ĸ�Ч�⻯�����ṩ���������ݡ�
1 Au-I--H2Oϵ�ĵ绯ѧƽ��
1.1 ��Һ�����Au��ƽ��
Au-I--H2Oϵ��һ���Ⱥ��м�����Au+��Au3+���ֺ����������AuI2-��AuI4-�ĸ�����ϵ������Au+��Au3+��AuI2-��AuI4-�����Au�ĵ绯ѧ��Ӧ���ֱ���ʽ(1)~(4)��ʾ��
1) Au+�����Au��ƽ��
 ��
�� (1)
(1)
2) Au3+�����Au��ƽ��
 ��
��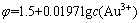 (2)
(2)
3) AuI2-�����Au��ƽ��
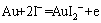 ��
�� (3)
(3)
4) AuI4-�����Au��ƽ��
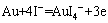 ��
�� (4)
(4)
��ˣ�����ͬʱƽ��ԭ������Au-I--H2Oϵ�Ħ�sol/Au������ͬʱ������Һ����4�������������ƽ�⡣
Au-I--H2Oϵ���������������������γ�ƽ�⣬�仹ԭ��λ������ȵģ���Au-I--H2Oϵ�л�ԭ��λֻ��1����ʽ(1)~(4)�еĦ���ȡ���cT(Au)Ϊ��Һ�к�����ֵ���Ũ�ȣ�cT(I-)Ϊ��Һ�к�����ֵ���Ũ�ȣ�������Һƽ�ⷽ����ʽ(5)��(6)��ʾ��
 (5)
(5)
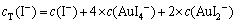 (6)
(6)
��ʽ(1)~(4)�ֱ����ʽ(5)��(6)�У��ɵã�

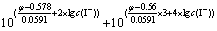 (7)
(7)
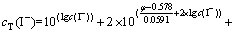
 (8)
(8)
ʽ�У���Ϊ��ԭ��λ��V��c(I-)Ϊ��Һ�������I-����Ũ�ȣ�mol/L��
����ʽ(7)��(8)��֪�����¶Ⱥ㶨������£�Ӱ����Һ�����Auƽ��ı�����4������cT(Au)��cT(I-)���պ�c(I-)������4������֮����ʽ(7)��(8)�������̣����̶�cT(Au)��cT(I-)ʱ�����������ͱ����2������ˣ�ͨ���̶�cT(Au)���ı�cT(I-)������������cT(I-)���Ӧ�Ħպ�c(I-)�����ݲ�ͬ���������������ƽ�⣬������ȷ��Au+��Au3+��AuI2-��AuI4-��ƽ��Ũ�ȡ�
1.2 AuI���������Au��ƽ��
��һ��������Au-I--H2Oϵ�л������AuI����������������Һ�����Au��ƽ���⣬����AuI���������Au��ƽ����ʽ(9)��ʾ��
 ��
�� (9)
(9)
Ϊ��ȷ����Һ��AuI�������ڵ�����������Ҫ�����AuI/Au������ͬʱƽ��ԭ������ʽ(1)~(4)��(9)�ֱ����ʽ(5)��ʽ(6)���ɵã�

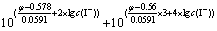 (10)
(10)

 (11)
(11)
����ʽ(10)��(11)��֪�����¶Ⱥ㶨������£�Ӱ�����AuI������Au-I--H2Oϵƽ��ı���Ҳ��4������cT(Au)��cT(I-)���պ�c(I-)������4������֮����ʽ(10)��(11)�������̣����̶�cT(Au)��cT(I-)ʱ�����������ͱ����2������ˣ�ͨ���̶�cT(Au)���ı�cT(I-)����������cT(I-)���Ӧ�Ħպ�c(I-)��ͬ�����ݲ�ͬ���������������ƽ�⣬ȷ����Ӧ�������ӵ�ƽ��Ũ�ȡ�
2 Au-I--H2Oϵ����ѧ����
һ����Au-H2Oϵ�У����˽��������Ӧ�������ڵĻ�ѧ��Ӧ��ʽ(12)��ʾ��
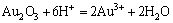
 (12)
(12)
�ڸ�pHֵ������Au������OH-��Ӧ���ɲ�ͬ�ĺ��������ӣ���H2AuO3-��HAuO32-��AuO33-�����ڵ⻯�����������Һ��pHֵһ���������������[23]��Ϊ�˸��Ӽ�����˵��ڦ�-pHͼ��ͻ��I-����Ũ�ȶԦպ�pHֵ��Ӱ�죬ʵ���к���H2AuO3-��HAuO32-��AuO33-���������ڦ�-pHͼ�еĴ�������
2.1 Au-I--H2Oϵ��-pHͼ
������Һ�����Au��ͬʱƽ�ⷽ�̺���AuI�����Au��ͬʱƽ�ⷽ�̼�ʽ(12)�����ƵIJ�ͬ��ҺcT(Au)��cT(I-)��Au-I--H2Oϵ��-pHͼ��ͼ1��2��ʾ��
ͼ1��ʾΪ25 ������Һ��cT(I-)Ϊ10 mol/L��cT(Au)�ֱ�Ϊ1��1��10-4 mol/Lʱ�Ħ�-pHͼ����ͼ1���Կ�����Au-I--H2Oϵ��Һ��cT(Au)Ϊ1 mol/L��cT(I-)Ϊ10 mol/Lʱ����sol/Au�ɽ�ı���ԭ��λ1.5 V���͵�0.47 V����AuI/AuΪ0.449 V����sol/Au���ڦ�AuI/Au����ʱ��Һ�л����AuI����������Һ�е�cT(Au)���͵�10-4 mol/Lʱ����sol/Au��һ������0.223 V�����ڦ�AuI/Au��0.443 V������Һ���ȶ������ڲ������AuI���������ᷢ��AuI������һ���ܽ�ķ�Ӧ��ʽ(13)��ʾ��
 (13)
(13)

ͼ1 Au-I--H2Oϵ��-pHͼ
Fig. 1 ��-pH diagrams for Au-I--H2O system (cT(I-)=10 mol/L, cT(Au)=1 mol/L, 10-4 mol/L)
��ˣ���Au-I--H2Oϵ�н�����Һ��cT(Au)�ɽ��ͦ�sol/Au�ͱ���AuI���������ɣ������ڴٽ���ĵ⻯������
ͼ2��ʾΪ25 ������Һ��cT(Au)=10-4 mol/L��cT(I-)�ֱ�Ϊ1��10-4��1��10 mol/Lʱ�Ħ�-pHͼ����ͼ2���Կ�����Au-I--H2Oϵ��Һ��cT(Au)Ϊ1��10-4 mol/Lʱ������cT(I-)�����ӣ���sol/Au���AuI/Au�����ͣ�Au3+/Au2O3��ƽ��pHֵ������Һ��cT(I-)Ϊ1��10-4 mol/Lʱ����sol/Au���ڦ�AuI/Au�������������Һ�л����AuI����������Һ�е�cT(I-)���ӵ�1 mol/Lʱ�� ��sol/AuΪ0.342 V�����ڦ�AuI/Au��0.502 V����Һ���ȶ������ڲ������AuI��������ʱAu3+/Au2O3��ƽ��pHֵ����19.8������������Һ�е�cT(I-)��10 mol/Lʱ����sol/AuΪ0.223 V��Զ���ڦ�AuI/Au��0.443 V����Һͬ��������AuI������Au3+/Au2O3��ƽ��pHֵ����21.8����ˣ���Au-I--H2Oϵ��������Һ��cT(I-)Ũ�ȿɽ��ͦ�sol/Au�ͱ�����Һ�г���AuI�������Խ�ĵ⻯�����dz�������
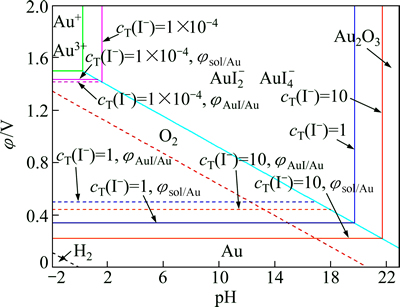
ͼ2 Au-I--H2Oϵ��-pHͼ
Fig. 2 ��-pH diagram for Au-I--H2O system (cT(Au)=1��10-4 mol/L, cT(I-)=1��10-4, 1, 10 mol/L)
2.2 Au-I--H2Oϵ��-lgcT(I-)ͼ
����ҺcT(Au)Ϊ1��10-4 mol/L��Au-I--H2Oϵ�У�Ϊ�˷���AuI�������ֵ�������������ͬʱƽ��ԭ�����Լ������ͬcT(I-)ʱ��Һ�Ļ�ԭ��λ�գ���ԭ��λ����lgcT(I-)�Ĺ�ϵ��ͼ3��ʾ��
��ͼ3���Կ�����������Һ��cT(I-)�����ӣ���λ���͡���cT(I-)���ӵ�0.0021 mol/Lʱ����λ���͵�0.663 V����������cT(I-)��0.1 mol/Lʱ����λ���͵�0.46 V��ͼ3�������߰�Χ�IJ���ΪAuI���ֵ���������cT(I-)�����ӣ����������ߵĵ�λ����������С��˵����Һ��AuI�������������Ӻ��С�����ơ���cT(I-)���ӵ�0.0021 mol/Lʱ��AuI�������ܽ⡢��ʧ�������߽���һ�㣬�õ�ΪAuI������������ת�۵㡣��������cT(I-)��AuI����������ʧ����ˣ��⻯��������м���������I-���ӿ��Դٽ���Ľ�����������AuI�����ij��֡�

ͼ3 Au-I--H2Oϵ��-lgcT(I-)ͼ
Fig. 3 ��-lgcT(I-) diagram for Au-I--H2O system (cT(Au)=10-4 mol/L)
2.3 Au-I--H2Oϵ������ֲַ�ͼ
����֪��ҺcT(Au)��Au-I--H2Oϵ�У�����ͬʱƽ��ԭ�����Լ������ͬ��ҺcT(I-)ʱ���ֺ�����ֵ�Ũ�Ⱥͷֲ��ʡ�ͼ4��ʾΪ��Һ��cT(Au)Ϊ1��10-4 mol/LʱAu-I--H2Oϵ�к�����ֲַ����ɡ�
��ͼ4��֪����Һ��cT(I-)��Au-I--H2Oϵ�ĺ�����ֲַ�Ӱ��ܴ���Һ��cT(I-)С��10-6 mol/Lʱ������Ҫ��Au+��Au3+����ʽ���ڣ�����cT(I-)̫С�����Խ�Au-I--H2Oϵ���ƿ���Au-H2Oϵ��������Һ��cT(I-)�����ӣ�����AuI��������������������Ӻ��С�����ƣ���Һ��c(Au+)��c(Au3+)��c(AuI2-)���٣�c(AuI4-)���ӣ���cT(I-)���ӵ�0.0021 mol/Lʱ��AuI�������ܽ⡢��ʧ(��ʽ(13))������������Һ��cT(I-)��c(AuI4-)Ũ�ȼ��ٲ�����0��c(AuI2-)Ũ�����ӣ���Ϊ��Һ�н����Ҫ������ʽ��

ͼ4 cT(I-)��Au-I--H2Oϵ�к�����ֲַ��ʵ�Ӱ��
Fig. 4 Effect of cT(I-) concentration in Au-I--H2O system on distribution rate of gold-bearing components (cT(Au)=1��10-4 mol/L)
3 �⻯����ʵ���о�
���������⻯��������ѧ�����������ij��ѡ���ij��ͭ�Ѵ����������Ϊ�о�����ֱ���е⻯����ʵ�顣���¶�Ϊ25 �桢Һ�̱�Ϊ4:1��pHֵΪ7.5�������ٶ�Ϊ400 r/min�����ʼŨ��Ϊ8 g/L�������4 h����ͭ����������2 h�������£��ֱ���е���I-����������Ϊ1:2��1:3��1:4��1:5��1:6��1:8�Ľ������飬ʵ������ͼ5��ʾ����ͼ5��֪���ڳ�ʼ��Ũ��һ���������£�����I-����Ũ�ȵ����ӣ���Ľ����������ߣ�������I-����������Ϊ1:6ʱ��������ʴﵽ88%���ҡ�������������������ѧ����������I-����Ũ�ȶԴٽ���Ľ��������һ�¡�
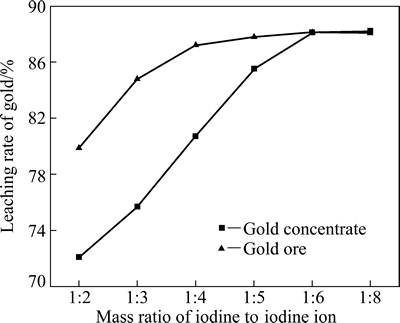
ͼ5 ����I-���������ȶԽ�����ʵ�Ӱ��
Fig. 5 Effect of mass ratio of iodine and iodine ion on leaching rate of gold
4 ����
1) ����ͬʱƽ��ԭ��������Au-I--H2Oϵ�Ľ�������ѧ���о�����Һ�����Au����AuI�����Auƽ��ʱ�Ħ�-pH��ϵ��������Һ��cT(Au)�Ľ��ͻ�cT(I-)�����ӣ���sol/AuѸ�ٽ��ͣ�Au3+/Au2O3��ƽ��pHֵ���dz������ڽ�ĵ⻯������
2) ����ҺcT(Au)Ϊ1��10-4 mol/L��Au-I--H2Oϵ�У�������Һ��cT(I-)�������ӣ�����AuI��������������������Ӻ��С�����ơ���cT(I-)���ӵ�0.0021 mol/Lʱ��AuI�������ܽ⡢��ʧ��
3) ����ҺcT(Au)Ϊ1��10-4 mol/L��Au-I--H2Oϵ�У�������Һ��cT(I-)�������ӣ�c(Au+)��c(Au3+)��С��c(AuI4-)�����Ӻ��С��c(AuI2-)�����ӡ���cT(I-)����0.0021 mol/Lʱ����Һ�еĽ���Ҫ��AuI2-���������ʽ���ڡ�
4) �⻯����ʵ�������������õ⻯��������ѡ��ͺ�ͭ�Ѵ���������������˽Ϻõ�Ч������Ľ����ʴﵽ88%���ҡ�
REFERENCES
[1] ������. �⻯��������������������о�[D]. ������: �������Ƽ�ѧԺ, 2010: 2-3.
L Jin-yun. Study on the mechanism and technical conditions of iodine leaching of gold[D]. Haerbing: Heilongjiang Institute of Science and Technology, 2010: 2-3.
Jin-yun. Study on the mechanism and technical conditions of iodine leaching of gold[D]. Haerbing: Heilongjiang Institute of Science and Technology, 2010: 2-3.
[2] WILMOT J C, MILOSAVLJEVIC E B, SOLUJIC L, HENDRIX J L. Fate of cyanide in gold ores containing reduced sulphur minerals[C]//Proceedings of 24th International Mineral Processing Congress. Beijing: Science Press, 2008: 2958-2964.
[3] DAI X, JEFFREY M I. The effect of sulfide minerals on the leaching of gold in aerated cyanide solutions[J]. Hydrometallurgy, 2006, 82(3/4): 118-125.
[4] �� ��, ������. �軯�����軯�������[J]. ����ұ��, 2010, 39(3): 9-12.
YU Han, HU Xian-zhi. Review of gold-leaching technologies by cyanidation and non-cyanidation[J]. Yunnan Metallurgy, 2010, 39(3): 9-12.
[5] ���, ¬�ٴ�. ���軯������ķ�չ[J]. �й���ҵ, 2003, 12(3): 1-5.
LI Gui-chun, LU Shou-ci. The development of non-cyanidation gold lixiviating technology[J]. China Mining Magazine, 2003, 12(3): 1-5.
[6] HILSON G, MONHEMIUS A J. Alternatives to cyanide in the gold mining industry: what prospects for the future[J]. Journal of Cleaner Production, 2006, 14(12/13): 1158-1167.
[7] SYED S. Recovery of gold from secondary sources��A review[J]. Hydrometallurgy, 2012, 115/116: 30-51.
[8] QI P H, HISKEY J B. Dissolution kinetics of gold in iodide solutions[J]. Hydrometallurgy, 1991, 27(1): 47-62.
[9] QI P H, HISKEY J B. Electrochemical behavior of gold in iodide solutions[J]. Hydrometallurgy, 1993, 32(2): 161-179.
[10] ANGELIDIS T N, KYDROS K A, MATIS K A. A fundamental rotating disk study of gold dissolution in iodine-iodide solutions[J]. Hydrometallurgy, 1993, 34(1): 49-64.
[11] SEDELNIKOVA G V, KRYLOV G S. Iodinated and brominated solvent of gold[J]. Schnigri, 2001, 3: 43-52.
[12] BAGHALHA M. The leaching kinetics of an oxide gold ore with iodide/iodine solutions[J]. Hydrometallurgy, 2012, 113/114: 42-50.
[13] ���, ¬�ٴ�. �⻯���������о�[J]. �й���ҵ, 2004, 13(7): 66-68.
LI Gui-chun, LU Shou-ci. Experimental investigation for iodine leaching of gold[J]. China Mining Magazine, 2004, 13(7): 66-68.
[14] WANG Hai-xia, SUN Chun-bao, LI Shao-ying. Study on gold concentrate leaching by iodine-iodide[J]. International Journal of Minerals, Metallurgy and Materials, 2013, 20(4): 323-328.
[15] Ԭϲ��,����Ӣ,������,������,�ﴺ��,���׳,�� �.ij��ͭ�Ѵ������ѡ���Խ��������о�[J].�й��Ƽ���������, 2014, 9(3): 351-354.
YUAN Xi-zhen, LI Shao-ying, ZHAO Liu-cheng, KANG Jin-xing, SUN Chun-bao, LI Gen-zhuang, ZHANG Wei. Experimental study on selective leaching of refractory gold ores[J]. China Sciencepaper Online, 2014, 9(3): 351-354.
[16] ����Ӣ, ����ϼ, �ﴺ��, ������, ��־ǿ. �⻯��Խ�⻯������Ӱ��[J]. �й���ɫ����ѧ��, 2013, 23(5): 1434-1439.
LI Shao-ying, WANG Hai-xia, SUN Chun-bao, ZHAO Liu-cheng, YAN Zhi-qiang. Effect of different iodide on gold concentrates leaching process in iodine-iodide solution[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(5): 1434-1439.
[17] ����Ӣ, ����ϼ, Ԭϲ��, ������, �ﴺ��. ��⻯�������̶���ѧ[J]. �й���ɫ����ѧ��, 2014, 24(3): 814-819.
LI Shao-ying, WANG Hai-xia, YUAN Xi-zhen, ZHAO Liu-cheng, SUN Chun-bao. Leaching dynamics of gold concentrates by iodine-iodide solution[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(3): 814-819.
[18] MARUN J N, MEISSL R J, LARA R F, GARCIA R A. Gold bearing ore processing with iodine-iodide solutions[C]// Proceedings of the XX International Mineral Processing Congress, 1997: 381-389.
[19] ���, ������. �⻯������̵Ļ�������[J]. �������Ƽ�ѧԺѧ��, 2009, 19(5): 345-347, 364.
LI Gui-chun, L Jin-yun. Basic theory of iodide leaching of gold process[J]. Journal of Heilongjiang Institute of Science and Technology, 2009, 19(5): 345-347, 364.
Jin-yun. Basic theory of iodide leaching of gold process[J]. Journal of Heilongjiang Institute of Science and Technology, 2009, 19(5): 345-347, 364.
[20] ����ǰ, ÷���, �̴���. Au-Cl--H2Oϵ������ѧ����[J]. �ƽ�, 1982(3): 44-49.
ZHONG Zhu-qian, MEI Guang-gui, CAI Chuan-suan. The thermodynamic analysis for Au-Cl--H2O system[J]. Gold, 1982(3): 44-49.
[21] ���ǻ�. Au-NH3-H2Oϵ�ĵ�λ-pHͼ��������ѧ����[J]. ����ұ��, 1988, 9(3): 56-60.
MENG Xing-hui. E-pH diagrams and thermodynamic analysis of Au-NH3-H2O system[J]. Engineering Chemistry and Metallurgy, 1988, 9 (3): 56-60.
[22] ����˵, ֣�ٻ�. ����Cu-Cl--H2Oϵ������ѧ��������λ-pHͼ[J]. ���Ͽ�ұѧԺѧ��, 1980(3): 12-24.
FU Chong-yue, ZHENG Di-ji. The thermodynamic analysis on the Cu-Cl--H2O system and its potential-pH diagram[J]. Journal of Central South Institute of Mining and Metallurgy, 1980(3): 12-24.
[23] DAVIS A, TRAN T, YOUNG D R. Solution chemistry of iodide leaching of gold[J]. Hydrometallurgy, 1993, 32(2): 143-159.
(�༭ �� ��)
������Ŀ���ߵ�ѧУ��ʿѧ�Ƶ�ר����л���������Ŀ(20100006110003)
�ո����ڣ�2014-04-30�������ڣ�2015-07-13
ͨ�����ߣ��ﴺ�������ڣ���ʿ���绰��010-62334953��E-mail��suncb@ustb.edu.cn
ժ Ҫ������ͬʱƽ��ԭ����Au-I--H2Oϵ�Ľ�������ѧ���з������ֱ��о���Һ�����Au�Լ�AuI���������Auƽ��ʱ�Ħ�-pH��ϵ��AuI������������Һ�к�����ֵı仯���ɡ����������������Һ�к�����ֵ���Ũ��cT(Au)�Ľ��ͻ���ֵ���Ũ��cT(I-)�����ӣ���ԭ��λ��sol/AuѸ�ٽ��ͣ�Au3+/Au2O3��ƽ��pHֵ���dz������ڽ�ĵ⻯������������Һ��cT(I-)�����ӣ�����AuI�����������������������С�����ƣ���cT(Au)Ϊ1��10-4 mol/L�������£�����Һ��cT(I-)Ũ�ȴ���0.0021 mol/Lʱ���ɱ���AuI���������ɣ�����Ҫ��AuI2-���������ʽ���ڡ�Au-I--H2Oϵ�Ľ�������ѧ����Ϊ��ĸ�Ч�⻯�����ṩ���������ݡ�
[1] ������. �⻯��������������������о�[D]. ������: �������Ƽ�ѧԺ, 2010: 2-3.
[4] �� ��, ������. �軯�����軯�������[J]. ����ұ��, 2010, 39(3): 9-12.
[5] ���, ¬�ٴ�. ���軯������ķ�չ[J]. �й���ҵ, 2003, 12(3): 1-5.
[13] ���, ¬�ٴ�. �⻯���������о�[J]. �й���ҵ, 2004, 13(7): 66-68.
[16] ����Ӣ, ����ϼ, �ﴺ��, ������, ��־ǿ. �⻯��Խ�⻯������Ӱ��[J]. �й���ɫ����ѧ��, 2013, 23(5): 1434-1439.
[17] ����Ӣ, ����ϼ, Ԭϲ��, ������, �ﴺ��. ��⻯�������̶���ѧ[J]. �й���ɫ����ѧ��, 2014, 24(3): 814-819.
[19] ���, ������. �⻯������̵Ļ�������[J]. �������Ƽ�ѧԺѧ��, 2009, 19(5): 345-347, 364.
[20] ����ǰ, ÷���, �̴���. Au-Cl--H2Oϵ������ѧ����[J]. �ƽ�, 1982(3): 44-49.
[21] ���ǻ�. Au-NH3-H2Oϵ�ĵ�λ-pHͼ��������ѧ����[J]. ����ұ��, 1988, 9(3): 56-60.
[22] ����˵, ֣�ٻ�. ����Cu-Cl--H2Oϵ������ѧ��������λ-pHͼ[J]. ���Ͽ�ұѧԺѧ��, 1980(3): 12-24.


