ǰ�����Ʊ�����������FePO4��2H2O��LiFePO4���ܵ�Ӱ��
���磬Ҷ���룬���������ԣ�����������Σ������������
(���ϴ�ѧ ��ѧ����ѧԺ������ ��ɳ��410083)
ժ Ҫ��
(Fe(NO3)3��9H2O)�Ͷ�ˮ�����������(NaH2PO4��2H2O)Ϊԭ�ϣ����÷��ӳ������Ʊ�FePO4��2H2Oǰ���塣��FePO4��2H2O��Li2CO3�������ǻ�Ͼ��Ⱥ��¹����ս�õ�LiFePO4/C������������ϡ�����ǰ���巴Ӧ�¶ȡ���Һ��pH�͵μ��ٶȶ�FePO4��2H2O������ò�������Լ�LiFePO4�ĵ绯ѧ���ܵ�Ӱ�졣����ɨ��羵(SEM)�ͼ������ȷ�����(LPSA)����Ʒ����ò���������б�����ʵ����������FePO4��2H2O�����������ͷ�ɢ��Ӱ��LiFePO4/C������������ϵĵ绯ѧ���ܣ�������С�Ҿ��ȷ�ɢ��ǰ�����Ƶõ�LiFePO4�ĵ绯ѧ���ܽϺá��Ż��������Ƶõ�ǰ�������ΪƬ״��ƽ������Ϊ1.08 ��m����Ӧ��LiFePO4��0.1C��ŵ籶���µ����ֳ������Ϊ159.3 mA��h/g���ŵ�����Ϊ159.0 mA��h/g���״γ�ŵ�Ч��Ϊ99.8%�����ϱ��ֳ����õ�ѭ���������ܺͽṹ�ȶ��ԡ�
�ؼ��ʣ�
���ӳ�������FePO4��2H2O��LiFePO4��
��ͼ����ţ�TQ152��O61 ���ױ�־�룺A ���±�ţ�1672-7207(2014)03-0695-08
Effect of precursor preparation condition on FePO4��2H2O and performance of LiFePO4
DONG Hong, YE Hongqi, HAN Kai, LIU Hui, DU Yumin, QIN Tao, HAO Mengqiu, LIU Gonggang
(College of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstracts: Precipitation of negative dropping was adopted to prepare FePO4��2H2O precursor. After high-temperature calcination, LiFePO4/C cathode materials were synthesized by carbothermal reduction. Experiments were presented to investigate the effect of reaction temperature, solution pH and dropping speed on FePO4��2H2O and LiFePO4/C. The morphology and particle size of samples were characterized by scanning electron microscopy (SEM) and laser particle size analyzer (LPSA). The results show that particle size and dispersity of FePO4��2H2O influence the electrochemistry properties of LiFePO4/C. LiFePO4/C prepared by FePO4��2H2O with small particle size and good dispersion has good electrochemical performance. Under optimum conditions, mean particle size of FePO4��2H2O is 1.08 ��m. The first charge and discharge capacity of LiFePO4 are 159.3 mA��h/g and 159.0 mA��h/g at 0.1C rate. The first charge-discharge efficiency is 99.8%. The cathode materials exhibite good cycling performance, rate capability and structure stability.
Key words: precipitation of negative dropping; FePO4��2H2O; LiFePO4
���ʯ���������(LiFePO4)����ɱ��͡���ȫ���������������ߵ��ŵ��ܵ������ע[1-4]����������ϵ�������������[5]��ȣ�LiFePO4�ĵ��ӵ����ʺ��������ɢ����С[6]�������˲��ϵ�ʵ��������Ϊ�˸���LiFePO4��ʵ�������������˴����ϳɷ����ĸĽ���LiFePO4�ĺϳɷ�����Ҫ�и��¹��෨[7-9]���ܽ�������[10-11]��ˮ�Ⱥϳɷ�[12-13]����������[14-15]�Լ����սᷨ[16]�ȡ���Ϊ���¹��෨�е�һ�ֹ��գ���FePO4��2H2OΪǰ�����̼�Ȼ�ԭ���Ѿ��㷺Ӧ����LiFePO4���Ʊ�[17-19]��Ӧ����LiFePO4�������ϵ�FePO4��2H2O��Ϊ��ؼ�FePO4��2H2O�������������ʺ������ҶԿ�������ò������Ҫ���ϸ�FePO4��2H2O����Ӧ����ʳƷ���Ӽ������Ʊ����ռ����ϸ��������ؽ����������������ؼ�FePO4��2H2O��Ҫ��ǰ������Ʊ���������Ӱ��ǰ�������ò������������Ӱ��LiFePO4�ĵ绯ѧ���ܡ�ǰ�����Ʊ���������о����٣��ر�������������Ϊԭ�ϵ�ǰ�����Ʊ����١�������[17]��֣������[20]����FeSO4��7H2O��������Ϊԭ�ϣ���H2O2Ϊ��������ͨ��Һ��������ϳ�ǰ����FePO4��xH2O���ֱ����Ʊ�����pH����ҺŨ�ȶ�ǰ����FePO4��xH2O��LiFePO4��Ӱ�졣�������߽�����Fe(NO3)3��9H2O��NaH2PO4��2H2OΪԭ�ϣ�ϵͳ�ؿ���ǰ�����Ʊ�����������ǰ�������ò��������Ӱ�죬��һ��������ͬ�����Ƶõ�ǰ����Գ�ƷLiFePO4�ĵ绯ѧ���ܵ�Ӱ�졣
1 ʵ��
1.1 ǰ����FePO4��2H2O�ͳ�ƷLiFePO4/C���Ʊ�
�ֱ��ȡ��ˮ��������(Fe(NO3)3��9H2O)�Ͷ�ˮ�����������(NaH2PO4��2H2O)����������ˮ����ܽ⣬����������ϡ���������Һ��pH���������������ҺΪ��Һ����Ӧ���еμ���������Һ�����Ʒ�Ӧ�¶ȡ��μ��ٶȺͽ����ٶȷ�Ӧһ��ʱ�����ɴ�����ɫ���������ϴ�ӳ��˺��˱���ɵõ�FePO4��2H2Oǰ���塣
��Ħ����1:0.53��ȡFePO4��2H2O��Li2CO3���ټ���16%(��������)�����ǻ�Ͼ��ȡ���N2����¯��300 ��Ԥ��5 h��700 ������10 h����¯��ȴ�Ƶ�LiFePO4/C�������ϡ�
1.2 ���Ͻṹ�����ܱ���
��������SU1510��ɨ����������о���������������ò������ŷ����SCF-106�ͼ������ȷ����Dz���������������
1.3 ��ص���װ�����
��������8:1:1��ȡLiFePO4/C�������ϡ������̿�ں����PVDF������������N-��������ͪ(NMP)�����ĥ�������Ͼ���Ϳ���ں��Ϊ0.06 mm�������ϣ�����105 ������и���3 h������Ƭ��ѹƬ�õ���ʽ���������Ƭ������Ϊ�����Ƭ�����ҺΪ1 mol/L��LiPF6�����Һ��EC��DMC��EMC������Ϊ1:1:1����ĤΪCelgard 2300���������Χ������������װ��CR2025�Ϳ�ʽ��أ��������ز���ϵͳ���г�ŵ���ԡ�
2 ���������
2.1 ǰ����ϳ��¶ȶ�FePO4��2H2O��LiFePO4��Ӱ��
ͼ1��ʾΪ��ͬ��Ӧ�¶�ʱ�Ƶõ�FePO4��2H2O��SEM���Կ���������Ӧ�¶�Ϊ40 ��ʱ�Ƶõ�ǰ����������С��������ѻ��γɵĶ��ο�����ɣ����ο���ƽ������Ϊ14.34 ��m�������¶�����50 ��ʱ������ò�������Ա仯��ΪƬ״�����ҷ�ɢ�Ժã���������Ϊ1.18 ��m�������¶ȵ����߿�����Ƭ״���ͽᾧ�ȱ�ã������������仯����ͼ2��ʾΪFePO4��2H2O�ϳ��¶Ȳ�ͬʱ�Ƶ�LiFePO4��SEM����ͼ2��֪��40 ���ºϳɵ�ǰ����С�������������պ����������γɿ�״LiFePO4������ͼ3��ʾΪ��Ӧ�¶Ȳ�ͬʱ�Ƶ�FePO4��2H2O����������Ӧ��LiFePO4�����ַŵ�����ͼ��LiFePO4�����ַŵ���������ǰ����ĺϳ��¶ȵ����߶�����40 ������50 ��ʱ�����������ӣ�����¶�����������������
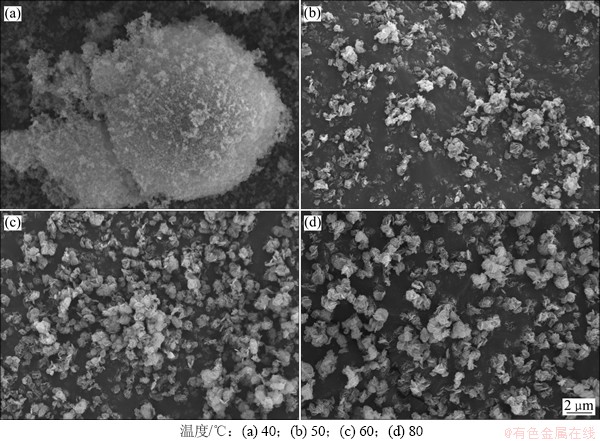
ͼ1 ��ͬ��Ӧ�¶�ʱ�Ƶ�FePO4��2H2O��SEM��
Fig. 1 SEM images of FePO4��2H2O prepared at different temperatures
�ۺϷ���ͼ1~3��֪��ǰ�����������ò����ɢ�Ժ�������LiFePO4�ĵ绯ѧ����Ӱ��������40 ���Ƶõ�ǰ����Ϊ���γ������ڸ��������С�Ŀ����ž��γɶ��ο��������������ͱȱ���������ѷ�ɢ�������������ʡ������ž��ѷ�ɢ�Ʊص����ڻ��Ϲ����������Dz��ܾ��ȵطֲ��ڿ����ı��棬������Ч���ڿ��������γ�̼������ֹ�����������������Ӷ����¿��������������ڲ��������ܲLiFePO4�ķŵ������͡�ͬʱ���������ʶԲ��ϵĵ绯ѧ�����и���Ӱ�졣FePO4��2H2O�ĺϳ��¶����ߣ�������������С���������ڷ�ɢ���������������������ڸ������չ�����������̼���ֽ��γɵ�����̼���ȵذ�����LiFePO4�������棬��ֹ������������������������С������FePO4��2H2O�ϳ��¶ȵ����ߣ�FePO4��2H2O�ᾧ�̶�����Ӧ��LiFePO4�Ľᾧ�ȱ�á����LiFePO4�ķŵ���������FePO4��2H2O�ĺϳ��¶����߶�����

ͼ2 FePO4��2H2O�ϳ��¶Ȳ�ͬʱ�Ƶ�LiFePO4��SEM��
Fig. 2 SEM images of LiFePO4 prepared with FePO4��2H2O synthesized at various temperatures
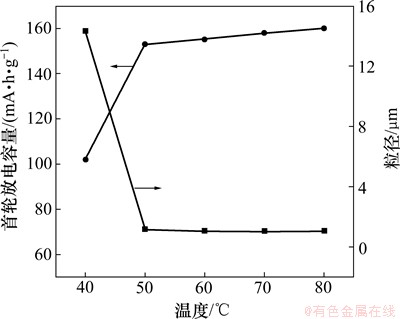
ͼ3 ��ͬ��Ӧ�¶�ʱ�Ƶ�FePO4��2H2O��ƽ����������Ӧ��LiFePO4�����ַŵ�����
Fig. 3 Average particle size of FePO4��2H2O prepared at different temperatures and first discharge capacity of LiFePO4
2.2 Fe(NO3)3��ҺpH��FePO4��2H2O��LiFePO4��Ӱ��
ͼ4��ʾΪFe(NO3)3��Һ��ͬpHʱ�Ƶ�FePO4��2H2O��SEM������pHΪ1.31ʱ����������Һδ����ϡ���ᡣͼ5��ʾΪFe(NO3)3��Һ��ͬpHʱ�Ƶ�FePO4��2H2O����������Ӧ��LiFePO4�����ַŵ���������ͼ4��ͼ5���Կ�������������ҺpH�Կ�������ò������Ӱ��ܴ�pHΪ0.45ʱ�Ƶõ�FePO4��2H2O��������Ϊ2.22 ��m�������ž����ء�pH����0.58ʱ����������С��1.08 ��m��������ɢ�Ժá�����������������Һ��pH��ǰ��������������仯�������ž۳̶���ǿ��LiFePO4�ķŵ���������pH��������������С��

ͼ4 Fe(NO3)3��Һ��ͬpHʱ�Ƶ�FePO4��2H2O��SEM��
Fig. 4 SEM images of FePO4��2H2O prepared at different pH of Fe(NO3)3 solution
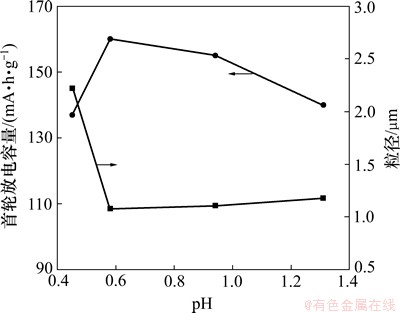
ͼ5 Fe(NO3)3��Һ��ͬpHʱ�Ƶ�FePO4��2H2O��ƽ����������Ӧ��LiFePO4�����ַŵ�����
Fig. 5 Average particle sizes of FePO4��2H2O prepared at different pH of Fe(NO3)3 solution and first discharge capacity of LiFePO4
FePO4��2H2O�����žۻᵼ��LiFePO4�����žۣ�����֮��ĵ����Լ�С�����ϵķŵ��������͡�FePO4��2H2O���γɷ�Ӧ����Ϊ��Fe3++PO43-+2H2O��FePO4��2H2O��ͬʱ������Fe3+��ˮ���H2PO4-���룺Fe3++3H2O��Fe(OH)3+3H+��H2PO4-��PO43-+2H+������������Һ�м��������������Fe3+��ˮ���H2PO4-�ĵ��롣pHС��0.58ʱ������Һ��Ƚϴ�Ӧ�ٶȽ����������ijɺ��ٶ�С�������ٶȣ��γɵĿ��������ϴ�pH����0.58ʱ��Ӧ�ٶȿ죬�����ijɺ��ٶȿ죬�����ž����ء�pH���������Ӧ�ӿ죬���������ٶȼӿ죬����������֮����
2.3 NaH2PO4��ҺpH��FePO4��2H2O��LiFePO4��Ӱ��
ͼ6��ʾΪNaH2PO4��Һ��ͬpHʱ�Ƶ�FePO4��2H2O��SEM����ͼ6���Կ�����NaH2PO4��ҺpH��FePO4��2H2O��������ò������Ӱ��������ͼ7��ʾΪNaH2PO4��Һ��ͬpHʱ�Ƶ�FePO4��2H2O��ƽ����������Ӧ��LiFePO4�����ַŵ�����ͼ��FePO4��2H2O��������������ҺpH�����߶���С��LiFePO4�����ַŵ���������pH��������������С��LiFePO4�ĵ绯ѧ������ǰ��������Ĵ�С�ͷ�ɢ���йأ�һ����˵��ǰ�����������Խ���Ƶ�LiFePO4������ҲԽ����ǰ�������������С���ž����أ�ǰ������������չ����������������Ƶõ�LiFePO4�����������������LiFePO4�����ڲ����ӵ����Բ�������ɢ·�̳���������ѳ���Ƕ�����ѣ��Ӷ�Ӱ����ϵĵ绯ѧ���ܡ�����Һ��pHΪ4.68ʱ���Ƶ�ǰ����FePO4��2H2O����������С�ҷ�ɢ�Ժã�����õ���LiFePO4�ĵ绯ѧ������á�

ͼ6 NaH2PO4��Һ��ͬpHʱ�Ƶ�FePO4��2H2O��SEM��
Fig. 6 SEM images of FePO4��2H2O prepared at different pH of NaH2PO4 solution
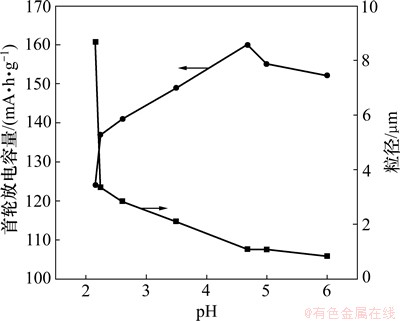
ͼ7 NaH2PO4��Һ��ͬpHʱ�Ƶ�FePO4��2H2O��ƽ����������Ӧ��LiFePO4�����ַŵ�����
Fig. 7 Average particle size of FePO4��2H2O prepared at different pH of NaH2PO4 solution and first discharge capacity of LiFePO4
2.4 �μ��ٶȶ�FePO4��2H2O��LiFePO4��Ӱ��
ͼ8��ʾΪFe(NO3)3��Һ��ͬ�μ��ٶ�ʱ�Ƶ�FePO4��2H2O��SEM��ͼ9��ʾΪFe(NO3)3��Һ��ͬ�μ��ٶ�ʱ�Ƶ�FePO4��2H2O��ƽ����������Ӧ��LiFePO4�����ַŵ�������Fe(NO3)3��Һ�μ��ٶ���ҪӰ���˳�����Ӧ���ʡ��μ��ٶȿ죬������ӦҲԽ�죬��Һ�Ĺ����ͶȾ�Խ�ߡ����μ��ٶ�Сʱ�����������ijɺ��ٶ�С�ڿ����������ٶȣ��õ��Ŀ��������ϴ�ɢ�ԽϺá����μ��ٶ�����2.8 mL/minʱ�����������ijɺ��ٶ�������������ٶ��൱���õ��ij�������������С�ҷ�ɢ�Ժá��μ��ٶȼ����������ijɺ��ٶȴ��ڿ����������ٶȣ�����������С���ž����ء�FePO4��2H2O��������Խ���Ƶ�LiFePO4��������ҲԽ���ϵķŵ�������С�����������������ޱ仯�������ž۳̶�����ʱ���Ƶ�LiFePO4������������ϵĵ绯ѧ���ܾͻή�͡�
2.5 �Ż��������Ƶ�LiFePO4�ĵ绯ѧ����
ͼ10��ʾΪ�Ż������ºϳ�LiFePO4/C��ŵ����ߡ�0.1C���ֳ������Ϊ159.3 mA��h/g���ŵ�����Ϊ159.0 mA��h/g���״γ�ŵ�Ч��Ϊ99.8 %����0.2C��0.5C��1C��3C�µķŵ������ֱ�Ϊ156.0��150.1��143.7��122.3 mA��h/g����С�����ŵ�ʱ��ѹƽ̨���ԣ�ƽ̨������3.4 V���ң�������ŵ�ʱ��ѹƽ̨�������͡�
FePO4��2H2O����������̼�Ȼ�ԭ��Ӧ�γ�LiFePO4/C������������ϡ�����FePO4��2H2O������ɢ�Ժã����ڵ������Ǿ��Ȱ�����ǰ����������棬������̼���ֽ⽫FePO4��2H2O��ԭ�γ�LiFePO4�����������̼���ȷֲ��ڿ������棬����˿���֮��ĵ����ԡ�ͬʱ���ڿ���������С���������ɢ·�̶̡�С�����ŵ�ʱ����Ӻ͵����ܹ����ٵĴ��ݣ����LiFePO4/C������������Ͽ��Ա��ֽϸߵķŵ��������������е�LiFePO4���FePO4����ӵ�������ӵ�����ھ����ԣ�������ŵ�ʱ��ѹƽ̨���ͣ��ŵ�������С��

ͼ8 Fe(NO3)3��Һ��ͬ�μ��ٶ�ʱ�Ƶ�FePO4��2H2O��SEM��
Fig. 8 SEM images of FePO4��2H2O prepared at different dropping speeds of Fe(NO3)3 solution
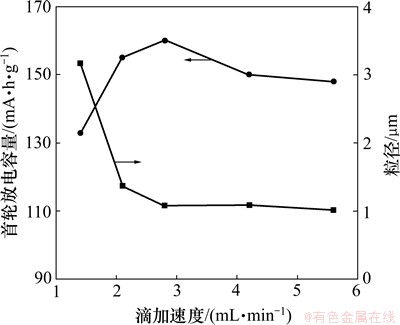
ͼ9 Fe(NO3)3��Һ��ͬ�μ��ٶ�ʱ�Ƶ�FePO4��2H2O��ƽ��������LiFePO4�����ַŵ�����
Fig. 9 Average particle sizes of FePO4��2H2O prepared at different dropping speeds of Fe(NO3)3 solution and first discharge capacity of LiFePO4
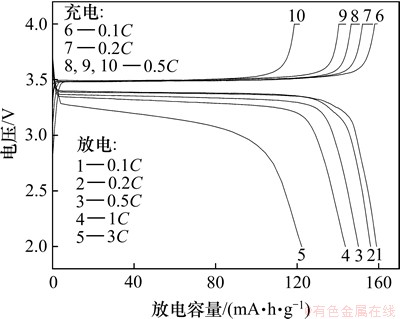
ͼ10 ��ͬ������LiFePO4/C�ij�ŵ�����
Fig. 10 Charge and discharge curves of LiFePO4/C at different rates
ͼ11��ʾΪ���ӳ������Ż������ºϳ�LiFePO4/Cѭ�������������ߡ���ͼ11���Կ�����LiFePO4/C�ڸ������µij�ŵ�ѭ���зŵ�����������˥����ѭ���������������������(3C)�ŵ���ٽ���С����(0.1C)��ŵ���ԣ�0.1C�ķŵ�����ά��������������99.6%�����������õ�ѭ�����ܣ�����LiFePO4/C�������õĽṹ�ȶ��ԡ�FePO4��2H2O����������̼�Ȼ�ԭ��Ӧ�õ��߽ᾧ�ȵ�LiFePO4/C��LiFePO4/C������ŵ������ת�������нṹ�仯��С����֤�˲��ϵĽṹ�ȶ��ԡ�
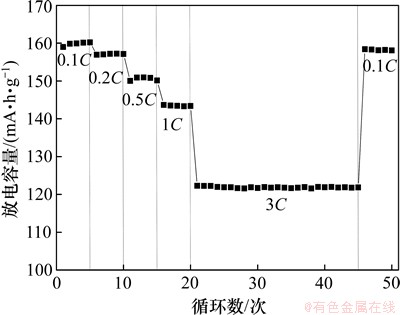
ͼ11 LiFePO4/Cѭ��������������
Fig. 11 Cycle performance of LiFePO4/C at different rates
3 ����
(1) �Ծ�ˮ��������(Fe(NO3)3��9H2O)�Ͷ�ˮ�����������(NaH2PO4��2H2O)Ϊԭ�ϣ����õμӳ������Ʊ�FePO4��2H2O��ʵ�鿼���˷�Ӧ�¶ȡ���Һ��pH�Լ��μ��ٶȶ�FePO4��2H2O������ò��������Ӱ�죬��������һ�������LiFePO4�ĵ绯ѧ���ܵ�Ӱ�졣ʵ�鷢��ǰ����FePO4��2H2O�����������ͷ�ɢ��Ӱ��LiFePO4/C������������ϵĵ绯ѧ���ܡ�������С�Ҿ��ȷ�ɢ��ǰ�����Ƶõ�LiFePO4�ĵ绯ѧ���ܽϺá�
(2) ͨ�������Ż�������Ʊ�FePO4��2H2O�Ľ�����������Ӧ�¶�Ϊ80 �棻��������ҺpHΪ0.58�������������Һ��pHΪ4.68����������Һ�ĵμ��ٶ�Ϊ2.8 mL/min���Ż������µõ���FePO4��2H2Oƽ������Ϊ1.08 ��m��
(3) �Ż�������Ӧ��LiFePO4��0.1C���ַŵ�����Ϊ159.0 mA��h/g�����ֳ�ŵ�Ч��Ϊ99.8%�����ϱ��ֳ����õ�ѭ���������ܺͽṹ�ȶ��ԡ�
�ο����ף�
[1] �²���, ���, ���ΰ�, ��. ̼�������������LiFePO4����ӵ�����ܵ�Ӱ��[J]. ���ϴ�ѧѧ��, 2011, 42(5): 1202-1208.
KE Changchun, LI Jie, ZHANG Zhian, et al. Effect of CNTs as conductive agent on performance of LiFePO4 lithium-ion battery[J]. Journal of Central South University, 2011, 42(5): 1202-1208.
[2] �ű�, ������. �ȴ��������ʯ��������﮵绯ѧ���ܵ�Ӱ��[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2007, 38(6): 1106-1109.
ZHANG Bao, PENG Chunli. Effect of heat treatment on electrochemical performance of olivine type lithium iron phospho[J]. Journal of Central South University (Science and Technology), 2007, 38(6): 1106-1109.
[3] ����, ��־��, ���º�, ��. ǰ�������-������ĥ��ԭ�Ʊ� Ti4+����LiFePO4[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2009. 40(2): 288-293.
WU Ling, WANG Zhixing, LI Xinhai, et al. Preparation of Ti4+ doped LiFePO4 by precursor-doping and room temperature reduction Via ball milling[J]. Journal of Central South University (Science and Technology), 2009, 40(2): 288-293.
[4] �ű�, ������, ��־��, ��. ��̼��ʽ��������﮶���ѧ���绯ѧ���ܵ�Ӱ��[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2007, 38(5): 863-866.
ZHANG Bao, PENG Chunli, WANG Zhixing, et al. Effect of adding carbon modes on kinetic and electrochemical performances of LiFePO4[J]. Journal of Central South University (Science and Technology), 2007, 38(5): 863-866.
[5] XU Bo, QIAN Danna, WANG Ziying, et al. Recent progress in cathode materials research for advanced lithium ion batteries[J]. Materials Science and Engineering, 2012, 73(5/6): 51-65.
[6] LI Huiqiao, ZHOU Haoshen. Enhancing the performances of Li-ion batteries by carbon-coating: present and future[J]. Chemical Communications, 2012, 48: 1201-1217.
[7] �Ⱞ��, �����, ¬����, ��. Li2CO3, FePO4�������Ǻϳ�LiFePO4�Ļ����о�[J]. ϡ�н���, 2010(6): 880-886.
WU Aide, ZHANG Xiangjun, LU Shigang, et al. Mechanism of Synthesizing LiFePO4 with Li2CO3, FePO4 and Glucose[J]. Chinese Journal of Rare Metals, 2010(6): 880-886.
[8] ������, ������, �ƿ���, ��. �����¶ȶԺϳ�LiFePO4�IJ�����ɺ͵绯ѧ���ܵ�Ӱ��[J]. ������ѧѧ��, 2007, 23(7): 1117-1122.
LIU Suqin, GONG Benli, HUANG Kelong, et al. Effect of calcination temperature on the compositions and electrochemical performance of products in the synthesis of LiFePO4[J]. Acta Physico-Chimica Sinica, 2007, 23(7): 1117-1122.
[9] Zhang S S, Allen J L, Xu K, et al. Optimization of reaction condition for solid-state synthesis of LiFePO4-C composite cathodes[J]. Journal of Power Sources, 2005, 147(1): 234-240.
[10] CHEN Quanqi, LI Xiaoshuan, WANG Jianming. Electro- chemical performance of LiFePO4/(C+Fe2P) composite cathode material synthesized by sol-gel method[J]. Journal of Central South University of Technology, 2011, 18(4): 978-984.
[11] Miran G, Robert D, Marjan B, et al. Porous, carbon-decorated LiFePO4 prepared by sol-gel method based on citric acid[J]. Solid State Ionics, 2005, 176(19): 1801-1805.
[12] Tajimi S, Ikeda Y, Uematsu K, et al. Enhanced electrochemical performance of LiFePO4 prepared by hydrothermal reaction[J]. Solid State Ionics, 2004, 175(1/2/3/4): 287-290.
[13] Meligrana G, Gerbaldi C, Tuel A, et al. Hydrothermal synthesis of high surface LiFePO4 powders as cathode for Li-ion cells[J]. Journal of Power Sources, 2006, 160(1): 516-522.
[14] Arnold G, Garche J, Hemmer R, et al. Fine-particle lithium iron phosphate LiFePO4 synthesized by a new low-cost aqueous precipitation technique[J]. Journal of Power Sources, 2003, 119/120/121: 247-251.
[15] WANG Ying, SUN Bing, PARK Jinsoo, et al. Morphology control and electrochemical properties of nanosize LiFePO4 cathode material synthesized by co-precipitation combined with in situ polymerization[J]. Journal of Alloys and Compounds, 2011, 509(3): 1040-1044.
[16] Masashi H, Katayama K, Azuma Y, et al. Synthesis of LiFePO4 cathode material by microwave processing[J]. Journal of Power Sources, 2003, 119/120/121: 258-261.
[17] ������, ��, �ű�, ��. ��ҺŨ�ȶ�ǰ����FePO4��xH2O��LiFePO4���ܵ�Ӱ��[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2010, 41(5): 1668-1673.
PENG Chunli, SHEN Chao, ZHANG Bao, et al. Effect of solution concentration on FePO4��2H2O precursor and performance of LiFePO4[J]. Journal of Central South University (Science and Technology), 2010, 41(5): 1668-1673.
[18] ���Ҷ�, �ƴ���, ������, ��. ���ȳ������Ʊ�LiFePO4/C����绯ѧ����[J]. �й���ɫ����ѧ��, 2012, 22(5): 1319-1325.
PENG Zhongdong, TANG Daichun, HU Guorong, et al. Synthesis and electrochemical performance of LiFePO4/C by homogeneous precipitation method[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(5): 1319-1325.
[19] �����, ֣��, �ܸ�ۿ, ��. �Ż�̼��������������LiFePO4/C�߱������ܵ�Ӱ��[J]. ������ѧѧ��, 2009, 25(11): 2186-2190.
YU Hongming, ZHENG Wei, CAO Gaoshao, et al. Effects of optimized carbon-coating on high-rate performance of LiFePO4/C composites[J]. Acta Physico-Chimica Sinica, 2009, 25(11): 2186-2190.
[20] ֣����, ���º�, ��־��, ��. �Ʊ�����pHֵ��FePO4��xH2O��LiFePO4���ܵ�Ӱ��[J]. �й���ɫ����ѧ��, 2008, 18(5): 867-872.
ZHENG Junchao, LI Xinhai, WANG Zhixing, et al. Effect of pH value on performance of FePO4��xH2O and LiFePO4 in synthesis process[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(5): 867-872.
(�༭ �°���)
�ո����ڣ�2013-04-08�������ڣ�2013-07-20
������Ŀ��������Ȼ��ѧ����������Ŀ(21276284)
ͨ�����ߣ�Ҷ����(1958- )���У����ռ�Ϫ�ˣ����ڣ���ʿ����ʦ�����·�����ϵ��Ʊ������о����绰��0731-88876605��E-mail: hongqiye@gmail.com
ժҪ���Ծ�ˮ��������(Fe(NO3)3��9H2O)�Ͷ�ˮ�����������(NaH2PO4��2H2O)Ϊԭ�ϣ����÷��ӳ������Ʊ�FePO4��2H2Oǰ���塣��FePO4��2H2O��Li2CO3�������ǻ�Ͼ��Ⱥ��¹����ս�õ�LiFePO4/C������������ϡ�����ǰ���巴Ӧ�¶ȡ���Һ��pH�͵μ��ٶȶ�FePO4��2H2O������ò�������Լ�LiFePO4�ĵ绯ѧ���ܵ�Ӱ�졣����ɨ��羵(SEM)�ͼ������ȷ�����(LPSA)����Ʒ����ò���������б�����ʵ����������FePO4��2H2O�����������ͷ�ɢ��Ӱ��LiFePO4/C������������ϵĵ绯ѧ���ܣ�������С�Ҿ��ȷ�ɢ��ǰ�����Ƶõ�LiFePO4�ĵ绯ѧ���ܽϺá��Ż��������Ƶõ�ǰ�������ΪƬ״��ƽ������Ϊ1.08 ��m����Ӧ��LiFePO4��0.1C��ŵ籶���µ����ֳ������Ϊ159.3 mA��h/g���ŵ�����Ϊ159.0 mA��h/g���״γ�ŵ�Ч��Ϊ99.8%�����ϱ��ֳ����õ�ѭ���������ܺͽṹ�ȶ��ԡ�


