LiNi1/3Co1/3Mn1/3O2�������ϵ��Ʊ��������
�ռ��ң� ���� ���ǹ㣬���ݻ�
(���ϴ�ѧ ���Ͽ�ѧ�빤��ѧԺ������ ��ɳ��410083)
ժ Ҫ��
ժ Ҫ�����û�е��ĥ��ǰ������л��������940 ���ڿ����������ս�12 h�Ʊ���״�ṹLiNi1/3Co1/3Mn1/3O2�������ϡ�ͨ��XRD��SEM�͵绯ѧ���ܲ��Զ����Ʊ����ϵĽṹ����ò���绯ѧ���ܽ��б�����������������ϳɵIJ���Ϊ�����������״�ṹ������һ�������������ȣ�Ϊ1~2 ��m�������žۿ���ƽ������Ϊ10 ��m���ң���2.75~4.3 V��ѹ���䣬���Ʊ���LiNi1/3Co1/3Mn1/3O2��0.2C(CΪ��ŵ籶��)���к������ŵ磬�״ηŵ�������146.3 mA��h��g-1���ڱ���Ϊ0.4C��0.8C��1.6C�� 2.0Cʱ�ķŵ������ֱ�Ϊ135.2��130.1��125.8��114.7 mA��h��g-1�����ʷŵ������������ڱ���Ϊ0.2Cʱ����30��ѭ�������Ϸŵ����������������ʷֱ�Ϊ143.3 mA��h��g-1��98%��ѭ���ȶ��Ժá�
�ؼ��ʣ�
����ӵ�������෨��LiNi1/3Co1/3Mn1/3O2��
��ͼ����ţ�TM912.9 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2008)02-0221-07
Preparation and characterization of LiNi1/3Co1/3Mn1/3O2 cathode material
SU Ji-tao, SU Yu-chang, LAI Zhi-guang, FANG Hui-hui
(School of Materials Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Layered structure of LiNi1/3Co1/3Mn1/3O2 cathode material was prepared by a solid state method with the precursor activated by ball milling. XRD, SEM and electrochemical tests were used to characterize the structure, micro-morphology and electrochemical properties of the as-prepared materials. The results show that pure phase LiNi1/3Co1/3Mn1/3O2 with hexagonal structure is obtained at 940 �� for 12 h in air. The average secondary particle size is about 10 ��m with uniform primary particles of 1-2 ��m in diameter. The as-prepared LiNi1/3Co1/3Mn1/3O2 delivers initial discharge capacity of 146.3 mA��h��g-1 at 0.2C rate in the voltage of 2.75-4.3 V, and the discharge capacities at 0.4C, 0.8C, 1.6C and 2.0C are 135.2, 130.1, 125.8 and 114.7 mA��h��g-1, respectively, indicating good rate capability. After 30 cycles at 0.2C, the discharge capacity and capacity retention ratio are 143.3 mA��h��g-1 and 98%, respectively, indicating good cycling stability.
Key words: Li-ion battery; solid state method; LiNi1/3Co1/3Mn1/3O2
LiCoO2��ʵ����Ʒ���������������������豸���ֻ����ʼDZ����Ե����㷺�����ɳ��Դ�������ϣ������Ʊ��������һ���Ľ������ƣ����⣬������Դȱ������Լ��LiCoO2����ȫ�Ե�Ӱ�죬LiCoO2�ڴ���������е�Ӧ���ܵ�����[1-2]��LiNiO2��LiMn2O4��һ�ȱ���Ϊ�ǽϺõ����LiCoO2�IJ� �ϣ���LiNiO2�ĺϳ��������̣�����ʵ�ֹ�ҵ�����Ҹò��ϱ������ڰ�ȫ���ܵ����⣬�谭����ʵ��Ӧ��[3]��LiMn2O4�������䰲ȫ���ܺá��۸���ˣ������ڻ����Ѻò��϶��ܵ���ע[4]��Ȼ�����ò�������ƫ�ͣ�������������Ϊ148 mA��h��g-1����ͨ�����Ʊ��IJ������������ֻ�ܴﵽ110 mA��h��g-1���ң����ڵ��Һ�У������ڸ����£������̵��ܽ�����²���ѭ��˥���ӿ죬���Դ����ƹ�Ӧ�á�LiFePO4�ɳ�Ϊ����Ⱦ���ϣ�������۸���˺߰�ȫ�Զ��������ӣ����������ò��ϵõ��㷺�о���Ӧ�ã����ò��ϵ絼�ʵͣ�����ʵ�ܶ�С���������Ӧ�������ܵ��ܴ����ơ�
��T. Ohzuku��[5]��LiNi1/3Co1/3Mn1/3O2�������Ͻ����о��������������ǶԴ˽����˴����о�[6-8]��LiNi1/3Co1/3Mn1/3O2�ۺ���LiNiO2��LiCoO2��LiMnO2��3����ϵ��ŵ㣬�γ���LiNiO2/LiCoO2/LiMnO2�Ĺ�����ϵ���������Ե���ԪЭͬ���á�����������ڳ�ŵ�������ܱ��ֲ�״�ṹ�������������״LiMnO2��⾧ʯ�ṹת�䡣Ŀǰ���ϳ�LiNi1/3Co1/3Mn1/3O2�ķ�����Ҫ�й��෨[9]����������[10-11]����������һ���ǰѻ�ѧԭ������Һ״̬��ϣ�������Һ�м���������������ʹ��Һ���Ѿ���Ͼ��ȵĸ�����ְ���ѧ�����ȳ�����������������Һ���ȷ�Ӧ������1���м����ٰ������շֽ��Ʊ�ϸ���ϵIJ�Ʒ������������ʵ�ֶ�Ԫ�صľ��Ȼ�Ϸ���ͻ�Գ����Ե����ƣ�����Ӱ�����ض࣬���ƹ��̸��ӣ�����ɲ�Ʒ�������ȶ���������ʵ�ֲ�ҵ����Ϊ�ˣ���������ͨ����е��ĥ��ǰ������л������ʵ�ֶ���ԭ�ϵĸ߾��ȶȻ�ϼ����������ǰ����ķ�Ӧ���ԣ���ͨ�������ս��Ʊ���һ���LiNi1/3Co1/3Mn1/3O2�������ϡ�
1 ʵ ��
1.1 LiNi1/3Co1/3Mn1/3O2���Ʊ�
ʵ��ԭ��Ϊ����Զ(�人)�²�������˾������Li2CO3(����Ϊ99.5%)���������н���ܵ�ز�������˾������Ni(OH)2(99.0%)�������еڰ˻�������˾������Co3O4(99.0%)����̶�绯�Ƽ��ɷ�����˾�����ĵ��MnO2(98.0%)������ѧ�����ȳ�ȡ��ԭ�ϲ���Ͼ��ȣ����ǰ���壬����ת������ʽ��ĥ�����л�е������ϱ�Ϊ10?1��ת��Ϊ200 r/min�����붨����ҵ�Ҵ���Ϊ��ɢ�����ʱ��Ϊ2 h��������ǰ���彬��ȡ����70 ����������õ�ǰ��������ڿ����������ڲ�ͬ�¶��ս���Сʱ�õ�������Ϊ��ƷA��B��C��D��E������Ʒ���ս������������£�900 ��/12 h��920 ��/12 h�� 940 ��/8 h�� 940 ��/12 h��960 ��/8 h�����ս�õ���Ʒ��ĥ����50 ��mɸ�������ڸ������б��á�
1.2 ���ϱ��������
�����ձ���ѧRigaku D-MAX2500VB��X���������Ƕ��Ʊ��IJ��Ͻ��нṹ�ⶨ����Cu�е�K��Ϊ����Դ(������=1.5406��10-10 m)������Ϊ0.02?��������ѹΪ40 kV����������Ϊ300 mA��ɨ�跶ΧΪ15?~80?��ͨ��FEI Sirion ������ɨ�����������ԭ�ϼ����Ʊ����ϵ���ò���з���������������ѹΪ20 kV��
1.3 �绯ѧ���ܲ���
���ϵ绯ѧ���ܲ��Է������£����������Բ�������Ȳ�ڡ�PVDF��������88?7?5��ϣ���������������ͪ���ô���������ɾ��Ƚ��ϣ�����Ϳ���������ϣ���120 ����ո���24 h���á��ڳ����������������װ���ʽ(CR-2032)���Ե�أ�����Ϊ�����Ƭ�����ҺΪ1 mol/L LiPF6(EC+DEC)����ĤΪCelgard2400�ױ�Ĥ���������£��ö�ͨ����ز�����(LIXING���ͺ�PCBT-110-8D-B)�Ե����2.75~ 4.3 V��ѹ֮����г�ŵ�ѭ�����ԣ�������EG&G��˾��263A�ͺ��λ�ǶԵ����2.5~4.5 V��ѹ��Χ����ѭ���������ԡ�
2 ���������
2.1 X�����������
Ϊ�˿����е���ǰ����ṹ�ĸı䣬�Ի�е�ǰ/���ǰ�����������XRD��������ͼ1��ʾ���ɼ���������ĥ���ǰ������Li2CO3��Co3O4��Ni(OH)2�������������˲�ͬ�̶ȵĿ����ͼ�������Ϊ�������ǣ�Li2CO3��36?��39?������2������������ʧ������Ҫ�ǻ�е�ʹ���ϱ���������ྦྷ��ȱ�����¡�
��ʵ�������õ���ԴΪ����-MnO2�����ڦ�-MnO2�ı����ᾧ�Ȳ����ߣ���ͼ1�Ц�-MnO2��XRDʵ��ͼ�����г��Ա�۲�����ĥ��������������λ�ı仯����ͼ1���Կ���������ĥ���-MnO2��42.4?��56.2? 2�����������Կ�������ͽǶ�ƫ����λ�â�͢�22?������������ʧ����-MnO2��Ȼ�Ǿ��壬���ǽᾧ������[12]���䷴Ӧ���Դ�ȱ��������֮��(����ȱ��)������������Ӧ�IJ�λ�������뷴Ӧ�Ĺ��壬��״̬�Է�Ӧ������Ӧ�ٶ���ֱ��Ӱ�졣��ԭ��֮һ�ǻ��Ĺ����д��ڴ����ĵ���ȱ�ݡ����ֵ���ȱ�ݰ�����ԭ�Ӽ��ĵ�ȱ�ݡ�λ����������������������д�����������ȱ�ݣ��߽ǶȾ��缰����λ�����ȡ�ͨ����е���������Ӧ��ĵ���ȱ�ݺͱȱ��������߷�Ӧ��ϵ�������ܣ��Ӷ�ʹ��Ӧ����˳�����С�������е������������˵�����ϵĵ���ȱ�ݺ;�����������ǣ����þ���ȱ�������ͦ�-MnO2���������ο�����ƫ���Dz����ģ���Ϊ����ѽ��ͦ�-MnO2��42.4?��56.2?������ڻǰ�����ľ�ƫ�ơ��ⶼ˵����е��еĶ���ѧ���ʴ�ʹLi2CO3��ij����ʽ���-MnO2������ѧ��Ӧ�������µ��������ɡ���е�ʹLi2CO3�ͦ�-MnO2Ƶ���Ӵ������������ܷdz���2��ԭ������þ��γɴ����������С���ˣ������µĻ����N. V. Kosova��[13]��LiOH�ͦ�-MnO2����ĥ���ϵ�������о�����Ϊ����ĥ���������һ�����͵�ˮ�������������������ɣ����ڱ�ʵ���У����ڻ���ԭ����Ҫ�Ա�����-MnO2������壬��ˣ���Ϊ���ֻ�������ˮ��﮻��������̡�
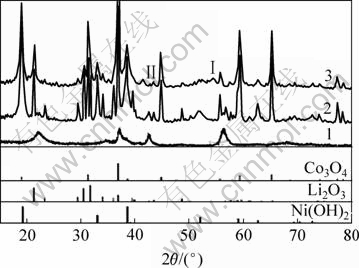
1������-MnO2��2��δ�ǰ���壻3�������ǰ����
ͼ1 ��е�ǰ/��ǰ�������ϵ�XRDͼ��
Fig.1 XRD patterns of precursor before and after mechanical activation
ͼ2��ʾΪ�ڿ����������ڲ�ͬ�¶ȡ���ͬʱ���ս����Ʒ��XRDͼ�ף�����Si��Ϊ�˾�ȷ�������Ʊ����ϵľ������������ӵ��ڱ��ࡣͼ2(a)��ʾΪ900 ��/12 h���������Ʊ���Ʒ��XRDͼ����ʱLiNi1/3Co1/3Mn1/3O2�������Ѿ��γɣ���������LiCoO2������壬�ɼ����ڴ������¾��Ц�-NaFeO2�ṹ�IJ��������ɣ���Ni��Co��Mn 3�ֹ��ɽ���Ԫ�ز�û���γɺܺõĵ�һ������壻�����ս��¶ȵ�����(��ͼ2(b)��(c))����920 ��/12 h��940 ��/8 h�����¾����γɵ�һ��IJ�״LiNi1/3Co1/3Mn1/3O2��������廹���������Ҵ�ͼ2�зŴ�ͼ����Ҳ���Կ���������� (108)��(110)�岢û����ȫ���룬˵�����״�ṹ�����Ǻ�����[14-15]������������ȱȽϵͣ������ս�ʱ����ӳ����ս��¶ȵĽ�һ�����(��ͼ2(d)��2(e))����������ø��Ӽ���(108)��(110)�����Ҳ���Է��룬���������ս��¶ȵ���ߺ�ʱ����ӳ�������ľ����̶ȼ�����������Ƚ�һ����ߣ�ͬʱ�����ս��¶ȸ���940 ��ʱ��(108)��(110)�����Ե�ka2������ԣ���Ҳ�Dz��Ͼ����̶ȸߵı��֡���������Ʒ��XRDͼ��֪��LiNi1/3Co1/3Mn1/3O2��������ϵ��R-3m�ռ�Ⱥ��
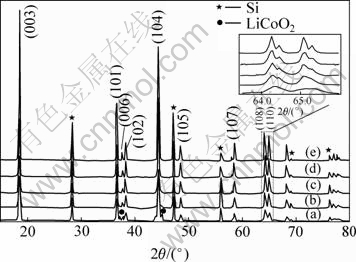
(a) ��ƷA, 900 ��, 12 h; (b) ��ƷB, 920 ��, 12 h; (c) ��ƷC, 940 ��, 8 h; (d) ��ƷD, 940 ��, 12 h; (e) ��ƷE, 960 ��, 8 h
ͼ2 ��ͬ�������Ʊ�����Ʒ��XRDͼ��
Fig.2 XRD patterns of samples prepared under different conditions
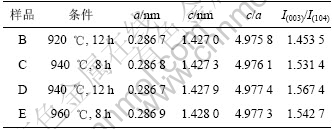
����XRD���ݼ�����ƷB��C��D��E�ľ�������a��c��c/a�������(003)��(104)��ǿ��֮�� (I(003)/I(104))�����1��ʾ���ɼ��������ս��¶ȵ�����ս�ʱ����ӳ�����������a�仯������������c������c/a��������С���Բ�״��-NaFeO2�͵缫���϶��ԣ�c/aҲ�DZ���������״�ṹ����ȵ���Ҫ��־����ӳ�˾�������̶�[16]���ɼ����ʵ�����ս��¶Ⱥ��ӳ��ս�ʱ�䣬��������ǿ���ϵĶ�ά�ṹ�ȶ��ԣ�ʹ��״�����������ԣ����ս��¶���ߵ�960 ��ʱ����ƷE��c/a�ֿ�ʼ��С����Ҫ��������960 ������������Li�ӷ������²���Ni����ռ�ݾ���ṹ������Li���ӵ�3aλ�ö��γ�С�ṹ�������������˲��ϵľ������䣻(003)��(104)�����ǿ��֮�ȷ�ӳ�������ӵĶ�ά����ȣ����ں�Ni�������������ϣ���I(003)/I(104)����1.2ʱ����������ȼ�С�����²��ϵ绯ѧ���ܵĶ�[17-18]����1����ƷB��C��D��I(003)/I(104)������1.2���ҳ����������ƣ��ɼ����ʵ�����ս��¶ȼ��ӳ��ս�ʱ���������������������ȣ������ս��¶���ߵ�960 ��ʱ����ƷE��I(003)/I(104)�������ƷD���������ͣ���Ҫ����Li�ӷ����²���Ni����ռ��Li���ӵ�3aλ�ö��γ�С�ṹ��������ͬʱ�������˲��ϵ�����������ȡ�
��1 ����Ʒ��صľ���ѧ����
Table 1 Relative crystal parameters of samples
2.2 SEM����
����ɨ�����������ԭ�ϼ����Ʊ���Ʒ����ò���б�����ͼ3(a)��3(b)��ʾΪ�����ԭ����ĥ�ǰ�ͻ���SEM��Ƭ���ɼ�����ĥ�ǰԭ�Ͻ�����������Ͼ��ȣ�����ԭ�ϵĽṹ��δ��ɢ�����������������νṹ��������������ĥ�2 h��ԭ�Ͼ����黯������������ָ߶Ⱦ��Ȼ�ϣ��Ҿ��нϸߵı����ܣ������ں����ս�����й��෴Ӧ��ԭ�Ӽ����ɢǨ�ƵĽ��У�ͼ3(c)��ʾΪ940 ��ʱ�ս�12 h�Ʊ�����ƷD����ò��Ƭ����ͼ3(c)���Կ���������һ��ԭ����������Ϊ1~2 ��m�������࣬�����̶ȸߣ���һ�����ӽ��ܶѻ����ž�Ϊ���ο��������ο�������Ϊ10 ��m���ң������ֲ����ȡ�

(a) δ����ĥ�ԭ�ϣ�(b) ��ĥ�ԭ�ϣ�(c) ��ƷD
ͼ3 ԭ�ϼ����Ʊ�LiNi1/3Co1/3Mn1/3O2 (��ƷD)��SEM��Ƭ
Fig.3 SEM photographs of precursor and as-prepared LiNi1/3Co1/3Mn1/3O2 (sample D)
2.3 �绯ѧ����
2.3.1 ѭ����������
Ϊ�о�LiNi1/3Co1/3Mn1/3O2���ϵ���/Ƕ﮻��ƣ�����ƷE����ѭ���������ԡ�ǰ2��ѭ������������ͼ4��ʾ��ɨ���ѹ����Ϊ2.5~4.5 V�����״�ѭ���У���3.95 V���������Ե������壬����Ӧ����Li+�����������ѳ��Ĺ��̣���Ӧ����3.75 V�Ļ�ԭ�����ӦLi+��Ƕ���������ϵĹ��̡�ֵ��ע����ǣ��ڵ�2��ѭ��ʱ����ԭ��������״�ѭ��ʱ�Ļ�ԭ���غϣ�������������͵�λ������3.85 V������Ҫ�����״�ѭ��������Li+Ǩ�Ƶ�ͨ������ͨ�绯ѧ������С���¡���ͼ4���Կ�������ÿ��ѭ�������о�ֻ����1������/��ԭ�壬δ����LiNiO2ѭ������ͼ�е�3����ת���壬����LiNi1/3Co1/3Mn1/3O2�� ��/�ŵ�ѭ�������в�û�з���������LiNiO2����ת�䡣�ڲ�״Li2/3(Ni1/3Mn2/3)O2��Mn3+/Mn4+������/��ԭ��λ��3 V����[16]�����ڲ�״LiNi1/3Co1/3Mn1/3O2��Co3+/Co4+������/��ԭ��λԼΪ4.6 V������LiNi1/3- Co1/3Mn1/3O2���������й��ɽ���Ni��Co��Mn�ļ�̬�ֱ�Ϊ+2��+3��+4[19-20]����ˣ�LiNi1/3Co1/3Mn1/3O2ѭ�������е�1������/��ԭ������Ӧ����Ni2+/Ni4+�����״�ѭ����ȣ���2��ѭ���е�����������Լ�С������ԭ����������״ε��غϣ�����LiNi1/3Co1/3- Mn1/3O2���нϸߵij�/�ŵ�����Լ����������ʡ�
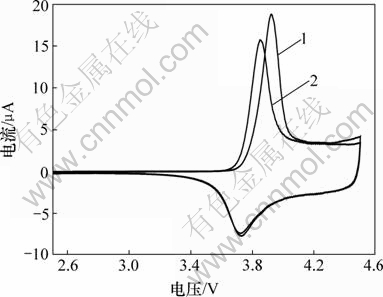
1����1��ѭ����2����2��ѭ��
ͼ4 LiNi1/3Co1/3Mn1/3O2(��ƷE)ѭ������ͼ
Fig.4 Cyclic volt-ampere curves for LiNi1/3Co1/3Mn1/3O2 (sample E)
2.3.2 ��������
ͼ5��ʾΪ��ƷB��C��D��E��2.75~4.3 V��ѹ������0.2C(��30 mA��g-1)��ŵ���״γ�ŵ����ߡ�������ƷA��δ�ϳɵ�һ��LiNi1/3Co1/3Mn1/3O2����û�ж���绯ѧ���ܽ��з��������ڸ���Ʒ�״� ��/�ŵ�������Ч�ʣ���ƷBΪ168/128.3 mA��h��g-1��76.4%�� ��ƷCΪ170.8/135.1 mA��h��g-1��79.1%����ƷDΪ178.7/146.3 mA��h��g-1��81.9%����ƷEΪ176.4/142.2 mA��h��g-1��80.6%������960 ���ս�12 h���Ʊ�����ƷD��������ѣ���ŵ�������Ŀǰ����LiCoO2(Լ145 mA��h��g-1)���൱�������ս��¶ȵ������ս�ʱ����ӳ������ϵ���������ŵ�Ч�ʶ�������ߣ�����Ҫ����������ս��¶ȼ��ӳ��ս�ʱ�䣬����������߲��ϵľ����̶ȼ��������״�ṹ���Ӷ���/�ŵ�������ߣ������ս��¶�������960 ��ʱ����ƷE����������/�ŵ�Ч������ƷD����ȷ������ͣ��������������960 ������������Li�ӷ����γ��˲���Liȱλ��������Ni2+�ڿռ�Ⱥ��3aλ����(��Li+λ��)��ռ���ʣ���3aλ���ϵ�Ni2+����ɺ���������缫�״�ѭ������˥������Ҫԭ��֮һ��3aλ���ϵ�Ni2+����﮺��ڽ������������Ӱ뾶��С��Ni3+��������ɸ����Ӹ����ṹ���ݣ�������Ƕ﮹�����﮽�����Ƕ�������ݵ�λ���ϣ��Ӷ����Ƕ�����С���״ο���������С[21]��������Li���������Բ��ϵ绯ѧ���ܵ�Ӱ�����д��ڽ�һ���о���
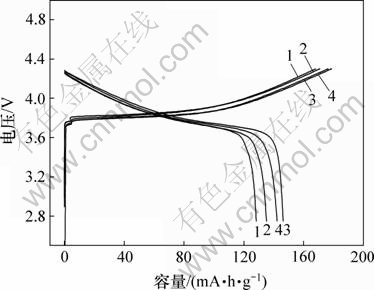
1����ƷB��2����ƷC��3����ƷD��4����ƷE
ͼ5 ��ƷB, C, D��E��0.2C�״γ�ŵ�����
Fig.5 Initial charge/discharge curves of samples B, C, D and E at 0.2C rate
��ͼ5���Կ������տ�ʼ���ʱ����ѹ�ܿ�������3.85 V���ң���3.85~4.0 V֮�䱣�ֽϳ��ij��ƽ̨����Ȼ����������4.3 V������K. M. Shaju��[19]�������Ľ������һ�¡���LiNi1/3Co1/3Mn1/3O2���������й��ɽ���Ni��Co��Mn�ļ�̬�ֱ�Ϊ+2��+3��+4��Mn4+�ȶ����ڱ�����Mn3+�ڳ�ŵ�����в���Jahn-Teller���䡣��������Ϊ����Գɷ֣��ڳ�ŵ������Ni2+![]() Ni3+
Ni3+![]() Ni4+��Co3+
Ni4+��Co3+![]() Co4+����֤�˵�ؾ��нϸߵı�������
Co4+����֤�˵�ؾ��нϸߵı�������
2.3.3 ��������
Ϊ����LiNi1/3Co1/3Mn1/3O2���ϵı��ʷŵ����ܣ��Ƚ�ʵ������0.2C���������4.3 V��Ȼ�ֱ���0.2C��0.4C��0.8C��1.6C��2.0C�����ܶȺ����ŵ���2.75 V��1C��������150 mA��h��g-1��ΪLiNi1/3Co1/3Mn1/3O2���ϵ�������������ó��ġ�ͼ6��ʾΪ��940 ���ս�12 h���Ʊ���ƷD�ڲ�ͬ�����µķŵ����ߣ�0.2C��0.4C��0.8C��1.6C��2.0C�����µķŵ������ֱ�Ϊ146.3��135.2��130.1��125.8��114.7 mA��h��g-1�����0.2C�����µķŵ�������0.4C��0.8C��1.6C��2.0Cʱ�ŵ����������ʷֱ�Ϊ92%��89%��86%��78%��ͨ�������ʷŵ�������Ҫ�ܲ���ƽ�����ȵ�Ӱ�죬��ƷD��ƽ������ԼΪ10 ��m������ͼ3���Կ�����Ʒ��ĩ��������Ϊ1~2 ��m��һ��ԭ�������ž۶��ɣ���ˣ������Ա��������ı��ʷŵ����ܣ�����T.H. Cho��[8]�������Ľ��һ�¡�
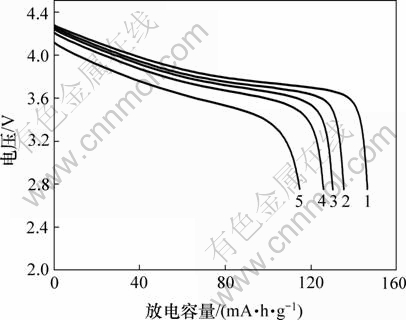
1��0.2C��2��0.4C��3��0.8C��4��1.6C��5��2.0C
ͼ6 �ڲ�ͬ��������ƷD�ķŵ�����
Fig.6 Discharge curves of sample D at different rates
2.3.4 ѭ������
ͼ7��ʾΪ��ƷD��0.2C��ŵ��ǰ30��ѭ��ͼ���ɼ�����ǰ8��ѭ�������г�ŵ��������²���������Ҫ�dz�ŵ�����е缫���滺����Ĥ�����������ȶ����£��Ե�9��ѭ���𣬲��ϳ�ŵ����������ȶ��������״ηŵ�����Ϊ146.3 mA��h��g-1������30��ѭ�������Ϸŵ���������143.3 mA��h��g-1������������Ϊ98%��ѭ�������Ըߡ�
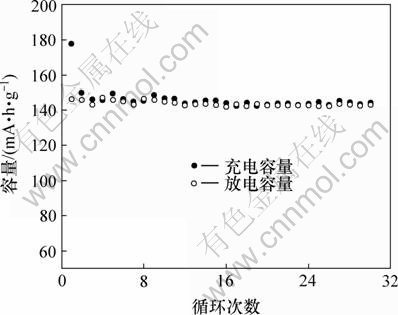
ͼ7 ��ƷD��2.75~4.3 V��ѹ������0.2C��ŵ��ǰ30��ѭ��ͼ
Fig.7 Cycling performance for sample D up to 30 cycles at 0.2C rate in the voltage range of 2.75-4.3 V
3 �� ��
a. ����е�����ǰ���壬ͨ�����෨�ϳ��˵���������״LiNi1/3Co1/3Mn1/3O2�������ϡ������ս��¶����ߺ��ս�ʱ���ӳ������ϵľ���Խ����������״�ṹ����Խ���ԡ���940 ��/12 h�������Ʊ�����Ʒ���ͺã���ò������ƽ������ԼΪ10 ��m��
b. ��2.75~4.3 V��ѹ���䣬���Ʊ���LiNi1/3Co1/3- Mn1/3O2����������0.2C���к������ŵ磬�״ηŵ�������146.3 mA��h��g-1��������LiCoO2�ĵ������൱����0.4C��0.8C��1.6C�� 2.0C���к�����ŵ磬�ŵ������ֱ�Ϊ135.2��130.1��125.8��114.7 mA��h��g-1�����ʷŵ�����������0.2C�����¾���30��ѭ�������Ϸŵ����������������ʷֱ�Ϊ143.3 mA��h��g-1��98%��ѭ�������Ըߡ�
c. ���ô����෨�����ռ��ɿ��Ըߣ����Ʊ��IJ���������������Ŀǰ����LiCoO2����������Ʒ���ʺϽ��в�ҵ���ƹ㡣
�ο����ף�
[1] Randolph A L, Marcus J P, Esther S T, et al. A study of the overcharge reaction of lithium-ion batteries[J]. Journal of Power Sources, 2001, 97/98: 681-683.
[2] Tobishima S, Takei K, Sakurai Y, et al. Lithium ion cell safety[J]. Journal of Power Sources, 2000, 90(2): 188-195.
[3] �� ��, �� �, �� ӱ, ��. ����ӵ���������ϵ��о���չ[J]. ���ܲ���, 2004, 35(6): 667-671.
HE Hui, CHENG Xuan, ZHANG Yin, et al. Recent progress in cathode materials for Li-ion batteries[J]. Functional Materials, 2004, 35(6): 667-671.
[4] ������, ��Ծ��, ������. ���ù�����λ���Ʊ���ϸLiMn2O4��������[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2005, 36(3): 390-395.
CHEN Li-bao, HU Yue-hui, TANG Yi-wu. Preparation of ultrafine LiMn2O4 cathode materials by solid state coordination method[J]. J Cent South Univ: Science and Technology, 2005, 36(3): 390-395.
[5] Ohzuku T, Makimura Y. Novel lithium insertion material of LiNi1/3Co1/3Mn1/3O2 for advanced lithium-ion batteries[J]. Journal of Power Sources, 2003, 119/121: 171-174.
[6] Jung-Min K, Hoon-Taek C. Role of transition metals in layered Li[Ni,Co,Mn]O2 under electrochemical operation[J]. Electro- chimica Acta, 2004, 49(21): 3573-3580.
[7] Whitfield P S, Avidson I J, Cranswick L M D, et al. Investigation of possible superstructure and cation disorder in the lithium battery cathode material LiMn1/3Ni1/3Co1/3O2 using neutron and anomalous dispersion powder diffraction[J].Solid State Ionics, 2005, 176(5/6): 463-471.
[8] Cho T H, Park S M, Yoshio M, et al. Effect of synthesis condition on the structural and electrochemical properties of LiNi1/3Co1/3Mn1/3O2 prepared by carbonate co-precipitation method[J]. Journal of Power Sources, 2005,142: 306-312.
[9] LI De-cheng, Sasaki Y, Kageyama M, et al. Structure, morphology and electrochemical properties of LiNi0.5Mn0.5-xCoxO2 prepared by solid state reaction[J]. Journal of Power Sources, 2005, 148: 85-89.
[10] Seung-Taek M, Myung-Hun L, Shinichi K, et al. Hydrothermal synthesis of layered Li[Ni1/3Co1/3Mn1/3]O2 as positive electrode material for lithium secondary battery[J]. Electrochimica Acta, 2005, 50(24): 4800-4806.
[11] Todorov Y M, Numata K. Effects of the Li:(Mn+Co+Ni) molar ratio on the electrochemical properties of LiMn1/3Co1/3Ni1/3O2 cathode material[J].Electrochimica Acta, 2004, 50(2/3): 495-499.
[12] �� ��, �� ��. ��������������ӵ���е�Ӧ��[J]. ��Դ����, 1997, 21(3): 120-126.
XIA Xi, LIU Ling. Application of manganese dioxide in lithium ion batteries[J]. Chinese Journal of Power Sources, 1997, 21(3): 120-126.
[13] Kosova N V, Devyatkina E T, Kozlova S G. Mechanochemical way for preparation of disordered lithium-manganese spinel compounds[J]. Journal of Power Sources, 2001, 97/98: 406-411.
[14] Albrecht S, K��mpers J, Kruft M, Malcus S, et al. Electrochemical and thermal behavior of aluminum-and magnesium-doped spherical lithium nickel cobalt mixed oxides Li1-x(Ni1-y-zCoyMz)O2 (M=Al, Mg)[J]. Journal of Power Sources, 2003, 119/121: 178-183.
[15] Τ���, ������, �� ��, ��. ��״LiCo1/3Ni1/3Mn1/3O2�������ϵĺϳɼ��绯ѧ�����о�[J]. ����ѧѧ��, 2005, 21(7): 999-1003.
WEI Ni-ni, LAI Qiong-yu, GAO Yuan, et al. Synthesis and electrochemical characterization of layered LiCo1/3Ni1/3Mn1/3O2 cathode material[J]. Chinese Journal of Inorganic Chemistry, 2005, 21(7): 999-1003.
[16] ������, ����, ����ӡ, ��. ����ӵ����LixCo0.8Ni0.2O2[J]. ���ܲ���, 2001, 32(1): 59-61.
LI Yang-xing, WANG Chun-rong, JIAN Chang-yin, et al. Cathode material of LixCo0.8Ni0.2O2 for lithium-ion battery[J]. Functional Materials, 2001, 32(1): 59-61.
[17] Kosova N V, Devyatkina E T, Kaichev V V. Optimization of Ni2+/Ni3+ ration in layered Li(Ni, Mn, Co)O2 cathodes for better electrochemistry[J]. Journal of Power Sources, 2007, 174(2): 965-969.
[18] Paulsen J M, Thomas C L, Dahn J R. O2 structure Li2/3[Ni1/3Mn2/3]O2: a new layered cathode material for rechargeable lithium batteries: I. Electrochemical properties[J]. J Electrchem Soc, 2000, 147: 861-868.
[19] Shaju K M, Subba-Rao G V, Chowdari B V R. Performance of layered Li(Ni1/3Co1/3Mn1/3)O2 as cathode for Li-ion batteries[J]. Electrochimica Acta, 2002, 48(2): 145-151.
[20] Yasuhiro F, Hiroshi M, Naoto S, et al. Structural and electrochemical properties of LiCo1/3Ni1/3Mn1/3O2: Calcination temperature dependence[J]. Journal of Power Sources, 2007, 171(2): 894-903.
[21] �� ��, �� �, �� ӱ, ��. �ϳ����ն�LiNi0.75Co0.25O2���ܵ�Ӱ��[J]. ��Դ����, 2005, 29(2): 75-77.
HE Hui, CHENG Xuan, ZHANG Yin, et al. Influence of sintering atmosphere on the performance of LiNi0.75Co0.25O2 cathode materials for lithium ion batteries[J]. Chinese Journal Power Sources, 2005, 29(2): 75-77.
�ո����ڣ�2007-06-19�������ڣ�2007-08-20
������Ŀ���������ߵ�ѧУ�Ǹɽ�ʦ����������Ŀ(2000��)
ͨ�����ߣ�����(1964-)���У�������ˮ���ˣ����ڣ�������������ӵ�ز����о����绰��0731-8830785��E-mail��ycsu@mail.csu.edu.cn
[3] �� ��, �� �, �� ӱ, ��. ����ӵ���������ϵ��о���չ[J]. ���ܲ���, 2004, 35(6): 667-671.
[12] �� ��, �� ��. ��������������ӵ���е�Ӧ��[J]. ��Դ����, 1997, 21(3): 120-126.
[16] ������, ����, ����ӡ, ��. ����ӵ����LixCo0.8Ni0.2O2[J]. ���ܲ���, 2001, 32(1): 59-61.
[21] �� ��, �� �, �� ӱ, ��. �ϳ����ն�LiNi0.75Co0.25O2���ܵ�Ӱ��[J]. ��Դ����, 2005, 29(2): 75-77.


