ϡ��������Ը�������ȷֽ�����ü�����
�ϲ���ѧϡ�����ɹ��ܲ����о�����,�ϲ���ѧϡ�����ɹ��ܲ����о�����,�ϲ���ѧϡ�����ɹ��ܲ����о�����,�ϲ���ѧϡ�����ɹ��ܲ����о�����,�ϲ���ѧϡ�����ɹ��ܲ����о����� �����ϲ�330047,�����ϲ�330047,�����ϲ�330047,�����ϲ�330047,�����ϲ�330047
ժ Ҫ��
���ò����������̼����麟��������Ҷ����ܽ��������Ʊ��˶���ϡ��������, �ò��ȷ��������Ƚ��˲�ͬϡ��������Ը�������ȷֽ�Ĵ����á��������:����ϡ�����������ʹ������淋ĵ�һ���ȷ��ͺ�, ���ڶ����ȷֽ����ǰ;����ϡ��������������, ���ֽ������, ���պϲ�Ϊһ���ֽ���ȷ�, �ֽ���Ҳ�����ߡ���ͬϡ������������Ը�������ȷֽ�Ĵ�������һ���IJ���, ��ϡ������ϵ�������ʹ�ֽ�����Ϊǰ����ǿ�����������ķ�, ��ϡ���̺��ŵ����������Ϊ��һ��ǿ��, ����ϡ�����������������Ϊǰǿ���������������ķ��ȷ塣����ͬһ��ϡ��������, �Ʊ������IJ�ͬ�Դ�������淋��ȷֽ�Ҳ�в���, �������ıȱ�����й�, ���Ų���ȱ����������, ��Ч��Խ���ԡ����ܴ����۽���������ϡ����AP�ȷֽ���̵�Ӱ��, ������ϡ����Ϊ�뵼��������, �����������Ǵ�����ͷŵ��ӵĹ������ʵ�����AP��һ�ֽ����ͺ�͵ڶ��ֽ�����ǰ��
�ؼ��ʣ�
��ͼ����ţ� O611.3
����飺������ (E-mail:yxli@ncu.edu.cn) ;
�ո����ڣ�2006-10-11
����������Ȼ��ѧ���� (59764001, 201610002);����ʡ�������ص���Ŀ (2006) ����;
Role and Mechanism of Rare Earth Oxides in Decomposition of Ammonium Perchlorate
Abstract��
Various rare earth oxides were synthesized respectively by precipitation with oxalate acid, ammonium bicarbonate as well as glycol sol-gel methods.Their catalytic effects on the decomposition of ammonium perchlorate (AP) were studied using differential thermal analysis (DTA) techniques.It can be seen from their DTA curves that the addition of rare earth oxides could make the first exothermal peak of ammonium perchlorate hysteresised and the second exothermal peak advanced.With the addition amount of rare earth oxide increasing, the two exothermal peaks of AP came closer and finally merge into one strong peak with a great increase of decomposition heat.The catalyzing action caused by different rare earth oxides was different.Two adjacent exothermal peaks with former weak and later strong were observed in the DTA curves of AP mixed with 5% lighter rare earth oxides Pr6O11 or Nd2O3, one strong peak for middle rare earth oxides Sm2O3 or Gd2O3, and two separated peaks with former strong and later weak for heavier rare earth oxides Er2O3 or Yb2O3.Difference also existed among the Gd2O3 powders prepared by different methods, which was attributed to the difference of their specific surface area.The catalytic activity of oxides increased with their specific surface area increasing.The effect of rare earth oxides on the thermal decomposition of AP was explained by energy band theory.Rare earth oxides can be considered as typical semiconductors.It was their functional property of storing and releasing electron that resulted in the hysteresising of first exothermal peak or advancing of the second exothermal peak.
Keyword��
rare earth oxide;ammonium perchlorate;catalytic thermal decomposition;
Received�� 2006-10-11
������� (AP) �Ǹ��Ϲ����ƽ������õ�������, �����ȷֽ����ܶԹ����ƽ�����ȼ�չ����кܴ��Ӱ�졣 Ϊ�����AP���ƽ�Ч��, ������������ȷֽչ�˹㷺�о�, �����Ǹ������Ӽ���AP�ȷֽ���̵�Ӱ��
1 ʵ ��
1.1 ϡ����������Ʊ�
���������: �ֱ�ȡ1 g Sm, Yb, Nd, Pr, Er, Gd 6��ϡ��������, ���ձ��м���10 ml�����ܽ�, ���50 ml����Һ�� �ڼ��������¼��뺬2 g���������Һ, ��ֽ���, ʹϡ����ȫ������ �»�2 h�����, �õ�����ϡ�������� ����������������, ������¯��800 ��������1 h, ��ȴ��ȡ��, �õ���Ӧ��ϡ������� ������Ϊ[C]��
̼����麟�����: �ο�����
�Ҷ����ܽ�-������
1.2 DTA����
ȡ��AP, ��һ��������ϡ���������������麟����ĥ�õ�AP��ϡ��������Ļ��� �� (CDR-4P, �Ϻ����ܿ�ѧ��������˾) �ȷ����ǶԻ��������ȷֽ�ʵ��, ������3 mg, �ھ�̬������������10 �桤min-1�������ٶȼ���, ��ʼ�¶�Ϊ30 ��, ��ֹ�¶�Ϊ600 �档
2 ���������
2.1 �����ŵĶԸ�������ȷֽ��Ӱ��
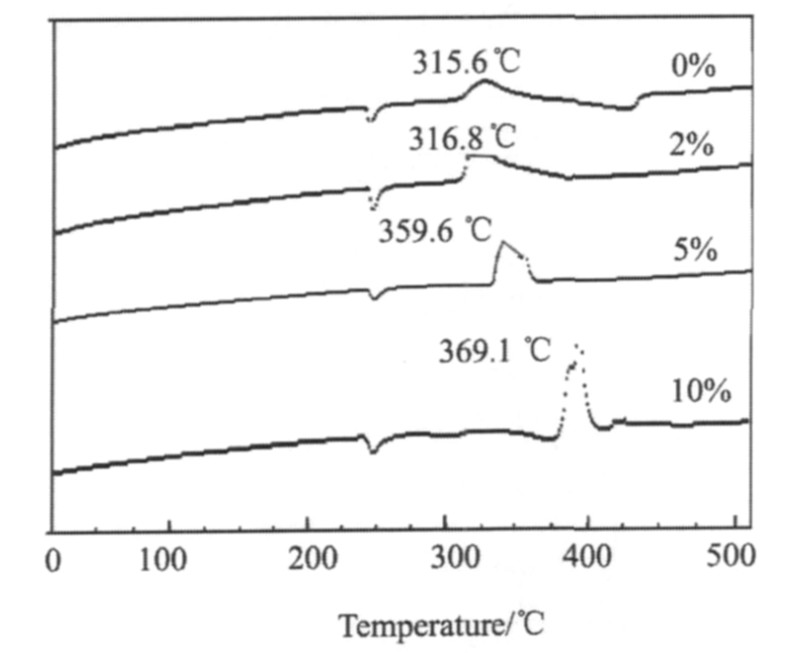
ͼ1Ϊ���в�ͬ�������Ҷ����ܽ�-�������Ƶõ������ŵĸ�����淋�DTA���߱Ƚϡ� ��1�жԱ��г���AP������������ź��DTA���ݽ���� �ڴ�������淋�DTA�����Ͽ��Թ۲쵽һ�����ȷ���������ȷ�, ���ȷ�ķ�ֵ�¶�Ϊ242 ��, ��Ӧ��AP����ת�䡣 �������ȷ�ķ��·ֱ�λ��315.6��412 ��, ��Ӧ��AP�������ȷֽ���̡� ���е�һ���ȷ����ЧӦ��, ���ڶ����ȷ����ЧӦС��
ͼ1 ���в�ͬ�������Ҷ����ܽ�-�������Ƶõ������ŵĸ�����淋�DTA���߱Ƚ�
Fig.1 Comparison of DTA curves of AP doped with different amounts of Gd2O3 prepared by glycol sol-gel method
ͼ1�������: �����ŵļ�������Ӱ����AP���ȷֽ����, �������ż���������, Ӱ��Խ�� ������Ϊ2%ʱ, ��һ���ȷ�ķ����������, ����ǿ��������ǿ, ͬʱ, �ڶ����ȷ弸���������� ��������ߵ�5%ʱ, ��һ���ȷ�ķ����нϴ���ȵ����, �ɴ�AP��315.6 �����ߵ�359.6 ��, ��ǿ���봿AP�����Ҳ�д����ߡ� ���ͬʱ, �ڸ÷���������һ������ķ��ȷ�, ��ֵ�¶���369 �档 ���������ż����������ӵ�10%, ��һ���ȷ�ķ��¼�������, ��369.1 ��, ǿ��Ҳ��������, ����������һ����ǿ�ķ��ȷ�, ����Ϊ369 ��, �������һ���ȷ��غϡ�
������ʵ˵��: �����ŵļ����������ı�AP���ȷֽ���̺ʹ����߷ֽⷴӦ����ЧӦ�� ����ϡ������������ӱ���Խ��, Ӱ��Խ������ ��ֱ�ӵĽ���������AP�ķֽ��Ⱥ���ʼ�ֽ��¶ȡ� ʹ������������Խ����ķ��ȷ�����������տ��Ժϲ���һ���dz�ǿ�ķ��ȷ塣 ������AP�ı�ը����ʹ�ð�ȫ����ʮ�������ġ�
2.2 �����ŵ��Ʊ�������AP�ȷֽ��Ӱ��
�Ӵ����õ��ص�����, ϡ���������������什Ӵ�Խ��, ���Ч��Ҳ��Խ�á� ���, ǿ����������AP֮�����Ӵ������AP�ȱ�ը������Ч������ ����ǰ��һЩ�о���Ҳ��֤�������Ӽ��ıȱ��������ֽ�����֮��������ȹ�ϵ�� Ϊ��, ���Ƿֱ�Ƚ���3�ֲ�ͬ�����Ʊ�����������5%�IJ�����ʱ��AP�ȷֽ����ܵ�Ӱ��, ���Ҳ�����1�С� �������: 3�ַ����Ʊ��������Ŷ�AP�Ĵ��ȷֽ�Ч�����ܺ�, ����Ȼ���ֳ����ԵIJ��졣 ���Ҷ����ܽ��������Ʊ���Gd2O3�ıȱ������ (����50 m2��g-1) , �������ȷֽ�Ч��Ҳ����õ�, �ܹ�ʹ������淋ĸ��·��ȷ����ʼ�¶Ƚ������ (354.5 ��) �� ̼����麟������Ʊ��������ŵıȱ������5��6 m2��g-1, ���ò���������Ʊ���Gd2O3�ıȱ������1 m2��g-1���ҡ� ���Ǵ�AP�ֽ�ķ��ȷ��¶ȷֱ�Ϊ356.5��361.6 �档 ��ǿ����¶ȴ�С���������Ƕ�Ӧ�ıȱ����С�����෴, ֤�����������ıȱ�����������AP���ȱ�ը��, ��������ֱ�ӵ����Թ�ϵ�� ˵�������õIJ�����Ҫ��Դ����Ʒ�����������, ��β������ǵı������С��
��1������識��京ϡ����������ƷDTA��������估�ȷֽ����¶ȱȽ�
Table 1Comparison of temperature of phase transformation and thermal decomposition peak on DTA curves of AP and its mixtures with rare earth oxides
| Samples | Phase trans- formation/�� |
First exothermal peak/�� |
The second exothermal peak/�� |
| AP | 241.5 | 315.6 | |
| 2%Gd2O3[Y]+AP | 244.5 | 316.8 | |
| 5%Gd2O3[Y]+AP | 247.8 | 337.8 | 359.6 |
| 10%Gd2O3[Y]+AP | 247.3 | 346.6 | 369.1 |
| 5%Gd2O3[C]+AP | 242.4 | 361.6 | |
| 5%Gd2O3[Y]+AP | 240.9 | 354.5 | |
| 5%Gd2O3[T]+AP | 241.3 | 356.5 | |
| 5%Pr6O11[C]+AP | 242.5 | 362.8 | |
| 5%Nd2O3[C]+AP | 240.6 | 333.1 | 366.3 |
| 5%Sm2O3[C]+AP | 241.0 | 367.8 | |
| 5%Er2O3[C]+AP | 241.1 | 348.1 | 358.8 |
| 5%Yb2O3[C]+AP | 239.1 | 332.0 | 364.0 |
* ����[Y], [T], [C]�ֱ��ʾΪ���Ҷ����ܽ�-�������� ̼����麟������Ͳ���������Ʊ��IJ���
2.3 ϡ�������������AP�ȷֽ����ܵ�Ӱ��
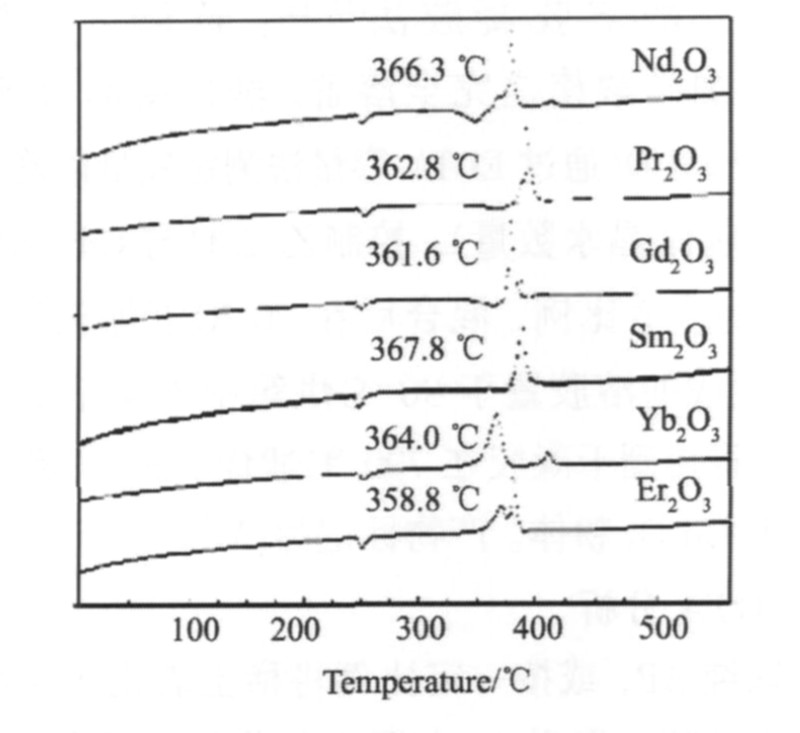
���ò���������ֱ��Ʊ����ᡢ �С� ��ϡ������� ����5%��������AP���, �ֱ����DTA����, �����ͼ2�� ��ͼ2��֪, ����ϡ���������AP���ȷֽ���̶���������Ӱ��, �ܺܺõش�AP���ȷֽ�, ��Ҳ����һ���IJ��졣 ��������Ϊ5%�������, ��ϡ������ϵ�������ʹAP�ķֽ�����Ϊǰ����ǿ�����������ķ�, ��ϡ���̺��ŵ���������ʹAP�ķֽ��Ϊ��һ��ǿ��, ������ϡ�������������������, AP�ķֽ��Ϊǰǿ���������������ķ��ȷ塣
ͼ2 ����5%��ͬϡ���������AP��DTA����
Fig.2 DTA curves of AP mixed with 5% different rare earth oxides
2.4 ���������
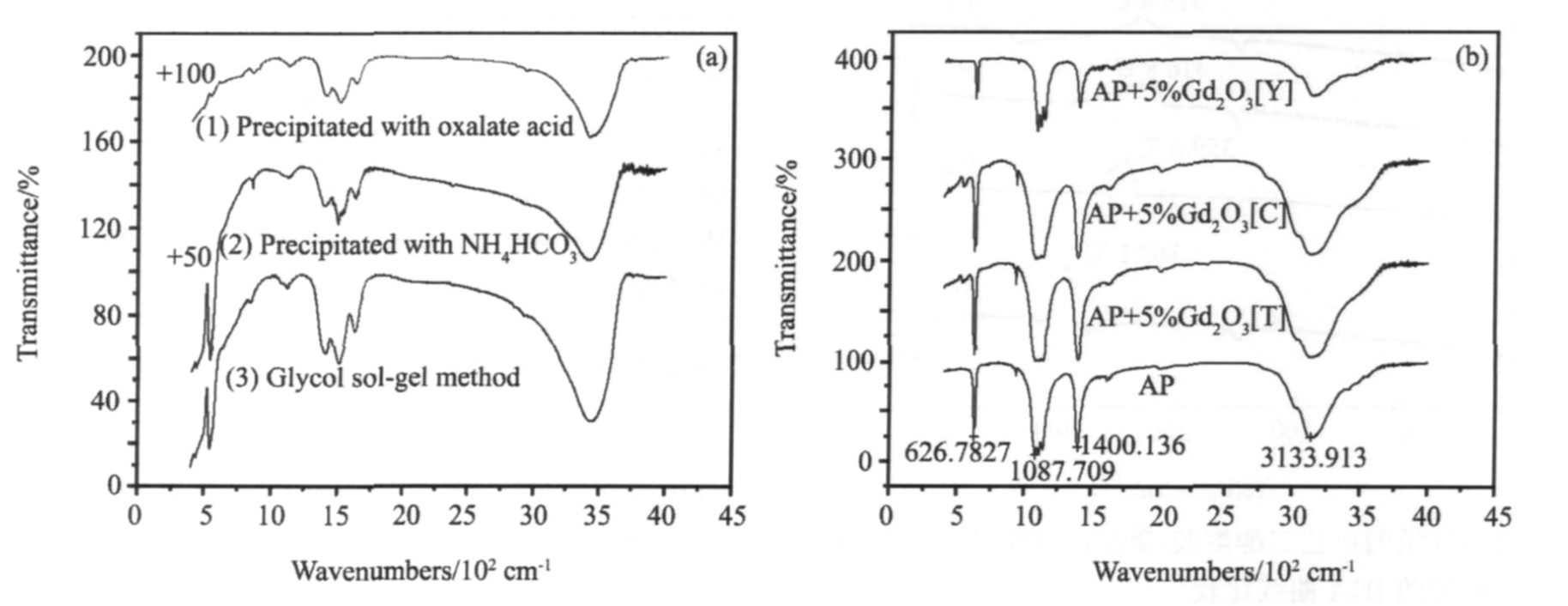
ͼ3Ϊ��ͬ�����Ʊ��������š� AP������5%�������Ż�Ϻ�ĺ������ͼ�Ƚϡ� �������: �ɲ�ͬ�����Ʊ��������ŵĺ�������и����շ��λ�û���һ��, �����ǿ���������IJ�� ����������542 cm-1����Gd-O������ǿ�����, ���Ų���ȱ����������, ��ˮ���Ӻ�̼�����ص����ǿ�ȴ����ǿ, ˵�����Ƕ�ˮ�Ͷ�����̼������������ǿ�� �봿AP�ĺ���������, ���������ŵ�AP�ĺ������շ�λ�ñ仯���� (��2) , ����: NH4+��3133 cm-1�������������շ��ڻ������Ҳ����������һλ��, ֻ������߱ȱ��������Ż�Ϻ���м��������ļ��١�
ͼ3 3�ֲ�ͬ�Ʊ�������Gd2O3 (a) , AP����AP��5%Gd2O3����� (b) �ĺ������ͼ
Fig.3 IR spectra of Gd2O3 powders prepared by three different methods (a) , AP and its mixtures with 5%Gd2O3 powders (b)
��2 Gd2O3, AP����AP��5%Gd2O3�����ĺ���������ݱȽ� (cm-1)
Table 2 Comparison of IR data (cm-1) of Gd2O3, AP and mixture of AP+Gd2O3
| AP | Gd2O3 | AP+5%Gd2O3[T] | AP+5%Gd2O3[C] | AP+5%Gd2O3[Y] |
| 3445.5 | ||||
| 3133.3 (NH4+��3) | 3133.7 | 3134.3 | 3126.2 | |
| 1615 | 1631.5 | 1633.8 | 1629.3 | 1633.8 |
| 1508.1 | ||||
| 11395.3; 1400.7 (NH4+��4) | 1404.4 | 1401.8 (1396-1408) | 1401.7 (1396-1408) | 1409.3 (1392-1413) |
| 1141.7; 1110.9; 1087.7 (ClO4, ��3) | 1139.8; 1110.8; 1089.8 | 1139.8; 1110.8; 1089.2 | 1141.4; 1114.7; 1089.6 | |
| 1121.6 | ||||
| 939.6 (ClO4, ��3) | 940.4 | 940.1 | 940.3 | |
| 856.1 | ||||
| 636.0 | 635.6��627.5 | 636.4��627.5 | 627.8��636.4 | |
| 542.1 (��Gd-O) | 540.6 | 542.0 | 543.9 |
˵���ڻ��������������AP֮����Ȼ��Щ��ѧ�����, �������ԡ� ��������
2.5 ϡ���������AP�ȷֽ�Ĵ����û���
����AP�ȷֽ�Ļ������й㷺���о�, ����û�дﵽһ�µ���ʶ�� ��Ҫ����������Ĺ۵�, ��: ����ת�ƻ��ƺ͵��Ӵ��ݻ��ơ� ��ֽ�����еļ�����Ҫ��ӦΪ:
[3] ����Cl-O���Ķ��Ѷ�����ClO4-���ȷֽ�
ʵ����, �ھ�����ȷֽ������, ���ֻ��ƶ��п��ܷ���, ֻ���ڲ�ͬ�ij���, �䷢������������Գ̶Ȳ�ͬ���ѡ� ���, Ҫ��������������, ������Ϊ����ת�Ƶ����ƶ����Ӵ��ݵĴ���, ����Ϊ���Ӵ��ݵ���Ҫ���ö��ڸ�����ת�ƵĴ��ڡ� �ھ����������, ���Dz����ֱ�ӻ�ѧ�ź����������������ʶijһ��Ӧ��ϵ�Ĺ��̻��ơ�
AP���ȷֽ�һ����Ϊ��һ�ֹ�-�����෴Ӧ, ��������������Ĺ���:
NH4ClO4=NH3 (����̬) +HClO4 (����̬) =
NH3 (��̬) +HClO4 (��̬)
AP�ķֽ�������º͵����ȷֽ�������Ҫ��, ������ȷֽ����Ҫ�ǹ�-�����෴Ӧ, ���ʵ��¶��·������������, ���������NH3��HClO4���ŷ���ϵ�з�Ӧ, ������N2O, O2, Cl2, H2O��������NO; AP�ĸ��·ֽ����Ҫ�����෴Ӧ, ������NO, O2, Cl2��H2O�ȡ�
����
ϡ�������������Ӧ��������������, �����백����λ����, ����ˮ���ӵĽ��������ǿ�� ���, �ӻ�ѧ����õĽǶ�����, Ӧ�ôӷֽ������ȶ�����˵���� ����ϡ��Ԫ�������4f���Ӳ�ṹ�Ͷ���۵��ӹ��, �ܹ��γ���d������Ԫ�ز�ͬ�������������, ���ر�������H2O�γ������[RE (H2O) n]3+�� ClO4-����Ϊ����λ��������������, ���, [RE (ClO4) n]3+�������γ�����Ӧ�ú�С, ��AP�ֽⷴӦ��Ӱ��Ҳ���Ժ��ԡ� ��AP�ķֽⷴӦʽ���Կ���, AP�ĸ��º͵����ȷֽⷴӦ���д�����H2O����, �dz������������[RE (H2O) n]3+���γɡ� ��Ҫ����ϡ��������������λ����, ��ô, ��AP�ĸ�����������������, ��������̬HClO4������ϡ�������γ������[RE (ClO4) n]3+, ����ʹ��Ӧ���١� ����, ϡ���������AP�ĵ��·ֽ����谭����, ���Ը����ȷֽⷴӦ�д����á� ��һ���뱾�ĵĽ������ϡ�
������ͬϡ��Ԫ�صĴ����ܲ�����������ļ���û��ֱ�ӵĹ�ϵ, Ҳ��ϡ���������ˮ����������û��ֱ�ӵĹ�ϵ�� ���, ����ϡ����AP�ķֽ����������ת�ƻ��Ƶ�����Բ��� ���º����������Ҳ����ϡ����������֮��Ļ�ѧ���ò����ԡ� ����, �����ӻ�ѧ����õĹ۵㲻����ȫ���ͱ��ĵ�ʵ������
���ɽ����������AP�Ĵ��ֽ���Ҫ��ͨ��������ԭѭ���м��ٵ���ת�ƶ�ʹAP��ǰ�ֽ�
��������
���������õĵ���, �Ӵٽ����Ӵ��ݵ���������Ҫ�������ڰ뵼�����ʵĽ�������� ����ʵ��������, ��AP�ĵ��·ֽ��, ���Ӵ�������Ϊ���ٶȿ��Ʋ���, ����˵��������ڲ�����֮��ĵ��Ӵ�������ֱ����ɶ�����Ҫͨ���������塣 �෴, ��Щ����Ĵ��ڻ��ɢ�����ڵĵ��Ӵ���, ʹ���·ֽ��¶�����, ��Ӧ�ͺ� ������Щ��ɢ�ڵ����ϵĵ��ӿ���Ϊ�����ֽⷴӦ�ṩ����֧��, ����ʹAP�ĸ��·ֽⷴӦ��ǰ����, �������ԵĴ����á� ���Ӽ��Ŀ���Խϸ, ��AP�Ӵ��ı����Խ��, ת�Ƶ��Ӻ��ͷŵ��ӵ�����ҲԽǿ, ʹ���·ֽ���¶����ߺ��·ֽ��Ľ��ͷ�������, ���ʹ�����ֽ��ϲ�Ϊһ���塣 ��һЧ���뱾��ϡ���������Ч�����ơ� ����ϡ���������뵼�廯����ͬ�����ԶԼ��ȹ�����AP�����ڵĵ����桢 ת�ƺͼ����ͷ����á� �����ܴ�����, ����ϡ�������ȹ�����, �䴦�ڼ۴��ϵĵ��ӿ��Ա��ȼ�����ԾǨ��������, ʵ�ֵ������Ѩ�ķ���, ͬʱ, AP�����ڲ��ĵ���Ҳ����Ǩ�Ƶ�ϡ����������, �����䵼��, ������ӵ�����, ������AP�ֽⷴӦ���̵ĵ���ת�ƽ���, ʹ���·ֽ���¶����ߡ� �����¶ȵĽ�һ������, ���������˶��ٶȵļӿ�����������, ��϶�ܽ��͡� �����͵�һ���̶Ⱥ�, �����ϴ���ĵ��ӽ������ͷų���, �������ٽ�AP�ĸ��·ֽⷴӦ, ʹ���·ֽ���¶����Խ���, ���������Ĵ����á�
3 �� ��
���ò��ȷ��������о���ϡ��������Ը������ (AP) �ȷֽ����ܵ�Ӱ�졣 �������: ��AP�м���ϡ��������, ����ʹAP�ĵ��·ֽ���¶�����, �����·ֽ���¶��½��� ����ı���Խ��, �Ը�����淋��ȷֽ��Ч��Խ��, ���տɺϲ�Ϊһ��ǿ�ķ��ȷ塣 ���, ϡ��������ļ��벻�������ʹ�ú���������еİ�ȫ��, ���Ҵ������˸�����淋ķֽ��ȡ� ��ͬϡ������������Ը�������ȷֽ�Ĵ�������һ���IJ��졣 ��5%�������������, ��ϡ������ϵ�������ʹ�ֽ�����Ϊǰ����ǿ�����������ķ�, ��ϡ���̺��ŵ����������Ϊ��һ��ǿ��, ����ϡ�����������������Ϊǰǿ���������������ķ��ȷ塣 ϡ���������AP�ȷֽ����ܵ�Ӱ��ͻ��ƿ����ð뵼���ܴ����������͡� ��ϡ�������������¹����жԵ��ӵĴ����뼯���ͷŹ��ܵ��������Ƕ�AP���·ֽⷴӦ���谭���·ֽⷴӦ��ǿ�����á�
�����
[4] Boldyrev V V.Thermal decomposition of ammonium perchlorate[J].Thermochimica Acta, 2006, 443:1.
[8] ����, ����Ӣ, �����, ������, ����ѫ.����������Ժ������ȷֽ�Ĵ�����[J].�ƽ�����, 2002, 23 (4) :329.
[9] ������, �����, ̸�Ừ, ����, ����.�������۶Ը�������ȷֽ����Ե�Ӱ��[J].Ӧ�û�ѧ, 2004, 21 (5) :488.
[10] �°���, �����, ����Ҷ, ����.��ϸTMO���ϴ����Ը�������ȷֽ��Ӱ��[J].���ܲ���, 2004, 12 (6) :321.
[12] ������, ��ƽ��, ��С��.̼��ϡ���ᾧ��������[P].�й�����ר��, CN1141882A, 1997.
[4] Boldyrev V V.Thermal decomposition of ammonium perchlorate[J].Thermochimica Acta, 2006, 443:1.
[8] ����, ����Ӣ, �����, ������, ����ѫ.����������Ժ������ȷֽ�Ĵ�����[J].�ƽ�����, 2002, 23 (4) :329.
[9] ������, �����, ̸�Ừ, ����, ����.�������۶Ը�������ȷֽ����Ե�Ӱ��[J].Ӧ�û�ѧ, 2004, 21 (5) :488.
[10] �°���, �����, ����Ҷ, ����.��ϸTMO���ϴ����Ը�������ȷֽ��Ӱ��[J].���ܲ���, 2004, 12 (6) :321.
[12] ������, ��ƽ��, ��С��.̼��ϡ���ᾧ��������[P].�й�����ר��, CN1141882A, 1997.