DOI�� 10.11817/j.issn.1672-7207.2019.10.003
��ϸ�������Ƶ��Ʊ������ȵ���
����,��ϲ��,�����,���,ʯ����
�����ϴ�ѧ ұ���뻷��ѧԺ������ ��ɳ��410083��
ժ Ҫ��
>2O3Ϊԭ�ϣ���������������Ʊ���ϸ�������ơ�����X��������(XRD)��ɨ���������(SEM)�ͼ������ȷ����Խ������ƵĽṹ����ò�����Ƚ��б��������Խ������Ƴɷֽ��з������о������ٶȡ���ʯ��(C4H6O6)���Ȼ���(NaCl)�����Լ�������Ӧʱ��Խ����������ȵ�Ӱ�졣�о�����������ڽ����μ����ʯ�ὫSb2O3�ܽ������������ڼ��������������������ƽ������ƿ����ij����ٶȣ��������ȴ�39.62 ��m����2.61 ��m����ò���ķ�ת��Ϊ���ο������������ƾ����������ڳ���-�̬ܽƽ�⡣�ڽ����ٶ�Ϊ400 r/min�����ʵ����ȼ�n(C4H6O6):n(NaCl):n(Sb2O3)=5:12:1��������Ӧʱ��Ϊ120 min�������£��ɵõ�ƽ������Ϊ2 ��m���ң����������Ľ������Ʋ�Ʒ������������Ϊ49.02%�����ȴ���99%��
�ؼ���:��ϸ���壻�������ƣ���������������ȿ���
��ͼ�����:TF818 ���ױ�־��:A ���±��:1672-7207��2019��10-2352-08
Preparation and particle size control of ultrafine sodium pyroantimonate
CAO��Sheng, YANG��Xiyun, LI��Jishen, XU��Hui, SHI��Xichang
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Ultrafine sodium pyroantimonate was prepared by combination of complexing and oxidation method with Sb2O3 as raw material. The structure, morphology and particle size of sodium pyroantimonate were characterized by using X-ray diffraction(XRD), scanning electron microscopy(SEM) and laser particle size analysis. The composition of sodium pyroantimonate was analyzed. The effects of stirring rate, amount of tartaric acid and sodium chloride, pulping time on the particle size of sodium pyroantimonate were studied. The results show that the addition of tartaric acid in the pulping stage can dissolve antimony trioxide and get a Sb-complexing solution. The growth rate of sodium pyroantimonate is greatly inhibited by oxidation of this solution in an alkaline medium with the size decreasing from 39.62 ��m to 2.61 ��m and morphology changing from square to sphere. The growth process of sodium pyroantimonate presents a precipitation and dissolution equilibrium. Under the conditions of stirring rate of 400 r/min, n(C4H6O6):n(NaCl):n(Sb2O3)=5:12:1, pulping reaction time of 120 min, sodium pyroantimonate crystal is obtained with a size of 2.0 ��m antimony mass fraction of 49.02% and purity greater than 99%.
Key words: ultrafine; sodium pyroantimonate; complexing-oxidation process; particle size control
�������ƣ���ɫ��ĩ������ʽΪNaSb(OH)6��Na2H2Sb2O7��4H2O[1]����������ˮ������ˮ�з���ˮ���γɽ���[2-3]���������ƾ����ȶ��Ļ�ѧ���ʺ�����ľ�Ե���ܣ����������Ʋ���ɫ�����ȣ��㷺Ӧ��������ܲ�������ѧ�����������ߵ������ij��������ɫ����������֯Ʒ��������Ʒ����ȼ���������´ɺ��մ���Ʒ������Լ�������������IJ������ϵȡ����Ž������Ƶ�������������Ҫ����ߣ��Խ������Ʋ�Ʒ����Ҳ���˸��ߵ�Ҫ��[4-10]��Ŀǰ�г��Ͻ������Ʋ�Ʒ��ƽ������Ϊ40 ��m���ң�ϸ���ȵĽ��������ڲ���Һ�в���ϸС�Ҿ��ȵ����ݣ������ڲ���Һ�и��ŵ����ݳ��������ݵ��ų�������Ч�����ѣ����ܸ����졣�������Ƶ��Ʊ������������������Ʊ���������ԭ�ϰ�����ۡ��ྫ��ͻ����[11-13]�����ྫ��ͻ����Ϊԭ���ƵõĽ������ƴ��Ƚϵͣ������ɱ��ߣ������������̡���۴��ȸߣ���ҵ�϶�ʹ�����Ϊԭ�ϣ�����˫��ˮ��������ȡ�����Ľ������ơ�Ŀǰ�������Ƶ��о��������Ʊ������Լ���Ʒ���ȿ��Ʒ��棬�йؽ������Ƶ����ȿ����о����٣���������������ֱ��Ӱ���Ʒ��ʹ�����ܡ�Ϊ�ˣ����������о���ϸ�������Ƶ��Ʊ������ȿ��ơ��Ծ�ʯ����Ȼ�����Ϊ��ϼ����ܽ���ۣ�����ڼ�����ϵ���ȶ���Sb3+�����Һ��Ȼ������������ƣ�������˫��ˮ������Sb3+�����Һ�Ʊ��������ơ�
1 ʵ��
1.1��ֱ���������Ʊ���������
����˫��ˮ�������Ʊ��������ƣ�������200 mL����ˮ��50 g�����������ĩ���ȣ������ٶȱ�����400 r/min��Ȼ�����8 mol/L NaOH��Һ93.75 mL����Ӧ������������[14]��������70 mL��������Ϊ30%��˫��ˮ�����Ʒ�Ӧ�¶�Ϊ90��C����Ӧһ��ʱ�����ˡ�ϴ�ӡ���ɵõ��������ơ�
1.2������������Ʊ���������
��������������Ʊ��������ƣ�������200 mL����ˮ��25 g�����������ĩ���ȣ������ٶȱ�����400 r/min�������������ľ�ʯ����Ȼ�����ϼ����ܽ����������࣬����ڼ�����ϵ���ȶ���Sb3+�����Һ��Ȼ�����8 mol/L NaOH��Һ155 mL����Ӧһ��ʱ�䣬����70 mL��������Ϊ30%��˫��ˮ����Sb3+�����Һ�Ʊ��������ơ�
1.3���������Ƶı��������ܼ��
����X�������� (Rigaku-TTR ����X�������ǣ�����ԴCu K��1��������=0.154 6 nm���ܵ�ѹΪ40 kV���ܵ���Ϊ250 mA ��ɨ���ٶ�Ϊ10 (��)/min������Ϊ0.02�㣬ɨ�跶ΧΪ10��~80��) ������Ʒ��������ɡ�����ɨ���������(�ձ�JEOL��˾������JSM-6360LV��ɨ��羵��������ѹΪ20 kV)�Խ������Ƶ���ò���з��������ü����������ȷ�����(MS2000��)���н����������ȵķ������ຬ������������ζ������вⶨ��̼�������ú���̼������Dzⶨ�������Ӻ������÷ֹ��ȷ��ⶨ��
2 ���������
2.1��ֱ���������Ʊ��������ƾ���������̷���
�������Ƶ��Ʊ����̷�Ϊ2���Σ�������Ӧ��������Ӧ�������������������������ƽ�����Ӧ���ټ�˫��ˮ�����õ���������(NaSb(OH)6)����������������Ϊ4 ��m���ң�����ҵ�ϵõ��Ľ������Ʋ�Ʒ����Ϊ40 ��m���ҡ�Ϊ���Ʊ���ϸ�Ľ������ƣ���������Ӧ�����в������ȵı仯���м�⡣ͼ1��ʾΪ��ͬʱ��ȡ�����ԵIJ������ȱ仯��ͼ2��ʾΪ��Ӧ�����SEMͼ����Ӧ������Ϊ���ڷ�Ӧ��ʼʱ����NaOH��Һ��90 minʱ������������Ϊ30%��˫��ˮ��Һ�������ٶ�ʼ�ձ�����400 r/min��
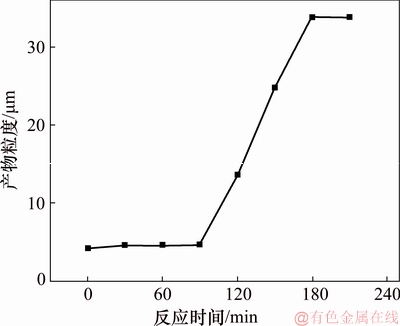
ͼ1������������ʱ��ı仯
Fig. 1��Product size change with reaction time
��ͼ1���Կ������ڽ�����Ӧ������(��Ӧǰ90 min)����������û�����Եı仯��������������ԭ�ϵ����Ȼ�����ͬ������������Ӧ������(��Ӧ90~180 min)����������Ѹ�٣���Ӧ180 min��ƽ�����Ƚӽ�40 ��m��˵�����������Ʊ����������ȵij�����Ҫ������˫��ˮ���������У�ͨ�����ƽ����������������о��������Ϳ�����Ч�ؽ��ͽ������ƵĿ���������
��ͼ2��֪������������Ϊ������Ŀ���״(ͼ2(a))���ڽ�����Ӧ�Σ�������ò�����Ա仯(ͼ2(b))������������Ӧ�Σ������������������Ϊ�����������(ͼ2(c))���Ӿ�����ò�ı仯���Կ����������������ȴִ����Ҫԭ���Ǿ�����������Ӧ�γ����ٶȿ죬���ԣ����ƽ������Ƶij����ٶ��ǵõ���ϸ��Ʒ�Ĺؼ���
2.2�������������ȵĿ���
2.2.1�������ٶȶԽ����������ȵ�Ӱ�졡
���������������������ƽ�����Ӧ30 min������˫��ˮ������Ӧ90 min�������£���������ٶȶԽ����������ȵ�Ӱ�죬������ͼ3��ʾ��

ͼ2����ͬ��Ӧʱ��ȡ����SEMͼ
Fig. 2��SEM images of products for different reaction time
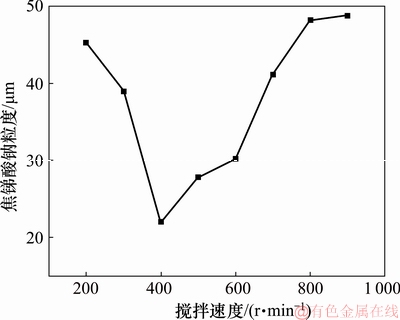
ͼ3�������ٶȶԽ����������ȵ�Ӱ��
Fig. 3��Effect of stirring rate on particle size of sodium pyroantimonate
��ͼ3��֪�����Ž����ٶȵ����������Ƶ������ȼ�С�����������ٶȴ�200 r/min����400 r/minʱ�������������ȴ�45.36 ��m����22.08 ��m�����������ٶȴ�400 r/min����800r/minʱ�������������ȴ�22.08 ��m����38.23 ��m��
�������ٶȽϵ�ʱ����������ٶ����������Ϸֲ����ȣ������������������������ž�����������Ҳ�����ܹ���Ч���ƽ��������ž���ij��������ٶȴ���400 r/min�Ҽ������������ǽ����ٶȴ���800 r/minʱ����Һ��ɽ�����Ӧ�����ϲ��������ϣ����ܶ��������Ч���裬�����γɴ�����ž����ʹ������������������ˣ�ѡ����ѽ����ٶ�Ϊ400 r/min��
2.2.2����ʯ�������Խ����������ȵ�Ӱ�졡
��ʯ������Sb3+�γ��ȶ��� [Sb2(C4H2O6)2]2-�����[15]���ڽ�����Ӧ�����У������ʯ�ᣬʹ�����������ܽ�����������ʹ�������Ƶĺϳɹ����ɹ�-Һ��Ӧת��ΪҺ-Һ��Ӧ���ﵽ�������ȵ�Ŀ�ġ��ڽ����ٶ�Ϊ400 r/min���ı��ʯ�����������첻ͬ��ʯ������������������ʵ�����(��n(��ʯ��):n(����������))�Խ����������ȵ�Ӱ�죬�����ͼ4��ʾ��
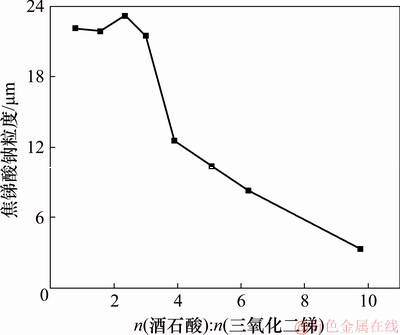
ͼ4��n(��ʯ��): n(����������)�Խ����������ȵ�Ӱ��
Fig. 4��Effect of molar ratio of tartaric acid to Sb2O3 on size of sodium pyroantimonate
��ͼ4���Կ�����n(��ʯ��):n(����������)С��4ʱ�����Ӿ�ʯ���������������Ƶ����������Ա仯����n(��ʯ��):n(����������)����4ʱ���������Ƶ�������n(��ʯ��):n(����������)���������Խ��ͣ���n(��ʯ��):n(����������)Ϊ9.75ʱ����������������С������ʱ��ʯ�������̫�ɱ����ߡ�
��n(��ʯ��):n(����������)С��4ʱ�����Ӿ�ʯ���������������������ޱ仯����Ϊ��ʯ����������٣����������ܽ����������࣬�����γ�������n(��ʯ��):n(����������)����4ʱ��������������ȫ�ܽ⣬��ʯ��Խ������Ƶ�����Ӱ�����ԣ���n(��ʯ��):n(����������)Ϊ5ʱ�������������ȴ�22.08 ��m����11.92 ��m������ѡ��n(��ʯ��):n(����������)Ϊ5��
Sb2O3���ʯ���γ�����Ȼ�������Ʊ��������Ƶ����ɹ���[16-21]���Ա�ʾΪ��
Sb2O3+2[C4H4O6]2-+2H+= [Sb2(C4H2O6)2]2-+3H2O (1)
[Sb2(C4H2O6)2]2-+2H2O2+2Na++4H2O+4OH-=2NaSb(OH)6��+2[C4H4O6]2- (2)
�ӷ�Ӧʽ(1)��֪�������������ܽ�����Ӿ�ʯ��Ũ�������ڷ�Ӧʽ(1)���ҽ��У�ʹSb3+���ʯ���γ��ȶ���������ͼ1��ͼ2��֪���������ƾ����ij�����Ҫ�������������̡��ӷ�Ӧʽ(2)�ɿ�����[Sb2(C4H2O6)2]2+����ˮ����������Ϊ��ϳ���������������ͨ��OH-ȡ��[C4H4O6]2-���γɾ��ˣ�Ȼ�˳���õ��������Ʋ�Ʒ����ˣ���ʯ��ļ��������Ч���ٹ����Ͷȣ����ƽ������ƾ����γɺ;���������ٶȡ�
2.2.3���Ȼ��������Խ����������ȵ�Ӱ�졡
�Ӿ�ʯ����ϵĽ�����Կ�����������ϼ����Խ��ͽ������Ƶ����ȣ����ھ�ʯ��(C4H4O6)�۸�ߣ���������̫��������Ҳ��Sb3+����ϼ���ͬʱ�Ȼ��ƻ���һ��ǿ����ʡ��ڽ����ٶ�Ϊ400 r/min��n(C4H6O6):n(Sb2O3)= 5:1���������������������ƽ�����Ӧ30 min������˫��ˮ������Ӧ90 min�������£������Ȼ��������Խ����������ȵ�Ӱ�죬������ͼ5��ʾ��
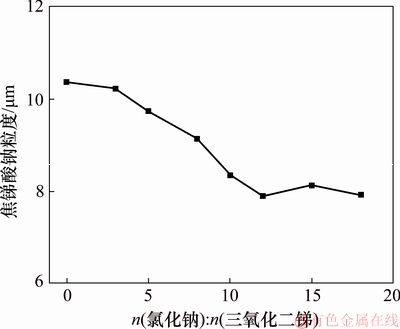
ͼ5��n(�Ȼ���):n(����������)�Խ����������ȵ�Ӱ��
Fig. 5��Effect of molar ratio of NaCl to Sb2O3 on size of sodium pyroantimonate
��ͼ5���Կ�����n(�Ȼ���):n(����������)С��8ʱ���Ȼ��ƶԽ�����������Ӱ���С����n(�Ȼ���):n(����������)����10ʱ�����������������Լ�С������n(�Ȼ���):n(����������)Ϊ12ʱ������Ϊ7.89 um�����������Ȼ��������������������ȱ仯�����ԡ��Ȼ��������٣������������������Ӳ����γ������[22]�����⣬NaCl�ܹ������Na+��Cl-�����������Һ�е�����ǿ�ȡ�����Һ������ǿ���㹻ǿʱ�����ɵĹ��������Χ�������Na+��Cl-�����Ӽ����������ܹ���Ч���ƾ���ij���Ϳ������žۣ��Ӷ��ﵽ���ͽ�������ƽ�����ȵ�Ŀ�ģ���ѡ��n(�Ȼ���):n(����������)Ϊ12��
2.2.4��������Ӧʱ��Խ����������ȵ�Ӱ�졡
�ڽ����ٶ�Ϊ400 r/min��n(C4H6O6):n(NaCl):n(Sb2O3)= 5:12:1���������������������ƽ�����Ӧ������˫��ˮ����90 min�������£����콬����Ӧʱ��Խ����������ȵ�Ӱ�죬������ͼ6��ʾ��
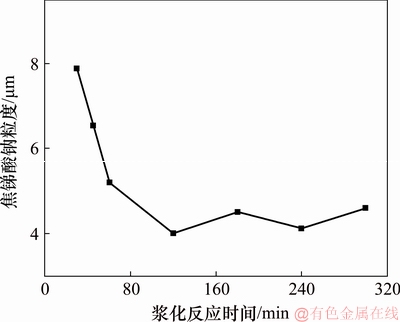
ͼ6��������Ӧʱ��Խ����������ȵ�Ӱ��
Fig. 6��Effect of pulping time on size of sodium pyroantimonate
��ͼ6��֪��������Ӧʱ���ӳ��������������������½�����������Ӧʱ�䳬��120 minʱ�������ӳ�����ʱ�䣬�������Ƶ����Ȳ�û�н�һ����С������4~5 ��m֮�䲨�����ڽ�����Ӧ�����У�Sb2O3���ʯ���γ������[Sb2(C4H2O6)2]2-�������������ƿ�ʹ��������ȶ����ڡ���������������ǿ����������OH-ȡ��[C4H2O6]2-�γ�NaSb(OH)6��������������Ӧ120 min֮����ϵ�ȶ������ӳ�������Ӧʱ�䲻��Խ����������Ȳ����ϴ�Ӱ�졣��ˣ�ѡ����ѽ�����Ӧʱ��Ϊ120 min��
2.2.5������������Ʊ��������ƹ��������ȿ��ƻ�����
�ڽ����ٶ�Ϊ400 r/min��n(C4H6O6):n(NaCl):n(Sb2O3)= 5:12:1���������������������ƽ�����Ӧ120 min������˫��ˮ����һ��ʱ��������£�̽���������Ƶ��γɱ仯���̣���������������������Լ���������Ũ�ȵı仯���������1��
��1��������������н������������Լ�������Ũ�ȵı仯
Table 1��Change of sodium pyroantimonate size and antimony mass concentration with complexing oxidation time

�ӱ�1���Կ���������������Ӧ�Ľ��У�����������������ټ�С����Һ��������Ũ���ȼ�С��������Ҫԭ�������ɽ������ƵĹ��̴��ڶ�̬ƽ�⣬��Ӧ�����練Ӧ����ʽ(2)��ʾ��������Ӧǰ60 min����Һ��������Ũ����С������������������˵����Һ�в����Ľ��������γɾ��ˣ�������������Ӧ60 min����Һ��������Ũ�����������������ȼ�С��˵����ʱ���ɵĽ������ƴ�����ܽ⣬�������ƴ��ڳ���-�ܽ�Ķ�̬ƽ��֮�С���ˣ�����Ϊ����Ĵ������������ʱ����ʵ��ӳ��ᷢ���ܽ⡣�ʵ��ӳ�����ʱ�������Ч���ƽ����������ȵij�����ϸ���������ƾ���������[23]����ˣ��ӳ�����ʱ����120 min��
2.3������������Ʊ��������ƵIJ�Ʒ����
2.3.1����ò�ͽṹ������
ͼ7��ͼ8��ʾ�ֱ�Ϊ������������Ʊ��õ��������Ʋ�Ʒ��SEMͼ��XRD�ס�

ͼ7�������ʯ����Ȼ��ƺ��Ʒ��SEMͼ
Fig. 7��SEM image of product after addition of tartaric acid and NaCl
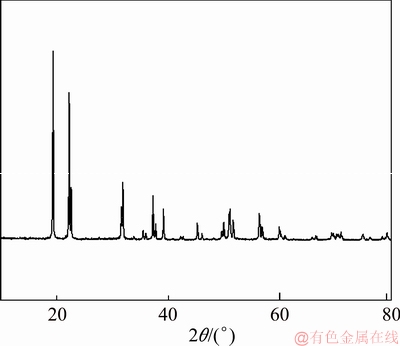
ͼ8�������Ȼ��ƺ;�ʯ����Ƶò�Ʒ��XRD��
Fig. 8��XRD pattern of product after addition of tartaric acid and NaCl
�Ա�ͼ7��ͼ2(c)���Կ����������ʯ����Ȼ��ƺ������Ƶ���ò���ķ��α�Ϊ���λ��״���������ֱ仯�����ھ�ʯ��ı��˽������ƾ����γɺ��������ơ�����ֱ������������ʱ����������ֱ���ڹ���Sb2O3����������������ͨ��ԭ�����������ķ���������������ϳ�����ʱ��[Sb2(C4H2O6)2]2-�ڼ����������������ﵽNaSb(OH)6���������ͶȺ��γ�С���ˣ�Ȼ��С���˾ۼ����������ο�������ͼ8���Կ��������Ƶò�Ʒ�뽹������NaSb(OH)6(��ͼ��PDF85-0363)����������ȫһ�£�û������壬��Ʒ���������κã���������������
2.3.2�����ȷ�����
ͼ9��ʾΪֱ�������������Ʊ��õ��Ľ������Ʋ�Ʒ���ȷֲ�ͼ��ͼ10��ʾΪ��ϳ������Ʊ��õ��������Ʋ�Ʒ�����ȷֲ�ͼ��
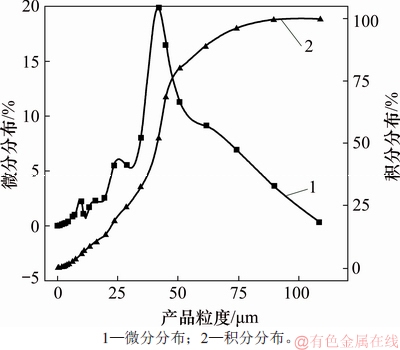
ͼ9��ֱ�ӳ����������Ʊ��õ��������Ƶ����ȷֲ�ͼ
Fig. 9��Size distribution of sodium pyroantimonate obtained by precipitation oxidation
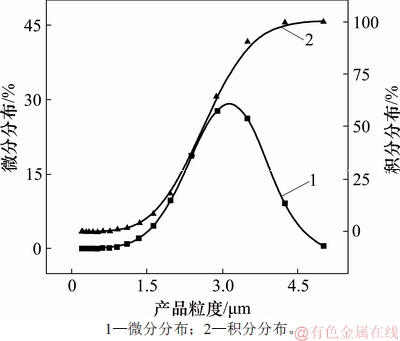
ͼ10����ϳ��������ò�Ʒ���ȷֲ�ͼ
Fig. 10��Size distribution of sodium pyroantimonate obtained by complexing oxidation
��ͼ9��֪��ֱ�������������ƵõĽ�������ƽ����������D50=39.62 ��m���������ȷֲ���ΧΪ0.2~120 ��m������ͼ��������˵�����ȷֲ��������Ϸ�ɢ����ͼ10��֪����ϳ������ƵõĽ�������ƽ����������D50=2.61 ��m���������ȷֲ���ΧΪ0.2~5.0 ��m�����ȷֲ��dz����У��õ��Ľ����������Ⱦ�һ������ϸС��
2.3.3���������Ƴɷַ�����
����ϳ������Ʊ��õ��Ľ������Ʋ�Ʒ�ijɷֽ����ຬ���������õ���Ʒ������������Ϊ49.02%����������NaSb(OH)6��������������Ϊ49.40%����ҵҪ������������Ϊ48.0%~50.0%�����Ⱥ�̼��������Ҫ����ˣ��ò�Ʒ���Ϲ�ҵҪ���Ҳ�Ʒ���ȴﵽ99%���ϡ�
3 ����
1) ֱ�������������Ʊ��������ƵĹ��̷�Ϊ2���Σ�������Ӧ��������Ӧ������������������Ѹ�٣������ִ��ڽ����μ����ʯ���ܽ��������������������پ�˫��ˮ����������Ч���������������о���ij���ͬʱʹ����������ò���ķ�ת��Ϊ���ο�����
2) �������Һ�м����Ȼ���һ����ٽ��ܽ⣬��һ�����ܹ�������Һ�е�����ǿ�ȣ���һ�����ƽ������ƾ������������ƾ����������ڳ���-�̬ܽƽ�⡣
3) ��n(C4H6O6):n(NaCl):n(Sb2O3)= 5:12:1�������ٶ�Ϊ400 r/min��������ӦΪ120 min��������Ӧ120 min�������¿��Եõ�ƽ������Ϊ2 ��m���ң����������Ľ������ƣ���Ʒ����������Ϊ49.02%�����ȴ���99%��
�ο����ף�
[1] �ܽ���.dz����Ч���ϳ���������Լ���ѡ��[J].�������´�, 1992, 20(2): 44-62.
ZHOU Jinzhang. Characteristics and selection of high efficiency compound clarifier [J]. Glass and Enamel,1992, 20(2): 44-62.
[2] �����. ��ұ��[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1987: 358-462.
ZHAO Tiancong. Antimony metallurgy[M]. Changsha: Central South University of Technology Press, 1987: 358-462.
[3] ANDERSON C G. The metallurgy of antimony[J]. Geochemistry, 2012, 72(4): 3-8.
[4] �ź�. ����ϵ��ȼ��[J]. �Ϻ�����, 2012, 40(1): 6-10.
ZHANG Heng. Inorganic antimony flame retardant [J]. Shanghai Plastics, 2012, 40(1): 6-10.
[5] ������.�����������������о�[J]. ������ɫ����, 2008, 24(5): 24-26.
DU Xinling. Research on the production process of sodium pyroantimonate[J]. Hunan Nonferrous Metals, 2008, 24(5): 24-26.
[6] ����, ����ƽ, �����, ��. �ҹ�����Դ���Ʒ������ɳ�����չ����[J]. �й���ҵ, 2014, 23(5): 9-13.
WANG Xiu, WANG Jianping, LIU Chonghao, et al. Analysis of antimony resource situation and sustainable development strategy in China[J]. China Mining Industry, 2014, 23(5): 9-13.
[7] ZHANG Zaoli. Synthesis and microstructure of antimony oxide nanorods[J]. Journal of Materials Research, 2002, 17(7): 1698-1701.
[8] YU Zhongping, LIU Bo, YE Bo, et al. Synthesis of monodispersed antimony doped tin oxide nanoparticles and its self-assembly[J]. Rare Metal Materials and Engineering, 2010, 39(Suppl 2): 142-144.
[9] ������. �ҵ����Ӧ���뷢չ[J]. ��ɫ��ұ, 1998, 14(1): 33-37.
LIU Shiyou. Application and development of industrial production in Handan[J]. Nonferrous Metallurgy, 1998, 14(1): 33-37.
[10] ������. ��ȼ������������Ʊ���Ӧ�����ܼ���ȼ�����о�[D]. ��ɳ: ���ϴ�ѧ��ѧ����ѧԺ, 2001: 30-45.
YANG Weijun. Preparation, application properties and flame retardant mechanism of bismuth oxychloride for flame retardant[D]. Changsha: Central South University. School of Chemistry Chemical Engineening, 2001: 30-45.
[11] ����. �����ʪ����ȡ�������������о�[J]. ��ұ����, 2014, 34(5): 113-117.
CHEN Pu. Experimental study on sodium pyroantimonate from crude antimony by wet process[J]. Mining and Metallurgical Engineering, 2014, 34(5): 113-117.
[12] ����. ���ྫ��ʪ�����ұ���¹����о�[D].��ɳ: ���ϴ�ѧұ���뻷��ѧԺ, 2011: 20-36.
GAO Liang. Research on new hydrometallurgical process of antimony sulfide concentrate[D]. Changsha: Central South University. School of Metallurgy and Environment, 2011: 20-36.
[13] ����, �·���, ����Ԫ. �й���ұ����������״�뷢չ[J]. �ƽ�, 2018, 39(5): 55-60.
LIU Yong, CHEN Fangbin, LIU Gongyuan. Current situation and development of antimony smelting technology in China [J]. Gold, 2008, 39(5): 55-60.
[14] ����ս, �����, ����ƽ, ��. һ�����ϳ������Ƶ��о�[J]. ���ϻ���, 1998, 24(2): 22-23.
ZHANG Yongzhan, LIU Jindun, ZHANG Xiangping, et al. Synthesis of sodium antimonate by one-step method [J]. Henan Chemical Industry, 1998, 24(2): 22-23.
[15] ����ϲ, ������, ����, ��. ���-ˮ���������ϳ�����Ӷ�����������ĩ[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2006, 37(2): 247-251.
JIANG Mingxi, YANG Tianzu, CHU Guang, et al. Synthesis of antimony-doped tin dioxide nano-powder by combined hydrothermal oxidation[J]. Journal of Central South University (Science and Technology), 2006, 37(2): 247-251.
[16] ��ϲ��, ��ϰ�. ��ʯ������ϵ�Ʊ�SbSbS4����������[J]. �й���ɫ����ѧ��, 2014, 24(2): 528-534.
YANG Xiyun, DUAN Xitao. SbSbS4 prepared by tartrate system and its lubrication properties[J]. The Chinese Journal of Non-ferrous Metals, 2014, 24(2): 528-534.
[17] POKROVSKI G S, BORISOVA A Y, ROUX J, et al. Antimony speciation in saline hydrothermal fluids: a combined X-ray absorption fine structure spectroscopy and solubility study[J]. Geochimica et Cosmochimica Acta, 2006, 70(16): 4196-4214.
[18] OELKERS E H, SHERMAN D M, RAGNARSDOTTIR K V, et al. An EXAFS spectroscopic study of aqueous antimony(III)-chloride complexation at temperatures from 25 to 250 �� [J]. Chemical Geology, 1998, 151(14): 21-27.
[19] WIJERATNE A B, GRACIA J, YANG S H, et al. New structural insight for antimony(III)-tartrate[J]. Inorganic Chemistry Communications, 2010, 13(12): 1504-1508.
[20] TELLA M, POKROVSKI G S. Antimony(III) complexing with O-bearing organic ligands in aqueous solution: an X-ray absorption fine structure spectroscopy and solubility study[J]. Geochimica et Cosmochimica Acta, 2009, 73(2): 268-290.
[21] ����. ����������������Ʊ������ʼ��Ի�����֬��ȼ���õ��о�[D]. ��ɳ: ���ϴ�ѧұ���뻷��ѧԺ, 2005: 41-62.
ZHANG Li. Preparation, properties and flame retardant effect of antimony pentoxide on epoxy resin [D]. Changsha: Central South University. School of Metallurgy and Environment, 2005: 41-62.
[22] �, ���˸�, ���, ��. ��ʽ̼��þ��ķ�Ӧ�ᾧ����[J]. ����ѧ��, 2013, 64(2): 718-724.
YANG Chen, SONG Xingfu, WANG Jin, et al. Crystallization process of basic magnesium carbonate microspheres [J]. CIESC Journal, 2013, 64(2): 718-724.
[23] ��ϲ��. �����������Ʊ��������Ϻ�Fe3O4�ŷۼ����������о�[D]. ��ɳ: ���ϴ�ѧұ���뻷��ѧԺ, 2005: 50-65.
YANG Xiyun. Preparation of iron black pigment and Fe3O4 magnetic powder from pyrite cinders and basic theoretical research [D]. Changsha: Central South University. School of Metallurgy and Environment, 2005: 50-65.
���༭ ����ƽ��
�ո����ڣ� 2019 -03 -01; �����ڣ� 2019 -05 -17
������Ŀ(Foundation item)��������Ȼ��ѧ����������Ŀ(51574286)���й���ʿ���ѧ����������Ŀ(2016M592448)�����ϴ�ѧ��ʿ�����������Ŀ(155203) (Project(51574286) supported by the National Natural Science Foundation of China; Project (2016M592448) supported by the Postdoctoral Science Foundation of China; Project(155203) supported by the Postdoctoral Foundation of Central South University)
ͨ�����ߣ���ϲ�ƣ���ʿ�����ڣ�����ʪ��ұ�绯ѧ�о���E-mail:yxy7412@csu.edu.cn
ժҪ:��Sb2O3Ϊԭ�ϣ���������������Ʊ���ϸ�������ơ�����X��������(XRD)��ɨ���������(SEM)�ͼ������ȷ����Խ������ƵĽṹ����ò�����Ƚ��б��������Խ������Ƴɷֽ��з������о������ٶȡ���ʯ��(C4H6O6)���Ȼ���(NaCl)�����Լ�������Ӧʱ��Խ����������ȵ�Ӱ�졣�о�����������ڽ����μ����ʯ�ὫSb2O3�ܽ������������ڼ��������������������ƽ������ƿ����ij����ٶȣ��������ȴ�39.62 ��m����2.61 ��m����ò���ķ�ת��Ϊ���ο������������ƾ����������ڳ���-�̬ܽƽ�⡣�ڽ����ٶ�Ϊ400 r/min�����ʵ����ȼ�n(C4H6O6):n(NaCl):n(Sb2O3)=5:12:1��������Ӧʱ��Ϊ120 min�������£��ɵõ�ƽ������Ϊ2 ��m���ң����������Ľ������Ʋ�Ʒ������������Ϊ49.02%�����ȴ���99%��
[Sb2(C4H2O6)2]2-+2H2O2+2Na++4H2O+4OH-=2NaSb(OH)6��+2[C4H4O6]2- (2)
[1] �ܽ���.dz����Ч���ϳ���������Լ���ѡ��[J].�������´�, 1992, 20(2): 44-62.
[2] �����. ��ұ��[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1987: 358-462.
[3] ANDERSON C G. The metallurgy of antimony[J]. Geochemistry, 2012, 72(4): 3-8.
[4] �ź�. ����ϵ��ȼ��[J]. �Ϻ�����, 2012, 40(1): 6-10.
[5] ������.�����������������о�[J]. ������ɫ����, 2008, 24(5): 24-26.
[6] ����, ����ƽ, �����, ��. �ҹ�����Դ���Ʒ������ɳ�����չ����[J]. �й���ҵ, 2014, 23(5): 9-13.
[9] ������. �ҵ����Ӧ���뷢չ[J]. ��ɫ��ұ, 1998, 14(1): 33-37.
[10] ������. ��ȼ������������Ʊ���Ӧ�����ܼ���ȼ�����о�[D]. ��ɳ: ���ϴ�ѧ��ѧ����ѧԺ, 2001: 30-45.
[11] ����. �����ʪ����ȡ�������������о�[J]. ��ұ����, 2014, 34(5): 113-117.
[12] ����. ���ྫ��ʪ�����ұ���¹����о�[D].��ɳ: ���ϴ�ѧұ���뻷��ѧԺ, 2011: 20-36.
[13] ����, �·���, ����Ԫ. �й���ұ����������״�뷢չ[J]. �ƽ�, 2018, 39(5): 55-60.
[14] ����ս, �����, ����ƽ, ��. һ�����ϳ������Ƶ��о�[J]. ���ϻ���, 1998, 24(2): 22-23.
[16] ��ϲ��, ��ϰ�. ��ʯ������ϵ�Ʊ�SbSbS4����������[J]. �й���ɫ����ѧ��, 2014, 24(2): 528-534.
[21] ����. ����������������Ʊ������ʼ��Ի�����֬��ȼ���õ��о�[D]. ��ɳ: ���ϴ�ѧұ���뻷��ѧԺ, 2005: 41-62.
[22] �, ���˸�, ���, ��. ��ʽ̼��þ��ķ�Ӧ�ᾧ����[J]. ����ѧ��, 2013, 64(2): 718-724.
[23] ��ϲ��. �����������Ʊ��������Ϻ�Fe3O4�ŷۼ����������о�[D]. ��ɳ: ���ϴ�ѧұ���뻷��ѧԺ, 2005: 50-65.


