������ʱ��: 2016-07-11 13:34
�尷N235��ʯú���Һ�з��븻����
�人������ѧ��Դ�뻷������ѧԺ
����Դ��Ч���ú���ʡЭͬ��������
�人�Ƽ���ѧ��Դ�뻷������ѧԺ
ժ Ҫ��
�о������尷N235��ʯú�������Һ����ȡ������, ��������ȡ����ɡ���ԭҺp Hֵ����ȡʱ��, ����ȡ����ɡ�����ʱ������ض���ȡ�ʼ������ʵ�Ӱ��, ��̽������ȡ�뷴�����з��������������ӵķ���Ч��������������:���ڷ�����Ũ��Ϊ1.89 g��L-1�ĺ������Һ, ��20%N235+5%TBP+75%�ǻ�ú������ȡ��, ��p HΪ1.7�����O/A=1��3��������ȡ2 min, ��������ȡ����90%����, ��������������ȡ, ��������ȡ�ʴﵽ98%����;���ڸ���9.92 g��L-1�����л���, ��6%Na2CO3��Һ�����ͼ����ͷ�, �������O/A=3��1, ����ʱ��4 min, ���ĵ��������ʴ�58%, ������������ȡ, ���ķ����ʴﵽ99%����, ͬʱ�����������нϺõķ���Ч��, ���ж���������þ����ȥ���ʴﵽ99%����, ���ס������ȥ���ʴﵽ60%���ϡ��÷���Һͨ����γ���������������������Ʒ�����ﵽYB/T 5304-2011ұ��98������
�ؼ��ʣ�
��ͼ����ţ� TF841.3
����飺�ȴ� (1992-) , Ů, �����人��, ˶ʿ, �о�����:ʯú���Һ�ľ�������, E-mail:chen_chun914@163.com;;��һ��, ����, �绰:13907158287, E-mail:zym126135@126.com;
�ո����ڣ�2015-11-06
����������Ȼ��ѧ������Ŀ (51404177);����ʡ��Ȼ��ѧ������Ŀ (2014CFB857) ����;
Separation and Enrichment of Vanadium from Stone Coal Acidic Leach Solution Using Tertiary Amine N235
Chen Chun Zhang Yimin Bao Shenxu Huang Jing Yang Xiao
College of Resources and Environment Engineering, Wuhan University of Technology
Hubei Collaborative Innovation Center for High Efficient Utilization of Vanadium Resources
School of Resources and Environmental Engineering, Wuhan University of Science and Technology
Abstract��
The extraction of vanadium (V) from stone coal sulfuric acid leach solution using tertiary amine N235 was studied. The effects of composition of extraction and stripping agent, initial p H, extraction and stripping time on extraction and stripping efficiency were investigated, and the separation efficiency of the impurity ions in the process of extraction and stripping vanadium was explored.The results showed that the total extraction efficiency after one-stage extraction was more than 90% under the optimum conditions including the initial p H of 1. 7, with 20% N235 and 5% TBP as mixed extractant, the O/A ratio of 1/3, and the extraction duration of 2min for the fed solution containing 1. 89 g��L-1V2O5. After two-stage countercurrent extraction, more than 98% vanadium in the leaching solution was extracted; the total stripping rate after one-stage stripping was 58% under the optimum conditions including concentration of stripping agent of 6% Na2CO3 with the O/A ratio of 3, and the stripping duration of 4 min for the loaded organic phase contained 9. 92 g��L-1V2O5. More than 98% vanadium was stripped with two-stage back-extraction. Simultaneously, the separation efficiency between impurity ions and vanadium was good. More than 99% of Al, Fe, Mg and 60% of P, Si could be removed from the leaching solution. The production quality could meet YB/T5304-2011 Metallurgical 98 standard.
Keyword��
vanadium; N235; solution extraction; stone coal;
Received�� 2015-11-06
����ʯú���ҹ���Ҫ�ķ���Դ֮һ, ���ŷ�Ӧ������IJ�������, ��ʯú����ȡ�����о����ϼ�ǿ[1]��������з������ʸ�, ������Ⱦ�����ŷ�, �Ի�����ȾС���ŵ㱻�ᷰ��ҵ�㷺����[2]���������������ͨ�����õ��Ǹ�Ũ�ȵ�����, ���������淰һ�𱻽���, ���յ��½���Һ�ɷָ��ӡ����ʺ����ܸ�[3]��Ϊ�����������Ҫ��, ��Ժ������Һ�������Ӳ���������Ŀǰ��ʯú���Һ�з��븻�������о��༯��������������ȡ��P204����ȡ���ռ�������[4,5,6], ��P204��ȡ���ڵ�����ȡ�ʲ��ߡ���ȡ�������Լ������ʷ��벻��������[7]��������ȡ�����е�����ȡ�ʸߡ���������ӷ���Ч���õ��ŵ㱻�㷺Ӧ���ڴ�ʯúˮ��Һ�Լ��Ϸ���������Һ�л��շ�[8,9]���������ȡ�������ͷ�������ʯú���Һ���о��༯���ڶԷ�����ȡЧ��, �����ʵ�ȥ��Ч���о����١����о�������尷��ȡ��N235��ʯú���Һ�о���������, ̽�ֺ��ʵ���ȡ����;ͬʱ�о�N235����ȡ�ͷ������ж���������ȥ��Ч��, ���Ʊ�������������Ʒ��
1 ʵ��
1.1 ԭ�����Լ�
����ij��ʯúԭ���հױ���, ����ȹ��մ����õ����Һ�����Һ������, �����е�V (��) ����ΪV (��) , ���ù��˵õ���ԭҺ, ��ԭҺ�ɷּ���1��
����p H�Ʋⶨ��p HֵΪ0.5���ӱ�1���Կ���, ��ԭҺ�����ӳɷֽ�Ϊ����, ������Ҫ���������ΪAl3+, Fe3+, Mg2+, K+��, ��Ҫ���������������������ӡ����������, �������ӵ�Ũ�Ƚϵ͡�
��Ҫ�Լ�:������尷N235 (ʹ��ǰ����1mol��L-1H2SO4ת��Ϊ��Ӧ�İ���) , ���ƻǻ�ú��, ����������TBP, ������, Ũ����, ̼����, ��ʯ��, ̼������, ̼���, ̼�����, ��������, �Ȼ���, ������, ��Ϊ������;��Ҫ����:PHS-3Cp H��, SCZL-2A���������ܿ��´���������, ��Һ©����
��1 ��ԭҺ�ɷַ���Table 1 Chemical composition of feed (mg��L-1) ����ԭͼ

��1 ��ԭҺ�ɷַ���Table 1 Chemical composition of feed (mg��L-1)
1.2 ������ԭ��
ȡһ��������ԭҺ���л������ձ���, �ô������������һ��ʱ��, ������ɺ����Һ©�����÷�Һ������Һ���������������Һ�������ζ�������, ������ȡ��, ��PHS-3C p H�Ʋⶨ����ȡ���ȡ��ɺ��л��ྭ��һ��ˮϴ����, ��һ������뷴�ͼ���Ӧһ��ʱ��, ���õ�����Һ��ʵ����������½��С�
ʵ������з�����ȡ�ʼ�������:

N235, ������, �����Ϊֱ��CnH2n+1 (n=8, 10) , ��ѧʽ�ɼ�дΪR3N, ����ȡԭ��[10,11]����:
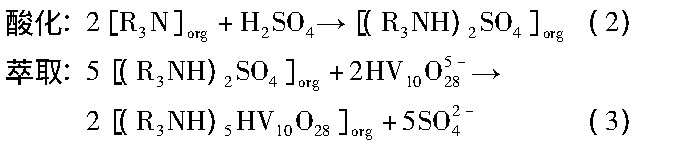

2 ���������
2.1 ��ȡ
2.1.1 �������
��ȡ��Ũ����һ����Ҫ�Ĺ��ղ���, ������Ӱ����ȡ���տɲ����Ժ;�����[12]����N235Ϊ��ȡ��, �ǻ�ú��Ϊϡ�ͼ�, ��ԭҺ���100 ml, ���O/A=1��5, ��ȡʱ��6 min, ���첻ͬ��ȡ��Ũ�ȶ���ȡ�ʵ�Ӱ��, �����ͼ1��
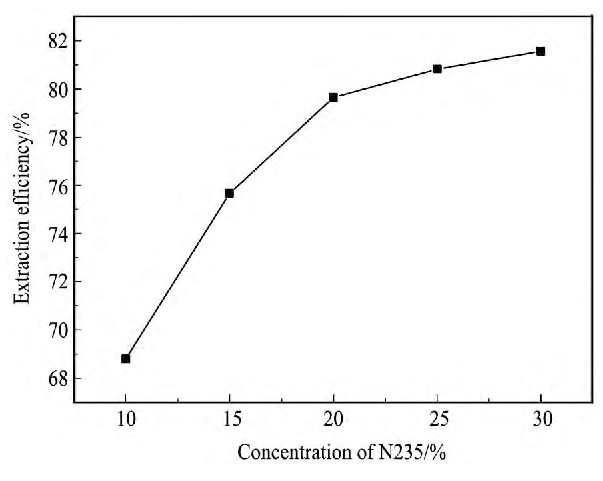
ͼ1 N235Ũ�ȶ���ȡ�ʵ�Ӱ��Fig.1 Effect of concentration of N235 on extraction rate
��2 ��ͬ�л�����ɶ���ȡ��Ӱ��Table 2 Effect of organic phase on extraction efficiency ����ԭͼ
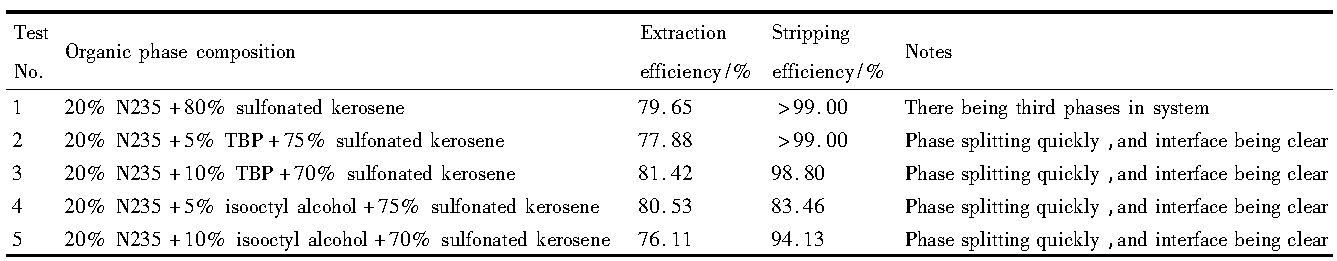
��2 ��ͬ�л�����ɶ���ȡ��Ӱ��Table 2 Effect of organic phase on extraction efficiency
��ͼ1����ʾ, N235Ũ�����, ��ȡ�����нϴ����, ��N235Ũ��Խ��, �л���ճ��Խ��, �����ٶȼ���, ��������, ͬʱ�ɱ�����, �ۺϿ��ǹ�ҵ�����ɱ�����ȡ����, ѡ��20%N235��Ϊ��ȡ����
����ȡ�����з�����ϵ���ֵ�����, Ϊ�˸����л�������, ��Ҫ����TBP��������������ڼ�[13], ����ͬ��ȡ����������ȡ, ͬʱ�ڷ������O/A=2��1, ����ʱ��10 min�����½��з���, ���첻ͬ���л�����ɶ���ȡ�ͷ��͵�Ӱ��, ��������2��
��2����:���벻ͬŨ��TBP��������, ������Ч���Ʋ������ܡ���ȡ��ϵΪ20%N235+5%TBP+75%�ǻ�ú��ʱ, ��ȡ�ʺͷ����ʾ��ϸ�, ���TBP����, �������½�, ������������TBPʱ, ���нϺõ���ȡЧ��, ��������Ҳ�ϵ͡�Ϊ��ʹ������ȡ���뷴��ȡ���ϸ�, �л������Ϊ20%N235+5%TBP+75%�ǻ�ú�͡�
2.1.2 ��ȡp H��ѡ��
�л�������Ϊ20%N235+5%TBP+75%�ǻ�ú��, ��ԭҺ���Ϊ100 ml, O/A=1��5, ��ȡʱ��6 min, ���е�����ȡʵ��, ������ԭҺp H����ȡ�ʵ�Ӱ��, ��������3��
��3����:������ԭҺp H������, ��ȡ�ʲ�������p HΪ0.67ʱ, ����ȡ�ʽ�Ϊ30.84%;��p H��0.67������1.73, ��ȡ�������59.03%;����p Hֵ��������, ��ȡ�����5.28%, ����ˮ�����г�������, ��������, �Ʋ�ԭ��Ϊ��Ӧ����p H����, �����Һ�е�Fe3+ˮ����������ǵ�p HΪ1.7ʱ������ȡ�ʽϸ�, ͬʱ�����������, ����ѡ����ԭҺp HΪ1.7���ҡ�
��3 ��ͬ����ԭҺp H����ȡ�ʵ�Ӱ��Table 3 Effect of feed p H on extraction rate ����ԭͼ

��3 ��ͬ����ԭҺp H����ȡ�ʵ�Ӱ��Table 3 Effect of feed p H on extraction rate
2.1.3 ��ȡʱ�����ȡ�ʵ�Ӱ��
�л�������Ϊ20%N235+5%TBP+75%�ǻ�ú��, ��ԭҺ���Ϊ100 ml, O/A=1��5, ����̽������ȡʱ�����ȡ�ʵ�Ӱ��, ������ͼ2��
��ͼ2����ʾ, ��ȡʱ��Ϊ10 sʱ, ������ȡ��Ϊ55.16%, ��10~50 s֮��, ��ȡ��Ѹ�����, 50 s�Ժ���ȡ�ʻ�������, ��120 sʱ����ƽ��, ������ȡ�ʴﵽ91.16%��ԭ��Ϊ��ȡ������, ������ȡʱ�������, ˮ���еķ�����Ũ�Ȳ��Ͻ���, �л����з�����Ũ�Ȳ�������, ��������ƽ��, ������ȡ�����ӵ����Ʊ仺�����ǵ���ȡʱ��Ϊ120 sʱ, ���ĵ�����ȡ���Ѿ��ϸ�, ������ȡʱ����ȡ�ʲ��ϴ����, ��ѡȡ��ȡʱ��Ϊ120 s��
ͼ2 ��ȡʱ��Է���ȡ�ʵ�Ӱ��Fig.2 Effect of extraction time on extraction rate
2.1.4 ��� (O/A) ����ȡ�ʵ�Ӱ��
�л�������Ϊ20%N235+5%TBP+75%�ǻ�ú��, ��ԭҺ���л���������Ϊ90 ml, ��ȡʱ��120 s, ����̽���˲�ͬ��ȶ���ȡ�ʵ�Ӱ��, ������ͼ3��
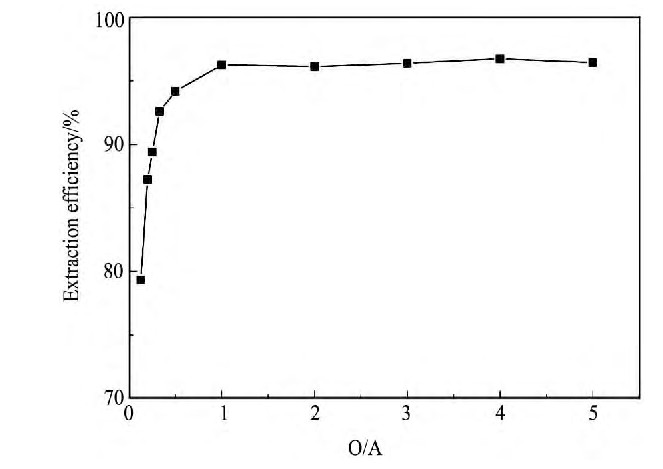
�о����ֽϸ����, ��ȡ�ʽϸ�, ����λ�л��������ʽ���;�����ýϵ����, ��ȡ�ʽϵ�, �л��������ʸ�[14]��ͼ3����, ��� (O/A) ��1��1����5��1�Ĺ���, ��ȡ�ʱ仯����, ������96%����, ��ʱ�л������ȡ�ʸ�, ���������ʵ�;�����1��8����1��1�Ĺ�������ȡ�ʴ�79.33%���ߵ�96.27%, �����ʲ��Ͻ���, ��ȡ�ʲ�����ߡ�Ϊʹ��ȡ������, �л�����ȡ�ʼ������ʾ��ϸ�, ѡ����� (O/A) Ϊ1��3��
2.1.5 ������ȡʵ��
ͼ3 ��� (O/A) �Է���ȡ�ʵ�Ӱ��Fig.3 Effect of O/A on extraction rate
���������������:�л������20%N235+5%TBP+75%�ǻ�ú��, p HΪ1.7, ʱ��120 s, ��� (O/A) =1��3, ˮ�ྭ����������ȡ�õ������л��༰ˮ��, ����ȡ��98%����, �л��Ũ��c (V) =9.92 g��L-1, ���������ӵķ����������4��
�ӱ�4���Կ���, N235����ȡ�����жԸ����������ӵķ���Ч�����ϸߡ���������������ȡ, ��������������ȥ���ʾ��ﵽ95%����, ��Si��ȥ����Ҳ�ﵽ77.8%��
2.2 ����ȡ
2.2.1 ���ͼ���ѡ��
�����л�������Ϊ20ml, �����л�����c (V) =9.92 g��L-1, O/A=2��1, ����ʱ��10 min, ���鿼���˲�ͬ���ͼ��Է���ȡ�ʵ�Ӱ��, �������5��
���5��ʾ, Ӧ��������η�����ϵ���з��;��ܵõ��ϸ���ȡ�ʡ�����η�����ϵ�ķ����������ɶ��麟���, �����ڷ������������ˮ��, ���д���������[15], ʹ����ν��з��ͺ����ö��林��Ȳ���, ��β�������ѵķ��ͼ�����������ϵ��������, ѡ�����η�����ϵ��һ�����еķ������Աȼ��ַ��ͼ�Ч��, Na2CO3��������ߡ��ۺϿ��Ƿ����ʡ������Լ��ɱ�, ����ѡ��Na2CO3��Ϊ���ͼ���
2.2.2 ̼����Ũ�ȶԷ����ʵ�Ӱ��
�����л�������Ϊ20 ml, �����л�����c (V) =9.92 g��L-1, ���ͼ�Ϊ��ͬŨ�ȵ�Na2CO3��Һ, O/A=2��1, ����ʱ��10 min, ���鿼���˷��ͼ���Ũ�ȶԷ���ȡ�ʵ�Ӱ��, �����ͼ4��
��4 ����Һ�ɷַ���Table 4 Analysis of raffinate ����ԭͼ

��4 ����Һ�ɷַ���Table 4 Analysis of raffinate
��5 ��ͬ���ͼ��Է����ʵ�Ӱ��Table 5 Effect of stripping agent on extraction rate ����ԭͼ

��5 ��ͬ���ͼ��Է����ʵ�Ӱ��Table 5 Effect of stripping agent on extraction rate
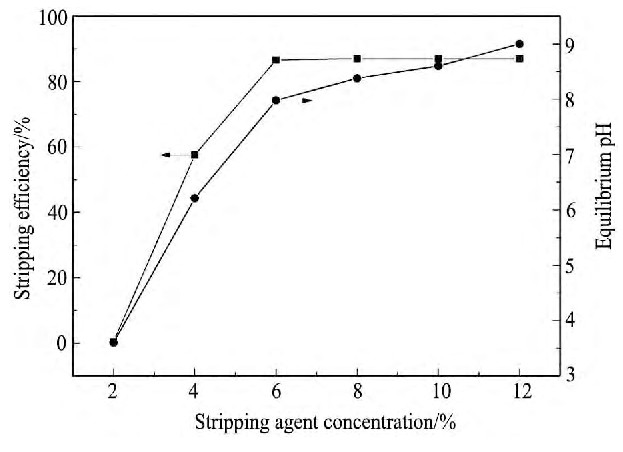
��ͼ4��֪, Na2CO3Ũ����2%~6%֮��, ����Na2CO3Ũ�ȵ�����, ��������0.4%������86.64%, ��������p HֵҲ��֮��ߡ���Na2CO3Ũ����6%���ߵ�12%ʱ, �����ʻ������ֲ���, ��p H���߽�Ϊ����, ԭ�����Ϊ�������д�������Ĺ���, ����̼����, ��ɷ������ʱ仯����, ��p H����Ѹ��;����̼����Ũ������, �����������, ��Ӧ����Һp H���������Ʊ仺���ۺϿ���, ѡ����������6%Na2CO3��Һ��Ϊ���ͼ���
2.2.3 ����ʱ��Է����ʵ�Ӱ��
�����л�������Ϊ20 ml, �����л�����c (V) =9.92 g��L-1, O/A=2��1, ���ͼ�Ϊ6%Na2CO3, ���鿼���˷���ʱ��Է���ȡ�ʵ�Ӱ��, �����ͼ5��
ʵ��������, ���ŷ���ʱ�������, �������Ȳ������ߺ������ȶ�������ʱ��Ϊ0.5 minʱ, ������Ϊ59.65%, ��0.5~4 min֮��, ��ȡ��Ѹ������, 4 min����ȡ����������ƽ��, �����ʴﵽ86.27%���������ڷ�������, ���ͼ��еķ�Ũ�Ȳ�������, �л����з�Ũ�Ȳ��Ͻ���, ��������ƽ�⡣���ǵ�����ʱ��Ϊ4 minʱ, �������Ѿ��ϸ�, ���ӷ���ʱ�䷴�������߲�����, �ʷ���ʱ��Ϊ4 min��
ͼ4 ���ͼ�Ũ�ȶԷ���ȡ�ʵ�Ӱ��Fig.4 Effect of Na2CO3concentration on stripping rate
ͼ5 ����ʱ��Է���ȡ�ʵ�Ӱ��Fig.5 Effect of extraction time on stripping rate
2.2.4 ������� (O/A) �Է����ʵ�Ӱ��
�����л����뷴�ͼ������������Ϊ90 ml, �����л�����c (V) =9.92 g��L-1, ���ͼ�Ϊ6%Na2CO3, ����ʱ��4 min, ���鿼���˷�����ȶԷ���ȡ�ʵ�Ӱ��, �����ͼ6��
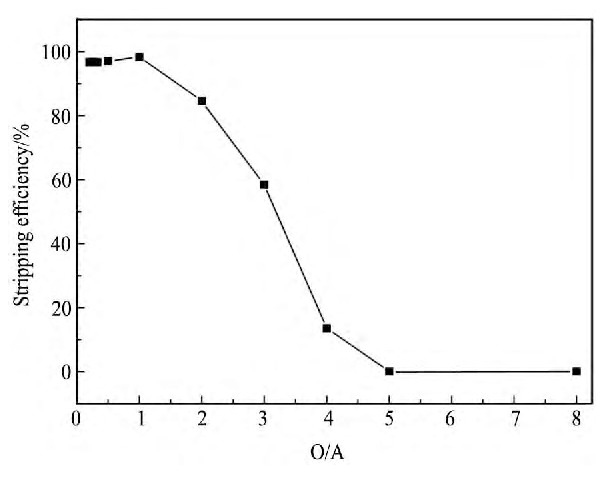
����ͼ6��ʾ, ��O/AΪ1��1ʱ�����ʴﵽ���ֵ98.33%, �������ͼ�������������ڷ�����, ��O/A��1��5�仯��1��1�Ĺ���, �����ʻ�������, ˵�����ͼ�����Ѿ�����;O/A��5�仯��1����, ������ȼ�С�����ʲ������;��O/A����5ʱ, ��ȡ�ʻ���Ϊ0, ����ԭ��Ϊ�л�������ȡ����������Na2CO3, ʹ����δ�������͡�Ϊ��ʹ���ͼ��нϸ������ʼ�������, ͬʱ��߷���Һ�з�Ũ��, ����ѡȡO/A=3��1��
2.3 �ۺ���֤����
�����ȡ������������, �Խ���ij��ʯú���Һ�Ĵ���ȷ����������:p HΪ1.7, �л������Ϊ20%N235+5%TBP+75%�ǻ�ú��, ���O/AΪ1��3, ��ȡʱ��2 min, ������������ȡ, ������ȡ��Ϊ98%����;��6%Na2CO3Ϊ���ͼ�, ����ʱ��4 min, ���O/AΪ3��1, ����������99%���ϡ���ȡǰ��������ɼ���6��
��6����:����������ȡ��������, ��Ũ����1895 mg��L-1������13374 mg��L-1, ͬʱ�����ʱ�����, ���ж�Al, Fe, Mg��ȥ���ʴ�99%����, P��ȥ���ʴﵽ62.7%, Si��ȥ���ʴﵽ69.6%��
ͼ6 ��ȶԷ���ȡ�ʵ�Ӱ��Fig.6 Effect of O/A on stripping rate
��6 ��ȡǰ������Ũ��Table 6 Ion concentration before and after extraction (mg��L-1) ����ԭͼ
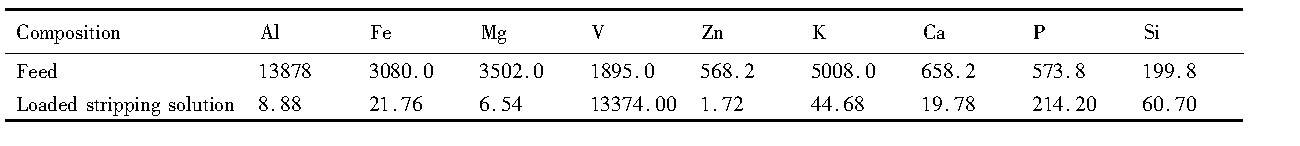
��6 ��ȡǰ������Ũ��Table 6 Ion concentration before and after extraction (mg��L-1)
��7 ��Ʒ�ɷ�XRF����Table 7 Composition of product by XRF analysis (%, mass fraction) ����ԭͼ

��7 ��Ʒ�ɷ�XRF����Table 7 Composition of product by XRF analysis (%, mass fraction)
����Һ��P, Si��, ��p H��8.0����NH4Cl���г���, ���ó���ϴ�Ӻ�ɺ���550�決��2 h��V2O5������V2O5��Ʒ�����, �ﵽYB/T5304-2011ұ��98��������Ʒ������������7��
3 ����
��Խ���ij�ض����ʵͺ�����ʯú���Һ, ��20%N235+5%TBPΪ��ȡ��, 6%̼������ҺΪ���ͼ�, ������������ȡ, ��������, ���ӳ�������, �ܽϺþ���������, ���ò�Ʒ���Ƚϸߡ���������ȡ��Ϊ98%����, �ܷ�����99%���ϡ���Ũ����1895 mg��L-1������13374 mg��L-1, ������Ϊ7.1, ��������þ���衢�����ʾ��ܱ���Ч����, ��ȥ���ʴﵽ99%���ϡ����ò�ƷV2O5��������Ϊ99.75%, ���������Ũ�Ⱦ��ϵ�, ���ȿɴﵽYB/T5304-2011ұ��98������
�����