�й���ɫ����ѧ�� 2004,(10),1759-1762 DOI:10.19476/j.ysxb.1004.0609.2004.10.024
����CaCl2-MgCl2��ϵ��ճ��
�й���ѧԺ���̹����о������෴Ӧ�ص�ʵ����,�й���ѧԺ���̹����о������෴Ӧ�ص�ʵ����,�й���ѧԺ���̹����о������෴Ӧ�ص�ʵ����,�й���ѧԺ���̹����о������෴Ӧ�ص�ʵ���� ����100080,�й� ,����100080,�й� ,����100080,�й� ,����100080,�й�
ժ Ҫ��
����ת���巨ϵͳ������CaCl2 MgCl2��������ϵ��ճ��,����������CaCl2 MgCl2��ϵճ�����¶Ⱥ���ɵı仯��ϵ���Ƚ���ʵ���õ����������ױ���ֵ,������������ϵճ�ȱ仯���ɶ�������ϵ�ṹ�������ƶϡ�ʵ������������ϵճ�����¶����߶����Խ���,���������Լ�������������,�����ױ����Ĵ�CaCl2��Mg Cl2��ճ��ֵ���,ʵ����ֵ����ƫ�����CaCl2 MgCl2�����ϵ��ճ������Ҫ�ȴ����ʵ�ճ�ȴ�,��˵��������������,CaCl2 MgCl2��ϵ����������ϴ�����������,����������ճ�ȡ��ڲ�ͬ���¶�������,�����в�ͬ��ɵ����������,��ϵճ�����ֵ��Ӧ�˲�ͬ������֡�
�ؼ��ʣ�
��ͼ����ţ� O522
����飺������(1978),��,��ʿ�о���.;Ԭ�¸�,����;�绰:01062527440;E mail:yuanzhf@home.ipe.ac.cn;
�ո����ڣ�2004-04-20
����������Ȼ��ѧ����������Ŀ(20306030);
Viscosity properties of molten CaCl2-MgCl2 system
Abstract��
The viscosities of molten CaCl2-MgCl2 system were measured using rotating cylinder method, and the variations with temperature and components were explored. The experimental data were compared with the literatural ones, the deduction and prediction to the structure of molten CaCl2-MgCl2 proceeded on the base of variating regulations of molten melts with temperature and components as well. The viscosities of molten chlorides were decreasing apparently with increasing temperature, however, because of the impurity in experimental reagents, there were discriminations between literatural and experimental values. As larger volume complex ions being formed, the viscosities of molten mixing CaCl2-MgCl2 melts were higher than those of the pure components. And different complex ions were formed at different temperatures, the highest points of viscosity in the system are corresponding with different compositions.
Keyword��
molten chloride melt; viscosity; rotating cylinder method;
Received�� 2004-04-20
ճ���Ǹ����������Ҫ���Բ���, ��Ӱ��������巴Ӧ���Ե���Ҫ����֮һ, ճ�ȶ�ұ���� �ᴿ�� ���졢 ����Ǿ�������Ʊ��� Һ���սᡢ �˷�Ӧ�ѵ�Һ̬������ȴ�����ӹ��̵ȶ���ѧ����������Ӱ�졣 ͬʱ, ����ճ�ȵı仯����ṹ�仯�ĺ�۷�Ӧ֮һ, ������ճ�ȵ��о�Ҳ�������о�����������۽ṹ�� ������ ŷ���ձ�
�Ȼ�����������ϵ��ճ���о��Ƚ���, �����ⱨ���������Ҳ����, ���Ȼ������ε�ճ�����Զ������Ȼ��� ���ε�������������TiCl4�ȹ���������Ҫ�����塣 �Ȼ��������ε�ճ�������������Ȼ����ղ����趨����Ҫ����, ���������Ȼ��ķ�Ӧ�������漰�������ﻯ������ճ�ȡ� �����������ܶ�
������������ת���巨(Rotating cylinder method)����ճ�ȼ�ϵͳ����������CaCl2-MgCl2��ϵ��ճ��, �����˴�CaCl2��MgCl2����ճ�����¶ȵı仯��ϵ, ͬʱ�о����ɶ�����ɵ�CaCl2-MgCl2��Ԫ��ϵճ�����¶Ⱥ���ֵı仯�� �����������ױ����Ĵ�����CaCl2��MgCl2�����ճ��ֵ
1 ʵ��
1.1 ʵ����Ϻ��豸
��Ҫʵ�������: ��ˮ�Ȼ���, CaCl2��������96%,������, �����Լ����ǻ�������˾����; ��ˮ�Ȼ�þ, ������, ����Strem Chemical�Լ���˾����, MgCl2����Ϊ97.5%, H2O����Ϊ2%��
���»�תճ�ȼ�װ��ʾ��ͼ��ͼ1��ʾ, ��ճ�ȼƿ��¾����ǡ�0.5 ��, ճ�Ȳ�ͷλ�����<1 mm, �������1%��
1.2 ʵ�����
����У��ճ�ȼ�ϵͳ�ij���, ������Ϊճ�Ȳ��������ļ�������� ��ʢ��Լ150 g(��֤��50 mm���ҵ��۳����)��ѧ������ʵ���Լ������������������ڸ���¯��ĺ��¶��м���, ���¹�����, ͨ�������������ȴˮ, ʹ¯�ڱ��ֶ������������Լ�¯������¶ȴ��ڳ���״̬�� ���µ��趨���¶Ⱥ�, ����40 min, ��֤¯���¶Ⱥ������۳��¶Ⱥ㶨ͳһ�� ����ճ�Ȳ�������, ����¯�����ߵ��趨�߶�ʹճ�Ȳ�ͷ���۳�Һ��10 mm����ת3 min�����ȶ�, ¯���������ʹճ�Ȳ�ͷ���뵽�۳����趨���(һ��Ϊ20 mm), ���۳�����ת3 min�ȶ���, �������ʼȡճ������, ÿ��5 sȡһ��ֵ, ����ȡ41�����ݵ���Ϊ1�鱣��, ��ͬһ�¶��µ�ÿ1�������ɷ�������ȡ5������, ��5�����ݽ��н��������
ͼ1 ճ�Ȳ����ǵ�ʵ��װ��ʾ��ͼ
Fig.1 Scheme of viscosity measurement equipment 1��Furnace bracket; 2��Heating furnace; 3��Crucible bracket; 4��Al2O3 tube; 5��Al2O3 crucible; 6��Molten reagent; 7��Detector; 8��Photoelectric sensor; 9��Synchronous dynamo; 10��Gas inlet; 11��Thermocouple; 12��Water inlet; 13��Water outlet; 14��Controller; 15��Computer system
2 ���������
2.1�¶ȶԴ�����CaCl2��MgCl2ճ�ȵ�Ӱ��
�¶���������ϵճ�ȵ���ҪӰ������֮һ, ��CaCl2���۵���1 055 K, ��MgCl2���۵���981 K
ͼ2 ������CaCl2��MgCl2ճ�����¶ȵı仯
Fig.2 Viscosity of molten CaCl2 and MgCl2 variating with temperature (a)��CaCl2(molten CaCl2 melt); (b)��MgCl2(molten MgCl2 melt)
2.2CaCl2-MgCl2��Ԫ�Ȼ���������ϵճ�����¶Ⱥͳɷֵı仯
���λ������ϵ��ճ����������ϵ�����һ���Ĺ�ϵ, �Ȼ��������Ѱ���������ճ�������Ҫ�����CaCl2��MgCl2�Ļ��� ��ʵ���о���CaCl2-MgCl2��ɵĶ�Ԫ�����ϵճ����ɷֺ��¶ȵı仯��ϵ, ��������1 073 K��1 373 K�¶ȷ�Χ��, CaCl2��MgCl2Ħ���ȷֱ�Ϊ1��1, 2��1, 3��1��4��1��ϵ��ճ�����¶ȵı仯��ϵ�� ��ͼ3��ʾ, ���е�������ϵճ�����¶����߶����Խ��͡�
ͼ3 ��ͬ���CaCl2-MgCl2��ϵճ�����¶ȵı仯
Fig.3 Variation of viscosity of different component molten CaCl2-MgCl2 with temperature
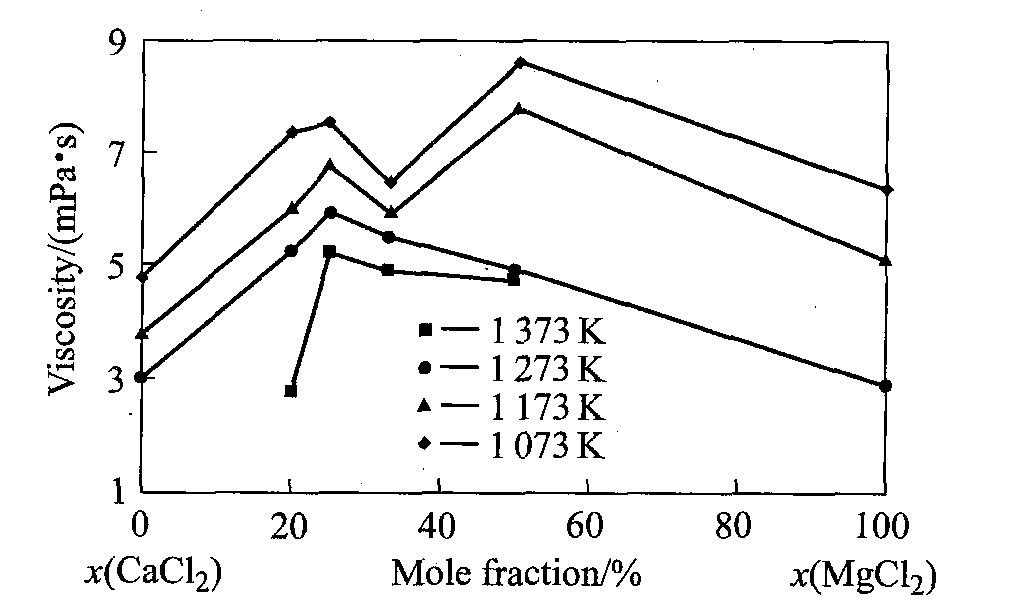
��ͼ4���Կ���, ����ͬ�¶�������, ���������ε�ճ�ȴ���������͵�, ������Ϊ��ͬ��Ԫ���μ�����ô�, �ڻ������״̬��������γ��������, �������������ϴ������, ����Ҳ������, ���������������ӵ������Ѷ�, �Ӷ������������ϵ��ճ�ȡ� �ڲ�ͬ�¶�ʱ, ������ϵճ����ߵ�������ͬ, ��˵���ڲ�ͬ���¶������������γ��˲�ͬ�����, ��������������������׳̶Ȳ���ͬ�� �Ƚ������¶������µ�����, �¶Ƚϵ�(1 073 K��1 173 K)ʱ������ϵճ����ߵ�����ڵ���Ԫ��������Ħ����Ϊ1��1(MgCl2Ħ��������50%), �����¶Ƚϸ�ʱ(1 273 K��1 373 K), ������ϵճ����ߵ�����ڵ���Ԫ��ɻ��Ħ����Ϊ3��1(MgCl2��Ħ��������25%)��
ͼ4 ��������ϵճ������ϵ��ɵı仯
Fig.4 Variation of viscosity of molten melt with component
3 ����
1) ʵ���������ε�ճ�ȱ����ױ��������ݴ�, ��������ʵ���Լ������������ʵ�ԭ��, Ҳ����˵��, ��������������(�Ȼ���ˮ��IJ���)�������������Ȼ���������ϵ��ճ�ȡ�
2) �����¶ȵ�����, ��������ϵճ�����Խ���, ��֤���¶���������������������ӵĻ���, ������������Ե����ۡ�
3) ��������ε�ճ������Ҫ�ȴ��������ʵ�ճ��Ҫ��, ˵��������״̬��, ������ϵ�γ�������ϴ�����������, ��������������ϵ�������Ѷ�, ��ϵճ�����ӡ�
4) �ڲ�ͬ�¶���, ����������ڲ�ͬĦ���������������ϵ�����ճ��ֵ, ��˵���ڲ�ͬ�¶�������, ��������ϵ�γɵ�������������������ͬ��
�����
[1] ��MudersbachD,DrissenPM,MichaelK��hn,etal.Viscosityofslags[J].SteelResearch,2001,72(3):8690.
[5] ��CuptaSK.ViscosityofPbO SiO2melts[J].MetallurgicalandMaterialsTransactionsB,1995,26B(2):281287.
[15] ��BlanderM.MoltenSaltChemistry[M].California:IntersciencePublisherPress,1963.569.