Ce������Al��3.5%NaCl��Һ�и�ʴ��ΪӰ����о�
������ѧ������ѧ�빤�̼���ѧԺ
������ѧ��ѧ�뻯��ѧԺ
������ѧԺ
ժ Ҫ��
ϡ��Ԫ�ؼ��京�������Ͻ���ʴ���ܵ�Ӱ�켰����������Ͻ����õ���Ҫ�о�����,���ø�Ƶ���������Ʊ�Al1-xCex(x=0,0.2%,2.0%(ԭ�ӷ���))�Ͻ�,ͨ��X�������䡢����������绯ѧ���ԡ�ɨ��羵�����ȷֱ���Ʊ���Al1-xCex�Ͻ�Ľṹ������λ����ɨ�輫�����ߡ�������绯ѧ��ʴǰ�������ò�ı仯�������о�;��Al1-xCex��3.5%NaCl��Һ����ʴ�������溬���Ĺ�ϵ������ϵͳ�ķ������������:����Cl-���ӵĴ���,����3.5%NaCl��Һ�з�����ʴ�ƻ�;ϡ��Ce�ļ����ܹ�ϸ������,���ƺϽ��۽ṹ,����Cl-���ӶԵ�ʴ��Ӱ��;CeԪ���ڸ�ʴ����㸻��,�������γ������ۻ�Ĥ,��ߺϽ���NaCl��Һ�е���ʴ����;��ϡ��Ce(0.2%)�ļ���ʹ�Ͻ���Ը�ʴ��λ����,��ʴ�����ܶȽ���,��ʴ���ܸ�������;������Ce����������,�����������������е��ܽ�Ⱥ�,�����潫�γɽ����仯����,����������仯���������Ĵ���ʹ�Ͻ����ʴ������������,Ce����Ϊ0.2%�Ͻ����ʴ���ܱ�Ce����Ϊ2.0%�ĺϽ�Ҫ�á����кϽ�ʴ�����Ҫ����ΪAl2O3��
�ؼ��ʣ�
��ͼ����ţ� TG172
����飺�º�÷(1973-),Ů,���Ͻ�����,˶ʿ,����;�о�����:�������ܲ���(E-mail:chenhm@gxu.edu.cn);
�ո����ڣ�2010-11-15
����������Ȼ��ѧ����(50761002);�����������(0832007);�����о����������¼ƻ���Ŀ(105930903079)����;
Effect of Ce on Corrosion Behaviors of Aluminum in 3.5% NaCl Solution
Abstract��
The effect and mechanism of rare earth elements on the corrosion-resistance of aluminum alloys was an important topic of development of aluminum alloys.Al1-xCex(x=0,0.2%,2.0%(atom fraction)) alloys were prepared by high-frequency melting method.The structure of alloys,potentiodynamic linear polarization cure,the changes of the surface morphology by immersing and electrochemical corrosion processing were investigated by X-ray diffraction,metallurgical microscope,electrochemical analysis,scanning electron microscopy and EDS.The influence of Ce content to the corrosion resistance of aluminum in 3.5% NaCl solution was systematically analyzed.The results indicated that pitting corrosion occurred for Al1-xCex in 3.5% NaCl solution due to the presence of Cl-.The addition of Ce in aluminum refined the microstructure of the alloy,and weakened the impact of Cl-.Ce aggregated in the surface of alloys during corrosion,which was beneficial to the formation of a continuous passive film,and the corrosion resistance of aluminum alloys was improved.The corrosion resistance was improved with minor addition of Ce(0.2%),which increased corrosion potential and decreased corrosion current.The corrosion resistance of Al99.8Ce0.2 was better than that of Al98.0Ce2.0 due to the existence of interface between the aluminum and intermetallic compound formed when the content of Ce was larger than the solution limit of Ce in Al.Al2O3 was the mainly corrosion products for the considered alloys.
Keyword��
Al1-xCex alloy;electrochemistry;corrosion behavior;
Received�� 2010-11-15
�������Ͻ�, ���ھ����������������, ���ܶ�С�� �����Ժá� ��ʴ������, ���㷺��Ӧ���ڸ������� ���ڴ����䵼���Ժ���ʴ��������Ͻ�, ����Ӧ���ڵ��ӵ�������ҵ, �й�����ʴ�������˽϶��о�
����ͨ�����Ӳ�ͬ�ɷֵ�Ce�Դ�����Cl-���ڻ����µ���ʴ����Ӱ����з���, ��ͨ��������3.5% NaCl��Һ�н��ݼ��绯ѧʵ����, �������溬��������ʴ���ܵ�Ӱ�졣
1 ʵ ��
Al1-xCex (x=0, 0.2%, 2.0%)�Ͻ���Ʊ�����Ϊ: �Ͻ��Ʊ����õĽ������ȷֱ�ΪAl(99.99%)��Ce (99.5%)�� �������ڿ�������������, �����ںϽ��Ʊ�����������Ar���������÷��Ժ���յ绡¯���Ʊ�Al-10Ce�м�Ͻ�, ������������4��, ʹ��Ͼ��ȡ� Ȼ������ɷ����������Ϻ�����ܷ���ʯӢ��������, �ø�Ƶ��Ӧ¯�����õ��Ͻ� ���������ľ���ṹ���ձ���ѧX����������(Rigaku-1350)���з���, ����Cu K������(��=0.1542 nm)�� �绯ѧ������Ʒ�ǽ��Ʊ��ĺϽ���û�����֬�ܷ�, ����һ��������, ��1200�Ž���ɰֽ��ĥ, ����2.5 ��m���ʯ��ĥ���⡣ ��XJZ-6�ͽ��������Բ�ͬ����ʱ�������ı�����ò���з����� �绯ѧ����ʹ������Gamry�绯ѧ����վ(PCI4/750), ��������ɨ�跨���Զ���λ��������, ɨ���ٶ�Ϊ1.0 mV��s-1, ɨ���ѹ��-1.5��0.0 V, ��ʴҺ����Ũ��Ϊ3.5% NaCl��Һ, �����Լ�Ϊ������, ������ˮ����, δ�������� ���Ե绯ѧ��ʴ�������ò���н����SEM������
2 ���������
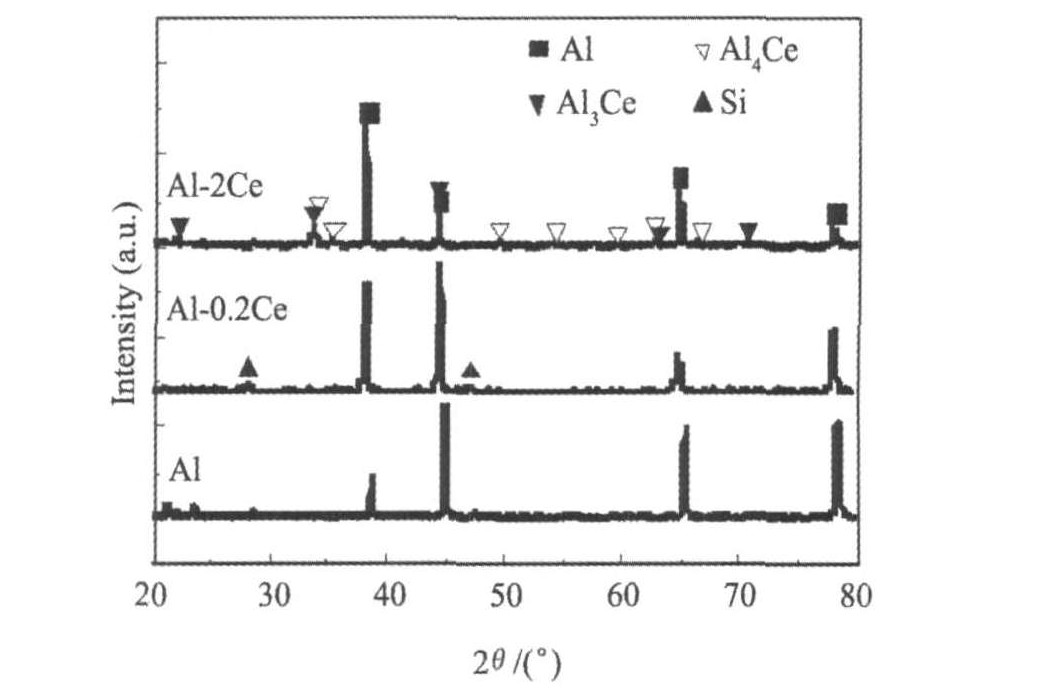
ͼ1�������Ʊ�Al1-xCex�Ͻ��XRDͼ�ס� ������Ce�ļ���(0.2%), ��ͼ1��������������, ������������ͽǶ��ƶ�, ��Ҫ�����ܽ��������γ�Al(Ce)�Ĺ�����, �������ԭ�Ӱ뾶������, ����������ʹ�������ͽǶ��ƶ��� �������϶�(2.0%)ʱ, ���γ�Al(Ce)��������, ���γ���������Al3Ce��Al4Ce�����仯���
ͼ2������Al1-xCex�Ͻ���3.5%NaCl��Һ�н���20 h��Ͻ�ı�����ò�� ���Կ���, ����20 h���ݺ�, ��Ʒ�ľ����������ֳ���, �������˵�ʴ�� ���ڴ���, ����Ϊ��״, �ߴ�ϴ�, ���й������, �ھ�������ֲ����ֵ�ʴ�� ������0.2%��Ce��, ������ò��ʼ��ò�����, �ߴ��봿�����������С�����н���, ��ͬ����ʱ���µ�ʴ�������١� ��Ce��������2.0%ʱ, ��������ϸ��, ����Ҳ��Ϊ����, ��ʴ��������, ��ʴ���ᡣ ˵������Al1-xCex�Ͻ�, Ce�ļ�����ʹ����ϸ��, ����������NaCl��Һ�еĵ�ʴ��������, ��ߺϽ���ʴ����
��ͼ3���Կ���, ������3.5% NaCl��Һ��, ���Ž���ʱ�������, 20 hʱ���總�����ֵ�ʴ(��ͼ2), ֮��ʴ�ڵ�ʴ������չ, ��40 hʱ�Ѿ��������Ե�ʴ��, ʱ���ټ�������, ʴ���ؾ��緢չ, ������һƬ(80 h), ��160 hʱ, ��������ʴ��һ�����µ�, ��������������ƻ��� ��ͼ4���Կ���, ��������������丯ʴ�����봿������, ֻ�Ǹ�ʴ�̶�Ҫ�����ࡣ ������������Կ���, ���Ž���ʱ�������, ��ʴ��ʼ������ʽ�ǵ�ʴ, ���ŵ�ʴ������չΪʴ��, Ȼ�����ž�����չ, ���չΪȫ�港ʴ��
ͼ1 Al-(Ce)�Ͻ�XRDͼ��
Fig.1 XRD patterns of Al-(Ce) as-cast alloy
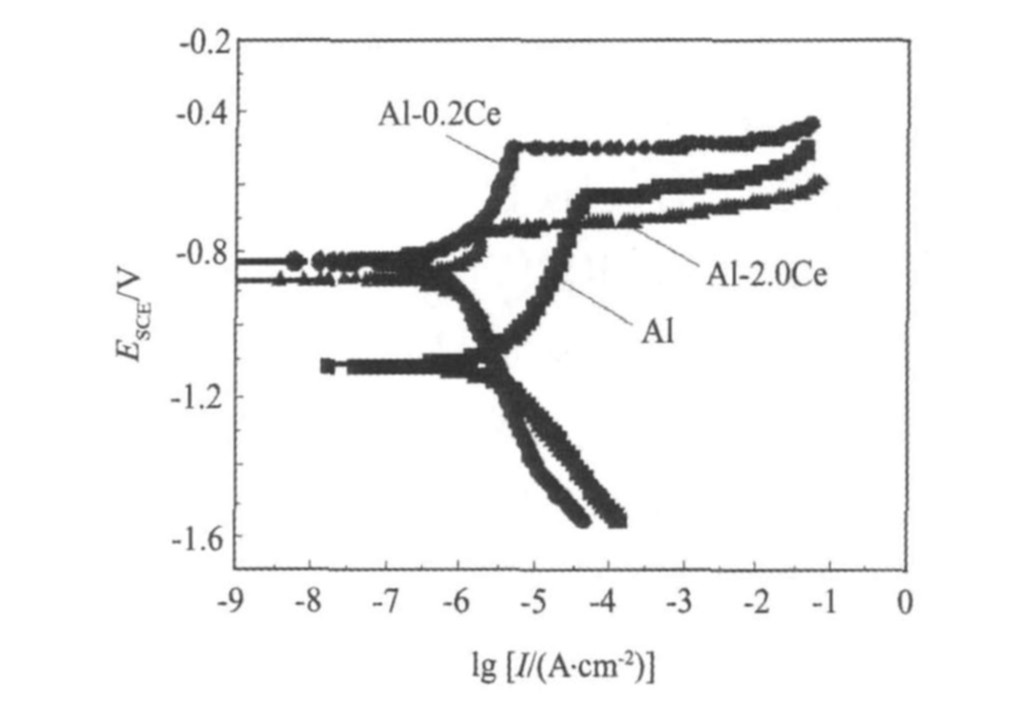
ͼ5Ϊ�����۵ĺϽ���3.5% NaCl��Һ�ж���λ����ɨ�輫������, ��1Ϊ��Ӧ�õĸ�ʴ������ ��ͼ5���Կ���, ��3.5% NaCl��Һ��, Al-(Ce)�Ͻ����߶������˶ۻ���, ���ŵ�λ�ļ�������, ���ﵽ�ٽ��λ��, ������������, �Ͻ������ָ�ʴС��, ��������ʴ�� ���ٽ��λΪ������λ, ����ʴ��λ(��ͼ2��3, �ǽ����·����ĵ�ʴ����)�� ����λ����ɨ�����ʱ, �����������ԭ��������������������, ��Ȼ����ϵ�ܹ�������̬, ������λ��������ʱ, ��δ�ﵽ���ۻ���λ��ǰ, �Ͻ�����һЩ���ϵĶۻ�Ĥ�Ϳ�ʼ�ֲ��ƻ��� �ڶۻ�Ĥ�����ֲ��ƻ���, �Ͻ�����Ծ�����������ܶȽ��������ܽ�, ����, ��ʱ�����缫�ܵ����������ܶȼ�������, �������߾ͳ���ͼ5��ʾ����״�� ��ʹ�����ߵĶۻ������Ϊ���̡� �����缫������ָ�ʴС��, ������ʴ�� Ce�ļ���, ʹ�Ͻ���Ը�ʴ��λEcorr����, ��ʴ�����ܶ�Icorr����, ˵��ϡ��Ce�����Al��NaCl��Һ�е���ʴ������ ��������ϡ���ĸ���, ��Al���������ܹ����ʡ� ϸ������������, �ڸ�ʴ��ϵ�������γɶۻ�Ĥ, ��ֹCl-���Ӷ�Al�������ʴ, ���ٵ�ʴ�ƻ�

ͼ5 Al1-xCex�Ͻ���3.5%NaCl��Һ������ɨ�趯��λ��������
Fig.5 Potentiondynamic polarization curve for Al1-xCex alloys in 3.5% NaCl solution
��1 Al1-xCex�Ͻ���3.5% NaCl��Һ�кϽ�ĸ�ʴ����
Table 1Corrosion parameters of Al1-xCexalloys in 3.5% NaCl solution
| Alloys | Ecorr/V (vs. SCE) |
Icorr/ (��A��cm-2) |
bA/ V |
bK/ V |
Rp/ (����cm2) |
| Al | -1.1100 | 4.000 | 0.3458 | 0.2850 | 16979.3 |
| Al-0.2Ce | -0.8196 | 0.914 | 0.2347 | 0.4703 | 74456.2 |
| Al-2.0Ce | -0.8746 | 1.220 | 0.1629 | 0.5039 | 43901.9 |
Ce�ļ������ԺϽ����ʴ����Ҳ��Ӱ�졣 ��ͼ5�ɼ�, ����0.2%��Ce, �ܹ�ʹ�Ͻ�ʴ�����ܶ�Icorr����, �������λ; ����������ߵ�2.0%ʱ, Icorr��������, ��������λ���Խ���, ����Ҫ����δ����ϡ��Ce�Ĵ����Ļ�����λ, ʹ�úϽ�Ķۻ������������̡� ���ܵ�ԭ����Al-2.0Ce���γ�Al3Ce��Al4Ce�����仯����, ���ڲ�ͬ���縺�Բ���, ��紦������ƻ�
Ϊ�˽�һ���˽�绯ѧ��ʴ����������״̬, ѡȡAl-0.2Ce�Ͻ����ɨ��羵(SEM)���������� ��ͼ6�ͱ�2������������Կ���, 3������Ԫ�سɷֲַ����, ��Ҫ����Al, O, Si��Ce��Ԫ��, ˵���Ͻ�������Ҫ����Al2O3, Si�Ľ��������ڲ���ʯӢ�����ܷ���, ��Ƶ����ʱSiO2��Al��Ӧ����Ͻ���档 Ce�ĺ����Դ��������ɷ�, ����ϡ��Ce�港ʴ�����ڱ��渻��, �Ӷ������ڶۻ�Ĥ���γɡ� ǿ��ʴ����(ͼ6(a)�е�C��)����Ԫ�غ������ڻ���A�еĺ���, ������ʴ��B������������С��A�к���, ��Ҳ˵��C��Al2O3�����ϸ�, ��B�к����ϵ�, Ҳ֤���˸ø�ʴ��Ӧ��Ҫ������Al2O3��
ͼ6�ͱ�2�����˸�ʴ����ϰ��ͽ�������������������ݡ� ���Կ���, �ϰ�������Ҫ�ɷ���O��Al, Si�ĺ�������; ����������Si�������� ��˵����Ʒ����������ʵ�����Si�Ľ����γ�Al-Si��Ԫ��ĸ�ʴ��� ���Կ������ʵ�����Һ��ϵ���ܽ�Ƚ�С, ���Ÿ�ʴ�ķ�չ���������渻��, ��ɱ���Si���������ࡣ ���ڸ��ʵ��������ĸ�ʴ��λ�IJ��, ������Ĵ��ڻ�ԺϽ�ʴ�������һ����Ӱ�졣
ͼ6 Al-0.2Ce�Ͻ�绯ѧ��ʴ��ɨ��羵ͼѡ��������
Fig.6 Constituency energy spectrum analysis (EDS) of Al-0.2Ce after the electrochemical corrosion (a) Surface analysis; (b) Point analysis
��2 ɨ��羵���������(%, ԭ�ӷ���)
Table 2Results of SEM energy spectrum analysis (%, atom fraction)
| Sample | Al | Ce | O | Si |
| A | 85.92 | 00.37 | 06.37 | 07.34 |
| B | 90.05 | 00.41 | 04.43 | 05.12 |
| C | 76.56 | 00.49 | 10.06 | 12.89 |
| D | 90.70 | - | 06.74 | 02.55 |
| E | 37.93 | - | 14.05 | 48.02 |
3 �� ��
����Al1-xCex�Ͻ���3.5% NaCl��Һ�и�ʴ, ����Cl-�Ĵ���, �Ͻ���������ʴ, ���港ʴʱ����ӳ��ؾ�������Χ��չ, ���շ���ȫ�港ʴ��
��ϡ��Ce(0.2%)�ļ���ʹ�Ͻ���Ը�ʴ��λEcorr����, ��ʴ�����ܶ�Icorr����, ���Ce�ĺ����Ը�ʴ���ܵĸ��������ԡ� Ce�ܹ����ƺϽ��۽ṹ, ϸ������, ���Ÿ�ʴ�ںϽ���渻��, �ٽ��ۻ�Ĥ���γ�, ������Cl-���ӶԸ�ʴ���к�����, �Ӷ���ǿ�Ͻ����ʴ������ ���ϸߵ�Ce�����������������������γɶ�ʹ����ʴ�����½���
�������������Al1-xCex�Ͻ�ʴ������Ҫ��Al2O3��
�����
[9] Szklarska-Smialowska Z.Pitting corrosion of aluminium[J].Corros.Sci.,1999,41:1743.