���±�ţ�1004-0609(2009)06-1148-07
��L113BΪ������Լ��Ʊ�W/O/WҺĤ����
��ˮ�е�Cr(��)
�λ�ΰ��֣ ������ ����������
(���ϿƼ���ѧ ���Ͽ�ѧ�빤��ѧԺ������ 621000)
ժ Ҫ��
��˫ϩ���������ǰ�(L113B)��Ϊ������Լ�������������(TBP)��Ϊ���壬ú����Ϊϡ�ͼ���NaOH��Һ��Ϊ��ˮ�࣬�Ʊ�W/O/W��˫����Һ�������黯�����ٶȡ��黯ʱ�䡢����ͱ�����Լ�������������ҺŨ�ȡ���ȡʱ�䡢���ڱ��Լ���ˮ�ȵ����ضԸ���ϵ�ȶ��Լ�Cr(��)��ȡ�ʵ�Ӱ�졣ͨ���Ƚϲ�ͬ�����鷽������Һ���յ�Ӱ�죬��ҺĤ��ȡ�������з����������������1.0 mol/L�����Ậ����Һ�У�����ϵ�������õ��ȶ��ԣ�ҺĤ���������Լ����������Խ��ͣ�Cr(��)����ȡ�ʸߴ�99.4%��
�ؼ��ʣ�
��ͼ����ţ�TF 803.23 ���ױ�ʶ�룺 A
W/O/W emulsion liquid membrane prepared using L113B as
surfactant for separation of Cr(��) from waste water
LIAO Hui-wei, ZHENG Min, MU Lan, MENG Yan-yan
(College of Materials Science and Engineering, Southwest University of Science and Technology,
Mianyang 621000, China)
Abstract: The water in oil in water (W/O/W) double emulsion was prepared using L113B as surfactant, tributyl phosphate (TBP) as extractant, kerosene as diluent and NaOH solution as internal aqueous phase. The effects of various parameters on the stability of emulsion liquid membrane and extraction efficiency of Cr(��) were discussed, which include the speed and time of emulsification, extractant and surfactant concentrations, internal phase concentration, extraction time, volume ratio of the membrane phase to internal stripping phase and that of the emulsions to the aqueous external phase. The effects of different demulsification methods on the recovery of emulsion were compared, and the extraction mechanism was studied. The results show that in the 1.0 mol/L sulphuric acid solution, the rates of swelling and breakage of emulsion liquid membrane decline and the extraction efficiency is 99.4%.
Key words: double emulsion; chromium; separation; enrichment
������ˮ��Դ������Խ��Խ�ܵ���ҵ�����Ĺ�ע[1]�����Ѱ��һ�־�����Ч�ķ���������д�����Ϊ�˹���о������߹�ע��һ���ص㡣Ŀǰ������Ժ�����ˮ�Ĵ���������Ҫ�л�ѧ������[2]���绯ѧ������[3]�����ӽ�����[4]��������[5?8]��Ĥ���뷨[9]�ȡ����У�ҺĤ������һ������ķ�����ᴿ�����������Ч�����á��������ص㣬�ڶ������õ�Ӧ��[10]��Ȼ��ҺĤ���ȶ��ԡ������Լ�������3�����������Ȼ����ԼҺĤ���뼼���ƹ��Ӧ����������[11]�������Щ��������غܶ࣬�����黯����ѡ���Լ�Ĥ������֮��ı�����ϵ����ؼ�����[12]������������ʹ��ҺĤ������ȡCr(��)[13?15]���о��У�������Dz���Span80��Ϊ�黯���Ʊ���״ҺĤ��ʵ���о�������Span80�Ʊ�����״ҺĤ�����Ի����е����ͽϴ���ҺĤ�ȶ����½���ʹ����Ӧ���ܵ�һ���̶ȵ����ơ���ˣ��������߲���˫ϩ���������ǰ�����Span80�Ʊ���Һ��������Һ�Ʊ����̡���ȡ�����Լ�������ֵı�����ϵ��ҺĤ�ȶ��ԡ������ʺ�Cr(��)��ȡ�ʵ�Ӱ�������ϸ���о���
1 ʵ��
1.1 ��Ҫ�������Լ�
��ʵ����������������?�ɼ�?������ֹ���UV?3600��AA2610ԭ�����շֹ��ȼƣ�JB40?C�͵綯��������pHS?3C������ʽ��ȼƣ���ѹ��������������ʵ�������Լ�������������(TBP)���ظ���أ�˫ϩ���������ǰ���Span80��ú��(��ҵƷ)��NaOH������ҩƷ��Ϊ������������ˮΪʵ�������ơ�
1.2 ʵ�����
1.2.1 ��Һ�Ʊ����ȶ��Բ���
��25 ���£��ֱ���˫ϩ���������ǰ���Span80Ϊ������Լ�����TBP��ú�Ͱ������5?20?75�ı�����4 500 r/min��ת���½�����Ⱥ�������Ũ��Ϊ0.1 mol/L��NaOH��Һ������������ֱ����Һ��ɢ���ȡ�ȡһ��������Һ���뵽1.0 mol/L������������Һ�У���250 r/min��ת���������ⶨ������ҺpHֵ�Լ�ҺĤ����ı仯��������Һ���ȶ��ԡ�
1.2.2 Cr(��)����ȡ
��Ũ��Ϊ100 mg/L��K2Cr2O7ˮ��Һģ�⺬����ˮ����H2SO4(1+1)���ڷ�ˮ��Һ�е�pHֵ������״Һ��ģ���ˮ�������3?10��ϣ���250 r/min��ת����ȡ5~6 min��Ȼ���÷ֲ㡣����Һ��������� 2 000 V��ѹ���������飬���÷ֲ㡣ʹ��ԭ�����չ����ⶨ�²���Һ��Cr(��)�ĺ�����������ȡ�ʣ��ϲ��л�����������Ʊ���Һ��
2 ���������
2.1 ��Һ�Ʊ�������ѡ�����ȶ��Բ���
2.1.1 ������Լ���ѡ��
ȡ���ݵ�������˫ϩ���������ǰ���Span80����ʵ�鷽���Ʊ�����Һ���뵽Ũ��Ϊ1.0 mol/L��������Һ�У���250 r/min��ת�ٽ���,��1~10 min�������ⶨ������ҺpHֵ����Һ����ı仯���ֱ���ʽ(1)��(2)������Һ�ı���������(y)��������(��)��
![]()
![]()
ʽ�� VtΪҺĤ��ȡ��������V0ΪҺĤԭʼ�����![]() ��
��![]() �ֱ�Ϊ������ȡǰ��H+��Ũ�ȣ�Vin��[OH?]in�ֱ�Ϊ������ʼ�������OH?��Ũ�ȣ�Vo��Ϊ������ȡ��������ʵ������ͼ1��2��ʾ����ͼ1��2��֪��ʹ��L113B�Ʊ�����Һ�ı��������ʺ������ʾ���ʹ��Span80�Ʊ�����Һ��Ҫ�͡�������ΪL113B�ķ���������Span80��Ҫ���ݡ�λ���� ����[16?17]ԭ����֪��Һ��֮������ѧ��ֵ����ʱ���ų���������Ч��ֹҺ����ۼ������ѡ�ͬʱ��L113B���������ܽϺã���ǿ�ỷ���в��������ֽ⣬ʹ�����ڱ�����Լ��ֽ�������Ĥ�������ʽ��͡���˱�ʵ��ʹ��L113B����Span80��ΪĤ����黯����
�ֱ�Ϊ������ȡǰ��H+��Ũ�ȣ�Vin��[OH?]in�ֱ�Ϊ������ʼ�������OH?��Ũ�ȣ�Vo��Ϊ������ȡ��������ʵ������ͼ1��2��ʾ����ͼ1��2��֪��ʹ��L113B�Ʊ�����Һ�ı��������ʺ������ʾ���ʹ��Span80�Ʊ�����Һ��Ҫ�͡�������ΪL113B�ķ���������Span80��Ҫ���ݡ�λ���� ����[16?17]ԭ����֪��Һ��֮������ѧ��ֵ����ʱ���ų���������Ч��ֹҺ����ۼ������ѡ�ͬʱ��L113B���������ܽϺã���ǿ�ỷ���в��������ֽ⣬ʹ�����ڱ�����Լ��ֽ�������Ĥ�������ʽ��͡���˱�ʵ��ʹ��L113B����Span80��ΪĤ����黯����
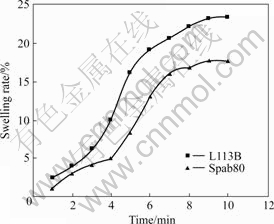
ͼ1 ��Һ��������ʱ��Ĺ�ϵ
Fig.1 Relationship between time and swelling rate of emulsion
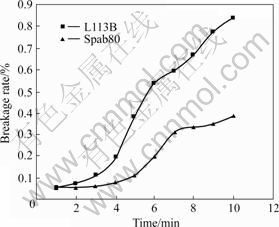
ͼ2 ��Һ��������ʱ��Ĺ�ϵ
Fig.2 Relationship between time and breakage rate of emulsion
2.1.2 �黯�����ٶȵ�ѡ��
�黯�����ٶȶ���Һ�ȶ��Ե�Ӱ����ͼ3��ʾ����ͼ3��֪��ת����500~2 000 r/minʱ��Ĥ�������ʽϸߣ���ʱ��Һ����֮�������Ե�������棻��תͨ��2 000~4 000 r/minʱ��ҺĤ�����������Խ��ͣ�ת��Ϊ4 500 r/min����ʱ��Ĥ���ȶ���ã���Һ�����������ɫ��ת�ٴ���4 500 r/min֮��Ĥ������������������ơ���������ת�ٽ�СʱҺ�νϴ�����Լ���������Һ��ɢ�����ȣ�ʹ���γ�Һ�ε��л����б�����Լ���Ũ����Խϵͣ��������黯Ч�ʣ����ҽϴ��Һ��������������Ѹ�ٳ�������һ�������������ʡ���ת�ٽϴ�ʱҺ�α�С��������Լ���������Һ��ɢ���ȣ�����������ҺĤ���ȶ��ԣ�ͬʱ���ڱȱ��������λʱ���ڸ�����ȡ��Ҳ��֮������ת�ٹ���ʱ��������Լ��������������Ч�ؾۼ���ʹ�����������������������ʵ�����ת��Ϊ4 500 r/min��
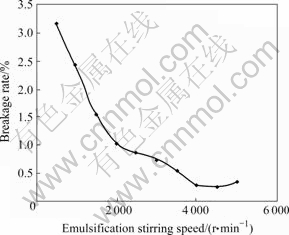
ͼ3 �黯�����ٶȶ���Һ�ȶ��Ե�Ӱ��
Fig.3 Effect of emulsification stirring speed on stability of emulsion
2.1.3 �黯ʱ��Ŀ���
�黯ʱ�����Һ�ȶ��Ե�Ӱ����ͼ4��ʾ����ͼ�ɼ�����Һ�ȶ������黯ʱ�����Ӷ�������ߣ���4~6 min��ҺĤ���ȶ��ԽϺã������黯ʱ����ӳ�����Һ�ȶ������͡�������Ϊ����ʱ�����ʱ���γ��ȶ���СҺ�Σ��������Ľ���ʱ���ʹ�л���ӷ���ҺĤճ�Ƚ��͵���Ĥ����������������黯ʱ��ѡ��Ϊ5 min��
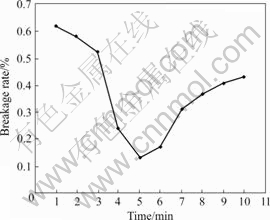
ͼ4 �黯ʱ�����Һ�ȶ��Ե�Ӱ��
Fig.4 Effect of emulsification time on stability of emulsion
2.1.4 ���庬��ѡ��
���庬������Һ�ȶ��Ժ���ȡ�ʵ�Ӱ����ͼ5��ʾ����ͼ5�ɼ����������庬�������ӣ�Ĥ���ȶ������͡�������Ϊ����ļ���������Ĥ�����ԣ���������ʹ���������������Ӹ�����ȡ�����п��Կ������������庬�����ӣ�������ȡ������������ӵ����ƣ������庬��Ϊ20%ʱ��������ȡ�����ڻ��ͣ�����Ҫ�Ǵ�ʱ�����������ӽϿ����¡���Ȼ�������庬�������ڸ�����ȡ�������������������Ӷ����ĵ���ҺҲ��֮���ӣ�����ۺϿ���ѡ�����庬��Ϊ20%��
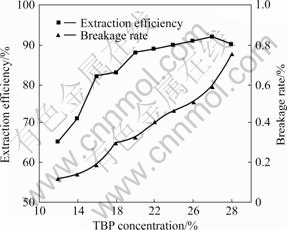
ͼ5 ���庬������Һ�ȶ��Ժ���ȡ�ʵ�Ӱ��
Fig.5 Effect of extractant concentration on stability of emulsion and extraction efficiency of Cr(��)
2.1.5 ������Լ���ϡ�ͼ������ض�Ĥ�ȶ��Ե�Ӱ��
ʵ�鿼���˱�����Լ�������ϡ�ͼ�������������ҺŨ�Ⱥ����ڱȶ�ҺĤ�ȶ��Ե�Ӱ�죬������1���С��ɱ�1��֪��Ĥ���ȶ������ű�����Լ����������Ӷ����ӣ����京������5%ʱ�仯���ڻ��͡�������������״Һ�γɵĹ����У���ˮ������������ͽ��������ӣ�ʹ��ϵ���ڲ��ȶ�״̬[18]��������Լ��ļ�����Ч�ؽ�������ˮ����Ľ����ܣ���ǿ��ҺĤ���ȶ��ԡ�������Լ���Ӱ��ҺĤ�ȶ��Ե�ͬʱ����Ӱ�쵽Cr(��)������������ܵ��Ĵ���������������Լ�������ʹ���������������ӣ�����������������������ܵ��Ĵ���������������Cr(��)����ȡ��Ҳ����������̵��Ѷȡ���ˣ�ʵ��ѡ�������Լ�����Ϊ5%��
��1 L113B��ú�͵���������Լ�NaOHŨ�Ⱥ����ڱȶ�ҺĤ�ȶ��Ե�Ӱ��
Table 1 Effects of volume fractions of L113B and kerosene, NaOH concentration, volume ratios of membrane phase to internal stripping phase on stability of emulsion liquid membrane

ʵ���ԷǼ����ܼ�ú����Ϊϡ�ͼ�����Ŀ�����ڱ������������������ڼ����ܼ��к��ܼ�����֮���γ��������������ԡ�ϡ�ͼ������ӿ�������Ĥ�ĺ�ȣ��Ӷ����Ĥ���ȶ��ԡ������������75%ʱ��Ĥ���ȶ��������Ա仯�����dzɱ��ʹ������������أ�ʵ��ѡ��ϡ�ͼ�������ı���Ϊ75%��
�ӱ�1�л��ܿ�������NaOHŨ�ȵ���0.18 mol/Lʱ��NaOH����Һ�ȶ���Ӱ���С������NaOHŨ�ȵ����ߣ���Һ�������������ߡ�������Ϊ��������ʹ�ò���TBP����������ı�����Լ������ڵ�������������ˮ�⣬ʹ��Ĥ��������ǿ���ȶ����½���NaOH��Ũ�ȹ������Ӱ��������Ľ������ȡ�ʣ���ˣ�ʵ��ѡ��NaOHŨ��Ϊ0.1 mol/L��
�����������Һ�����(���ڱ�)��ѡ�����Һ�ȶ��Ժ�Cr(��)����ȡ�ʶ��нϴ��Ӱ�졣ͨ����1��ʵ�����ݿ�֪�����ڱ�����ʱ��ҺĤ�ĺ�����ӣ��ȶ�����ǿ��Ȼ��ʵ����ȡ������Ҫ����Cr(��)��ҺĤ�������ܵ�����������Ӱ�졣���ڱȹ���Ӱ��������Ľ��뵼����ȡ���½������ʵ��ѡ�����ڱ�Ϊ1.5?1��
2.1.6 ��ȡ�����ٶȶ���Һ�ȶ��Ե�Ӱ��
��ͬ����ȡ�����ٶȶ���Һ�ȶ��Ե�Ӱ����ͼ6��ʾ����ͼ6�ɼ������Ž����ٶȵ������ӣ���Һ�ȶ����ȼ�С��������ת��Ϊ250 r/minʱ��ҺĤ����������͡����ǽ���ʹҺ�ε������仯������ġ���ת�ٽ���ʱ����Һ��ɢ�����ȣ����γɽϴ�������Һ�Σ�Ĥ��ճ�Ⱥͺ�ȼ�С������������������ת������ʱ��Һ�εijߴ���٣���Ч����ȡ�������ת�ٹ���ʱ�������黯����ʹ��Һ�������С���γ�Һ�εı��������������������ߡ����ʵ��ѡ��ת��Ϊ250 r/min��
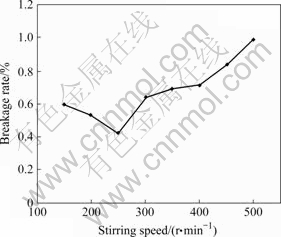
ͼ6 ��ȡ�����ٶȶ���Һ�ȶ��Ե�Ӱ��
Fig.6 Effect of extraction stirring speed on stability of emulsion
2.2 ������ȡ�����������
2.2.1 ��Һ��������Һ����ȵ�ѡ��
��Һ��������Һ�����(��ˮ��)�Ĵ�С��Cr(��)����ȡ���нϴ��Ӱ�졣ȡһ��������Һ��ģ��� Һ���ձ�����ϣ����첻ͬ��ˮ�ȶ���Һ�ȶ��Ժ�Cr(��)��ȡ�ʵ�Ӱ�죬�����ͼ7��ʾ����ͼ7�ɼ���������ˮ�ȵ���������Һ�ȶ���Խ�ã�Cr(��)��ȡ��Ҳ���ߡ����ɴ����ĵ���Һ�����ϴ���ɻ��յijɱ����ߡ���ˣ����ھ���Ч�����ȡЧ���Ŀ��ǣ�ʵ��ѡ����ˮ��Ϊ3?10��

ͼ7 ��ˮ�ȶ���Һ�ȶ��Ժ���ȡ�ʵ�Ӱ��
Fig.7 Effect of volume ratio of emulsion to external phase on stability of emulsion and extraction efficiency of Cr(��)
2.2.2 ��ȡʱ�����Һ�ȶ��Ժ���ȡ�ʵ�Ӱ��
��ȡʱ�����Һ�ȶ��Ժ���ȡ�ʵ�Ӱ����ͼ8��ʾ����ͼ8�ɼ���������ȡʱ������ӣ���ȡ�������ߣ���5 min���һ������ֲ��䣬7 min���������½�������������ȡʱ�������ҺĤ��������Ҳ��ʱ������Ӷ�������ȡʱ����5~6 minʱ����Һ�ȶ� �Ժ���ȡ�ʾ��ȽϺã����ʵ��ѡ����ȡʱ��Ϊ5~6 min��
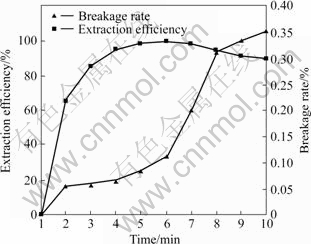
ͼ8 ��ȡʱ�����Һ�ȶ��Լ�����ȡ�ʵ�Ӱ��
Fig.8 Effect of extraction time on stability of emulsion and extraction efficiency of Cr(��)
2.2.3 ���鼰��Һ�Ļ�������
Ŀǰ���õ����鷽����Ҫ�и�ѹ�������鷨����ѧ���鷨�ͼ��ȷ��ȡ�ͨ���Ƚ�3�ֲ�ͬ�����鷽�����֣���ѧ���鷨��Ҫ���뷴�黯��������������ʲ�����Ӱ�쵽���պ���л����ٴ��Ʊ�����Һ�Ը�����ȡЧ��������������Ч��Ҳ���Ǻ����룻���ȷ���Ȼ�ܹ���Ч�ؽ������飬�����ڼ��ȹ����л���л��൱�еı�����Լ��Լ����廯ѧ�ṹ����ƻ���������Һ�Ļ��ճɱ����ߵ����⣻��ѹ�������鷨���ܹ��ڶ�ʱ������Ч�ؽ������飬ͬʱ���л����е����ʳɷֲ�������ƻ�����ˣ�ʵ��ѡ�ø�ѹ�������鷨����2 000 V��ѹ������10 min�����÷ֲ㣬�ϲ�Ϊ�л��࣬�²��Ǻ���Cr(��)��ˮ��Һ������ԭ�����չ����ⶨ����Cr(��)�ĺ������ϲ��л��ྭ��ˮϴ֮����������Ʊ���Һ��ʵ����������Cr(��)����ȡ��Ϊ99.4%����Һ����������Ϊ85.2%����ȡ�������Һ��Cr(��)�ĺ�������0.6 mg/L��
2.2.4 ��ȡ���̵����û���
ˮ��Һ��Cr(��)�Ĵ�����ʽ��Ҫ��HCrO4?��CrO42?��Cr2O72?��HCr2O7?�����������������£�HCrO4?��CrO42?ռ������λ����ǿ�ỷ���У���CrO42?��Cr2O72?�����ת��ʱ��CrO42?��Ũ��ԼΪ(1.26~1.74)��10?2 mol/L[19]����˵���Ũ�ȵ���1.74��10?2 mol/Lʱ����Һ�е�Cr(��)��Ҫ����HCrO4?����ʽ���ڡ�ʵ��ѡȡ�˸���ˮģ��Һ��TBP�Լ����߷�ӦҺ��190~600 nm������Χ�ڽ���ɨ�裬������ͼ9��ʾ����ͼ9��֪����Һ�е�K2CrO4�ֱ���200��278��374 nm���в�ͬ�̶ȵ����գ�TBPֻ��200 nm���������ա��������ˮģ��Һ�м���һ������TBP֮�����������շ�λ�������K2CrO4���������ƣ���������CrO42?��TBP֮���������Ϻ�CrO42?�е���ԾǨ�������¡��ɴ˿ɼ���TBP��ȷ����Я��Cr(��)��������

ͼ9 ����?�ɼ����չ���
Fig.9 UV-Vis absorption spectra
Ϊ�˽�һ���о�TPB����Һ��K2CrO4�����������ʵ�鿼���˲�ͬpHֵ�»����Һ�ڲ���Ϊ350 nm��������ȡ�ʵ�������������������pHֵ�ļ�С������˵��H+�μ���TPB��CrO42?�Ľ�Ϲ��̡�CrO42?�����������º�TBP���������ʽ��ϣ�����ɢ��������TPBЯ��CrO42?������Һ���࣬Ȼ������ˮ���е�NaOH��Ӧ�����ͷų�TBP���壬����ȡ���̿ɹ���Ϊ����������Ӧ��
![]()
3 ����
1) �Ʊ���Һʱ�������������£��黯����ת��Ϊ4 500 r/min��������Լ�������ͷ�ɢ��������Ϊ5?20?75�����ڱ�Ϊ1.5?1��NaOH������ҺŨ��Ϊ0.1 mol/L����ʱ�Ʊ�����Һ�ȶ�����á�
2) ����ˮ��Ϊ3?10ʱ����1.0 mol/L������������Һ�в���250 r/min��ת�ٽ�����ȡ5~6 min��Cr(��)����ȡ�ʿ��Դﵽ99.4%����Һ����������Ϊ85.2%��
3) �÷�������Ч�ظ����ͻ��շ�Һ�еĸ����������ɱ��ͣ���Һ���ظ����á�
[1] ��اӢ, �� ��, ������. ���ķ����븻��[J]. �Ϻ�������ѧ, 1999, 18(1): 33?36.
GAO Pi-ying, DA Hong, ZHOU Tian-ze. Separation and concentration of chromium[J]. Shanghai Environmental Science, 1999, 18(1): 33?36.
[2] ZHOU Xiao-jing, KORENAGA T, TAKAHASHI T, MORIWAKE T, SHINODA S. A process monitoring/controlling system for the treatment of wastewater containing chromium(��) [J]. Water Research, 1993, 27(6): 1049?1054.
[3] KONGSRICHAROERN N, POLPRASERT C. Chromium removal by a bipolar electrochemical precipitation process[J]. Water Science and Technology, 1996, 34 (9): 109?116.
[4] TIRAVANTI G, PETRUZZELLI D, PASSINO R. Pretreatment of tannery wastewaters by an ion exchange process for Cr(��) removal and recovery[J]. Water Science and Technology, 1997, 36(2/3): 197?207.
[5] DAKIKY M, KHAMIS M, MANASSRA A, MER'EB M. Selective adsorption of chromium (��) in industrial wastewater using low-cost abundantly available adsorbents [J]. Advances in Environmental Research, 2002, 6(4): 533?540.
[6] AKSU Z, ?ZER D, EKIZ H, KUTSAL T, CALAR A. Investigation of biosorption of chromium(��) on C. crispata in two-staged batch reactor[J]. Environmental technology 1996, 17(2): 215?220.
[7] DAHBI S, AZZI M, DE LA GUARDIAM. Removal of hexavalent chromium from wastewaters by bone charcoal. Fresenius[J]. Anal Chem, 1999, 363(4): 404?407.
[8] DEMIRBA? A. Adsorption of Cr(III) and Cr(��) ions from aqueous solutions on to modified lignin[J]. Energy Sources, Part A: Recovery, Utilization and Environmental Effects, 2005, 27(15): 1449?1455.
[9] CHAKRAVARTI A K, CHOWDHURY S B, CHAKRABARTY S, CHAKRABARTY T, MUKHERJEE D C. Liquid membrane multiple emulsion process of chromium(��) separation from wastewaters[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 1995, 103(1/2): 59?71.
[10] J?NSSON J ?. Liquid membrane techniques[J]. Comprehensive Analytical Chemistry, 2002, 37: 503?530.
[11] ����, ����. ��״ҺĤ������ȡ�������ӵ��о���չ[J]. �Ϸ�ұ��ѧԺѧ��, 2002, 23(1): 4?7.
SHEN Jiang-nan, HUANG Wan-fu. The progress of study on extraction metal ion by using technology of emulsible membrane [J]. Journal of Southern Institute of Metallurgy, 2002, 23(1): 4?7.
[12] Ҧ�绪, ʯ����, ����ʤ. �黯ҺĤ�ȶ��Ե��о�[J]. ��������ѧԺѧ��, 2002, 16(4): 254?256.
YAO Shu-hua, SHI Zhong-liang, WANG Chuan-sheng. Study on stability of emulsion liquid membrane[J]. Journal of Shenyang Institute of Chemical Technology, 2002, 16(4): 254?256.
[13] ̷����, ����Ȫ, ������, ����Ӣ. ���������������������ȡ�����(��)[J]. ������չ, 2003, 22(12): 1323?1326.
TAN Xiong-wen, YANG Yun-quan, DUAN Zheng-kang, LIU Wen-ying. Extraction of chromium(��) by TBP in hydrochloric acid[J]. Chemical Industry and Engineering Progress, 2003, 22(12): 1323?1326.
[14] ELICECHE A M, CORVAL?N S M, ROM?N M F S, ORTIZ I. Minimum membrane area of an emulsion pertraction process for Cr(��) removal and recovery[J]. Computers and Chemical Engineering, 2005, 29: 1483?1490.
[15] HO W S, PODDART K. New membrane technology for removal and recovery of chromium from waste waters[J]. Environmental Progress, 2001, 20(1): 44?52.
[16] TESCH S, GERHARDS C, SCHUBERT H. Stabilization of emulsions by OSA starches[J]. Journal of Food Engineering, 2002, 54(2): 167?174.
[17] YOSHIOKA K, SAKAI E, DAIMON M, KITAHARAA. Role of steric hindrance in the performance of superplasticizers for concrete[J]. American Ceramagnet Society, 1997, 80(10): 2667?2671.
[18] �Գ���, ���ѹ�, �촺Ӣ. ҺҺ���洫�ʹ��̵ļ�����淨�о�[J]. ��ѧ����, 2007, 35(6): 1?4.
ZHAO Chao-fan, MA You-guang, ZHU Chun-ying. Study on the liquid-liquid interfacial mass transfer process using holographic interferometer[J]. Chemical Engineering, 2007, 35(6): 1?4.
[19] BHOWAL A, DATTA S. Studies on transport mechanism of Cr(��) extraction from an acidic solution using liquid surfactant membranes[J]. Journal of Membrane Science, 2001, 188(1): 1?8.
������Ŀ���Ĵ�ʡ�Ƽ�֧�żƻ�������Ŀ(2008GZ0038)
�ո����ڣ�2008-10-27�������ڣ�2009-03-12
ͨѶ���ߣ��λ�ΰ�������ڣ��绰��13547133951��E-mail: liaohw6709@163.com
ժ Ҫ����˫ϩ���������ǰ�(L113B)��Ϊ������Լ�������������(TBP)��Ϊ���壬ú����Ϊϡ�ͼ���NaOH��Һ��Ϊ��ˮ�࣬�Ʊ�W/O/W��˫����Һ�������黯�����ٶȡ��黯ʱ�䡢����ͱ�����Լ�������������ҺŨ�ȡ���ȡʱ�䡢���ڱ��Լ���ˮ�ȵ����ضԸ���ϵ�ȶ��Լ�Cr(��)��ȡ�ʵ�Ӱ�졣ͨ���Ƚϲ�ͬ�����鷽������Һ���յ�Ӱ�죬��ҺĤ��ȡ�������з����������������1.0 mol/L�����Ậ����Һ�У�����ϵ�������õ��ȶ��ԣ�ҺĤ���������Լ����������Խ��ͣ�Cr(��)����ȡ�ʸߴ�99.4%��


