����CeO2�������Ʊ����ȴ�����������Ӱ��
��ҵ��, ÷ ��, ������, ������
(������ҵ��ѧ ���Ͽ�ѧ�빤��ѧԺ, ����100022)
ժ Ҫ��
��Ce(NO3)3��6H2OΪ��Դ�� NH3��H2OΪ������, �û�ѧ������ͨ���Գ»�ʱ��Ŀ���, �Ʊ��˵���ɢ�ĵ�������CeO2����, ����XRD�� TEM�� ED�� BET�� TG-DTA�Ȳ����ֶζԲ��������ṹ�� ��ò�����׳߶Ƚ����˱����� XRD��������, �Ƶõ�����CeO2����Ϊөʯ�ṹ�Ҿ��ͱȽ������� ͨ�������ȴ������¶Ⱥͳ»�ʱ����Կ������ӵĴ�С�� TEM��ED�������������������Ϊ����, ��ɢ�ԽϺ���Ϊ������ ͨ��TG-DTA������Զ϶����Ʊ���ǰ����ṹʽΪCeO2��1/2H2O��
�ؼ���: ����CeO2; ����; �Ʊ�; �ṹ����; �ȴ��� ��ͼ�����: O614; O643
���ױ�ʶ��: A
Synthesis of single nanocrystal CeO2 and influence of thermal treatment on grain size
HAN Ye-bin, MEI Yan, NIE Zuo-ren, ZUO Tie-yong
(College of Materials Science and Engineering,Beijing University of Technology, Beijing 100022, China)
Abstract: Cerium oxide nanoparticles with single crystal were prepared by precipitation method using Ce(NO3)3��6H2O as cerium resource and NH3��H2O as precipitant through controlling aging time. The phase structure, morphology and nanosize were characterized by means of XRD, TEM, ED, BET and TG-DTA. XRD result shows that the nanoparticles CeO2 prepared by precipitation are fluorite structure with high crystallization integrity.The size of particles can be controlled by adjusting the temperature of thermal treatment and aging time. The results of TEM and ED show that the particles are spherical, dispersed well and single crystal. The products of CeO2��1/2H2O can be deduced according to the result of TG-DTA.
Key words: CeO2 nanoparticles; single crystal; synthesis; structure characterization; thermal treatment
�ҹ�ϡ����Դ�ḻ, Լռ������̽��������80%, ������ĺ�����ḻ[1]�� CeO2��һ�����ۡ� ��;�㷺����Ҫ��ϡ��������, �ѱ����ڷ�����ϡ� �����մɡ� ������ ��������� ���������ռ��ȷ���[2]�� �������CeO2������һЩ�µ����ʺ���;[3]�� �����о�����, ����CeO2���ж��صĴ��������ܺ��¿�������λ��ɢ����, ��˿ɹ㷺Ӧ��������β������������[4]�� ����������[CM(22]��[5]�� pH���в���[6]�� ����ȼ�ϵ���е�������[CM)] ��[7]�� ��ѧ��е�����[8, 9]�ȡ�
��������CeO2��Ѹ�ٷ�չ�㷺Ӧ��, ���Ƕ�����CeO2��Ҫ��ҲԽ��Խ�ߡ� ���, ����CeO2���Ʊ��� �������Ժ�Ӧ���о���Ϊһ��������Ҫ����Ŀ��⡣ Ŀǰ��������CeO2���Ʊ������ܶ�, ���ǹ����Ʊ���������CeO2�ı������١� �������߱���������ͨ��ѧ������, ͨ���Գ»�ʱ��Ŀ���, �Ʊ���������CeO2������������б���; �����˱����¶ȶԷ�ĩ������С��Ӱ�졣
1 ʵ��
��ȡһ������Ce(NO3)3��6H2O(AR)�ܽ�������ˮ����ɾ��ȵ�0.2mol/L Ce(NO3)3��Һ, ����������1~2mL/min���ٶȵμ�2mol/L NH3��H2O��Һ, �μӵ���ȫ��ӦΪֹ, ��������������2h, ��������������·ֱ�»�2h�� 5d��15d�� �����ķ���������� ϴ��(ˮϴ3��, �Ҵ�ϴһ��), Ȼ����70��������и���24h, ���õ���ͬ������CeO2������ĩ�� �Գ»�2h�õ�����Ʒ�ڲ�ͬ�¶����ȴ���2h, �õ���ͬ����������CeO2��
�����ձ�JEOL��˾������JEM-2010����羵�۲�������ò������; ���õ¹�BRUKER��˾D8-advance��X���������ǽ��нṹ����, ����Cu��K��1����, ������ʯī���嵥ɫ���˲�, ��������20 mA, ��ѹ40kV, ɨ���ٶ�4(��)/min, ����0.02��; ��Ʒ��BET����������Micromeritics��˾ASAP2020ȫ�Զ����ٱȱ���������Dz���, ����ǰ��Ʒ����200���³��ѻ4h; ��TA Instruments��˾��STA449C����-���ȷ���������Ʒ���ȷ���, ��������Ϊ10��/ min��
2 ���������
2.1 ����CeO2���ӵ���ò�������۲�
������������ĸҺһ����ʱ, ����Gibbs-ThomsonЧӦ, ������С�����ܽ���ʧ�ʹ����ӳ�������, ��Ostwald�컯[10]�� ����, �ڷ�Ӧ����������, �����������������ڸߵı����ܳ������ڽ���̬, �������ų������̵Ľ���, ���ֽ�������ת��Ϊ���ȶ��Ĺ�̬, �������˶���ת���� ����С�����γɺ�, Һ����ϵ�ͳ�Ϊ����������ϵ, ���ཫ�������С�ķ���չ, �����۽������� ���, �»���ͬ��ʱ���ܵõ���ͬ��ò�ʹ�С�Ŀ����� Ϊ���о����ϳɵ�����CeO2���ӵ���ò��������С, ���Ƕ����Ʊ�������CeO2��Ʒ��������羵����, �����ͼ1��ʾ�� ��ͼ�ɼ�, ���ϳɵ�����CeO2�����ڳ»�ʱ��ܶ�ʱ, �õ���������С��10nm�����ο����ҷ�ɢ�Բ���, ���ڳ»�15d��, �õ�����ԼΪ100nm����״����CeO2�����ҷ�ɢ�Ժܺá� ������CeO2���ӵ�ED��Ƭ(��ͼ1)���Կ���, �ڳ»�ʱ���ʱ, �õ�������Ϊ�ྦྷ�ṹ, ���»�15d��õ�������Ϊ�������ṹ��

ͼ1 ��ͬ�»�ʱ���õ�������TEM��ò
Fig.1 TEM morphologies of particles aged for different time
�������������ԭ�������Һ����������ľ������۽��н���: ���Ʊ�������Ĺ�����, ���˵��γ��ٶȺ������ٶ���Ӱ�������С�Ĺؼ����ء� ��ʵ����, �ڰ���ɺ˺;�����������������, �������ź����������������֮�����ϲ����γɽϴ���������� ����CeO2�������γ�ʱ, �����������������Ӽ����������, ���ɵ���������С����������(��ͼ1(a))�� �ڳ»���, ������ɵ�С��������CeO2�����ڸ߱����ܵ�������, ��������, �γ��������Դ�һЩ������CeO2����(ͼ1(b)); �����ų»����̵ļ���, ������С������CeO2���Ӿۼ����Դ������CeO2������, ͨ�����淴Ӧ�� ������ɢ�������ɢ�����ܺϡ����뵽�Դ������CeO2����֮��, �γɽϴ������CeO2����(ͼ1(c))�� �������֡��ܺϡ��ٶȺܿ�, �����ܺϡ���Ӧ����Ҫ��ʱ��С�����ڿ������ε���Ч��ײ���ʱ��, ����С���Ӻܿ�;ۼ��γ�һ�����������CeO2���ӡ� �»�������, ����������ʵ����������Ԫ���������в���ͨ����������뾧��Ĺ���[11]�� һ����С�����ܽ�ʹ��Һ�еĹ�����������, ��Щ��������ͨ�������������ľ�����ʹ��������, �õ������ϴ�ĵ�������CeO2���ӡ�
2.2 �����¶ȶԷ�ĩ�����ȵ�Ӱ��
������ĩ���Ʊ�������, �¶���ʹ��ĩ�����������۱仯����Ҫ���ء� ��ĩ�ڳ���ʱ�γɵĿ�����С, ���ȸ���ʱ�����ͻ������ž۲�����, ���ڸ��±���ʱ�����������������ԡ� ����о������¶ȶ�����ĩ�۱仯��Ӱ��, �Կ��Ʒ�ĩ����������Ҫ���������塣
2.2.1 X�����������
ͼ2��3��ʾ�ֱ�Ϊ�»�2h��õ��IJ����ڲ�ͬ�¶��±���2h���X����������(111)�����X���������ס�
ͼ2����������70�決�պõ����ͱȽ�������CeO2, �������ű����¶ȵ�����, �ṹ����, ���ǵ���������ϵ�ṹ, �ռ�ȺΪO5h-FM3M��CeO2��ĩ�� ͼ3���Կ��������¶���450������, ������߿�����, ��˵���������������ӵ��ž۵����˰�߿����仯; ������600���߿����Եı�խ, �����ǿ�ȼ�ǿ, �������������ڲ�

ͼ2 ��ͬ�¶��ȴ���2h������CeO2��X����������
Fig.2 XRD patterns of CeO2 calcined at various temperatures for 2h
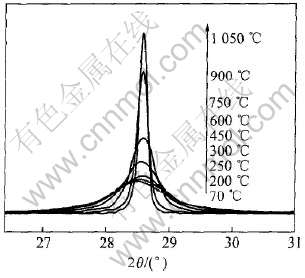
ͼ3 ��ͬ��Ʒ��(111)����������
Fig.3 XRD patterns of(111)crystal face for various samples
�ϵij���, ����������������ƽ�⡣ ��Ҳ˵�����Ʊ��ij�ʼ����Ϊ���žۡ� ��ͨ�����ձ��Ӳ�ž۵Ĺ�����, ��������, ����Ѹ�����ӡ� ��Ϊͨ�����������¶ȿ��ƾ�����С�ṩ���������ݡ�
����Scherrer��ʽ����õ���ϵ����Ʒ��ƽ���������ڱ�1��
![]()
ʽ�� dΪ������ƽ���ߴ�; ����k=0.89; ��=0.1542nm; ��Ϊ����(����); ��Ϊ����ǡ� �ӱ�1���Կ���450�����������仯����, 450�����������������ԡ�
��1 ��ͬ�����¶������ӵ�������С
Table 1 Size of grain calcined at various temperatures

2.2.2 BET����
Ϊ�˿������Ʊ����ӵı���״��, �Ծ���ͬ�¶ȱ���2h������ӽ�����BET����, �������ڱ�2�� �ɱ�2�ɼ�, ����ıȱ�������ű����¶ȵ���������, ������400�����½��͵ķ��ȱȽ�С, ������Ϊ����֮�䷢�������ž�; ����400�����ϱȱ�����½��ĺܴ�, ���������ӵ�Ӳ�žۺ;���������ɵġ� ����X��������ⶨ�Ľ��һ�¡� �������й�ʽ����ƽ������:
D=6/(S ����)
ʽ�� DΪƽ������; SΪ��õıȱ����; ��Ϊ��Ʒ���ܶȡ� �����ɲ�ͬ�¶ȱ����Ʊ���CeO2����ĩ���ܶ�[12], ������ƽ������, ���2���С� �ɱ��ɼ�, �����¶ȵ�����, ��Ʒ������������ ����BET�ȱ�����Խ���õ����������ڸ���X��������������õ��������� ���������������Ӿ��еĸ߱ȱ�����ʹ�䷢���ž�, ���±�����������������, �����õıȱ���ֵ�ϵ�, ��������ƫ��
��2 BET�ȱ�����Խ��
Table 2 Results of BET measurement

2.2.3 ���������Ķ���ѧ����
���������ڱ���ʱ����, �Ǿ�����������ѧ���̡� CeO2������������ѧ����Ϊ[13]:
![]()
ʽ�� DΪ����ʱ�䱺�պ�����ƽ���ߴ�, nm; D0Ϊ��ʼ������ƽ���ߴ�, nm; nΪ��������ָ��, ��һ���̶��Ϸ�Ӧ��CeO2�����������̵Ĵ��ʻ���, ��ͬ������ָ����Ӧ��ͬ���������ʻ���, ����ָ��n�ڲ�ͬ�����������·ֱ�Ϊ1~12���ȡ� ��������[14]�ı���, ��CeO2������ϵn��ȡ5; EΪ�����������, kJ/mol; R�����峣��; T�Ǿ����¶�, K; k0�dz����� һ�������D��D0, D0���Ժ��Բ��ơ� ����ȡ������������:
![]()
����X����������������ľ�����ƽ���ߴ�(����1), ��lnD��1/T��ͼ(��ͼ4), ��ô���õ���б��Ϊ-E/5R��
��ͼ4���Կ���, lnD��T-1��������ȫ�����Թ�ϵ, ������450��ʱ(��T-1=1.383��10-3) �����˹յ�, Ҳ����˵��450��ǰ���������Ļ���Dz�ͬ��: -E1/5R=-0.354, E1=14.72kJ/mol; -E2/5R=-3.147, E2=130.8kJ/mol�� �ɴ˿ɼ�, ������450�����µĻ��ԶԶС��450�����ϵĻ�ܡ� ������������ܱ仯�����غܶ�, ��������ѧ����������Ҫ�ġ� ����X������������BET���Խ��������Ϊ: �ڽϵ��¶���, ���ھ����ߴ��С, ������������[15]�� ȱ�ݽ϶�, �ȱ������, ������Ը�, ��ʱ��������������Ծͺ�С, ��˾���������ܽϵ�; ���ڽϸߵı����¶���, ����Ѹ�ٳ���, �����������������ȶ�, ����ȱ��Ҳ����, �ȱ��������С, ������Խ���, ��ʹ�þ�������������������, ������¾�����������������ӡ�
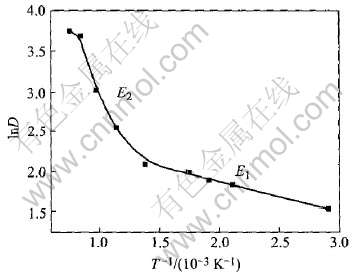
ͼ4 lnD��T-1��ϵ����
Fig.4 Curve of lnD��T-1
��������ļ����֪E1��E2, �����450��������������Ӧ�ô���450�����ϵ������ٶȡ� ����ͨ����Scherrer��ʽ�����ƽ�������ߴ�Ľ������, CeO2�������¶�Ϊ450�����µ������ٶ�ҪС��450�����ϵ������ٶȡ� ������Ϊ�ڵ�����, �����ij�����Ҫ��С�������ճ�������, �˹����Ǽ���������, ���Ծ������������ʲ��� ���ڸ�����, ϸ����Ҫ����, ���־���������һ���־�������Ҳ����һ���־�����С����ʧ�Ĺ���, �Ǿ����ƶ��Ľ���� ��������������ȡ���ھ����ƶ�������, �������ƶ��������¶ȳ�ָ����������[16], �Ӷ�����CeO2��������������
2.3 �ȷ������
һ�������, ��ˮ�������Ʊ���CeO2ǰ����ΪCeO2��nH2O, ����n��ֵһ����0~2֮��[17]�� ͨ����ǰ�����ȷ���(ͼ5)�������������Ĵ��ᾧˮ����Ŀ, ��n��ֵ��
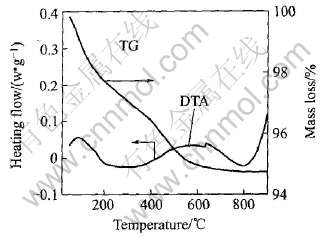
ͼ5 ����CeO2���ӵ�TG-DTA����
Fig.5 TG-DTA Curves of CeO2 nanoparticles
ͼ5��ʾ������CeO2���ӵ�TG-DTA���ߡ� ��ͼ�пɼ����������Ե����շ�, 100�����ҵ����ȷ���Ҫ����Ʒ�е�����ˮ���Ⱥ��ͷų�����ɵ�, ����Ӧ��������ʧ��Ϊ2.3%�� �ɴ˿ɼ�, �Ʊ�������CeO2���ӻ��Ժܸ�, �������տ����е�ˮ��; �ڶ������ȷ�ķ�ֵ�¶ȴ�ԼΪ600��, ������ϵ�нᾧˮ���Ⱥų��ı���, ������ȷ����̬�ȽϿ�, ��Ҳ˵���ǽᾧˮ����ʧȥ, �����������Ӧ��������ʧ��Ϊ3%����, ͨ�������nֵΪ1/2�� ��˿��Զ϶����Ʊ���ǰ����ΪCeO2��1/2H2O��
3 ����
1) ͨ����ͨ��ѧ����������ֱ���Ʊ������ͱȽ�����������CeO2����, ����������ϵөʯ�ṹ, �ռ�ȺΪO5h-FM3M��
2) ͨ�����Ƴ»�ʱ����Եõ���ͬ����������CeO2����, �ô˹��տ��Դﵽ�������Ӵ�С��Ŀ�ġ� �ɹ����Ʊ����˾��������ĵ���CeO2����, ��ɢ�Ժ�, ������100nm���ҡ�
3) BET�������, ����ıȱ�������ű����¶ȵ����߶����͡�
4) ���þ�����������ѧ��ʽ����õ�, ��450��ǰ�����������E1��E2, ˵�������ٶ����¶��������͡� ��X��������������, ���ű����¶ȵ�����, �������ӵ������������ٶȶ��������� ����Ҫ����Ϊ�ڵ�����, ��Ҫ��С�����ճ��Ľ��; �ڸ������Ǿ����ƶ��Ľ��, �������ƶ����������¶ȳ�ָ����������, �Ӷ�����CeO2��������������
5) �ȷ�������������Ʊ��IJ����ܵ�������ʧ��Ϊ5.3%, ���нᾧˮ������ʧ��Ϊ3%, ��˿��Զ϶�ǰ����ΪCeO2��1/2H2O��
REFERENCES
[1]���Dz�, ����÷, �. ϡ�������������Ӧ������������[J]. ���Ƽ����ҵ, 2002, 106(9): 67-68.
JIANG Ya-chang, WANG Qiao-mei, LI Hua. Application and product technology of nano rare earth oxide[J]. Nanotechnology and Industry, 2002, 106(9): 67-68.
[2]�����. �ҹ�ϡ��Ӧ�ÿ�����״����չ��[J]. ���ϵ���, 2000, 14(1): 3-5.
MA Yan-he. Current status and prospects of rare earth applications in china[J]. Chinese Materials Review, 2000, 14(1): 3-5.
[3]Dong X T, Qu X G, Hong G Y, et al. Preparation and application in electrochemistry of naocrystalline CeO2[J]. Chinese Science Bulletin, 1996, 41(16): 1396-1401.
[4]Ф��, ������, ��־��, ��. Ce-Zr������Ĵ��ȼ�������Ч�����е�����[J]. ���Ӵ�, 2000, 14(2): 81-86.
XIAO Li, LIN Pei-yan, YANG Zhi-bo, et al. Phase purity of Ce-Zr solid solutions and their effects on three-way catalysts[J]. Journal of Molecular Catalysis, 2000, 14(2): 81-86.
[5]Izu N, Shin W, Murayama N, et al. Resistive oxygen gas sensors based on CeO2 fine powder prepared using mist pyrolysis[J]. Sensors and Actuators B, 2002, 87: 95-98.
[6]Shuk P, Ramanujachary K V, Greenblatt M. New material-oxide-type PH sensors[J]. Solid State Ionics, 1996, 86-88: 1115-1120.
[7]Mori T, Drennan J, Yarong Wang, et al. Influence of nano-structure on electrolytic properties in CeO2 based system[J]. Journal of Thermal Analysis and Calorimetry, 2002, 70: 309-319.
[8]XU Hua-rui, GAO Lian, GU Hong-chen Gu, et al. Synthesis of solid, spherical CeO2 particles prepared by the spray hydrolysis reaction method[J]. Journal of Ceramic Society, 2002, 85(1): 139-144.
[9]LI Yong-xiu, ZHOU Xue-zhen, WANG Yong, et al. Preparation of nano-sized CeO2 by mechanno-chemical reaction of cerium carbonates with sodium hydroxide[J]. Materials Letters, 2003, 58: 245-249.
[10]½��, ������. ��Ӧ�ᾧ(����)�о���չ[J]. ��ѧ����, 1999, 27(4): 24-27.
LU Jie, WANG Jing-kang. Research process of reaction precipitation crystalline[J]. Chemical Engineering, 1999, 27(4): 24-27.
[11]�����, ʩ��η, ��ά, ��. ��������λ������������Ԫ������ģ���뾧����ò[J]. �˹�����ѧ��, 1999, 28(2): 117-125.
LI Wen-jun, SHI Er-wei, ZHONG Wei-zhuo, et al. Anion coordination polyhedron growth unit theory mode and crystal morphology[J]. Journal of Synthetic Crystals, 1999, 28(2): 117-125.
[12]����͢, ����, ��ΰ, ��. �������Ʊ�CeO2���������[J]. �й�ϡ��ѧ��, 2001, 19(1): 24-26.
DONG Xiang-ting, LI Ming, ZHANG Wei, et al. Preparation and characterization of nano crystalline CeO2 by precipitation method[J]. Journal of the Chinese Rare Earth Society, 2001, 19(1): 24-26.
[13]Baldo J B, Pandlfelli V C, Casarimi J, et al. Grain growth of the lime and periclase phases in a synthetic dolomite[J]. Journal of American Ceramic, 1988, 11(9): 720-725. [14]����. ����������������ϳɼ����ɢ���о�[D]. ��ɳ: ���ϴ�ѧ, 2004.
YANG Zhen-hua. Synthesis and Dispersion Property of CeO2 Nanoparticles by Precipitation Method[D]. Changsha: Central South University, 2004.
[15]�����, �����, ����, ��. ����CeO2���ȴ��������еĽṹ�����ܱ仯[J]. �й���ɫ����ѧ��, 2004, 14(11): 1934-1939.
SONG Xiao-lan, QIU Guan-zhou, QU Peng, et al. Structure and property changes of CeO2 nanocrystalline in thermal treatment process[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(11): 1934-1939.
[16]½����. �����Ͽ�ѧ����[M]. �人: �人��ҵ��ѧ������, 1999.
LU Pei-wen. Science Foundation of Inorganic Materials[M]. Wuhan: Wuhan University of Technology Press, 1999.
[17]YUAN Wen-hui, BI Huai-qing, WEI Chao-hai. Structure characterization of nanosized cerium oxide particles prepared by homogeneous precipitation[J]. Journal of South China University of Technology (Nature Science Edition), 2004, 32(4): 52-56.
�ո�����: 2005-08-01; ������: 2005-11-11
ͨѶ����: ������, ����, ��ʿ; �绰: 010-67391536; E-mail: zrnie@bjut.edu.cn
[1]���Dz�, ����÷, �. ϡ�������������Ӧ������������[J]. ���Ƽ����ҵ, 2002, 106(9): 67-68.
[2]�����. �ҹ�ϡ��Ӧ�ÿ�����״����չ��[J]. ���ϵ���, 2000, 14(1): 3-5.
[4]Ф��, ������, ��־��, ��. Ce-Zr������Ĵ��ȼ�������Ч�����е�����[J]. ���Ӵ�, 2000, 14(2): 81-86.
[10]½��, ������. ��Ӧ�ᾧ(����)�о���չ[J]. ��ѧ����, 1999, 27(4): 24-27.
[12]����͢, ����, ��ΰ, ��. �������Ʊ�CeO2���������[J]. �й�ϡ��ѧ��, 2001, 19(1): 24-26.


