���ᷨ�Ʊ�����һ狀�������
�·���1, 2��������1, 2
(1. ��̶��ѧ ��ѧѧԺ������ ��̶��411105��
2. ��̶��ѧ �����Ѻû�ѧ��Ӧ��ʡ�������������ص�ʵ���ң����� ��̶��411105)
ժ Ҫ��
ժ Ҫ���������ȡ��15.84% P2O5�����ƶ����ȡ�����ᣬ�������谷Ϊ������������з������ᣬ�о�������ʵ�������·�Ӧ�¶ȡ�����ʱ�䡢��Ӧ��Ħ�����Լ������谷���Ϸ�ʽ����������ʵ�Ӱ�죬������������мд����η��Ȼ��Ƶ�ϴ��������о������������25~30 �桢�����谷������Ħ����Ϊ2?1�������谷�ֳ����ݽ�������������������60 minΪ�����谷�������������������ڴ���������������ʴ���99%�������������谷�����мд����Ȼ����ڹ�Һ������1?5���¶�40 ��ͽ���60 min����ˮ����ϴ��3�κ�ɱ���ȫȥ�����ٽ�����������������谷�백ˮ��Ӧ���Ƶ��˷���GB 10205��2001��������һ狀������鱗�Ʒ���ù���·�߿��У���Ӧ�����ºͣ��м�ý�������谷��ѭ��ʹ�ã����Ȼ��Ƹ���Ʒ�������ʯ��IJ���������������Դ�����ģ�������������������谷������Ӱ�죬�ʺ���ƶ����Դ�Ŀ�������
�ؼ��ʣ�
ƶ�������ᷨ�������谷������һ������������Ʊ����ա���
��ͼ����ţ�TD985��TQ442.14�� ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)02-0352-05��
Preparations of monoammonium phosphate and
diammonium phosphate by hydrochloric acid
CHEN Fang-fei1, 2, YANG Li-xin1, 2
(1. College of Chemistry, Xiangtan University, Xiangtan 411105, China;
2. Key Laboratory of Environmentally Friendly Chemistry and Applications of Ministry of Education,
Xiangtan University, Xiangtan 411105, China)
Abstract: The crude phosphoric acid was prepared by the Liuyang poor phosphate ore containing 15.84% P2O5 and hydrochloric acid, and the phosphoric acid was separated using trimeric cyanamide as phosphoric acid precipitant. The effects of reaction temperature, stirring time, the mole ratio of reactants and the washing manner of precipitant on the precipitation rate of phosphorus acid and the wash rate of calcium chloride were emphatically researched. The results indicate that the precipitation rate of phosphoric acid is larger than 99% under the conditions of 25-30 ��, the mole ratio of trimeric cyanamide to phosphoric acid 2?1, two-step precipitation by trimeric cyanamide divided into two portions and separately stirring 60 min. The salt component calcium chloride entrained in the precipitation of trimeric cyanamide phosphate can be fully removed in the mass ratio of solid to liquid 1?5, at temperature 40 ��, stirring time 60 min and repeatedly washing three times with water. Then through the purified trimeric cyanamide phosphate reacting with ammonia water, the products of monoammonium phosphate and diammonium phosphate which conform to GB 10205��2001 standard are fabricated. The preparation conditions of the process are gentle, the middle medium trimeric cyanamide can be recycled, the consumption of sulfur resource is slowed down by calcium chloride by-product substituted for the output of phosphogypsum, the influence of sulfate radical on trimeric cyanamide precipitation is avoided, and it is suitable for the development of low-grade phosphate ore resource.
Key words: poor phosphate ore; hydrochloric acid method; trimeric cyanamide; monoammonium phosphate; diammonium phosphate; preparation process
ƶ��Ŀ�������һֱ�����������е���Ҫ����[1]���ҹ�ƶ����Դʮ�ַḻ��������P2O5�����͡���Ĵ����ô�����Ũ�ȵͺ����ʶ��ȱ�㵼��ʵ��Ӧ�����ޡ�ʪ�����������Ǵ�����ʯ����Ч���������ȷ�������Ⱦ����ܺ�С�������ɱ��͵����ƣ����������̳�����Ʒ�����ᴿ�������ӡ�ʪ�����ᰴ����������IJ�ͬ�ɷ�Ϊ���ᷨ�����ᷨ�����ᷨ�ȡ����ᷨ[2]��ʪ�������������������������������ʯ�࣬���Ĵ���������Դ������1 t�������4~6 t��ʯ�࣬��������ɫ��ѧ��չҪ�����ᷨʹ������粒̸ƣ��ɻ�����ʵ���̬����Ԫ���Ϸʣ��ۺ�Ч����ڴ�ͳ�������泥���������۸������Ӱ�쵱ǰ������Ӧ�ò��ࡣ�����ᷨ[3-4]�������ù�ҵ�������ᣬ��Դ�㷺����Ȼ��ɫ�е�IMI��˾����20����60��������ѽ����ᷨ��ҵ���Ʊ����ᣬ���ù��ղ��ö��������[5]��Ϊ��ȡ��������������ķ��벻��ȫ����ͨ��������һ��ȥ�����豸����Ҫ��ߡ�
����һ狀����������ĵ�һ����Ʒ�������ᷨʪ������Ϊԭ�ϣ��������谷Ϊ��Ӧý�����������ε��о����������в������ױ���[6-8]������δ�����ᷨ�������谷��ϵĹ��ռ���·���о�����������ͨ���������ȡƶ���Ʊ�ʪ�����ᣬ�о������谷����������ʪ��������������һ狀������淋Ĺ���·�ߡ�ϵͳ�о��м�������������谷�ij�����ϴ��������������������Ĺ���������ƶ����Դ�����úͲ�Ʒ����[9]������Ҫ���塣
1 ʵ ��
1.1 ԭ�Ϻ�����
ԭ���У����ƶ������(AR)�������谷(AR)����ˮ(AR)�������У��������JJ-1���������綯��������DF-101S����ʽ���¼���ˮԡ����SHB-��ѭ��ˮʽ������ձã�101-1A�͵��ȹķ�����䣬AB204-N÷����-��������ӷ�����ƽ��
1.2 ʵ��ԭ������������
�����谷�ֳ��۰���ѧ��Ϊ2,4,6-����������ຣ��ṹ�ȶ�����Ԫ���ϴ��������м���Nԭ���ϵĵ������ܶȽϵͣ���ԭ�ӶԳ��������ԣ�pKb1 = 9.0�����������ᷢ����Һ���������Ӧ���������ܵ����������谷��������Ӧ����ʽΪ��
![]()
���ɵ����������谷������ϴ�Ӻ��ٽ�һ���백ˮ��Ӧ�ֱ���������һ李������狀������谷�������Ӧʽ���£�
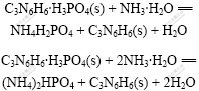
25 ��ʱ�����谷��100 gˮ�е��ܽ��Ϊ0.4 g[10]�������������ɵ��ε��ܽ�ȸ�С�������������������谷���������ɡ������谷������ᷴӦʱ�������еĽ������Ӳ����������谷������Ӧ�������������ʱ�������谷�����������������ɳ������������������������ɿ����Ե����������谷�����������ᷨ�ƵõĴ������к��д������Ȼ��ƣ����������谷����ʱ�Ȼ��ƻᱻ�����д��������У���ˣ��ó�����Ҫ��������ϴ�ӡ����˳�ȥ�������Σ��Ӷ�ʵ�ִ������е��������Ȼ��Ƶķ��롣��ƶ�����ᷨ�Ʊ�����һ狀������淋Ĺ���������ͼ1��ʾ��
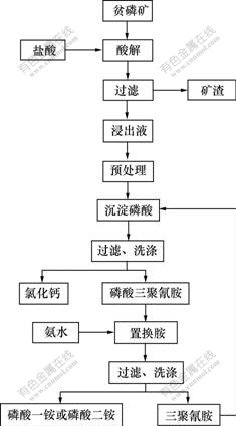
ͼ1 ���ᷨ�Ʊ�����һ狀������淋Ĺ�������ͼ
Fig.1 Process flowchart of monoammonium phosphate and diammonium phosphate prepared by hydrochloric acid
1.3 ��������Ʊ�
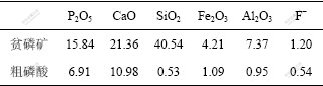
��ȡһ���������(������76 ��m)�������е������ƺ����������������������ȡ������������5%������(V(HCl)?V(H2O)=1?1)����75 ���������һ����衢��Ӧ3 h����ճ��ˣ���ҺΪdz��ɫ�Ĵ�������Һ���ܶ�Ϊ1.295 9 g/mL��Ȼ�ֱ��û���̿��Na2CO3�������������ֲ�ȥ����Һ�е��л��ʡ�F-��Fe3+���õ�Ԥ��������Ҫ�����Ȼ��ƺ�����Ļ��Һ����۵���ɺ����Һ�и���Ҫ�ɷֵĺ������1��ʾ��
��1 ���ƶ�����ɺ��ƵõĴ�������ֺ���
Table 1 Main components of Liuyang poor phosphate ore and
crude acid prepared w/%
1.4 ������ij���
����ͬ���������谷�ӵ�Ԥ������Ĵ������У���10~90 ����ٽ���20~110 min����Ӧ�������������谷�����������ˡ�����ϴ�Ӻ����õ���Ʒ��
1.5 ���������谷�İ�����Ӧ
�����������谷��Ʒ�ڽ�����������ȷ������Ũ��ˮ�������·�Ӧ20 min��Ȼ����ճ��ˣ��˱������谷��ϴ�ӡ������ѭ��ʹ�á�����Һ����Ũ���ᾧ�����˺�����Ƶ�����һ狀������鱗�Ʒ��
1.6 ��������
��Ʒ�е�P2O5��CaO��SiO2��F-�����ֱ������������������������ؼ�ӷ�����������������ͷ�����ѡ��缫���ⶨ[11]����Ʒ�е��ܵ������������ζ����ⶨ[12]��
2 ���������
2.1 ��Ӧ��Ħ���ȶ���������ʵ�Ӱ��
���������谷�������Ħ���ȶԴ���������������ʵ�Ӱ�죬��25 ����¿��ٽ���60 min��ʵ������ͼ2��ʾ����ͼ2���Կ��������������谷������Ħ���ȵ����ӣ�����������ij������������ӡ���Ħ���ȵ���1.0ʱ������ij�����Ϊ55.71%��������Ϊ�ó�����Ӧ���ڹ�Һ���淴Ӧ��ֻ�й������������谷��������Һ�е�����ֱ�ӽӴ��������������︲���ڹ�������ϣ���ֹ�˷�Ӧ�Ľ�һ�����С���Ħ���ȵ���2.0ʱ��������ij����ʴﵽ98.27%����Һ�о��������Ѿ��������谷������������ˣ���ʵ��ѡ��Ħ���ȵ���2.0Ϊ����������������
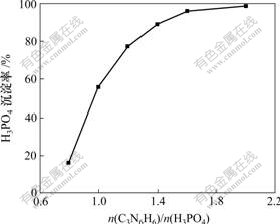
ͼ2 ��Ӧ��Ħ���ȶ���������ʵ�Ӱ��
Fig.2 Effect of mole ratio of reactants on precipitation rate of phosphoric acid
2.2 ��Ӧ�¶ȶ���������ʵ�Ӱ��
�������谷�������Ħ����Ϊ1?1ʱ���������谷��ĩֱ�Ӽӵ���������Һ�У���10~90 ����¿��ٽ���60 min����Ӧ�¶ȶ���������ʵ�Ӱ����ͼ3��ʾ����25 ��ʱ������ij����ʳ��ֳ����ֵ�����¶ȵ���20 ��ʱ����Ӧ�������Ա����������¶Ƚϸ�ʱ�������¶ȵ���������ij����ʷ����½����������������谷���ܽ�ȱ�����¡������ɵij������ȹ��ˣ��ձ��е���Һ��ȴ�����а�ɫ��״�������������ۺϿ��ǣ������谷��������ʱӦѡ���¶�25~30 ��Ϊ�ˡ�

ͼ3 ��Ӧ�¶ȶ���������ʵ�Ӱ��
Fig.3 Effect of reaction temperature on precipitation rate of phosphoric acid
2.3 ��Ӧʱ�����������ʵ�Ӱ��
���¶�Ϊ25 �棬�����谷�������Ħ����Ϊ1?1ʱ����Ӧʱ�����������ʵ�Ӱ����ͼ4��ʾ����ͼ4�ɼ������ŷ�Ӧʱ�����������ij�������ߡ�������Ӧʱ�䳬��60 minʱ������ij��������Ӳ������߱仯����ƽ����Ϊ�˱�֤������������ij����ʴ���55%��ʹҺ�̽���ij�����Ӧ������֣��䷴Ӧʱ���˿�����60~80 min��
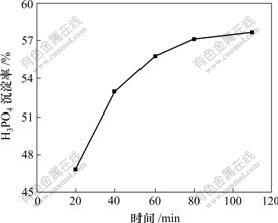
ͼ4 ��Ӧʱ�����������ʵ�Ӱ��
Fig.4 Effect of reaction time on precipitation rate of phosphoric acid
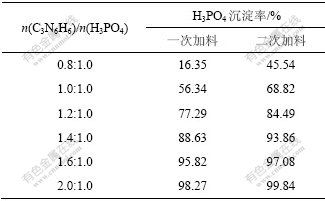
2.4 �����谷���Ϸ�ʽ����������ʵ�Ӱ��
�ڸ�Ħ�����½�ȷ�����������谷�������ֳ�2�ȷݣ��Ȱ�����һ�ݼ����������Һ�У���25 ����¿��ٽ���60 min��ѹ�Һ�������ˡ��ڻ�õ���Һ���ټ����2�������谷��ĩ����ͬ�������½��е�2�����������Ӧ�����Ű���Һ�еĹ�����˷��룬������Һ�е�ʣ�����Ậ�����з�����������2��ʾ���ӱ�2��֪���������谷������ͬ������£����γ�����һ�γ���ʹ�������Ч��������ߣ��ر������������������Ħ���Ȳ��������£�����������ʵ�Ӱ��������ԡ��������谷�������Ħ���ȵ���0.8?1ʱ�������һ�γ�����Ϊ16.35%������Ϊ���γ����ij����ʴﵽ45.54%���������谷�������Ħ���ȵ���2?1ʱ������Ķ��γ����ʴﵽ99.84%����ʱ����Һ�м������е�H3PO4����ת�������������谷����������ˣ����������ʽ����2�μ�����ʽ���С�
��2 �����谷���Ϸ�ʽ����������ʵ�Ӱ��
Table 2 Effect of charging manner of trimeric cyanamide on precipitation rate of phosphoric acid
2.5 ���������谷������ϴ��
�����ᷨ���ƶ���������Һ�У��Ȼ��������е������Ũ�ȴﵽ2.75 mol/L���������谷���������ͬʱ�������൱�����Ȼ��Ʊ��д��������У���ˣ���������������谷�������з���ϴ�ӡ�ʵ�����������¶�����������Ȼ��Ƶ�ϴ�������������谷������Ħ����1?1���¶�Ϊ25 ��ͽ���60 min��ij�����Ʒ������Һ������1?5������30 min�����½���ϴ�ӣ������ͼ5��ʾ���ɼ���20 ��ʱ�Ȼ��Ƶ�һ��ϴ����Ϊ54.68%��70 ��ʱ��һ��ϴ����Ϊ85.54%�����ǵ��¶�̫�������谷�ᷢ��ˮ�⣬�������ε��ܽ��Ҳ��Ӧ����ϴ�ӳ������¶�ѡ��40 ��Ϊ�ˡ��������谷������Ħ����2?1����2�μ�����25 ��ͽ���60 min�����Ļ����Ʒ������ͬ��Һ�����ȡ��¶�Ϊ40 ��ͽ���30 min����ˮ����ϴ��3�Σ����Ȼ��Ƶ�ϴ���ʷֱ�Ϊ70.34%��70.05%��67.68%����ͬ�������¸ı����ʱ��Ϊ60 min����ˮ����ϴ��3�ε��Ȼ���ϴ���ʷֱ�Ϊ84.53%��82.62%��87.75%����ʱ���Ȼ��Ƶ���ϴ���ʴﵽ99.67%����ʵ�����������谷���Ȼ��Ƶij����롣�����������谷������ĸҺ��ϴ��Һ���д�������Ũ�����ᾧ������Ƶø���Ʒ�Ȼ��ơ�
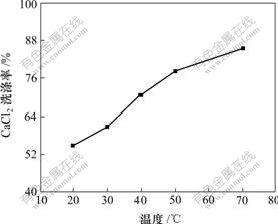
ͼ5 �¶ȶԳ������Ȼ���ϴ���ʵ�Ӱ��
Fig.5 Effect of temperature on wash rate of calcium chloride in precipitation
2.6 ������Ӧ����鱗�Ʒ���Ʊ�
�����������谷�зֱ����Ũ��ˮ���������¿��ٽ���20 min�����ˣ��˱������谷��ϴ�Ӻ�ѭ��ʹ�ã�����������Ļ�����Ϊ96%����Һ�����Ũ����Ȼ����ȴ���ᾧ���ֱ��Ƶ�����һ狀������粒����Ʒ�����������ﵽGB 10205��2001�����Ͻ���һ��Ʒ����Ҫ��
3 �� ��
a. ͨ����ƶ������ᷴӦ�ƵõĴ��������������谷��Һ�̳�����Ӧ���Ƶ����������������谷�м���������Ե��Ȼ��Ƹ�������룬Ȼ���백ˮ��Ӧ�Ĺ��չ��̣��Ʊ��˲�Ʒ�������Ϲ��ұ�������һ狀������鱗�Ʒ��
b. ��25~30 �棬�������谷������Ħ����Ϊ2:1�����������谷�ֳ�2����������������60 min�������£�������ķ����ʴ���99%�������мд����Ȼ����ڹ�Һ������Ϊ1?5���¶�Ϊ40 ��ʱ������ͨ��3��ϴ�������������谷��ȫ���롣
c. �ù��չ��̶���ʯ��ƷλҪ�ߣ���Ӧ�����ºͣ��ܺĵͣ���Һ����˳�����м�ý�������谷��ѭ��ʹ�ã��ʺ���ƶ����Դ�Ŀ������ã���ͬʱ�����Ȼ��Ƹ���Ʒ�����������������ʯ�࣬����������Դ�����ġ�
�ο����ף�
[1] ������, ����־, �鲨, ��. �й�����Դƶ��Σ������ս[J]. ���ι�ҵ, 2005, 37(5): 1-4.
LIU Dai-jun, JIANG Shao-zhi, LUO Hong-bo, et al. The challenge for crisis of phosphate rock deficiency and dilution in China[J]. Inorganic Chemicals Industry, 2005, 37(5): 1-4.
[2] ������, ������. һ�ֶ�ˮ��ʪ�������������շ���: �й�, 01138286.4[P]. 2004-09-01.
HUANG Wen-xiong, GUO Guo-qing. A production technique of wet-process phosphoric acid by dihydrate process: China, 01138286.4[P]. 2004-09-01.
[3] ��ʾ��, ŷ���ݵ�, ����ƽ, ��. ���������������䷢չ����[J]. ����ʱ��, 2003, 17(2): 18-20.
JIN Shi-wei, OUYANG Yi-de, BAO Chuan-ping, et al. Production of phosphoric acid and its development direction[J]. Chemical Industry Times, 2003, 17(2): 18-20.
[4] ������. һ����������ȡ��ȡ����ķ���: �й�, 94111777.4 [P]. 1999-05-05.
GONG Jia-zhu. A method for preparation of phosphoric acid with hydrochloric acid: China, 94111777.4[P]. 1999-05-05.
[5] Hanna A A, Youssef N S, Ali A F. Purification of wet-process phosphoric acid by solvent extraction[J]. Egyptian Journal of Chemistry, 1995, 38(3): 311-317.
[6] ������, ������, ţ����, ��. ѭ������ʪ�����������������ξ���Ч���о�[J]. ���ι�ҵ, 1999, 31(2): 18-20.
ZHAO Sheng-lan, DANG Jie-xiu, NIU Cun-zhen, et al. Purification in producing pure potassium dihydrogen phosphate from wet-process phosphoric acid by circulation method[J]. Inorganic Chemicals Industry, 1999, 31(2): 18-20.
[7] ����֮, ������. ��Ӧýѭ������ʪ�����������������淋�ʵ���о�[J]. �Ĵ����ϴ�ѧѧ��: ���̿�ѧ��, 1997, 1(1): 57-62, 69.
ZHANG Ling-zhi, DANG Jie-xiu. The experimental study of producing feed diammonium phosphate from wet-process phosphoric acid with medium recycle[J]. Journal of Sichuan Union University: Engineering Science, 1997, 1(1): 57-62, 69.
[8] Sheridan R C, McCullough J F. Manufacture of purified diammonium phosphate: United States, 4239739[P]. 1980-12-16.
[9] ֣�Ž�, ������, ���շ�, ��. �����������������������������������ˮ[J]. ���Ϲ�ҵ��ѧѧ��: ��Ȼ��ѧ��, 2002, 33(2): 141-144.
ZHENG Ya-jie, GONG Zhu-qing, ZHANG Qin-fa, et al. Treating municipal living sewage with new type coagulant PPFS[J]. Journal of Central South University of Technology: Natural Science, 2002, 33(2): 141-144.
[10] Chapman R P, Averell P R, Harris R R. Solubility of melamine in water[J]. Industrial and Engineering Chemistry, 1943, 35(2): 137-138.
[11] ��ʯ���������д��. ��ʯ�������[M]. ��һ�ֲ�(3��). ����: ���ʳ�����, 1991: 150-185.
The Writing Group of Analysis of Rock Minerals. Analysis of Rock Minerals[M]. First Fascicule (3rd Ed.). Beijing: The Geological Publishing House, 1991: 150-185.
[12] GB/T 10209. 1��2001, ����һ李����������ܵ������ⶨ(�����ζ���)[S].
GB/T 10209. 1��2001, Determination of total nitrogen content for monoammonium phosphate and diammonium phosphate (Titrimetric method after distillation)[S].
�ո����ڣ�2008-06-25�������ڣ�2008-09-25
������Ŀ������ʡ��Ȼ��ѧ����������Ŀ(06JJ5018)
ͨ�����ߣ�������(1961-)���У���������ˣ����ڣ�������Դ�뻷���Ѻû�ѧ�о����绰��0732-8292229��E-mail: ylx@xtu.edu.cn
4239739[P]. 1980-12-16." target="blank">[8] Sheridan R C, McCullough J F. Manufacture of purified diammonium phosphate: United States, 4239739[P]. 1980-12-16.
" target="blank">[12] GB/T 10209. 1��2001, ����һ李����������ܵ������ⶨ(�����ζ���)[S].GB/T 10209. 1��2001, Determination of total nitrogen content for monoammonium phosphate and diammonium phosphate (Titrimetric method after distillation)[S].


