���±�ţ�1004-0609(2010)S1-s0425-04
���Ȼ�ԭ�Ʊ�������������ѧ�Ͷ���ѧ
ţ��Ƽ����͢�����ź�������־��
(������ѧ ������ұ��ѧԺ������ 110004)
ժ Ҫ��
�Խ��ʯ��������������ϵ����ѧ�����˼��㡣�����������Al��Ca��Mg��Ba��Li��Na�Ƚ�������ԭ���ǿ��еģ���̬�·�Ӧ�ļ���˹�����ܱ仯���ܸ�������ѡ����Щ�����ĺϽ���Ϊ���ϻ�ԭ����DSC����ѧ�������������Al��ԭTiO2��Fe2O3��1 000 �����ҿ�ʼ���У���Al��ԭTiO2��Fe2O��ϵ������CaO����Ӧ�ͺ���1 236 �����ҷ�����Ӧ��
�ؼ��ʣ�
��ͼ����ţ�TF111.13���� ���ױ�־�룺A
Thermodynamics and kinetics of preparation of
high titanium ferroalloy by thermite reaction
NIU Li-ping, ZHANG Ting-an, ZHANG Han-bo, DOU Zhi-he
(School of Metallurgical Science and Engineering, Northeastern University, Shenyang 110004)
Abstract: The thermodynamic of the system of rutile, ilmenite and aluminum powder was calculated. The results show that Al, Ca, Mg, Ba, Li and Na can be used as reducing agent. The Gibbs free energy changes have very high negative value, so all of the metals can be used as composite reducing agent. The dynamic analysis by DSC shows that the reaction of reducing TiO2, Fe2O3 by Al occurs at 1 000 ��, and the initial reaction temperature delays to 1 236 �� when adding CaO.
Key words: high titanium ferroalloy; rutile; thermodynamics; kinetics
�����Ѻ����ĸߵͣ������Ͻ��Ϊ3���ȼ������к���65%~75%�ij�Ϊ����������������һ����Ҫ����������Ͻ���ұ����ȹ�ҵ������Ͻ�ֲ����������Ҫԭ���ϡ�Ŀǰ������������������Ҫ�����۷������Ȼ�ԭ�������۷����Է��ѲĻ�����Ϊԭ�ϼ������ۣ���Ŀǰ�Ʊ����ʸ���������Ҫ���������Ȼ�ԭ�����Խ��ʯ��������ʯ�Һ������Ϊԭ�ϣ��������Ȼ�ԭ��Ӧ���и����������������������ڹ�ģ�������������ķ�����Ҫ�����Ȼ�ԭ����Ȼ���ҹ����ȷ������ĸ�������������ʸ�������Ȼ��������������ߡ����ʶ��ȱ�㡣�������߶Ի������Ȼ�ԭ���Ľ��ʯ������������Ȼ�ԭ��ϵȼ���Ȼ�ѧ������ѧ�Ͷ���ѧ���з������Ӷ�Ϊ���ϻ�ԭ����ѡ���ṩ��������[1-2]��
1 ʵ�鷽��������ѧ����
�������Ӹ��·�Ӧ�У������¶�Tad����SHS��Ӧ���ȳ̶ȵ����ۼ��ޡ��о���Ϊ[3]��ֻ������ϵTad��1 800 Kʱ��Ӧ�����Է�������ά����ȥ������Tad�ķ����Ǽٶ���Ӧ�ھ��������·��������еķ�Ӧ��ȫ�����IJ���û�и���Ӧ��������ˣ��ͷų�������ȫ���������Ȳ��ͨ���Ѿ����¶�Tad�������۵�Tmp�ͷе�TB���бȽϣ������жϲ�������������ij��Һ������ࡣ����һ����Ӧ����ų�������Ϊ
![]() (1)
(1)
ʽ�У�![]() Ϊ��Ӧ��298.15 K�ı��ʱ䣻QΪ�Ǻ��������¾��ȷ�Ӧ�ķ�������
Ϊ��Ӧ��298.15 K�ı��ʱ䣻QΪ�Ǻ��������¾��ȷ�Ӧ�ķ�������![]() Ϊ�����������֮�͡�����ʱ����Ӧ����ЧӦȫ������������ʹ�����¶����߶������ݵ����������Q=0�������¶�Tad�ɸ�����ʽ�����¼���������㣺
Ϊ�����������֮�͡�����ʱ����Ӧ����ЧӦȫ������������ʹ�����¶����߶������ݵ����������Q=0�������¶�Tad�ɸ�����ʽ�����¼���������㣺
�������¶ȵ��ڲ����۵�Tmp����Tad��Tmpʱ�� ![]() (2)
(2)
���Tad=Tmp����
![]() (3)
(3)
ʽ�У���Ϊ���ﴦ������״̬�ķ������Ǧ�fusHΪ������ۻ��ȡ�
���Tad��Tmp����Ӧ�Ĺ�ϵʽ��Ϊ
 (4)
(4)
����Ӧ�����з������ת�䣬��
![]()
![]() (5)
(5)
cP��T�Ĺ�ϵ������ʽ��ʾ��
cp=(a+10-3bT+105cT-2+10-6dT2) (6)
ʽ�У�a��b��c��dΪ�����¶�ϵ����
������Ҫ���TiO2-Al��TiO2-Mg 2����Ӧ��ϵ�����о���
ʵ������й�ʹ��Al�ۡ�Mg�ۡ�TiO2�ۺ�CaO��4��ԭ�ϣ���Ϊ�������Լ���ʵ��ԭ�ϵ�������37 ��mΪ����ʵ���У�Al�ۡ�Mg��ֱ��ʹ�ã���TiO2�ۺ�CaO����Ҫ������¯�ں濾���Գ�ȥˮ�֡���ԭ�ϰ�������ϣ����ұ�֤��Ͼ��ȡ���Ϸ�ĩ����������²�������TA��˾Q600���в������ط������������������������Ʒ������ԼΪ10 mg��
2 ���������
���Ȼ�ԭ��������������������ԭTiO2�ķ�Ӧ������Ҫ��Ӧ����ѧ����ʽ���£�
3TiO2(s)+4Al(s)=3Ti(s)+2Al2O3(s) (7)
��������¶�ʱ������ѧ�������1���У�����Щ�������뷽��ʽ5���Tad=1 805 K��˵��TiO2-Al��ϵ�����Ӹ��ºϳɷ�Ӧ�ܹ����С�
��TiO2-Mg��ϵ��ԭ����Ti����������¶ȵĻ�ѧ��Ӧ���£�
TiO2(s)+2Mg(s)=Ti(s)+2MgO(s) (8)
��TiO2-Al��ϵ��������¶ȵķ�����ͬ�����ݱ�1�еIJ������������ϵ��Tad=2 065 K������1 800 K��˵����Ӧ���ڽ��С�
��1 �������ѧ����[4]
Table 1 Relational thermodynamic data
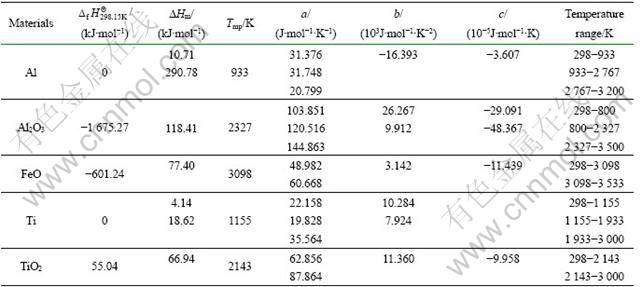
���Ȼ�ԭ��������������������ԭTiO2�ķ�Ӧ������Ҫ��Ӧ����ѧ����ʽ���£�
TiO2+4/3A1=Ti+2/3A12O3,
��G��=-167472+12.1T (J/mol) (9)
2TiO2+4/3Al=2TiO+2/3Al2O3,
��G��=-1081150+3.43T (J/mol) (10)
2TiO+4/3Al=2Ti+2/3 Al2O3
��G��=-117585+9.92T (J/mol) (11)
TiO��ǿ������������� Al2O3 ��SiO2 ��ɸ��ϻ������ʹTiO2 ��ԭ��Ӧ������TiO�ķ�����С�Ϊ�ˣ�ʹ��ǿ�ļ���������(CaO)������TiO2��ԭ��TiO�ĸ���Ӧ�ķ�����
TiO2+4/3A1+2/3CaO=Ti+2/3( CaO?A12O3 )
��G��=-45575+2.9T (J/mol) (12)
1) Fe2O3-TiO2-Al��Ӧ��ϵ
����������¶�Fe2O3-TiO2-Al��Ӧ��ϵ���в�ʾɨ������������������Ϊ20 K/min�������ͼ1��ʾ��
ͼ1�У�660 ��ʱ��һ�����ȷ壬�������ۻ����¶ȡ�1 000 ��������һ���ϴ�ķ��ȷ壬�������ȷ�Ӧ�ڴ��¶�ʱ�ѿ�ʼ������
��Origin�����ɼ���ͼ1��λ��1 000 ��ķ��ȷ����S=48.22 J/g��
��Freeman-Carroll�ַ���ͼ1��1 000 �����ҵķ��ȷ�������ݴ�����������lg��T/��lgS��- ��(1/T)/��lgS��ͼ(��ͼ2)��
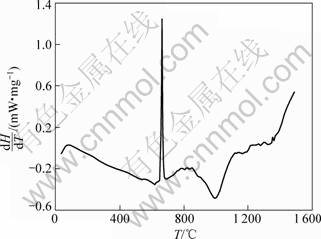
ͼ1 Fe2O3-TiO2-Al��Ʒ��DSC����
Fig.1 DSC curve of Fe2O3-TiO2-Al system
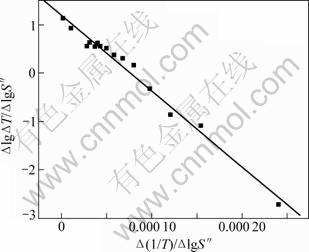
ͼ2 Fe2O3-TiO2-Al��Ӧ��Freeman-Carroll����
Fig.2 Freeman-Carroll curve of Fe2O3-TiO2-Al system
��ͼ2��ֱ�ߵ�б�ʼ��ؾ���������ѧ����ʽ�����ʽΪY=-15706.8X+1.2������õ����E=300.74 kJ/mol����Ӧ����n=1.2����Ӧ����ѧ����Ϊ
![]()
����������¶�Fe2O3-TiO2-Al-CaO��Ӧ��ϵ���в�ʾɨ������������������20 K/min�������ͼ3��ʾ��
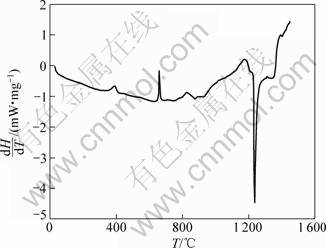
ͼ3 Fe2O3-TiO2-Al-CaO��Ʒ��DSC����
Fig.3 DSC curve of Fe2O3-TiO2-Al-CaO system
ͼ3�У�660 ��ʱ��һ�����ȷ壬�������ۻ����¶ȡ�1 236 ��������һ�����͵ķ��ȷ壬�������ȷ�Ӧ�ڴ��¶�ʱ�ѿ�ʼ������
��Origin�����ɵõ�������ȷ�����S=60.63 J/g��
��Freeman-Carroll�ַ���ͼ3��1 236 �����ҵķ��ȷ���д����������ͼ4��ʾ����ͼ4��ֱ�ߵ�б�ʼ��ؾ���������ѧ����ʽ�����ʽΪY=-360 044.6X+4.6������õ����E=6 893.8 kJ/mol����Ӧ����n=4.6����Ӧ����ѧ����Ϊ
![]() (13)
(13)
Fe2O3-TiO2-Al��ϵ��Fe2O3-TiO2-Al-CaO��ϵ��ȣ��俪ʼ��Ӧ�¶ȵ͡����С��˵��Fe2O3-TiO2-Al-CaO��ϵ�ķ�Ӧ���ѽ��У���ԭ������CaO�ļ��������һ����������ʹ��Ӧ��ϵ�������½�����Ҫ��һ�����Ȳ���ʹ��Ӧ���С�
Fe2O3-TiO2-Al��ϵ���ȷ�����С��Fe2O3-TiO2-Al-CaO��ϵ���ȷ���������˵��Fe2O3-TiO2-Al-CaO��ϵ��Ӧ����ʱ�ķ���������

ͼ4 Fe2O3-TiO2-Al-CaO��Ӧ��Freeman-Carroll����
Fig.4 Freeman-Carroll curve of Fe2O3-TiO2- Al-CaO system
3 ����
1) ����ѧ��������������Al��Ca��Mg��Ba��Li��Na�Ƚ�������ԭ�������У�2 273 Kʱ��Ӧ�ļ���˹�����ܶ��ܸ�����˿��Կ���ѡ����Щ�����Ͻ�ĸ��ϻ�ԭ���������ԭЧ����ͨ�������ȷ�Ӧ�����¶��Լ���λ��ЧӦ�ļ��㣬�ó�����ԭ��ƽ��ֵ�ϵͣ�������Ӧ�����е������ȷ�Ӧ�ų���������ά����ϵ������ƽ���Dz����ģ���Ҫͨ��������ϵ�ṩ������ά�ַ�Ӧ���������С�
2) DSC�������������Al��ԭTiO2��Fe2O3�� 1 000 �����ҿ�ʼ���У����ۻ��Ϊ300.74 kJ/mol����Ӧ����Ϊ1.2����Al��ԭTiO2��Fe2O3��ϵ������CaO����Ӧ�ͺ���1 236 �����ҷ�����Ӧ�����ۻ�����ߣ�Ϊ6 893.8 kJ/mol����Ӧ����Ϊ4.6��
REFERENCES
[1] ţ��Ƽ, ��͢��, �ռ���, ��־��, Ҧ����, ������, ʷ����. ���Ȼ�ԭ-��վ����Ʊ���������������״̬���о�[J]. ϡ�н��������빤��, 2008 , 37(S3): 78-81.
NIU Li-ping, ZHANG Ting-an, HE Ji-chen, DOU Zhi-he, YAO Jian-ming, JIAO Li-na, SHI Guan-yong. Study on forms of occurrence of oxygen for high titanium ferroalloy by alumino-thermic reduction-vacuum melting[J]. Rare Metal Materials and Engineering, 2008, 37(S3): 78-81.
[2] �˹���. ��ұ��ҵ�е������߶˲�Ʒ[J]. ��������, 2005, 26(4): 60-63.
DENG Guo-zhu. Three top products in titanium metallurgy industry[J]. Iron Steel Vanadiumtitaniu, 2005, 26(4): 60-63.
[3] ����ѧ, �Ŷ���. �����Ӻϳɼ�����ԭλ�������ϲ���[M]. ������: ��������ҵ������, 2002: 8-9.
JIN Xue-yun, ZHANG Er-lin. Self-propagating high-temperature synthesis (SHS) technology and the in situ composites[M]. Harbin: Harbin Insitute of Technology Press, 2002: 8-9.
[4] ��Ӣ��, �����. ��������ѧ�����ֲ�[M]. ����: ������ѧ������, 1993: 45-47.
LIANG Ying-jiao, CHE Yin-chang. Handbook of thermodynamic data of inorganic[M]. Shenyang: Northeastern University Press, 1993: 45-47.
(�༭ ����Ⱥ)
������Ŀ��������Ȼ��ѧ����������Ŀ(50704011��50644016��50874027)�������ص�����о���չ�ƻ�������Ŀ(2007CB613504)����ѧ�ع�����������Ŀ(20081201-9)
ͨ�����ߣ�ţ��Ƽ�������ڣ���ʿ���绰��024-83681563��E-mail��niulp@smm.neu.edu.cn


