������ʱ��: 2015-04-07 09:27
�Ų���TiO2���ܵ��Ʊ������·��������о�
�����ѧ���Ͽ�ѧ�빤��ѧԺ
ժ Ҫ��
�����ܽ�-��������500�����չ����Ʊ��˴��ĺͲ�ͬGd��������TiO2����,������Ϊǰ����,ͨ����ˮ�Ⱥϳɷ��Ʊ�����Ӧ��TiO2����,���ó�����ɨ��羵(FESEM),��������羵(FETEM),X��������(XRD)��ӫ�����(FS)�ǵȶ���Ʒ���б���,���첻ͬGd�IJ�������TiO2���ۼ�������ò���ᾧ�Ⱥ��·������ܵ�Ӱ�졣�������,����TiO2����Ϊ15 nm����,����Gd�����������,���պ�TiO2������������;��Gd����Ϊ2%ʱ,TiO2����������С��10 nm���ҡ����ĺͲ���Gd��TiO2������ò��Ϊ���˿���,���п�,�ܵ�ֱ��Ϊ8 nm����,����Ϊ100~500 nm,˵��Gd���Ӻ�����TiO2���ܵ���òӰ�첻��XRD��������,TiO2���ܵĽᾧ���ձ�������۵Ľᾧ��,���ʵ�GdԪ�ز���ʹTiO2�����ܱ���һ���Ľᾧ�ȡ�����,Gd������ҲӰ��TiO2�����Լ����ܵ�FS�ź�ǿ�ȡ�����Gd������������,TiO2���ܵ�FS�ź�ǿ���������Ӻ͵ı仯����,��Gd������Ϊ0.5%��0.2%ʱ,TiO2���ܵ�FS�ź�ǿ�ȴﵽ���ֵ��
�ؼ��ʣ�
��ͼ����ţ� TB383.1;O614.411
����飺Ѧ����(1968-),��,�����Ͼ���,��ʿ,������,�о�����:���ײ���;�绰:023-65111212;E-mail:hsxuecqu@126.com;
�ո����ڣ�2014-04-22
������������Ȼ��ѧ������Ŀ(CSTC,2011BB4096);�����У��������ҵ��ѿ���ר����Ŀ(CDJZR12130044)����;
Synthesis and Photoluminescence of Gd-Doped TiO2 Nanotubes
Xue Hansong Gu Ming Xing Zhihui Rao Jinsong Pan Fusheng
College of Materials Science and Engineering,Chongqing University
Abstract��
Pure and Gd-doped TiO2 nanopowders were prepared by a sol-gel process and 500 �� heat treatment,which were used as precursor subsequently. The corresponding TiO2 nanotubes were synthesized by hydrothermal method under microwave irradiation and then were characterized by field emission scanning electron microscopy( FESEM),field emission transmission electron microscope( FETEM),X-ray diffraction( XRD) and fluorescence spectrum( FS). The effects of Gd content on morphology,crystallinity and photoluminescence of TiO2 nanopowders and nanotubes were investigated. The results showed that the diameter of TiO2 nanopowders decreased with the increase of Gd dopant content,and the diameter decreased to about 10 nm when Gd dopant increased to 2%. Pure and Gd-doped TiO2 nanotubes were both 8 nm in diameter and 100 ~ 500 nm in length with open ends and hollow inside. The Gd content had few influences on the morphology of TiO2 nanotubes. The XRD results showed that the crystallinity of TiO2 nanotubes was generally less than that of TiO2 nanopowders,but Gd dopant could maintain crystallinity of TiO2 nanotubes an appropriate content. Moreover,the effects of Gd content on FS intensity for TiO2 nanopowders and nanotubes were discovered. The results showed that FS intensity of TiO2 nanotubes firstly increased and then decreased with the increase of Gd content. The maximum of FS intensity was reached when the Gd contents were 0. 2% and 0. 5%.
Keyword��
TiO2; nanotubes; Gd dopant; photoluminescence;
Received�� 2014-04-22
Ti O2��Ϊ�����İ뵼�����,�ڹ�������Լ��ڽ���ˮ�ܽ��л������ж��صı��֡�Ti O2�����������ԡ��ɱ����Լ�������������Ⱦ���ص�,���㷺Ӧ����ˮ�����о���Ȼ��Ti O2�нϸߵĵ���( e-) �Ϳ�Ѩ( h+) ������,��һ���̶���Ҳ������Ti O2Ӧ�÷�Χ[1]��
Ϊ�����Ti O2�Ĺ����,������������й����߶�������Ti O2�ĸ����о�,�����ǽ������ӡ������Ԫ�����Ρ�ϡ��Ԫ�ظ��Ժ�����Ti O2�ȱ�����ȵ�[2,3,4]��Ashai��[5]������ͨ������������N�滻�����е�O,���Խ���Ti O2�Ĵ�϶����,�Ӷ���������ٶȡ�Liang��[6]�о�����, �ڲ���Ϊ462 nm�Ŀɼ�����,Y����Ti O2���۵Ĺ������������δ���ӵ�Ti O2���ۡ������о���ʾ,����Ԫ����Ҫͨ������̬�ͺ����ı仯,ǿ��Ӱ���Ź������ӺͿ�Ѩ�ĸ���,�����ı�Ti O2�Ĺ��ЧӦ���������о���ʾ[7,8],ͨ��ӫ�����( FS) ����,�ɻ�ð뵼�����ײ��Ϲ���������Ǩ�ơ�������ϵ���Ϣ,��˿�����ӫ����IJ��Գ������ٵ�������Ʒ������ԡ�
���о�����[9,10,11],Ti O2���ͽṹ�ͱ�����̬Ҳ��Ti O2������ܵ���Ҫ����,Ti O2���ܱ�Ti O2���۾��и���ıȱ��������Խ���������������ܹ�ע����ͳ��ˮ�Ⱥϳɷ��Ʊ�Ti O2������Ҫ�ϳ��ķ�Ӧʱ��ʹ�������Դ����[12]�� �������������µ�ˮ�Ⱥϳɻ���,��������Ѹ��,��Ӧ�����¾���,���Һϳ�Ti O2����Ч�ʿ�,�ɱ�����[13,14]���ڹ�ȥ���о���,���ӵ�Ti O2�������Է��塢�����ߺͱ�ĤΪ��,Gd����Ti O2�����Ʊ����о��ʼ�����������ͨ���ܽ�- �������Ʊ���ͬGdԪ�ز�������Ti O2����,������Ϊǰ����,Ӧ����ˮ�Ⱥϳɷ��Ʊ����ĺ�Gd���ӵ�Ti O2���ܡ��о���ͬGdԪ�ز�������Ti O2���ۺ����ܵ���ò���ᾧ���Լ����·������ܵ�Ӱ�졣
1ʵ��
1. 1��Ʒ�Ʊ�
ʹ���ܽ�-�������Ʊ���ͬGd��������Ti O2����: ��40 ml��ˮ�Ҵ�,10 ml����ˮ,10 ml�������Լ�һ������Gd N3O9�ڴ��������¾��Ȼ�ϳ�AҺ����40 ml��ˮ�Ҵ�,20 ml���ᶡ���ڴ��������¾��Ȼ�ϳ�BҺ��ͨ����ʽ�ζ��ܽ�AҺ�����μ���BҺ��,�»�40 h,�õ������塣 ����,����500 �����պ�,��ĥ�õ�Gd��Ti�����������ȷֱ�Ϊ0% ,0. 2% ,0. 5% ,1. 0% ��2. 0% ����Ti O2����,���ֱ���ΪGd0-Ti O2, Gd0. 2-Ti O2,Gd0. 5-Ti O2,Gd1-Ti O2,Gd2-Ti O2��
��ˮ�Ⱥϳɷ��Ʊ���ͬGd��������Ti O2����: ��ȡ0. 2 g��������50 ml��Na OH��Һ( 10 mol��L- 1) �г�����ɢ10 min��,������ķ���ϩ��ƿ��,��ˮ�Ⱥϳ�90 min������ϴ��ֱ����Һp HΪ7�����������,��ĥ,�õ����ĺ�Gd���ӵ�Ti O2����,���ݲ������IJ�ͬ�ֱ���ΪGd0-Ti O2NT,Gd0. 2-Ti O2NT,Gd0. 5-Ti O2NT, Gd1-Ti O2NT,Gd2-Ti O2NT��
1. 2��Ʒ����
Ti O2����������������������ձ���ѧ��˾D/MAX-2500PC��X����������( XRD,�� = 0. 15418nm) ���������۽ṹ����ò�ı���,��������FEI��˾NOVA400�ͳ�����ɨ���������( FESEM) ��ZEISS��˾LIBRA200�ͳ��������������( FETEM) ����Ʒ�Ĺ��·������ܵ��о������ձ�����������RF-5301PC��ӫ�������( FS) ��
2���������
2. 1 SEM��TEM������
ͼ1����Gd N3O9Ϊ����Դ�Ʊ��Ĵ��ĺͲ���Gd��Ti O2���ܵ�SEM��ò����ͼ1�п��Կ���,ͨ����ˮ�Ⱥϳɷ��Ʊ���Ti O2����ֱ����Сһ��,�ܵij���Ϊ100 ~ 500 nm,ϡ��Ԫ��Gd�IJ�������Ti O2������òӰ�첻��
ͼ2�Ǵ��ĺͲ���Gd��Ti O2���ۺ����ܵ�TEM����ò��ͼ2( a ~ c) Ϊ�ܽ�-�������Ʊ�����500 �� ���յĴ��ĺͲ��ӵ�Ti O2����,������Ϊ8 ~ 20 nm���ҡ�δ����Ti O2����( ͼ2 ( a) ) ������Ϊ17 nm����,���Ų�����������, Gd���ӵ�Ti O2����������С,�ر��ǵ�Gd������Ϊ2% ʱ( ͼ2 ( c) ) ,��������С��10 nm���ҡ�����Ҫ������: һ��������Gd N3O9���ܽ�-����������,NO3 -���������ε�ǰ�������Ӧ,����Ti O( NO3)2,����NO3 -Ҳ�����ܽ�-�������������������ϼ�������,���߶����һ���������Ϸ�Ӧ����,�Ӷ�������ɺ��Լ����������̵ľ�����[15]����һ����,���о���ʾ,GdԪ����ǿ������Ti O2���������ת��[16],�����500 �� ���չ�����,ϡ��GdԪ�ز��ӻ��谭��Ti O2���������չ����еij���ͼ2( d ~ f) �ֱ�Ϊ��ƷGd0-Ti O2NT,Gd1-Ti O2NT, Gd2-Ti O2NT����ò, TEM�����ʾ,��ˮ�Ⱥϳɷ��Ʊ���Ti O2�������˿���,���пա�����Gd����������,�ܳ��ܾ���������һ��,��ܾ���8 nm����,����Ϊ100 ~ 500 nm,�˽��ۺ�SEMͼ��Ľ��һ�¡�
ͼ1 Ti O2���ܵ�SEM��òFig. 1 SEM images of Ti O2nanotubes
(a)Gd0-TiO2NT;(b)Gd0.2-TiO2NT;(c)Gd1-TiO2NT;(d)Gd2-TiO2NT
ͼ2 Ti O2��TEM��òFig. 2 TEM images of Ti O2
(a)Gd0-TiO2;(b)Gd1-TiO2;(c)Gd2-TiO2;(d)Gd0-TiO2NT;(e)Gd1-TiO2NT;(f)Gd2-TiO2NT
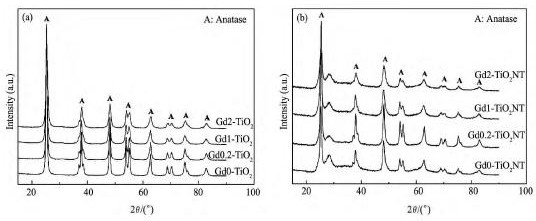
2. 2 XRD�������
ͼ3Ϊ���ĺ�Gd����Ti O2�����Լ�������Ʒ��XRDͼ�ס����۵�������С�ɸ���Debye-Sherrer��ʽ[17]����:

ʽ��,DΪ����( ��λnm) ,�� ΪX��������IJ���( �� = 0. 1541874 nm) ,FW( S) Ϊ����������ǵİ�߿�,�� Ϊ����Ƕȡ���Ʒ�Ľᾧ�ȸ�������MDI jade 5. 0��������1Ϊͨ����Ʒ����������, �������õ�Ti O2��������ƽ��ֵ���ᾧ��ƽ��ֵ����1��������ʾ,����Ti O2��������Ϊ15. 9 nm,����Gd����Ũ�ȵ�����,�������Լ�С,��Gd�IJ������ﵽ2. 0% ʱ,������������10. 8 nm,�÷��������TEM�������һ�¡�Ti O2���ۺ�����XRDͼ��( ͼ3) ��ʾ�����Ե����ѿ�������,û�з�������������,˵����Ʒ��Ϊ���ѿ��ࡣ�ڴ��ĺ�Gd���ӵ�Ti O2������Ʒ��( ͼ3( a) ) ,����Gd������������,��Ʒ����������ֲ�ͬ�̶ȵĿ���������ǿ�ȵĽ��͡���������Gdԭ�ӵİ뾶( 94 pm[17]) ���Դ���Tiԭ�ӵİ뾶( 68 pm[18]) ,Gdԭ�Ӻ��ѽ���Ti O2������,���Gd�滻����Tiԭ��,�ֲ���Ti O2������,�����ѿ������γ�Gd - O - Ti��,��ɵ�Ӧ��ʹ�þ�����������,������������,����ǿ�Ƚ���, �ᾧ�Ƚ���( ��1) ��
ͼ3 Ti O2��XRDͼ��Fig. 3 XRD patterns of Ti O2
(a)Pure and Gd-doped TiO2nanopowders;(b)Pure and Gd-doped TiO2nanotubes
��1 Ti O2����������Table 1 Physicochemical properties of Ti O2 ����ԭͼ
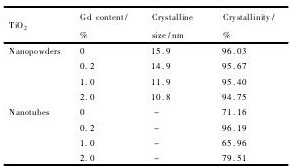
��1 Ti O2����������Table 1 Physicochemical properties of Ti O2
��Ti O2������Ʒ��, ������ƷGd0- Ti O2NT,Gd1-Ti O2NT��Gd2-Ti O2NT��XRDͼ��( ͼ3( b) ) ���Ӧ���۵�XRDͼ��( ͼ3( a) ) , �������MDJ jade 5. 0��������,Ti O2��������������ǿ�������Ӧ�����������������, ���߿��Ӵ�,˵������������; ����MDJ jade 5. 0���������ᾧ��Ҳ��������( ��1) ������Ҫ����Ϊ���Ʊ�Ti O2���ܹ�����,Ti O2�����ᱻNa OH���������Ƭ,�ھ�����Ӽ��������������¾����ɹ�,��ɵľ���仯,���½ᾧ�Ƚ���( ��1) ����ƷGd0. 2-Ti O2NT����ƷGd0. 2-Ti O2��������ǿ�ȺͿ��Ȼ�������һ��,˵���ʵ��IJ���GdԪ��������Ti O2���ܱ���һ���Ľᾧ��, ��ԭ���д���һ���о���
2. 3ӫ�������
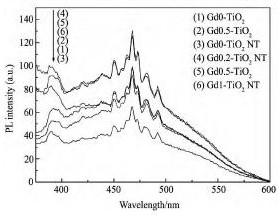
ͼ4Ϊ���ĺͲ��ӵ�Ti O2���ۼ����ܵ�FSͼ��,�伤������Ϊ350 nm������ͼ4��ʾ,������Ʒ�ڿɼ���400 ~ 600 nm��Χ�ڱ��ֳ�ǿ�����ķ����ź�,���ֱ���450,468��482 nm����FS��,450��468 nm���ڴ������ɼ��ӷ���,����482 nm�����ֵ�FS���������������ӷ���,����ҪԴ����Ʒ���������λ��ȱ�ݵ�[19]��������Ʒ��FSͼ�������Ƶ����Խṹ,��FS��ֵҲһ����û�в���������ֵ,����ǿ�ȷ����˱仯,˵������GdԪ�ز��������µ�FS����,����ʹ���ź�ǿ�ȷ����仯����ƷGd0. 5-Ti O2( ͼ4( 2) ) ����ƷGd0-Ti O2( ͼ4( 1) ) ���,��FSͼ���ź�ǿ��������ǿ,����Ҫ����Ϊ: ����0. 5% ��Ti O2���������ȴ���Ti O2����С,��һ����˵,����ԽС,������ѨŨ��Խ��,������λ�����������ӵ�����,���¿�λ���������γɼ��ӵĸ���Խ��, ������ź�Խǿ���Աȴ���Ti O2����( ͼ4 ( 3) ) ,��ƷGd-Ti O2NT( ͼ4 ( 4,5��6) ) ��FSͼ���ź�ǿ�ȳ��ֳ�������,�͵�����,��ƷGd0. 2-Ti O2NT��Gd0. 5-Ti O2NT��FSǿ�Ȼ�������һ����Ϊ���ֵ������Ҫ����Ϊ,������GdԪ�ز�����ʹTi O2���ܾ���������,Ti O2���ܵĹ�״�ṹʹ������������λ��ȱ��Ũ������,���������GdԪ�ز���ʱ,������Gd - O - Ti���γɷ���ʹ������λ��ȱ��Ũ�ȼ���[19,20], �Ӷ�����FSǿ�Ƚ��͡����о���ʾ[13],FSǿ������������һ���Ĺ�ϵ,һ����˵,FS�ź�Խǿ,��������Խ�ߡ������о�����,������0. 2% ��0. 5% ��ϡ��Ԫ��Gdʱ,Ti O2���ܵ�FS�ź�ǿ�ȴﵽ���ֵ,˵��������λ��ȱ��Ũ�ȸ���,����ڹ��������Ti O2���ܱ��沶�����( e-) �Ϳ�Ѩ( h+) ��������ǿ,����Ti O2���ܶ��صĹ�״�ṹʹ����нϸߵıȱ��������Խ����������,����Ԥ����ƷGd0. 2-Ti O2NT��Gd0. 5-Ti O2NT�Ĺ����������Ti O2���ۡ� ������Ϊ��һ���IJ��Ӻ�����Χ��,����ʹTi O2���ܵ�FS�ź�ǿ�ȴﵽ�ϸ�ֵ���Ա������ݶ�����,0. 2% �IJ�������0. 5% �IJ������ǽϽӽ���������,��ʹ��FS�ź�ǿ�ȴﵽ���ֵ,˵����������ܵõ����ʵ�����Ѩ��ȱ��Ũ�ȡ�
ͼ4 Ti O2��FSͼ��Fig. 4 FS patterns of Ti O2
3����
1. ϡ��Ԫ��Gd�IJ�����ֱ��Ӱ��Ti O2���������Ĵ�С,����ҪӰ���������������: һ�������ܽ�-����������,��Gd N3O9Ϊ����Դ��NO3 -��������Ϸ�Ӧ����,�Ӷ�������ɺ��Լ����������̵ľ����ԡ���һ����,GdԪ����ǿ������Ti O2���������ת��,�Ӷ�����Ti O2���������չ����еij���
2. ������ˮ�Ⱥϳɷ��Ʊ��Ĵ��ĺͲ��ӵ�Ti O2����,���˿���,���п�,��Ʒ�ܾ���Ϊ8 nm����,˵��Gd�IJ�������Ti O2���ܵ���òû������Ӱ�졣
3. Gd�IJ�����Ӱ��Ti O2�����Լ����ܵĽᾧ��,��������Gd����,������Ti O2���ܱ���һ���Ľᾧ�ȡ�
4. Gd������Ӱ��Ti O2�����Լ����ܵ�FS�ź�ǿ��,����0. 5% Gd��Ti O2����FS�ź�ǿ�����Ը��ڴ�Ti O2����,����Gd������������,Ti O2���ܵ�FS�ź�ǿ���������Ӻ͵ı仯����,Gd������Ϊ0. 2% ��0. 5% ʱ,��FS�ź�ǿ�����,��Ҫ�����ڲ��ӵ�Gdԭ�Ӵ��澧����Tiԭ��,����������,�������ܱ��������Ѩ��ȱ��Ũ�ȷ����仯,�Ӷ�Ӱ��Ti O2���ܵ�FS�ź�ǿ�ȡ�
�����