���±�ţ�1004-0609(2007)05-0693-06
TiO2�������е��Ʊ����ȴ������������
�պ������� ������ �ᣬ�� ��
(�Ͼ����պ����ѧ ���Ͽ�ѧ�뼼��ѧԺ���Ͼ� 210016)
ժ Ҫ��
ժ Ҫ�����ú�ѹֱ�������������Ʊ����й������е�TiO2�������У����о����ڿ����ȴ��������еľ���ת�䣬ͬʱ�ü��ȵĽ�����̱����������ܡ�������������Һ����0.5%(��������)HFˮ��Һʱ����ѹ��10~20 V֮�䣬ʱ��5 min���ϲ����γ�TiO2�������У�����������ѹ����ߣ����ܵ�ƽ���ܾ��ܳ���������������ʱ����ӳ������ܹܳ�����������ƽ���ܾ��仯�������������ڿ������ȴ���ʱ��280 �����ҳ������ѿ��࣬400 �����ҳ��ֽ��ʯ�࣬680 ���������ѿ�������ʯ���ת�������600 ���������нṹ��Ȼ�������������ʵ���������������ѹΪ20 V������ʱ��Ϊ20 minʱ��õ��������о���400 ���ȴ�������40 min�Ĺ���ʱ�Լ��ȵĹ�������ʸߴ�99.6%��
�ؼ��ʣ�
TiO2�������������������������
��ͼ����ţ�TG 146; TQ 153.6; X 703.1���� ���ױ�ʶ�룺A
Fabrication, anneal and photocatalysis applications of
self-organized TiO2 nanotubes
TAO Hai-jun, QIN Liang, WANG Ling, TAO Jie
(College of Materials Science and Technology, Nanjing University of Aeronautics and Astronautics,
Nanjing 210016, China)
Abstract: Self-organized TiO2 nanotube arrays were fabricated by anodic oxidation of a pure titanium sheet at constant potential. The results show that TiO2 nanotube arrays are regularly obtained when anodizing voltages ranges from 10 to 20 V, anodizing time keeps more than 5 min and HF concentration is 0.5%. The average diameter and length of the tube increase with increasing anodizing voltage. And the length of tube increases with longer anodization time obviously. After annealing for 3 h in ambient atmosphere, the anatase phase emerges at about 280 ��, the rutile phase emerges at about 400 ��, anatase transforms completely to rutile at about 680 �� and nanotube architecture can be preserved till 600 ��. Furthermore, TiO2 nanotubes, fabricated at anodizing voltage of 20 V for 20 min and then annealed at 400 ��, possess better photo-catalytic activity, i.e. the decolourisation of methyl orange irradiated for 40 min is 99.6%.
Key words: TiO2; nanotube arrays; anodic oxidation; photo-catalytic activity
TiO2�ѱ��㷺��Ӧ���ڹ����[1-3]���������С���[4-5]��������[6-7]��Ⱦ������̫���ܵ��(DSSC)[8-11]���������ǶԻ���������������ӣ��й�TiO2��������ˮ���к����巽����о�Ҳ��Ϊ�ȵ�[12]��TiO2��Ϊ������������ִ�����ʽ���������ױ�Ĥ���������������ߵȣ��Ʊ���Щ��ͬ��ʽ���ṹ��Ŀ���ǻ�þ����ܴ�ıȱ�������Ӷ����TiO2�Ĺ�����ܡ���ʹ�ʹ����ȱ���������ṹ���ϳ��֣����о��и߶ȹ���ṹ����������������ѧ�ߵĹ㷺��Ȥ��ĿǰΪֹ�����ܵ��Ʊ�������ģ�巨[13]��ˮ�ȷ�[14]���������̷�Ӧ��������������[15-18]�����������������������ɱ�����������ʵ�ֹ�ҵ�����ҿ��Ի�ô�������������нṹ����ˣ��������߲�ȡ��ѹ�����������Ʊ�TiO2�������У��о���TiO2�������е��γɹ��̡��ȴ���ʱ�ľ���ת�䡢����ʱ�Ľᾧ���̣�ͬʱ����������Լ��ȵĹ���������ܡ�
1 ʵ��
1.1 TiO2�������е��Ʊ�
�ߴ���(99.6%)�Ѳ�(25 mm��30 mm��0.1 mm)������ͪ����������ˮ����ϴ������HF��HNO3�����Ϊ1?1�Ļ����Һ�л�ѧ�⣬ȡ���������ö�������ˮϴ��������������N2���ɱ��á�
TiO2�������е��Ʊ��������缫��ϵ����Դ���ú�ѹֱ����Դ��������Ƭ�������PtΪ�Ե缫�����缫����뱣����5 cm�����ҺΪ0.5%�������ˮ��Һ������ʵ���������½��в�ʼ�հ���������衣ʵ����ͨ���ı�����������ѹ������ʱ�䣬�о�TiO2�������е��γɹ��̡�
1.2 TiO2�������е��ȴ���
�����������������Ĥ���Ѳ�ƽ����Al2O3�մ�Ƭ�ϣ�������¯�н����ȴ����������ȴ��������ɳ�����ƣ�����15 ��/min�ٶ����£��ﵽ�����¶Ⱥ���±���3 h�����������¯��ȴ�����º�ȡ�����á�ʵ����ͨ���ı��ȴ����¶ȣ��о�TiO2���������ڴ����ȴ��������µĽᾧ���̺;���ת�䡣
1.3 TiO2�������й�����ܱ���
��10 mg/L����ˮ��ҺΪĿ�꽵����������Ϊ��ȡ�ȴ����������Ƭ����10 mLĿ�꽵������Һ�У� ����ͼ1��ʾ�Ĺ����Ӧ���ÿ��һ���Ĺ���ʱ�佫������Һȡ��, ���û����Ϻ����������������ι�˾��6010����-�ɼ���ֹ��ȼƲⶨ������������ղ���463.5 nm�������ն�A������Beer���ɼ���ȥ���ʡ�
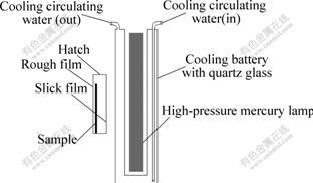
ͼ1 �����Ӧװ��ʾ��ͼ
Fig.1 Schematic diagram of photo-catalytic reactor
������������ò�ı�������LEO-1530VP������ɨ��羵�������нᾧ��Ϊ�ı�������BRUKER D8 Advance�ྦྷX����������(Cu K��)��
2 ���������
2.1 TiO2�������е��γ�
ǰ�ڵ��о�[19-20]�������ں���һ����HF��ˮ��Һ�У�ͨ���ı����������������Ի�������Ĥ�����������С���һ�����о�֤ʵ������������ѹ��Ӱ���������е��γ�(������[20]֪�����ҺΪ0.5%HFˮ��Һʱ������������10~20 V��Χ����)������ʱ��Թ����е��γ�Ҳ����Ҫ��Ӱ�죬���������еij��ִ���һ�������ݱ�Ĺ���(ͼ2)��
ͼ2��ʾΪ20 V������ѹ�£��������е��γɹ��̡�����ʱ��(ͼ2(a))Ϊ30 sʱ������Ĥ���������������С��״�ֲ�������ʱ����ӳ������浺״�ṹ������(ͼ2(b))������(ͼ2(c))��ȡ�����ɺ��ͼ���Կ�����ʱ����ӳ�ʹ����Ĥ������Ӹɾ������ܵĽṹҲ�������ԣ���ͼ2(d)��ʾ��
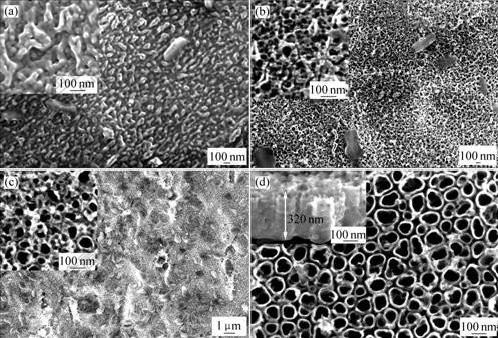
ͼ2 20 V��ѹ�²�ͬ����ʱ���γɵ�TiO2Ĥ�ı���������ò
Fig.2 FE-SEM top and cross-sectional images of TiO2 films anodized under 20 V for different time: (a) 0.5 min; (b) 1 min;���� (c) 2 min; (d) 5 min
����ʵ��֤�������ڲ�ͬ�ĵ��Һ��ϵ���γ���������������ض���ѹ��Χ���Dz�ͬ�ġ�����HFˮ��Һ��ϵ�ĵ��Һ��HF�ĺ���Խ�ߣ��γ�������������ĵ�ѹԽ�͡����Ҫ�����Ƕ��ڲ�ͬ�ĵ��Һ��ϵ����Ҫ���ջ���������е��ض�����������
2.2 ��������������������ò��Ӱ��
������ѹ����Ӱ���������еIJ��������Ӱ��������ò����ͼ3���������ŵ�ѹ���������ܵ�ƽ���ܾ��ܳ������Ե�������ѹ��10 V ���ӵ�20 Vʱ��ƽ���ܾ���50 nm����100 nm�����ܵij���Ҳ��170 nm���ӵ�390 nm��

ͼ3 ��ͬ��ѹ������20 min�γɵ��������еı���������ò
Fig.3 FE-SEM top and cross-sectional images of nanotube arrays for 20 min under different voltages: (a) 10 V; (b) 20 V
��ͼ2(d)��3(b)��ͼ4�������ԵĿ���������ʱ������ܵ�ƽ���ܾ�Ӱ�첻��(��ʱ����ӳ���������)�����Ƕ����ܵij���������Ҫ��Ӱ�졣���ܵij�����������ʱ����ӳ��������������Ϊ������5 minʱΪ320 nm��15 minʱΪ340 nm��20 minʱΪ390 nm��30 minʱ���ӵ�490 nm��

ͼ4 ����ʱ������ܳ��ȵ�Ӱ��
Fig.4 Effect of anodization time on length of nanotube
��������������������ѹ��ʱ������ܵ�ƽ���ܾ��ܳ�������Ҫ��Ӱ�죬ͬʱ�о���������ͬ�Ĺܳ���ƽ���ھ����������еĹ�������������Ҫ��Ӱ�졣��Varghese��[5]�о����֣���Ϊ����������ʱ����290 ��Ĺ����¶��£��ھ�Ϊ46 nm�Ĺ����б��ھ�Ϊ76 nm�Ĺ����о��и��ߵ��������жȣ�Maca��k��[11]�о����֣���ΪȾ������̫���ܵ��ʱ����2.5 ��m���ҵ�����������540 nm�ĵ�ɫ�����£��������ת��Ч��(IPCEmax)�ﵽ3.3%������500 nm���ҵ�����������530 nm�ĵ�ɫ�����£���IPCEmaxֻ��1.6%����ˣ�̽��ͬ�����������������Ʊ���ͬ�ṹ����(�ܳ���ƽ���ܾ����ܱں�ȡ��赲����)���������о��зdz���Ҫ��ʵ�����塣
2.3 �ȴ������������е�Ӱ��
�����е��ȴ�����TiO2�������е�Ӱ����������ģ�һ�����ܵ���ò������TiO2�ľ��͡�
��ͼ5���Կ������ȴ����¶Ƚϵ�ʱ(ͼ5(a)��(b))�����ܵ�ƽ�����ͱ��沢�ޱ仯�����ȴ����¶ȴﵽ550 ��ʱ�����ܱ������Źܱ��ڹܿڷ����л�״�ᾧ�ͼ5(d)�������ԡ����⣬��ͼ5(c)��(d)Ҳ�����Կ��������ܵ��пղ����ڼ�С��TiO2�����ɹܵײ�����ܿ�����������Щ��ò�ı仯�����ƶ����ܵĽᾧ���̴������£����ܵײ��ľ����������������ܱ������ܿڳ��ֻ�״�ᾧ�ֱ���������״�ṹ����ʧ��
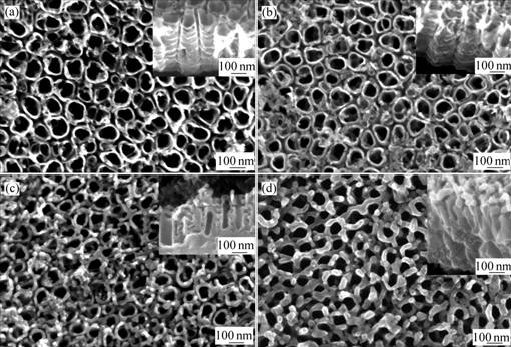
ͼ5 �ȴ����¶ȶ����ܱ���������ò��Ӱ��
Fig.5 Effect of heat treatment temperature on surface and cross-sectional morphologies of nanotube arrays: (a) 350 ��; (b) 400 ��; (c) 550 ��; (d) 600 ��
��ͼ5(d)����������ؿ�������600 ���ȴ�������£�����������Ȼ���нϺõĽṹ�ȶ��ԣ�Ϊ�书�����Եķ����ṩ�˱�֤��
�ڶ�ѧ���о���Ϊ�����ѿ����TiO2�Ͻ��ʯ��ľ��и��õĹ�����ܣ���Ҳ��һ����ѧ���о���Ϊ���ѿ�������ʯ�������Ϊ7?3ʱ��TiO2������õĹ�����ܡ����̽��TiO2���͵�ת����̾�����Ҫ��ʵ�ʼ�ֵ����ͼ6���Կ����������ѻ����TiO2���������ڱ�ʵ�������õ��ȴ��������£�280 �����ҿ�ʼ�������ѿ���((101)����)�������¶ȵ���ߣ����ѿ���ĺ��������ӣ����¶���ߵ�400 ������ʱ�����ʯ��((110)����)��ʼ���֣�ֱ���¶ȴﵽ680 ������ʱ��TiO2ȫ��ת��Ϊ����ṹ�����ȶ��Ľ��ʯ�ࡣ������ʵ�����ɿ�����400 ���ȴ��������������ھ��нϸ������ຬ����ͬʱ��������һ���ֽ��ʯ�ࡣ����������Ϊ���־��ͽṹ�����нϸߵĹ�����ԣ���ˣ�ѡ��400 ���ȴ���������������Ϊ���ʵ���������
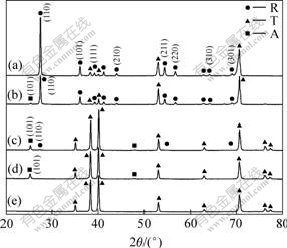
ͼ6 �������еľ���ת��
Fig.6 Crystalline phase transition of nanotube arrays: (a) 680 ��; (b) 650 ��; (c) 400 ��; (d) 280 ��; (e) 240 �� (A and R represent anatase and rutile, T represents titanium)
�������ṹ��ʽ��TiO2�Ĺ�����Բ��������ľ��͡�����״̬���йأ�������ȱ�����нϴ�Ĺ�ϵ(��ͬ�ıȱ���������л���ĺ�����ͬ)����ͼ5(c)��(d)�������Կ����������ȴ����¶ȵ���ߣ����ܵ��пղ��ֵij���Ҳ�����̣�����ȱ�����ڼ�С������ͼ5(b)���Կ�����400 ���ȴ������������м��������ڴ���������Ҳ������ѡ��400 ���ȴ��������������ʵ�����һ��ԭ�������ȴ����¶ȡ����ܵıȱ������������TiO2�ı���״̬�Թ�����ܵľ���Ӱ�콫��������������ϸ������
2.4 TiO2�������еĹ������
��ʵ����ͼ6��XRD�ף���20 V��ѹ������20 min����������ѡȡ��400 ����ȴ����¶ȡ�
��ͼ7���Կ��������Ź��ʱ������������ȵĽ����ʳ�ָ�����ӡ�������Ϊ�������Ӳ��ϵر�ˮ�������ӷ����������ɾ��и��Եij���������(��O2-) ���ǻ����ɻ�(��OH)�����Ź��ʱ����ӳ��������ֻ������ʵ���Ҳ���࣬�������Ź��ʱ�����������ת���ʽ��������ߡ�
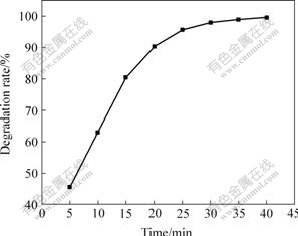
ͼ7 TiO2�������еĹ������
Fig.7 Photocatalytic ability of TiO2 nanotube arrays
3 ����
1) ���ҺΪ0.5%��HFˮ��Һ��ͨ����ѹ�����������ڵ�ѹΪ5~20 V������ʱ��Ϊ5 min����ʱ�������ڸߴ��Ѳ������Ʊ������������TiO2��������Ĥ��
2) TiO2���������ڿ������ȴ����ᷢ��һϵ�еľ���ת�䣺280 �����ҳ������ѿ��࣬400 �����ҳ��ֽ��ʯ�࣬680 ���������ѿ�������ʯ���ת�������600 ��ʱ�������нṹ��Ȼ����������
3) ���ܵĽᾧ������3�����������������ɣ��ɵײ����ܿڵ������������̡��عܿڵĻ�״�ᾧ���̺ܱڵĽᾧ���̡������ɹܵײ����ϵĽᾧ������Ϊ���ԣ��������ܽṹ�������ݵ���Ҫԭ��֮һ��
4) ��������ѹΪ20 V������ʱ��Ϊ20 minʱ��õ�TiO2�������о���400 ���ȴ������ڹ���40 minʱ�Լ��ȵĹ�������ʸߴ�99.6%��
REFERENCES
[1] Bahnemann D W, Kholuiskaya S N, Dillert R, et al. Photodestruction of dichloroacetic acid catalyzed by nano-sized TiO2 particles[J]. Applied Catalysis B: Environmental, 2002, 32(2): 161-169.
[2] LI Jing-yi, CHEN Chun-cheng, ZHAO Jin-cai, et al. Photodegradation of dye pollutants on TiO2 nanoparticles dispersed in silicate under UV-VIS irradiation[J]. Applied Catalysis B: Environmental, 2002, 37(4): 331-338.
[3] Sivalingam G, Nagaveni K, Hegde M S, Madras G. Photocatalytic degradation of various dyes by combustion synthesized nano anatase TiO2[J]. Applied Catalysis B: Environmental, 2003, 45(1): 23-38.
[4] Mor G K, Carvalho M A, Varghese O K, Pishko M V, Grimes C A. A room-temperature TiO2-nanotube hydrogen sensor able to self-clean photoactively from environmental contamination[J]. Journal of Materials Research, 2004, 19(2): 628-634.
[5] Varghese O K, Gong D, Paulose M, et al. Hydrogen sensing using titania nanotubes[J]. Sensors and Actuators B, 2003, 93(1/3): 338-344.
[6] Ruan C, Paulose M, Varghese O K, Grimes C A. Enhanced photoelectrochemical-response in highly ordered TiO2 nanotube-arrays anodized in boric acid containing electrolyte[J]. Solar Energy Materials & Solar Cells, 2006, 90: 1283-1295.
[7] Paulose M, Mor G K, Varghese O K, Shankar K, Grimes C A. Visible light photoelectrochemical and water-photoelectrolysis properties of titania nanotube arrays[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2006, 178: 8-15.
[8] Paulose M, Shankar K, Varghese O K, Mor G K, Hardin B, Grimes C A. Backside illuminated dye-sensitized solar cells based on titania nanotube array electrodes[J]. Nanotechnology, 2006, 17: 1446-1448.
[9] Mor G K, Shankar K, Paulose M, Varghese O K, Grimes C A. Use of highly-ordered TiO2 nanotube arrays in dye-sensitized solar cells[J]. Nano Letters, 2005, 6(2): 215-218.
[10] Paulose M, Shankar K, Varghese O K, Mor G K, Grimes C A. Application of highly-ordered TiO2 nanotube-arrays in heterojunction dye-sensitized solar cells[J]. J Phys D: Appl Phys, 2006, 39: 2498-2503.
[11] Maca��k J M, Tsuchiya H, Ghicov A, Schmuki P. Dye-sensitized anodic TiO2 nanotubes[J]. Electrochemistry Communications, 2005, 7: 1138-1142.
[12] ������, ������, ������, �ޡ�ӱ. ����Ӷ�����TiO2�Ľṹ��估�ɼ�������Ե�Ӱ��[J]. �й���ɫ����ѧ��, 2006, 16 (7): 1233-1238.
ZHOU Wu-yi, CAO Qing-yun, TANG Shao-qiu, LUO Ying. Effects of sulfur doping on structure phase transformation and visible-light photocatalytic activity of nano-TiO2[J]. The Chinese Journal of Nonferrous Metals, 2006, 16 (7): 1233-1238.
[13] Chu S Z, Wada K, Inoue S, Todoroki S. Fabrication of oxide nanostructures on glass by aluminum anodization and sol-gel process[J].Surface and Coatings Technology, 2003, 169-170: 190-194.
[14] Suzuki Y, Yoshikawa S. Synthesis and thermal analyses of TiO2-derived nanotubes prepared by the hydrothermal method[J]. J Mater Res, 2004, 19(4): 982-985.
[15] Gong D, Grimes C A, Varghese O K, et al. Titanium oxide nanotube arrays prepared by anodic oxidation[J]. J Mater Res, 2001, 16(12): 3331-3334.
[16] Mor G K, Varghese O K, Paulose M, et al. Fabrication of tapered, conical-shaped titania nanotubes[J]. J Mater Res, 2003, 18(11): 2588-2593.
[17] Mor G K, Varghese O K, Paulose M, et al. Transparent highly ordered TiO2 nanotube arrays via anodization of titanium thin films[J]. Adv Funct Mater, 2005, 15: 1291-1296.
[18] ZHAO Jian-ling, WANG Xiao-hui, CHEN Ren-zheng, LI Long-tu. Fabrication of titanium oxide nanotube arrays by anodic oxidation[J]. Solid State Communications, 2005, 134(10): 705-710.
[19] �պ������ա��ܣ��� �ᣬ�� �. ���Ѽ���Ͻ���������TiO2Ĥ���Ʊ��о�[J]. �Ͼ����պ����ѧѧ��, 2005, 37(5): 597-602.
TAO Hai-jun, TAO Jie, WANG Ling, WANG Wei. Fabrication of nano-porous TiO2 films on pure titanium and its alloy[J]. Journal of Nanjing University of Aeronautics & Astronautics, 2005, 37(5): 597-602.
[20] TAO Hai-jun, TAO Jie, WANG Tao, WANG Ling, QIN Liang, XU Lu-lu. Fabrication of self-organized TiO2 nanotubes by anodic oxidation and their photocatalysis[J]. Trans Nonferrous Met Soc China, 2005, 15(S3): 462-466.
������Ŀ������ʡ��Ȼ��ѧ����������Ŀ(BK2004129)�����ջ���������Ŀ(04H52059)
�ո����ڣ�2006-10-28�������ڣ�2007-03-05
ͨѶ���ߣ��� �ܣ����ڣ��绰��025-52112900; E-mail: taojie@nuaa.edu.cn
(�༭��������)


