DOI��10.19476/j.ysxb.1004.0609.2019.05.18
�Ȼ��ѡ���Խ������������м۽���
����1����־��1���� ��2�����˳1���� Ҷ1���Դ���1
(1. ����������ѧ ұ���뻯ѧ����ѧԺ������ 341000��
2. ����ʡұ���о����������ι�˾��֣�� 450053)
ժ Ҫ��
����ʪ���Ȼ��ķ���������Ч������ĺ������������ӵĽ����������Ȼ��-������ϵѡ���Խ��������������м۽���������������ڽ����¶�90 �桢����Ũ��2 mol/L����Һ��1:6������ʱ��90 min���������Ľ�����Ϊ89.45%���ܵĽ�����Ϊ88.56%���̵Ľ�����Ϊ90.23%�������Ľ�����ֻ��19.30%��ʵ�����ڵ�������µ�ѡ���Խ������Ժ��������в�ͬ������������Һ�еĽ��������������о���������������εļ�������������������ܽ⣬��������������Ӱ�첻��������ˣ����εļ��������������������м۽����Ľ������������������������Ľ�����
�ؼ��ʣ�
�Ȼ��������������ѡ���Խ��������������������
���±�ţ�1004-0609(2019)-05-1049-09���� ��ͼ����ţ�TF815���� ���ױ�־�룺A
�����ճ���������һ�ַdz���Ҫ����ɫ������������������õĵ����ԡ������ԡ���ʴ�ԣ����㷺���ڲ���֡����������Բ����Լ���Ƶ���ҵ���ǹ��Ҿ��ú���ᷢչ����Ҫս����Դ[1]������ԭ������Դ��Ҫ��Ϊ������������ͺ����̽�ˣ�½������Դ��65%Ϊ��������[2]��35%Ϊ����������������IJ��Ͽ��ɣ��俪���ѶȲ��ϼӴ���Դ����ݽߣ����Կ������ú���������Դ��������[3]��
����������Ժ��������ұ���о���Ϊ�о����ȵ㣬�������ն��ֶ�������Ҫ��Ϊ���պ�ʪ������[4-5]����ұ���ʺϴ�����þ�����͵ĸ�ֳ�����������Ҫ�Dz��û�ԭ���յķ����Ʊ������Ͻ�ͻ�ԭ������������ﳣ������ܺĸ��һ����������β��[6-8]��ʪ��ұ��������ԭ����-����������ѹ������ͳ�ѹ��������������ܺĵ͡����ʸ߽�����Ҳһֱ���ܹ�ע[9-12]����ԭ����-�������������ڹ�ҵ�������������й��ճ��졢�������ʸߵ��ŵ㣬ȱ�������̸��ӡ��ܻ����ʵ�[13]����ѹ��������������м۽��������ʸ߶��������ʵ��ܵ��㷺��ע�����ǿ��̵IJ���������������Ӧ��[14-15]����ѹ������վ��ܲ������м۽��������ʸߣ����ǹ��ߵ���ĺͽϵ͵�ѡ�������������ķ�չ[16-17]��
�Ȼ�ұ����һ�ֱ�����Ƶķ�����������ʵ���м۽������������ʽ�����þ�ȵĸ�Ч��������ܵ�ѡ������ȡ[18-22]��FAN��[23]������ˮ�Ȼ�����Ϊ�Ȼ������û���̼��ԭ��ĺ���������300~500 �����ѡ�����Ȼ��������ܵ��Ȼ��ʿ��Դﵽ90%���ϣ��������Ȼ�С��4%��FAN��[24]����ˮ���Ȼ�������Ϊ�Ȼ�����Ԥ��ԭ��ĺ�������ѡ�����Ȼ������Ȼ������Ȼ��ܣ������ܵ��Ȼ����Դﵽ90%���ң����������ʵ��Ȼ��õ����������ơ��������[17]�����Ȼ�����-�����ķ���������������ȡ�����г�Ч���о��ɹ������кܸߵ�ѧ����ֵ�����Ȼ�ʪ��ұ����������������ص����ƣ����Ȼ���ˮ��Һ��ϵ�������ܽ�ȡ������ӻ�ȡ��γ������ͻ�ԭ��λ�ȷ����������֮�⣬�����Ӿ��к�ǿ��ȥ�����������ۻ������ö�ʪ��ұ�����Ҳ������[19, 25-26]������������Щ���ƣ��Ȼ�ʪ��ұ����������ص����ƽ���Ϊδ����չ���ص㡣
�������߰��Ȼ�識��뵽ϡ������Һ�У�ͨ�����εļ��������������ӻ�ȴӶ�����������������ﵽ�������Ч����ͬʱ�������ʽ����Ľ�����ʵ�ֶԺ����������м۽���ѡ������ȡ������ͬʱ�����첻ͬ���ض��м۽���ѡ������ȡ��Ӱ�죬�Լ�ʵ��ѡ������ȡ�Ļ��������ĵ��о��ɹ�����Ϊ�Ȼ�ʪ��ұ��ķ�չ�ṩһ���µķ�չ����ͬʱҲΪ���������ʪ�����������ṩһ���µ�˼·��
1 ʵ��
1.1 ʵ��ԭ�ϼ�����
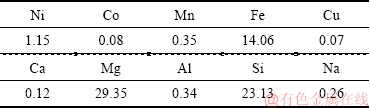
ʵ�����õ�Ʒλ������������Դ������Ԫ����ͬ�ر���ȵĺ���������������ĥ��Ͼ��Ⱥ����150 ��m��ɸ֮�����ʵ���о���ͨ����ʵ����Ʒ���гɷַ����������1��
��1 ����������Ʒ��ѧ�ɷַ���
Table 1 Chemical composition analysis of sample (mass fraction, %)
��ԭ��������������ͼ1��ʾΪԭ���XRD�ס���ͼ1���Կ������������Ҫ�ɷ�Ϊ����ʯ(Mg3[Si2O5(OH)4])��������(FeO(OH))����������(SiO2)������������(Fe3O4��Fe2O3)����Ͽ�ʯ�Ļ�ѧ�ɷ֣�����Ϊ�����ڹ�þ���ͺ�������
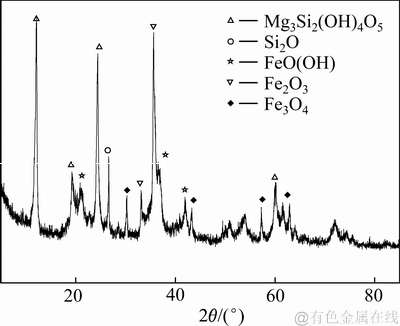
ͼ1 ԭ���XRD��
Fig. 1 XRD pattern of raw ore
1.2 ���鷽��
��ѹ�����£������Խ�����Һ�м���һ���������Ȼ�泥���һ���¶���ֱ�ӽ������������е��м۽��������岽��Ϊ��������һ��Ũ�ȵ�������Һ�����������Ȼ�狀������Ͷ����������ƿ�ڻ�ϣ����ƽ����ٶȺͷ�Ӧ�¶ȣ���Ӧһ��ʱ���Һ���룬�������̼�ͼ2��ʾ�������ڹķ�ɺ�����105 ���º�ɺ��ü�⣬������Һ�������ܡ��̡�����Ԫ�صĺ�����������ʡ��������ǽ���Һ�н������ӵĺ�����ԭ���н��������ı�ֵ(��)[27]���ɱ�ʾΪ
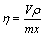
ʽ�У�VΪ����Һ�������V����Ϊ����Һ��Ũ�ȣ�g/mL��mΪԭ���������g��xΪԭ���еĽ����ĺ�����%��
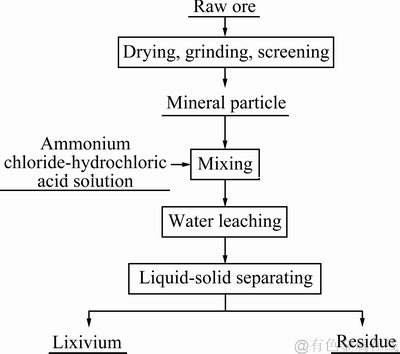
ͼ2 �Ȼ�������������ͼ
Fig. 2 Process flow of hydro-chloride leaching
1.3 ��������
���û�ѧ�ζ������ķ����ⶨ��Һ��������Ũ�ȣ�����WFX-1380��ԭ�����շֹ��ȼƷ�������Һ�������ܡ��̵Ƚ������Ӻ���������D8 Advance X-���������Ƕ�ԭ��ͽ�����������������������ձ�������˾SU8000�����������-�����ǶԽ���������SEM-EDS������
2 ���������
2.1 ��ͬ���ζ��м۽��������ʵ�Ӱ��
��ȡ����10 g������Ũ��Ϊ2 mol/L����Һ��1:6����Ӧ�¶�90 �棬����ʱ��1.5 h������һ���Ľ����ٶȣ�����������Ũ��3 mol/L�IJ�ͬ���ζ��м۽��������ܡ��̺���������Ӱ�죬���õ��������ܡ��̡����Ľ�������ͼ3��ʾ��
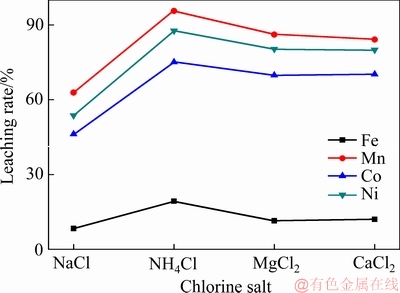
ͼ3 ��ͬ���ζԽ��������ʵ�Ӱ��
Fig. 3 Influence of different chlorine salt on leaching rate of metals
��ͼ3���Կ�������������Ũ�Ⱦ�Ϊ3 mol/L�IJ�ͬ���ν���ʵ��ʱ���Ȼ��ƶԸ������ӵĽ�������ͣ����Ȼ�臨Ը������ӵĽ�������ߣ��Ȼ�þ���Ȼ��ƶԸ����ӵĽ����ʴ�֮��������������ۺϿ��ǣ���ʵ����õ��������Ȼ�什��ˡ�
2.2 ����Ũ�ȶ��м۽��������ʵ�Ӱ��
��ȡ����10 g���Ȼ��Ũ��Ϊ3 mol/L����Һ��1:6����Ӧ�¶�90 �棬����ʱ��1.5 h������һ���Ľ����ٶȣ���������Ũ�ȶ��м۽��������ܡ��̺���������Ӱ�죬���õ��������ܡ��̡����Ľ�������ͼ4��ʾ��
��ͼ4���Կ�������������Ũ�ȵ����ӣ������ܡ��̡����Ľ����ʶ������ӡ�����Ũ����1mol/L���ӵ�2mol/Lʱ���ܵĽ�������������ԣ���45.66%���ӵ�75.09%��������̵Ľ����ʣ���70.21%���ӵ�95.60%�� ���������Ľ�������߲����������Ľ�������76.45%���ӵ�87.67%��������Ũ����2 mol/L���ӵ�4 mol/Lʱ�������ܡ���3�ֽ������ӵĽ�������߲����ԣ������Ľ�������19.3%���ӵ�60%�����������߷dz���������Ȼ������������������ڿ�����������Ľ������ӵĽ����������м۽������ӵĽ�����û�����Ե���ߣ����ǵ��������̼�����ĵijɱ��Լ���Ũ������豸�ĸ�ʴ��ͬʱ���Ժ����������������Ҫ������֤���Ľϵͽ����ʣ��Խ��ͺ��ھ��������Ĵ���������ˣ�ȷ������Ũ��Ϊ2mol/L��
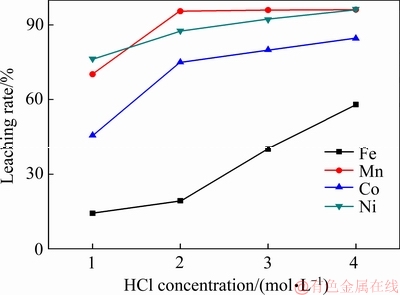
ͼ4 ����Ũ�ȶԽ��������ʵ�Ӱ��
Fig.4 Influence of hydrogen chloride concentration on leaching rate of metals
2.3 �Ȼ��Ũ�ȶ��м۽��������ʵ�Ӱ��
��ȡ����10 g������Ũ��Ϊ2 mol/L����Һ��1:6����Ӧ�¶�90 �棬����ʱ��1.5h������һ���Ľ����ٶȣ������Ȼ��Ũ�ȶ��м۽��������ܡ��̺���������Ӱ�죬���õ��������ܡ��̡����Ľ�������ͼ5��ʾ��
��ͼ5���Կ��������Ȼ��Ũ����0���ӵ�3 mol/Lʱ�����Ľ�������69.85%���ӵ�89.7%���ܵĽ�����45.26%���ӵ�75.09%���̵Ľ�������53.64%���ӵ�95.6%�������Ľ����ʻ������ֲ��䡣���� ���Ũ�ȳ���3 mol/Lʱ�����н������ӵĽ�����û����������ߡ��ۺϿ��ǣ��Ȼ�淋�Ũ��Ϊ3 mol/LΪ�ˡ�
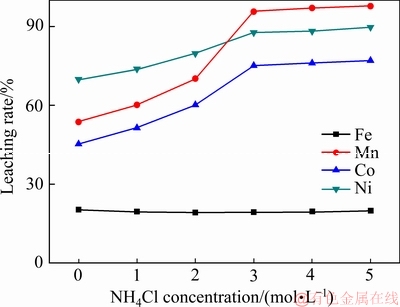
ͼ5 �Ȼ��Ũ�ȶԽ��������ʵ�Ӱ��
Fig. 5 Influence of ammonium chloride concentration on leaching rate of metals
��������-�Ȼ����Һ��ϵ�����������������ṩ�����Ӳ�����Һ�����Ի�������������Һ�м����Ȼ�泥����������ӵĺ������������������Һ�������ӻ��[28-29]����Ƚϴ�ͳ����ֻ����8 mol/L�ĸ��������²��ܻ�ýϸߵĽ�����[30]���ù����������������ʹ��[31]��ʵ�����������-�Ȼ�����Һ�����������������Ľ����������еĹ�ϵ���ڽϵ͵��¶��£���Ҫ����Һ�������������������Ũ����Ӱ�����������������أ������¶ȳ���80 ��ʱ���������ӵĽ�������ȡ�������Ũ�ȣ���ȡ���������ӵ�Ũ�ȡ�����������ı������ˮ�ϣ����ͨ�����Ӻ������ӵ����������沿λ�������ﵽ�ܽ��Ч��[32]��������Һ�ܽ�������Ļ����ɱ�ʾΪ��������������������ӽ���γ����ȵ������䷴Ӧ���£�
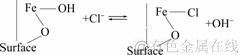
�γɵ����������Һ�е������ӽ���������Ŀ�������������ʵ���ڲ�������Ũ�ȵ������´ٽ�����������ķֽⷴӦ���䷴Ӧ���£�
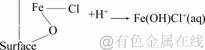
 ��
��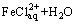
�ܷ�Ӧ��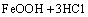 ��
��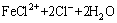
2.4 �����¶ȶ��м۽��������ʵ�Ӱ��
��ȡ����10 g���Ȼ��Ũ��Ϊ3 mol/L������Ũ��Ϊ2 mol/L����Һ��1:6������ʱ��1.5 h������һ���Ľ����ٶȣ���������¶ȶ��м۽��������ܡ��̺���������Ӱ�죬���õ��������ܡ��̡����Ľ�������ͼ6��ʾ��
��ͼ6���Կ������¶ȶ������ܡ��̺����Ľ������нϴ��Ӱ�죬��һ�����¶ȷ�Χ�ڣ����Ž����¶ȵ����ߣ������ܡ��̺����Ľ����ʶ���һ�������ӣ� �����¶ȶ������ܡ��̽����ʵ�Ӱ��̶ȴ���һֱ���������¶ȳ���80 ��ʱ�������ܡ��̵Ľ������������ƽ������������Ľ������������ƽ�С���������������¶ȵ����ӣ���Һ�������ӶԿ����Ӱ���������ӣ��������м۽��������ܡ��̵Ľ��������¶ȴﵽ90 ������ſ������м۽��������IJ��ϼ��٣������Ѷ����ӣ��ڼ��������¶����Ľ����ʽ����������ӡ����Ա�ʵ����ý����¶�Ϊ90 �档

ͼ6 �����¶ȶԽ��������ʵ�Ӱ��
Fig. 6 Influence of leaching temperature on leaching rate of metals
2.5 Һ�̱ȶ��м۽��������ʵ�Ӱ��
��ȡ����10 g������Ũ��Ϊ2 mol/L����Һ��1:6���Ȼ�淋�Ũ��Ϊ3 mol/L������ʱ��1.5 h������һ���Ľ����ٶȣ���������¶ȶ��м۽��������ܡ��̺���������Ӱ�죬���õ��������ܡ��̡����Ľ�������ͼ7��ʾ��
��ͼ7��֪������Һ�̱ȵ����ӣ������ܡ��̵Ľ����ʶ�������ߣ������Ľ����ʼ���û�����ӣ�����Һ�̱���6���ӵ�8ʱ���м۽����Ľ����ʼ������䣬�����Ľ��������ӽ�Ϊ����������Ҫ�����ڿ�ʼ����Һ�̱�ʱ��Ҫ�������������е��м۽������ﵽһ���̶Ⱥ��е��м۽������ӽ��٣����ѽ�����������Һ�̱Ȼ�ʹ�����������ӽ������ӡ����ݵ�����ʵ������ȷ������Ũ��Ϊ2 mol/L���Ȼ��Ũ��Ϊ3 mol/L�������ڿ���Һ�̱�ʱ����Һ��Ũ�ȶ���ȷ���ģ�����Һ�̱ȵ����ӣ���Ӧ��������Ȼ�淋�����Ҳ�����ӣ�������Һ�����Ľ�������Ӧ�����ӡ����Բ���Һ�̱�Ϊ6Ϊ�ˡ�
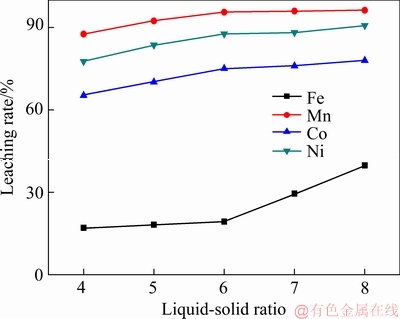
ͼ7 Һ�̱ȶԽ��������ʵ�Ӱ��
Fig. 7 Influence of liquid-solid ratio on leaching rate of metals
2.6 ����ʱ����м۽��������ʵ�Ӱ��
��ȡ����10 g������Ũ��Ϊ2 mol/L����Һ��1:6���Ȼ�淋�Ũ��Ϊ3 mol/L�������¶�90 �棬����һ���Ľ����ٶȣ��������ʱ����м۽��������ܡ��̺��������ʵ�Ӱ�죬�����ͼ8��ʾ��
��ͼ8��֪���ӷ�Ӧ��ʼ�Σ��м۽����Ľ���������ʱ����ӳ��Ϳ�ʼ���ӣ�ʱ����30 min��90 minʱ���м۽��������ܡ��̵Ľ����ʶ����Ӹ������������Ľ�������ȻҲ�����ӣ����ǽ�����������С����Ҫԭ�����������Ȼ��-������ϵ�Ľ�����Ӧ���м۽������������ܡ���Ҫ�����������Ƚ��������ŷ�Ӧ�Ľ��У��м۽����Ĵﵽһ���Ľ����ʺ����������������������90 min�Ժ��м۽����Ľ����ʼ������䣬�����Ľ��������ӽ�Ϊ��������ˣ��ϺõĽ���ʱ��Ϊ90 min��
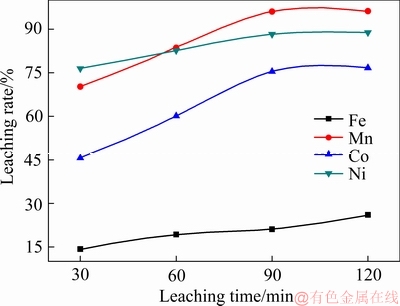
ͼ8 ����ʱ��Խ��������ʵ�Ӱ��
Fig. 8 Influence of leaching time on leaching rate of metals
3 ������������
����ԭ���������������֪�����������е��м۽�����Ҫ�����������ʽ�����ڲ�ͬ�����У��о����������в�ͬ������ܽ�������˽��м۽��������ܺ����Լ����ʽ������Ľ�����Ϊ����Ҫ���塣���ݿ���ѧ������֪����ʵ����Ҫ�ĺ���������Ŀ���������������Ͳ�ͬ�������IJ�״�����ε�����ʯ�ĺ�����ʯ������ǰ���о��ɹ��뷽��[33]�����������������-�Ȼ����ϵ�Ժ��������е��м۽����������������о���
�������������Ӧ�����У���Ҫ������ܽ����ã��������е��м۽����ܽ��Һ�С����м۽��������ܡ�����Ҫ�����������εĿ����У�ͬʱ��Ҳ�������������ʽ�����ڹ����ο����С�����ԭ�������о����������֪����������������Һ�н������ܷ�������Ҫ��ѧ��Ӧ��
NiFe2O4(s)+2H+=Ni2++Fe2O3(s)+H2O(l)
CoFe2O4(s)+2H+=Co2++Fe2O3(s)+H2O(l)
MnFe2O4(s)+2H+=Mn2++Fe2O3(s)+H2O(l)
2NiO��SiO2(s)+4H+=2Ni2++2SiO2(s)+2H2O(l)
2MnO��SiO2(s)+4H+=2Mn2++2SiO2(s)+2H2O(l)
NiO(s)+2H+=Ni2++H2O(l)
CoO(s)+2H+=Co2++H2O(l)
FeO(OH)(s)+3H+=Fe3++2H2O(l)
Fe2O3(s)+6H+=2Fe3++3H2O(l)
��Ͽ�����������п��ܷ����ķ�Ӧ����ʽ���Կ��������Ի����Կ�����ܽ��о����Ե����ã���������ܽ����ֱ�Ӿ����������ӵĽ�����Ϊ����ˣ��о������в�ͬ����������Һ���ܽ�仯����ʮ����Ҫ����ԭ���XRD��֪������������ڵ���Ҫ����Ϊ������ʯ����(Mg3[Si2O5(OH)4])�����������(FeO(OH))�����������(Fe2O3)�ʹ��������(Fe3O4)��ͨ���Բ�ͬ�����¿���Ľ������е�XRD�������Եó�����Ҫ�����ڽ���ʱ�����ı仯��������������������������Һ�еĽ���������
ͼ9��ʾΪ���������������䡢��ͬ��Ũ���º��������������XRD�ס���ͼ9��֪��������Ũ�ȵ����ӣ�����������ڲ�ͬλ�õ��������շ��нϴ�ı仯�����������������ֱ����ʧ������Ũ��Ϊ2 mol/Lʱ���������еĿ������Ѿ���������������࣬������ʯ�����������Ũ�ȵ�����Ҳ����ʧ�� �γ�SiO2������ͼ������ʯ���������������������������бȽϿ�֪������������ڽ�������������������ʯ������ȷ����ܽ⡣�����������ʹ������������Ũ�Ƚϵ�ʱ���ѷ�����Ӧ����Ҳ��ʵ���������Ľ����ʽϵ����Ǻϡ�
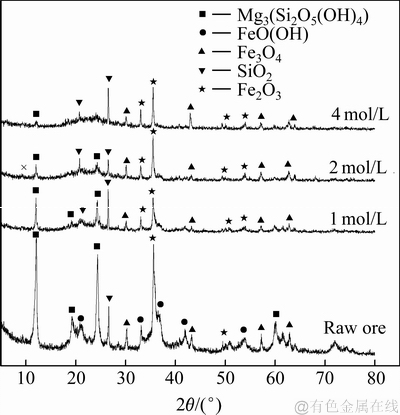
ͼ9 ��ͬ��Ũ�Ⱥ������������XRD��
Fig. 9 XRD patterns of leaching residue with different acid concentrations
ͼ10��ʾΪ�̶�����Ϊ��ѹ���������ͬ�����¶��º��������������XRD�ס���ͼ10��֪���������¶����ӵ�50 ���90 ��ʱ����������������ʯ�������ض�λ�õ��������շ嶼��������Щλ�õ�������������ʧ�����������¶ȴﵽ90 ��ʱ���������л���û����������࣬����������ʯ���࣬���������¶ȸ���������������ܽ⡣��Ͻ�����ʵ������֪�������¶ȵ������м۽����Ľ����ʲ������ӣ������Ľ��������Ӳ����ԣ�Ҳ��֤�¶ȶԺ��������п����Ӱ������������������ʹ�������������¶ȵı仯�����������¶ȴﵽ90 ��ʱ���������еij�����ʹ��������û�иı䣬˵���侧��ṹ���ȶ������������¶��������м۽����Ľ����ʣ���ʵ��������ϡ�
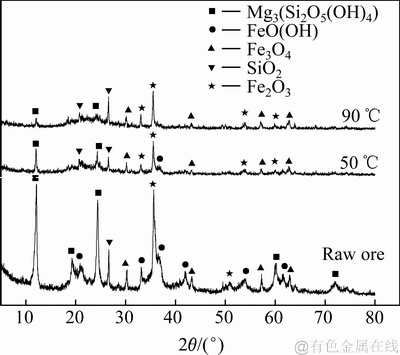
ͼ10 ��ͬ�����¶��º������������XRD��
Fig. 10 XRD patterns of leaching residue at different leaching temperatures
ͼ11��ʾΪ�̶���ʱ����������Ϊ��ѹ��������º������������XRD�ס���ͼ11��֪�����Ž���ʱ������ӣ�����������ڲ�ͬλ�õ��������շ��нϴ�ı仯��������ʱ��ﵽ60 minʱ��������������ض�λ�õ��������������ʧ������ʯ�����������������Ž���ʱ�������Ҳ�����Եı仯�������ڲ�ͬλ�û�����µ�SiO2��������壬������������ʯ����Ҳ���ϵķֽ⣬��������ƻ���������������е�SiO2�ͱ��ͷų�����������ʱ��IJ������ӣ����������ʹ����������Ե������ǿ�ȶ��Dz��ϼ��������ƣ����ʵ������֪�����Ž���ʵ��ʱ������ӣ����Ľ������������������м۽����Ľ����ʻ��������Ա仯��

ͼ11 ��ͬ����ʱ������������XRD��
Fig. 11 XRD patterns of leaching residue at different leaching time
4 ����
1) ʵ��ȷ��������-�Ȼ����ϵ���������������ѹ�������Ϊ�������¶�Ϊ90 �棬����Ũ��Ϊ2 mol/L����Һ��1:6������ʱ��Ϊ90 min�����������Ľ�����Ϊ89.45%���ܵĽ�����Ϊ88.56%���̵Ľ�����Ϊ90.23%�������Ľ�����ֻ��19.30%��ʵ����ѡ���Խ�����
2) ͨ��������-�Ȼ����Һ��ϵ��������������������о�������������й��������������������ֽⷴӦ������ʯ�����в����ܽ⣬�ͷų��м۽�������ͬʱҲ�����SiO2�������������ʹ���������Ϊ�ȶ���
REFERENCES
[1] �� ��, ����M, �밲��, �� ��. ȫ��������Դ����������״���������[J]. �������������, 2016(1): 64-69.
ZHANG Liang��YANG Hui-peng, FENG An-sheng, CAO Fei. Study on current situation and analysis of supply and demand of global nickel resource[J]. Conservation and Utilization of Mineral Resources, 2016(1): 64-69.
[2] ��С��, ������, �Կ�ѧ, ���ķ�, ��־��, ������. ��������ұ�������о���״����չ[J]. ���ϵ���, 2014, 28(5): 112-116.
LI Xiao-ming, BAI Tao-tao, ZHAO Jun-xue, LI Wen-feng, LI Zhi-guo, CUI Ya-ru. Status and progress of metallurgical technology on laterite nickel ore[J]. Materials Review, 2014, 28(5): 112-116.
[3] ʯ����, ��־��, ������, ������, ���º�, ���Ľ�. ����������ữ���շ�����������ȡ����[J]. �й���ɫ����ѧ��, 2013, 23(2): 510-515.
SHI Jian-feng, WANG Zhi-xing, HU Qi-yang, GUO Hua-jun, LI Xin-hai, PENG Wen-jie. Recovery of nickel and cobalt from nickel laterite ore by sulfation roasting method using ammonium bisulfate[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(2): 510-515.
[4] �� չ. �������������컯����-ˮ������Һ�л������ܵȼ۽������о�[D]. ��ɳ: ���ϴ�ѧ, 2011.
WU Zhan. Recovery of valuable metals such as nickel and cobalt from sulfuric acid roasting and water leaching of laterite nickel ore [D]. Changsha: Central South University, 2011.
[5] MCDONALD R G, WHITTINGTON B I. Atmospheric acid leaching of nickel laterites review. Part 2. Chloride and bio-technologies[J]. Hydrometallurgy, 2008, 91(1/4): 35-55.
[6] ��ѧ��, �� ��, ���컪, ʯ����. �����컯-���շ������������л��������ܶ���ѧ�о�[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2012, 43(4): 23-27.
GUO Xue-yi, LI Dong, TIAN Qing-hua, SHI Wen-tang. Kinetics of sulfation-roasting of nickel laterite for recovery of nickel and cobalt[J]. Journal of Central South University (Science and Technology), 2012, 43(4): 23-27.
[7] MARAGKOS I, GIANNOPOULOU I P, PANIAS D. Synthesis of ferronickel slag-based geopolymers[J]. Miner Engineering, 2009, 22(2): 196-203.
[8] MU Wen-ning, ZHAI Yu-chun. Desiliconization kinetics of nickeliferous laterite ores in molten sodium hydroxide system[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(2): 330-335.
[9] �� ɳ, ��С��, ֣ ��, �� ��. �����������ữ����-ˮ��ʵ���о�[J]. ϡ�н���, 2010, 34(3): 406-412.
QIU Sha, CHE Xiao-kui, ZHENG Qi, DUAN Jin. Experimental study on laterite-nickel ore with sulfating roasting-water immersion methods[J]. Chinese Journal of Rare Metals, 2010, 34(3): 406-412.
[10] B��Y��KAKINCI E, TOPKAYA Y A. Extraction of nickel from lateritic ores at atmospheric pressure with agitation leaching[J]. Hydrometallurgy, 2009, 97(1): 33-38.
[11] LI Guang-hui, RAO Ming-jun, LI Qian, PENG Zhi-wei, JIANG Tao. Extraction of cobalt from laterite ores by citric acid in presence of ammonium bifluoride[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(8): 1517- 1520.
[12] ������, ���⽿, �� ˶, �� ��, ������. �����������ѹ���������������[J]. ϡ�н���, 2016, 40(7): 715-720.
MA Bao-zhong, YANG Wei-jiao, WANG Shuo, YANG Bo, WANG Cheng-yan. High-pressure sulfuric acid leaching of laterite ores using nitrate ion as an oxidant[J]. Chinese Journal of Rare Metals, 2016, 40(7): 715-720.
[13] ZUNIGA M, PARADA F, ASSELIN E. Leaching of a limonitic laterite in ammoniacal solutions with metallic iron[J]. Hydrometallurgy, 2010, 104(2): 260-267.
[14] MA Bao-zhong, WANG Cheng-yan, YANG Wei-jiao, YANG Bo, ZHANG Yong-lu. Selective pressure leaching of Fe (II)-rich limonitic laterite ores from Indonesia using nitric acid[J]. Minerals Engineering, 2013, 45(3): 151-158.
[15] WHITTINGTON B, MUIR D M. Pressure acid leaching of nickel laterites: A review[J]. Mineral Processing and Extractive Metallurgy Review, 2000, 21(6): 527-599.
[16] LUO Jun, LI Guang-hui, RAO Ming-jun, PENG Zhi-wei, ZHANG Yuan-bo, JIANG Tao. Atmospheric leaching characteristics of nickel and iron in limonitic laterite with sulfuric acid in the presence of sodium sulfite[J]. Minerals Engineering, 2015, 78: 38-44.
[17] ������, �� ��, ����ǿ, �� ��, �� ��. �����������������������չ[J]. �й���ɫ����ѧ��, 2008, 18(1): 1-8.
WANG Cheng-yan, YIN Fei, CHEN Yong-qiang, WANG Zhong, WANG Jun. Worldwide processing technologies and progress of nickel laterites[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): 1-8.
[18] ZHAI Yu-chun, MU Wen-ning, LIU Yan, XU Qian. A green process for recovering nickel from nickeliferous laterite ores[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(S1): s65-s70.
[19] LAKSHMANAN V I, SRIDHAR R, CHEN J, HALIM M A. Development of mixed-chloride hydrometallurgical processes for the recovery of value metals from various resources[J]. Transactions of the Indian Institute of Metals, 2016, 69(1): 39-50.
[20] ZHOU Shi-wei, WEI Yong-gang, LI Bo, WANG Hua, MA Bao-zhong, WANG Cheng-yan. Chloridization and reduction roasting of high-magnesium low-nickel oxide ore followed by magnetic separation to enrich ferronickel concentrate[J]. Metallurgical and Materials Transactions B, 2016, 47(1): 145-153.
[21] ������, ������, ���º�, ��־��, ������. ��ʴ����ȡԤ��ԭ����������������[J]. �й���ɫ����ѧ��, 2012, 22(11): 3208-3213.
ZHAO Yu-xian, HU Qi-yang, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun. Extraction of nickel and cobalt from reductive laterite by corrosion process[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(11): 3208-3213.
[22] LI Jin-hui, LI Yang-yang, GAO Yan, ZHANG Yun-fang, CHEN Zhi-feng. Chlorination roasting of laterite using salt chloride[J]. International Journal of Mineral Processing, 2016, 148: 23-31.
[23] FAN Chuan-lin, ZHAI Xiu-jing, FU Yan, CHANG Yong- feng, LI Bin-chuan, ZHANG Ting-an. Extraction of nickel and cobalt from reduced limonitic laterite using a selective chlorination�Cwater leaching process[J]. Hydrometallurgy, 2010, 105: 191-194.
[24] FAN Chuan-lin, ZHAI Xiu-jing, FU Yan, CHANG Yong- feng, LI Bin-chuan, ZHANG Ting-an. Leaching behavior of metals from chlorinated limonitic nickel laterite[J]. International Journal of Mineral Processing, 2012, 110: 117- 120.
[25] ZHANG Pei-yu, GUO Qiang, WEI Guang-ye, MENG Long, HAN Lin-xin, QU Jing-kui, QI Tao. Leaching metals from saprolitic laterite ore using a ferric chloride solution[J]. Journal of Cleaner Production, 2016, 112: 3531-3539.
[26] DEHGHAN R, NOAPARAST M, KOLAHDOOZAN M. Leaching and kinetic modeling of low-grade calcareous sphalerite in acidic ferric chloride solution[J]. Hydrometallurgy, 2009, 96 (4): 275-282.
[27] ������. �����������м۽�����ȡ�����о�[D]. ����: ����������ѧ, 2015.
LI Yang-yang. Research on the extraction processof valuable metals in laterite nickel ore[D]. Ganzhou: Jiangxi University of Science and Technology, 2015.
[28] JU Shao-hua, ZHANG Li-bo, PENG Jin-hui, SHI Zhe, GUO Sheng-hui, LIU Bin-guo, WANG Ya-jian. Thermodynamics of leaching roasted jarosite residue from zinc hydrometallurgy in NH4Cl system[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(4): 1179-1183.
[29] ZHAO Pin, GAO Bao-yu, YUE Qin-yan, LIU Si-cheng, SHONB H K. The performance of forward osmosis in treating high-salinity wastewater containing heavy metal Ni2+[J]. Chemical Engineering Journal, 2016, 288: 569-576.
[30] LI Jin-hui, XIONG Dao-ling, CHEN Hao, WANG Rui-xiang, LIANG Yong. Physicochemical factors affecting leaching of laterite ore in hydrochloric acid[J]. Hydrometallurgy, 2012, 129/130: 14-16.
[31] SENANYAKE G. Review of theory and practice of measuring proton activity and pH in concentrated chloride solutions and application to oxide leaching[J]. Minerals Engineering, 2007, 20(7): 634-645.
[32] COMELL R M, POSNER A M, QUIRK JP. Kinetics and mechanisms of the acid dissolution of goethite (��-FeOOH)[J]. Journal of Inorganic and Nuclear Chemistry, 1976, 38(3): 563-567.
[33] ����, ���º�, ������, ��־��, ����Ԫ, ֣����, �� ��. �����ǿ������������������[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2010, 41(5): 1691-1697.
LI Jin-hui, LI Xin-hai, HU Qi-yang, WANG Zhi-xing, ZHOU You-yuan, ZHENG Jun-chao, WU Ling. Enhancement of nickel extraction from laterite in hydrochloride acid through activated roasting[J]. Journal of Central South University (Science and Technology), 2010, 41(5): 1691-1697.
Selectively leaching valuable metals from laterite nickel ore by ammonium chloride
LI Jin-hui1, XU Zhi-feng1, GAO Yan2, LI De-shun1, LIU Ye1, ZHAO Chun-die1
(1. School of Metallurgy and Chemical Engineering, Jiangxi University of Science and Technology, Ganzhou 341000, China;
2. Henan Institute of Metallurgy Co., Ltd., Zhengzhou 450053, China)
Abstract: The hydro-chloride leaching can reduce the impurity ion leaching and consumption of acid effectively. The selectively leaching valuable metals from laterite nickel ore with ammonium chloride hydrochloric acid solution were studied. The results show that when the leaching temperature is 90 ��, hydrochloric acid concentration is 2 mol/L, solid-liquid ratio is 1:6 and leaching time is 1.5 h, the leaching rates of nickel, cobalt, manganese and iron are 89.45%, 88.56%, 90.23% and 19.30%, respectively, which achieve selectively leaching in relatively low acid concentration. Based on the selective leaching mechanism research, the addition of chlorine salt is beneficial to dissolution of goethite than other iron minerals in laterite ore, leading to increasing leaching of valuable metals from goethite mineral and suppression leaching of iron from other iron minerals.
Key words: ammonium chloride; laterite nickel ore; selective leaching; leaching mechanism; ion activity
Foundation item: Project(GJJ160593) supported by the Jiangxi Department of Education, China; Project (20161ACG70010) supported by the Jiangxi Science and Technology Department, China; Project(2017KY17) supported by the Jiangxi Postdoctoral Fund, China
Received date: 2017-10-16; Accepted date: 2018-11-20
Corresponding author: XU zhi-feng; Tel: +86-797-8312047; E-mail:xzf_l@163.com
(�༭ ����)
������Ŀ������ʡ��������Ŀ(GJJ160593)������ʡ�Ƽ�����Ŀ(20161ACG70010)������ʡ��ʿ�������Ŀ(2017KY17)
�ո����ڣ�2017-10-16�������ڣ�2018-11-20
ͨ�����ߣ���־�壬���ڣ���ʿ���绰��0797-8312047��E-mail��xzf_l@163.com
ժ Ҫ������ʪ���Ȼ��ķ���������Ч������ĺ������������ӵĽ����������Ȼ��-������ϵѡ���Խ��������������м۽���������������ڽ����¶�90 �桢����Ũ��2 mol/L����Һ��1:6������ʱ��90 min���������Ľ�����Ϊ89.45%���ܵĽ�����Ϊ88.56%���̵Ľ�����Ϊ90.23%�������Ľ�����ֻ��19.30%��ʵ�����ڵ�������µ�ѡ���Խ������Ժ��������в�ͬ������������Һ�еĽ��������������о���������������εļ�������������������ܽ⣬��������������Ӱ�첻��������ˣ����εļ��������������������м۽����Ľ������������������������Ľ�����
[1] �� ��, ����M, �밲��, �� ��. ȫ��������Դ����������״���������[J]. �������������, 2016(1): 64-69.
[4] �� չ. �������������컯����-ˮ������Һ�л������ܵȼ۽������о�[D]. ��ɳ: ���ϴ�ѧ, 2011.
[9] �� ɳ, ��С��, ֣ ��, �� ��. �����������ữ����-ˮ��ʵ���о�[J]. ϡ�н���, 2010, 34(3): 406-412.
[27] ������. �����������м۽�����ȡ�����о�[D]. ����: ����������ѧ, 2015.


