DMSO���Ʊ�Eu-Fe�Ͻ�Ĥ���о�
��ɽ��ѧ��ѧ�뻯ѧ����ѧԺ������ѧ�о���,��ɽ��ѧ��ѧ�뻯ѧ����ѧԺ������ѧ�о���,��ɽ��ѧ��ѧ�뻯ѧ����ѧԺ������ѧ�о���,��ɽ��ѧ��ѧ�뻯ѧ����ѧԺ������ѧ�о���,��ɽ��ѧ��ѧ�뻯ѧ����ѧԺ������ѧ�о��� �㶫����510275 ,�㶫����510275 ,�㶫����510275 ,�㶫����510275 ,�㶫����510275
ժ Ҫ��
�о��˶������� (DMSO) ��Eu3+ ��Fe2 + ��Pt�缫�ϵĵ绯ѧ��Ϊ��Eu3+ �Ļ�ԭΪ���������滹ԭ , �Ȼ�ԭΪEu2 + , Eu2 + �ٻ�ԭΪEu ;��Fe2 + ��һ�������Ӳ�������̻�ԭΪFe, ������ѭ������������� 0 .0 1mol��dm- 3FeCl2 0 .0 2mol��dm- 3������ 0 .1 0mol��dm- 3Li ClO4 DMSO��Һ�� , Fe2 + ���ӵ���ɢϵ���ʹ���ϵ���ֱ�Ϊ 4 .90�� 1 0 - 6 cm2 ��s- 1 �� 0 .1 2����ͭΪ���� , ��Eu (NO3) 3 FeCl2 ������ LiClO4 DMSO��ϵ�� , - 1 .50�� - 2 .2 0V (vs.SCE) �����ں��λ����Ƶú�Eu�� 2 3 .34 %�� 86 .0 0 % (�������� ) ��Eu Fe�Ͻ�Ĥ��X��������֤ʵ���õ���Eu Fe�Ͻ�Ĥ���ǷǾ�̬�ġ�
�ؼ��ʣ�
Eu-Fe�Ͻ�;��������;��ɢϵ��;����ϵ��;�����;�Ǿ�̬;
��ͼ����ţ� TB383
�ո����ڣ�2004-02-27
�����㶫ʡ��Ȼ��ѧ����������Ŀ (0 1 1 2 1 5);
Electrodeposition of Eu-Fe Alloy Films in Dimethylsulfoxide
Abstract��
Cyclic voltammetry was used to investigate the electrochemical behavior of Eu 3+ ion and Fe 2+ ion in the 0.01 mol��dm -3 LiClO4+DMSO system on Pt electrode. Some electrochemical parameters were measured. Potentiostatic depositions between -1.50��-2.20 V were applied to deposit Eu-Fe films in Eu (NO3) 3-FeCl2-citric acid-LiClO4-DMSO system on Cu electrode. The Eu content in alloy films was in the range of 23.34% to 86.00% by altering deposition potentials and the ratio of Eu 3+ ion to Fe 2+ ion. Eu-Fe alloy films were amorphous proven by XRD.
Keyword��
Received�� 2004-02-27
ϡ������Ͻ�Ĥ��������Ĺ⡢ �š� �������, �ѹ㷺Ӧ���ڸ�������
1 ʵ ��
ʵ������DMSO (AR) �þ����0.4 nm����ɸ�������պͼ�ѹ������
������ԭ������D/MAX-3A X�����������ȷ�������, ��Hitachi S-520ɨ�����������Oxford ISIS 300����ɫɢ���Ƿ���������ı�����̬����ɡ�
2 ���������
2.1 DMSO��Fe2+�ĵ绯ѧ��Ϊ
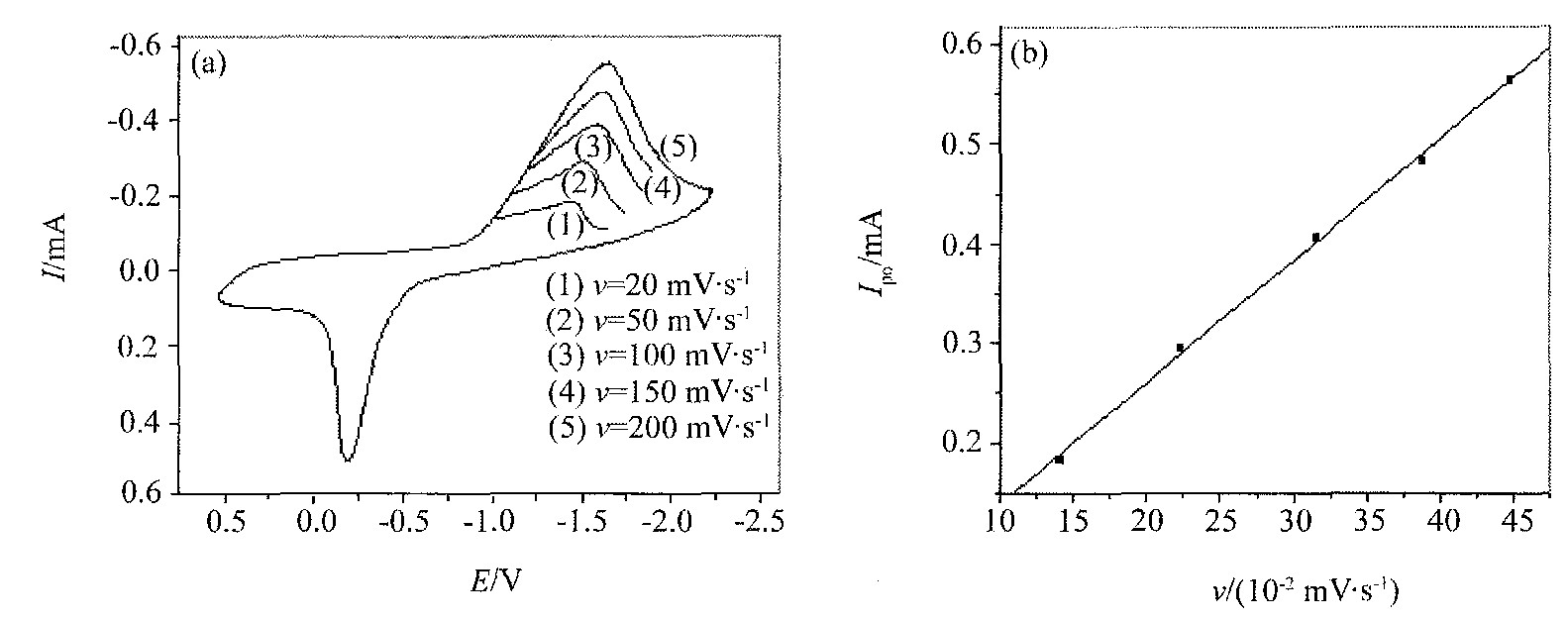
��DMSO�м���֧�ֵ����LiClO4, ��PtΪ�о��缫, ѭ���������߲ⶨ�������, ����ɨ��ʱ��������Ϊ-3.40 V, ����ɨ��ʱ��������Ϊ+0.95 V, ����ϵ�ĵ绯ѧ������ȫ���㱾ʵ���Ҫ�� ͼ1��0.01 mol��dm-3 FeCl2-0.02 mol��dm-3������-0.10 mol��dm-3 LiClO4-DMSO��Һ��Pt�缫�ϵ�ѭ����������, ��ɨ�������, ��ɨʱ����һ����ԭ��, ��ɨʱ����һ��������, �ֱ��Ӧ�����ĵ�������ܳ��� ��ͼ�л����Կ���, ����ɨ�����ʵ�����, ���������, �����λ���в�ͬ�̶ȵĸ��ơ� �����Fe (��) ��Pt�缫�ϵĻ�ԭΪһ����ɵIJ����������ӹ���
ͼ1 0.01 mol��dm-3 FeCl2-0.02 mol��dm-3������-0.10 mol��dm-3 LiClO4-DMSO��ϵ��ѭ���������� (a) (WE: Pt (0.060 cm2) , T=301 K) ��i��v1/2ͼ (b)
Fig.1 Cyclic Voltammograms on a Pt (0.060 cm2) electrode in the 0.01 mol��dm-3 FeCl2-0.02 mol��dm-3 citric acid-0.10 mol��dm-3 LiClO4-DMSO system (a) and Plot of ipc vs. v1/2 (b)
Fe (��) +2e��Fe
����, ���λEpc��ɨ�����ʵ���Ȼ����lnvҲ�����Թ�ϵ, �����һ��֤��Fe (II) �ڴ���ϵ�еĻ�ԭ��һ�������淴Ӧ��
����ijһ����IJ��������, ���λ��ɨ�����ʵĹ�ϵ�ɱ�ʾ����
Epc=K+RTlnv/ (2��nF)
����K=E0-RT [0.780+ln (D01/2/ko) +ln (��nF/RT) 1/2]/ (��nF) , n�ǵ缫��Ӧ�ĵ���ת������ ��һ���¶���, ����ijһ���巴Ӧ��˵, K��һ������, ��˸���Epc��lnv��ֱ��б��RT/ (2��nF) , �������=0.12��
���ڲ��������, ��301 K�·������ɨ�����ʵĹ�ϵΪ
ipc=2.97��105n3/2��1/2Ac*oDo1/2v1/2
����AΪ�缫���, DoΪ��ɢϵ��, c*oΪ�������Ũ��, nΪ�缫��Ӧ�ĵ���ת������ ��ipc��v1/2��ͼ�ɵ�һֱ�� (��ͼ1 (b) ��ʾ) , ����ֱ��б��K=2.97��105n3/2��1/2Ac*oD
2.2 DMSO��Eu3+�ĵ绯ѧ��Ϊ
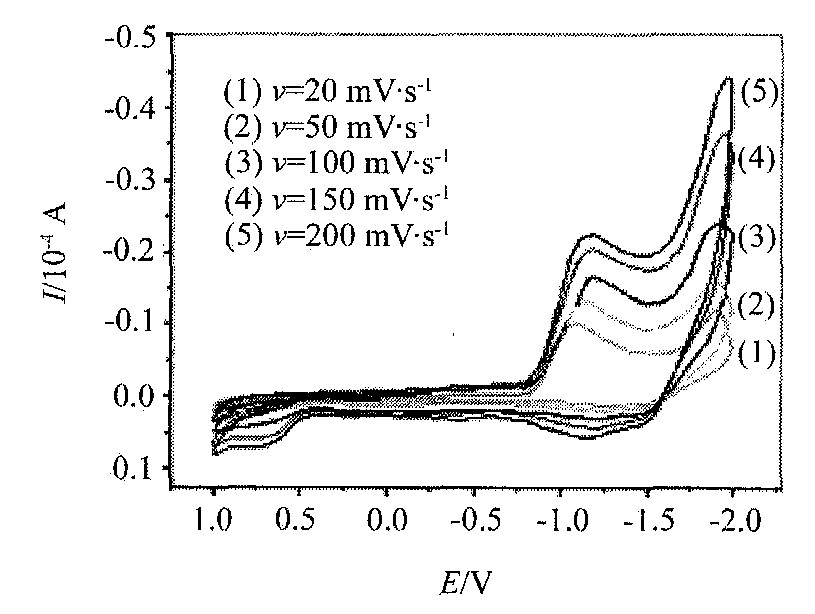
0.01 mol��dm-3 Eu (NO3) 3-0.10 mol��dm-3 LiClO4-DMSO��ϵ�ڲ�ͬɨ������ʱ��Pt�缫�ϵ�ѭ������������ͼ2��ʾ�� ͼ�����ֲ�ͬɨ�������µ����߾������ƵIJ���, ��ipc����ɨ�����ʵ����������, ��Epc������ɨ�����ʵ���������ơ� ��ͼ�п��Կ���Eu3+�ڻ�ԭ������, ����2����ԭ��, ������ΪEu3+�Ļ�ԭ�Ƿ��������еġ� ��������ԭ�������λ��������Ϊ, ��һ������Eu3+��ԭΪEu2+, �ڶ�������Eu2+��ԭ�õ���������Eu, ��������
2.3 ���λ�����Eu-Fe�Ͻ�Ĥ
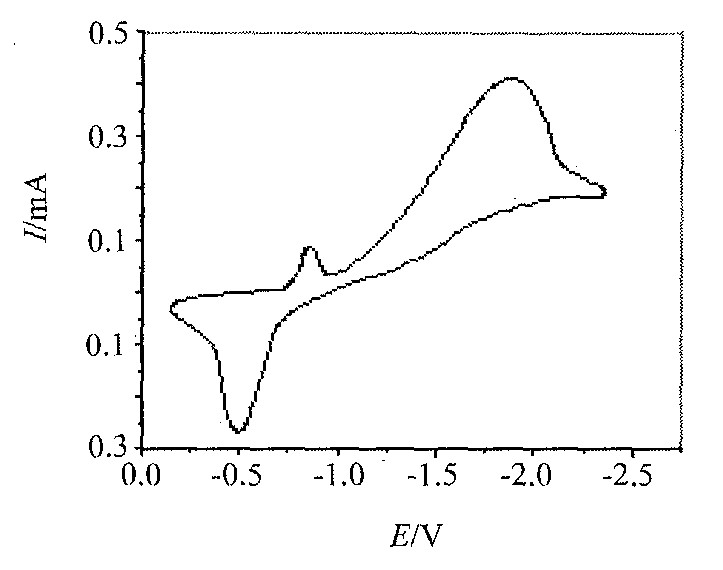
ͼ3��Eu (��) +Fe (��) ��ϵ��Cu�缫�ϵ�ѭ���������ߡ� ͼ�г���2����ԭ��, ������λ�ֱ�Ϊ-0.75��-1.00 V, ��Ϊ��ӦEu3++e��Eu2+��Fe2++2e��Fe֮��ı��缫��λ�ȷ�ӦFe2++2e��Fe��Eu2++2e��Eu֮��ı��缫��λ���ӽӽ�, ����Ϊ-0.75 V����ӦEu3+�ĵ�һ����ԭ��Fe2+�Ĺ���ԭ, -1.00 V����ӦEu2+�Ļ�ԭ; ����+0.5 V������������ӦΪEu-Fe�Ͻ�������� ���, ��-1.50��-2.20 V�����ʺϽ��е������
ͼ2 0.01 mol��dm-3 Eu (NO3) 3-0.10 mol��dm-3 LiClO4-DMSO��ϵ��ѭ���������� (WE: Pt (0.06 cm2) , T=301 K)
Fig.2 Cyclic voltammograms on a Pt (0.06 cm2) electrode in the 0.01 mol��dm-3 Eu (NO3) 3-0.10 mol��dm-3 LiClO4-DMSO system
ͼ3 0.01 mol��dm-3 Eu (NO3) 3-0.01 mol��dm-3 FeCl2-0.02 mol��dm-3 ������-0.10 mol��dm-3 LiClO4-DMSO��ϵ��ѭ���������� (v=50 mV��s-1, WE: Cu (0.06 cm2) , T=301 K)
Fig.3 Cyclic Voltammogram on a Cu (0.06 cm2) electrode in the 0.01 mol��dm-3 Eu (NO3) 3-0.01 mol��dm-3 FeCl2-0.02 mol��dm-3citric acid-0.10 mol��dm-3 LiClO4-DMSO system
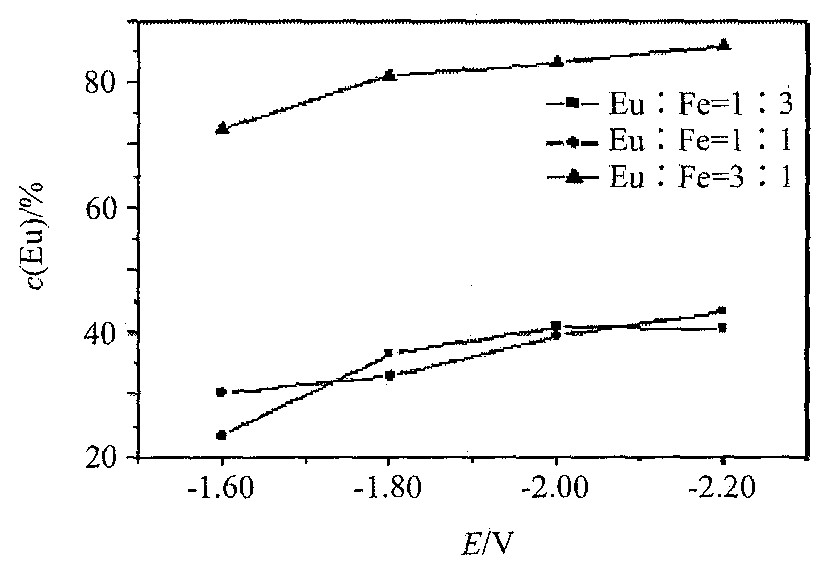
ʵ����-1.50��-2.20 V������ѡȡ4����λ���к��λ����, ����ʱ��Ϊ20 min�� ��Eu��Fe����Ũ�ȱ���0.20 mol��dm-3������, ������3����ͬ��ϵ (cEu��cFe=1��3, 1��1, 3��1) �����˳�����λ��Eu-Fe�Ͻ�Ĥ�����Ӱ����о�: (1) 0.05 mol��dm-3 Eu (NO3) 3-0.15 mol��dm-3 FeCl2-0.10 mol��dm-3 ������-0.10 mol��dm-3 LiClO4-DMSO; (2) 0.10 mol��dm-3 Eu (NO3) 3-0.10 mol��dm-3 FeCl2-0.10 mol��dm-3 ������-0.10 mol��dm-3 LiClO4-DMSO; (3) 0.15 mol��dm-3 Eu (NO3) 3-0.05 mol��dm-3 FeCl2-0.10 mol��dm-3 ������-0.10 mol��dm-3 LiClO4-DMSO�� ���õ���Eu-Fe�Ͻ�Ĥ��EDAX������������ĺ����� ȡ����Ϊ�Ͻ�Ĥ������ѡȡ��СƬ��������, ԼΪ�Ͻ�Ĥ�������20%, ����һ���Ĵ�����, ͬʱҲ���ɱ���ش���ƫ� ͼ4��ʾ��Eu-Fe�Ͻ�Ĥ�е�Eu�����������λ�Ĺ�ϵ�� ʵ��������: 3����ϵ����������ĺϽ�Ĥ��Eu������23.34%��86.00%֮��, ��ÿһ����ϵ�õ��ĺϽ�Ĥ�������ƹ���: ���ų�����λ�ĸ���, �Ͻ����������ӡ� �Ա�3�ֲ�ͬŨ�ȱȵ���ϵ, ��Eu3+��Fe2+Ϊ3��1ʱ�õ��ĺϽ�Ĥ��ϡ����ĺ���Զ������������Ũ�ȱȡ� ͼ5�DZ���Eu��Fe����Ũ��0.20 mol��dm-3, cEu��cFe=1��3, 1��1, 3��1 ������ϵ�³����ĺϽ�Ĥ��SEM��òͼ (������λ��Ϊ-2.00 V) �� �����ֲ�ͬŨ�ȱȵ���ϵ��SEM��òͼ�ɿ���, cEu��cFeԽ�� (����Һ��Eu2+���ӵ�Ũ��Խ��) , ����Ĥ�еĿ���Խ��, ����ϡ����ĺ���Ҳ����, �ر���cEu��cFe=3��1ʱ��ĺ�����Ϊ���ӡ� ��˵����ϵ������Ũ�ȱ�����ͬ, �ԺϽ�Ĥ����ò�����е�ϡ�������кܴ��Ӱ�졣 ���, ����ͨ��������ϵ�����ӵ���ɿ��ƺϽ�Ĥ��ϡ���ĺ������Ͻ�Ĥ����̬��
ͼ4 �Ͻ�Ĥ��Eu�����������λ��ϵͼ
Fig.4 Eu content of alloy films in different system
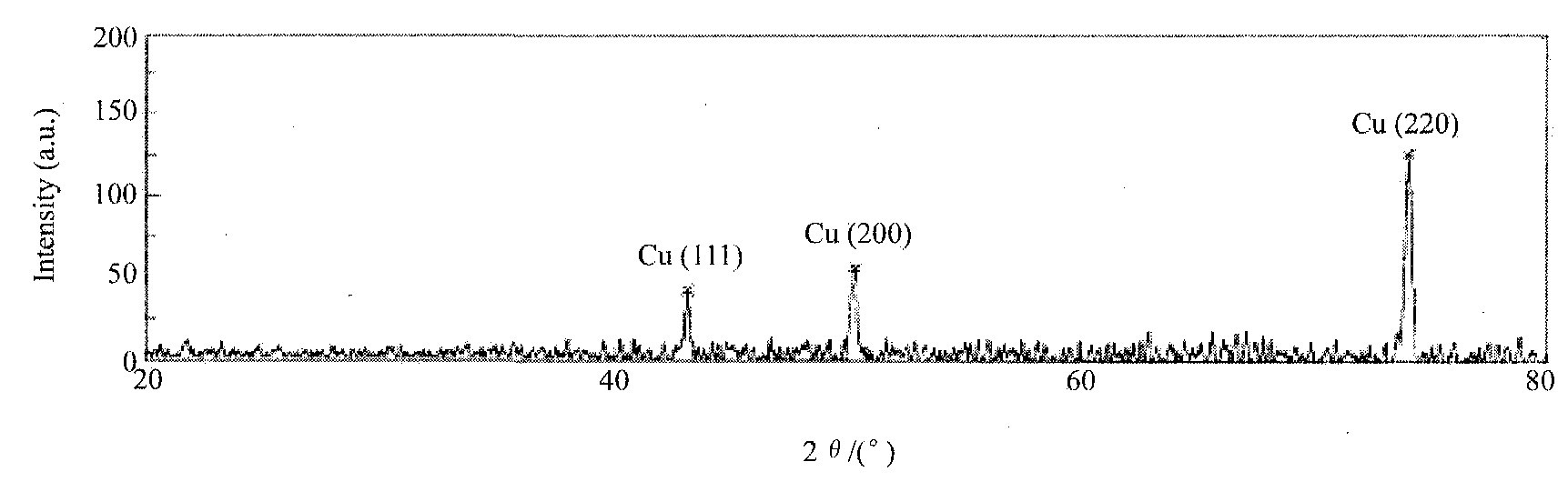
���ϳ������õĺϽ�Ĥ��ϡ���ᷴӦ�ܲ����������ȵ�С����, ���н�������, ֤�����õij������ǽ����� ���õĺϽ�Ĥ��D/MAX-3A X������������Ƿ�������Ĺ���, ����X��������ͼ�ϳ���3�������, ��XRD��ʵ�����ݷֱ�Ϊ0.2091, 0.1810, 0.1280 nm (��ͼ6��ʾ) , ͨ������JCPDS�ķ�ĩ���俨Ƭ�� (PDF)
3 �� ��
1. Fe2+������DMSO��ϵ��, Pt�缫�ϵĵ绯ѧ��ԭ����Ϊһ�����������, ����ѭ�������������301 K��0.01 mol��dm-3 FeCl2-0.02 mol��dm-3������-0.10 mol��dm-3 LiClO4-DMSO��Һ��, Pt�缫��Fe2+���ӵ���ɢϵ���ʹ���ϵ���ֱ�Ϊ4.90��10-6 cm2��s-1��0.12�� ��Eu3+�ĵ绯ѧ��ԭΪ�������������, �Ȼ�ԭΪEu2+, Eu2+�ٽ�һ����ԭΪEu��
ͼ5 Eu-Fe�Ͻ�ĤSEM��òͼ (a) cEu��cFe=1��3; (b) cEu��cFe=1��1; (c) cEu��cFe=3��1
Fig.5 Typical SEM images of Eu-Fe alloy films
ͼ6 Eu-Fe�Ͻ�Ĥ��XRDͼ
Fig.6 Typical XRD spectrum of Eu-Fe alloy films on Cu substrate
2. ��Eu (NO3) 3-FeCl2-������-LiClO4-DMSO��ϵ�С� -1.50��-2.20 V (vs. SCE) ������, ͭ�缫���Ƶ�ճ���Ժá� �н��������Eu-Fe�Ͻ�Ĥ�� �ı���ϵ��cEu��cFe�ı�������������Ͻ�Ĥ��Eu������23.34%��86.00%֮��䶯, ��ʹĤ�ı�����̬ͬʱ�����仯�� ���õ���Eu-Fe�Ͻ�Ĥ����X��������֤ʵ�ǷǾ�̬�ġ�
�����
[1] Disalvo F J. Thermoelectric cooling and power generation [J]. Science, 1999, 285: 703.
[4] ������, ͯҶ��, ����ƽ, ��. �л���Һ�е����ϡ���Ͻ� [J]. �й�ϡ��ѧ��, 1998, 16: 857.
[6] ��ɽ��ѧ����ϵ��. ϡ��������ѧ���� [M]. ����: ұ�������, 1978, 116.
[7] �ձ���ѧ��. ��������ϳ��ֲ�, �ڶ��� [M]. ����: ��ѧ��ҵ������, 1986, 254.
[9] �ظ���, ��Сϼ. ϡ���ڱ�ͪ�����еķ�����Ϊ [J]. �й�ϡ��ѧ��, 1990, 8 (2) : 166.
[10] Power Diffraction File Inorganic Phases [M]. JCPDS, Swarthmore, PA, 1992.
[1] Disalvo F J. Thermoelectric cooling and power generation [J]. Science, 1999, 285: 703.
[4] ������, ͯҶ��, ����ƽ, ��. �л���Һ�е����ϡ���Ͻ� [J]. �й�ϡ��ѧ��, 1998, 16: 857.
[6] ��ɽ��ѧ����ϵ��. ϡ��������ѧ���� [M]. ����: ұ�������, 1978, 116.
[7] �ձ���ѧ��. ��������ϳ��ֲ�, �ڶ��� [M]. ����: ��ѧ��ҵ������, 1986, 254.
[9] �ظ���, ��Сϼ. ϡ���ڱ�ͪ�����еķ�����Ϊ [J]. �й�ϡ��ѧ��, 1990, 8 (2) : 166.
[10] Power Diffraction File Inorganic Phases [M]. JCPDS, Swarthmore, PA, 1992.