�Ȼ��ƴ������廯��-ʮ����������Ȼ����ϵ��ѡ���벬���١�����о�
����������ѧ����ұ��ѧԺ,����������ѧ����ұ��ѧԺ,����������ѧ����ұ��ѧԺ,���������ѧ��ѧ�����\��ѧԺ,���������ѧ��ѧ�����\��ѧԺ,���������ѧ��ѧ�����\��ѧԺ ��������650031,���������ѧ��ѧ�����\��ѧԺ,��������650031,��������650031,��������650031,��������650031,��������650031,��������650031
ժ Ҫ��
�о����Ȼ��ƴ������廯��-ʮ����������Ȼ����ϵ��ѡ���벬���١���ķ���������, ��0.24 mol.L-1���������, �����١���ѡ��Ϊ93.2%-98.0%, 94.3%-97.6%, 93.4%-99.0%, ���������ڴӴ�����������з��벬���١���, ��ʵ����Ʒ�ķ����������������������������˸�ѡ�ǻ��ڲ����١��������������������ӱ��������ʮ����������Ȼ���γ����ӵ���Ļ��ơ�
�ؼ��ʣ�
��;��;��;�Ȼ���;�廯��;ʮ����������Ȼ��;��ѡ;
��ͼ����ţ� TF83
�ո����ڣ�2006-01-16
Flotation Separation of Pt, Pd and Au by Sodium Bromide-Cetyltrimethey Ammonium Bromide System in Presence of Sodium Chloride
Abstract��
The separating behaviors of Pt, Pd and Au in sodium bromide-cetyltrimethey ammonium bromide water system in the presence of sodium chloride were studied.The result showed that the system can separate Pt, Pd and Au completely in a given condition in 0.24 mol.L-1 medium.The flotation rate of Pt, Pd and Au was 93.2% 98.0%, 94.3%97.6%, 93.4% 99.0%, re-spectively.The separation results of the synthetic sample showed that this method can be used to separate Au, Pt and Pd from a great amount base metals such as Fe (��) , Pb (��) , Al (��) , Cu (��) , Zn (��) , Ca (��) , and the method was also used for the separation of Pt, Pd and Au from practical samples with satisfactory.
Keyword��
gold;platinum;palladium;flotation separation;sodium chloride;sodium bromide;cetyltrimetheylammonium;
Received�� 2006-01-16
���ӳɷ��е�Ʒλ��������������ķ����Ƿ����ѧ�е���Ҫ����, ������������һ�ֻ������������õĸ�ѡ���뷨
1 ʵ ��
1.1 ��������Ҫ�Լ�
7200�Ϳɼ��ֹ��ȼ� (�Ϻ�������Ϻ���������˾) �� �� (��) �� �� (��) �� �� (��) ����Һ (�����������о����ṩ) ; ��Ϊ100.0 mg��L-1 (0.6 mol��L-1 HCl����) ; 1.0��10-2 mol��L-1ʮ����������Ȼ�� (CTMAC) ˮ��Һ; 0.1 mol��L-1 NaBrˮ��Һ; 1.2 mol��L-1 HClˮ��Һ; Zn, Cd, Co, Al, Cu, Ni, Mn, Fe�Ƚ������ӵı�Һ��Ϊ50 ��g��ml-1; NaCl����; �����Լ���Ϊ������, ˮΪ���ӽ���ˮ��
1.2 ʵ�鷽��
��25 ml��ɫ����, �ֱ����һ�����IJ��� �١� �����Һ�� 0.1 mol��L-1 NaBrˮ��Һ�� 1.0��10-2 mol��L-1ʮ����������Ȼ�� (CTMAC) ˮ��Һ��1.2 mol��L-1 HClˮ��Һ, ϡ����20 ml, ����1.0 g����NaCl, �����, ����Ƭ��, ��ȥ��ˮ��, �ÿ�ȸʯ����ȡ�ֹ��ȷ��ⶨ��ˮ���б������ĺ���
�����ӻ����Һ���������ӵĺ�������ICP-AES���ⶨ��
2 ���������
2.1 ���� �١� ��ķ�������
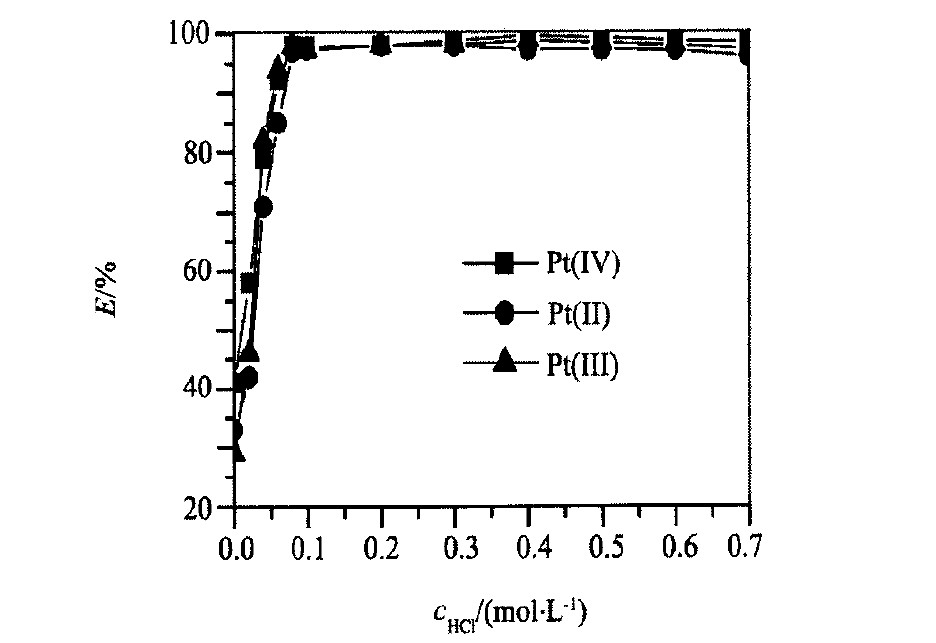
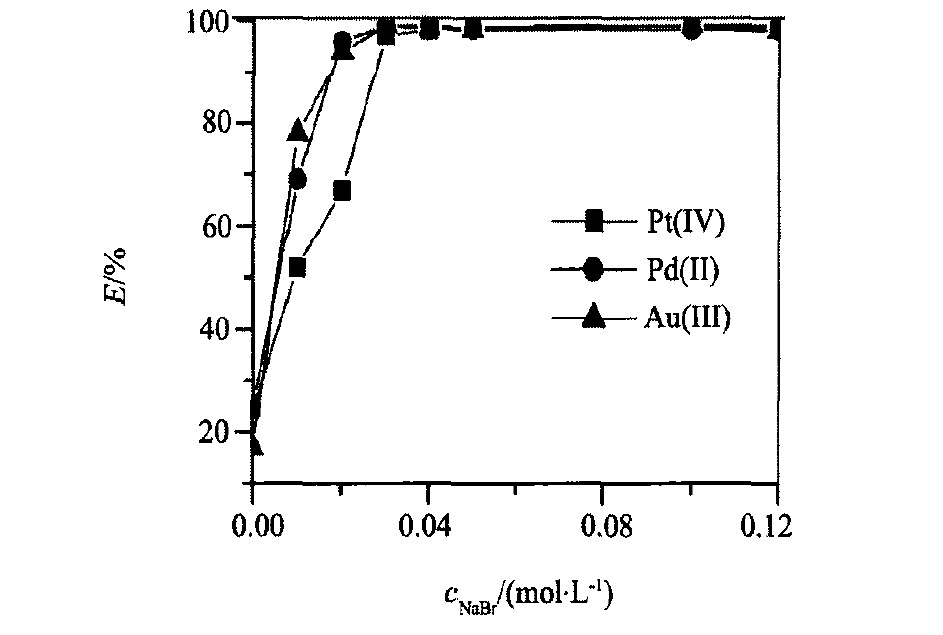
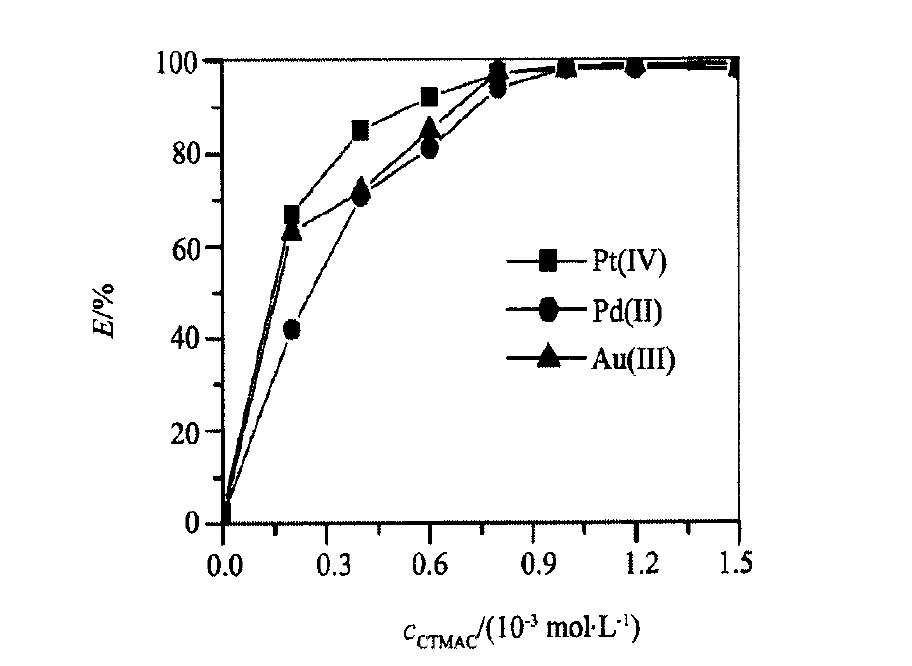
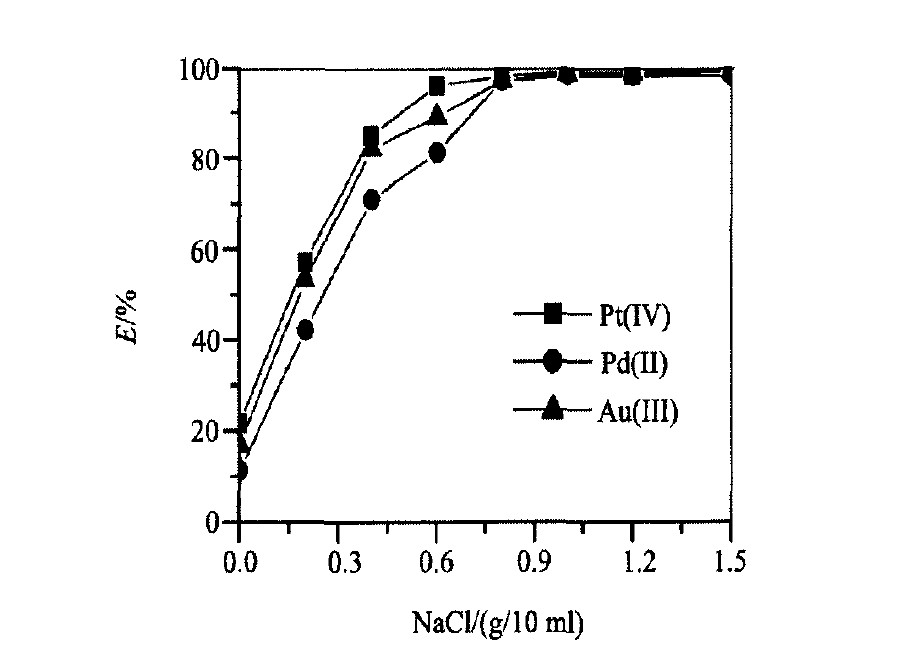
�̶��� (��) �� �� (��) �� �� (��) ����Ϊ100.0 ��g, �ֱ�����HClŨ�ȡ� NaBrŨ�ȡ� CTMAC������ NaCl�����Բ� (��) �� �� (��) �� �� (��) ��ѡ�ʵ�Ӱ�졣 ����Ũ�ȶԸ�ѡ�ʵ�Ӱ��ͬ��ͼ1, ��ѡ������HClŨ�ȵ����Ӷ�����, HClŨ����0.06��0.5 mol��L-1֮��, ��ѡ��������ȶ�, E (%) >97.3, ������ (��) �� �� (��) �� �� (��) ����ȫ������; �廯��Ũ�ȶԸ�ѡ�ʵ�Ӱ���ͼ2, ��NaBr����ʱ, �� (��) �� �� (��) �� �� (��) �ĸ�ѡ�ʽϵ�, ����24.7%, ��ѡ������NaBr��ҺŨ�ȵ����Ӷ�����; ��Ũ��Ϊ0.030 mol��L-1ʱ, �� (��) �� �� (��) �� �� (��) ��ѡ��E (%) >97.6, ��������NaBrŨ����0.12 mol��L-1ʱ, ��ѡ�ʱ��ֲ���; ͼ3��CTMACŨ�ȶԸ�ѡ�ʵ�Ӱ��, �ı�CTMAC����, ��ѡ������CTMAC���������Ӷ�����, ��CTMAC����ʱ, ��ѡ�ʽӽ�0, ����ϵ��CTMAC�����ﵽ1.0��10-3 mol��L-1ʱ, �� (��) �� �� (��) �� �� (��) ����ȫ��ѡ, ��������CTMAC����, ��ѡ�ʱ��ֲ���; NaCl�����Ը�ѡ�ʵ�Ӱ��Ľ����ͼ4, ������NaClʱ, ������������, ��ѡ��ֻ��21.0%, ��ѡ������NaCl���������Ӷ�����, ��NaCl�����ﵽ0.8g (8.0% w/V) ʱ, �� (��) �� �� (��) �� �� (��) ����ȫ��ѡ, ��������NaCl����, ��ѡ�ʱ��ֲ��䡣
ͼ1 ����Ũ�ȶԸ�ѡ�ʵ�Ӱ��
Fig.1 Effect of HCl concentration on flotation rate
cNaBr:0.06 mol��L-1, cCTMAC:0.001 mol��L-1, NaCl:0.8% (w/V)
ͼ2 �廯��Ũ�ȶԸ�ѡ�ʵ�Ӱ��
Fig.2 Effect of NaBr concentration on flotation rate
cHCl:0.24 mol��L-1, cCTMAC:0.001 mol��L-1, NaCl:0.8% (w/V)
ѡ��HClŨ��Ϊ0.24 mol��L-1, NaBr��Ũ��Ϊ0.06 mol��L-1, CTMAC����Ϊ1.0��10-3 mol��L-1, NaCl����Ϊ10.0% (w/V) �� ��ѡ����ʵ��������, �Բ�ͬ�����Ĺ���� (10��100 ��g) ���и�ѡ����, �� (��) �� �� (��) �� �� (��) �ĸ�ѡ�ʷֱ�Ϊ: 93.2%��98.0%, 94.3%��97.6%, 93.4%��99.0%��
2.2 ����ʵ��
(1) �ϳ�������ʵ��:
���ƺϳ���, �ñ��������з���, �������1, ��������ȫ��ѡ���벬 (��) �� �� (��) �� �� (��) , ���������������������������ѡ; �����������, �� (��) �ĸ�ѡ��Ϊ34.2%, ҿ (��) �ĸ�ѡ��Ϊ3.7%; ��˷����ɴӴ�����������з��벬 (��) �� �� (��) �� �� (��) ; ֵ��ע�����, ��NaCl-I--�����Ӽ���Ⱦ����ϵ���ܱ���ѡ��ͭ (��) �� �� (��) �ڱ��ĵ���ϵ�и�ѡ�ʺܵ�, ������ĵ���ϵ�ɱ�����ʹ�õ����Ӷ����µ�ͭ�� �ӵȽ�������Ҳͬʱ����ѡ�������������, ����һ����ʵ�����塣
ͼ3 CTMACŨ�ȶԸ�ѡ�ʵ�Ӱ��
Fig.3 Effect of CTMAC concentration on flotation rate
cNaBr: 0.06 mol��L-1, cHCl: 0.24 mol��L-1, NaCl:0.8% (W/V)
ͼ4 �Ȼ��������Ը�ѡ�ʵ�Ӱ��
Fig.4 Effect of NaCl amount on flotation rate
cHCl: 0.24 mol��L-1, cCTMAC: 0.001 mol��L-1, cNaBr:0.06 mol��L-1
(2) ʵ����Ʒ����ʵ��:
ȷ��ȡ3��5 gɰ�����ͭ��������Ʒ��50 ml ��������, ��650��750 ������¯�ڱ���1 h, ��ȴ����Ʒת��400 ml �ձ���, ��50 ml ��ˮ�ڵ��Ȱ������ܽ�2 h, ��������, ��10 mlŨHCI������3��, ������ɫ��, ��25 ml 2.4 mol��L-1 HCI��Һ, 3�Ų�ɰ©�����˳�ȥ����, ��Һ��ϴҺ�ϲ���100 ml�ձ�����������, ������������� (40��50 ��g) , ��0.24 mol��L-1 HCI�ܽ�ת������Һ©����, �����鷽�����и�ѡ�ⶨ, �������2, ��Ա�ƫ����5.1%��8.3%, �����������������������ϡ�
��1 �˹��ϳ����ķ���* ����ԭͼ
Table 1 Separation and determination of synthetic samples
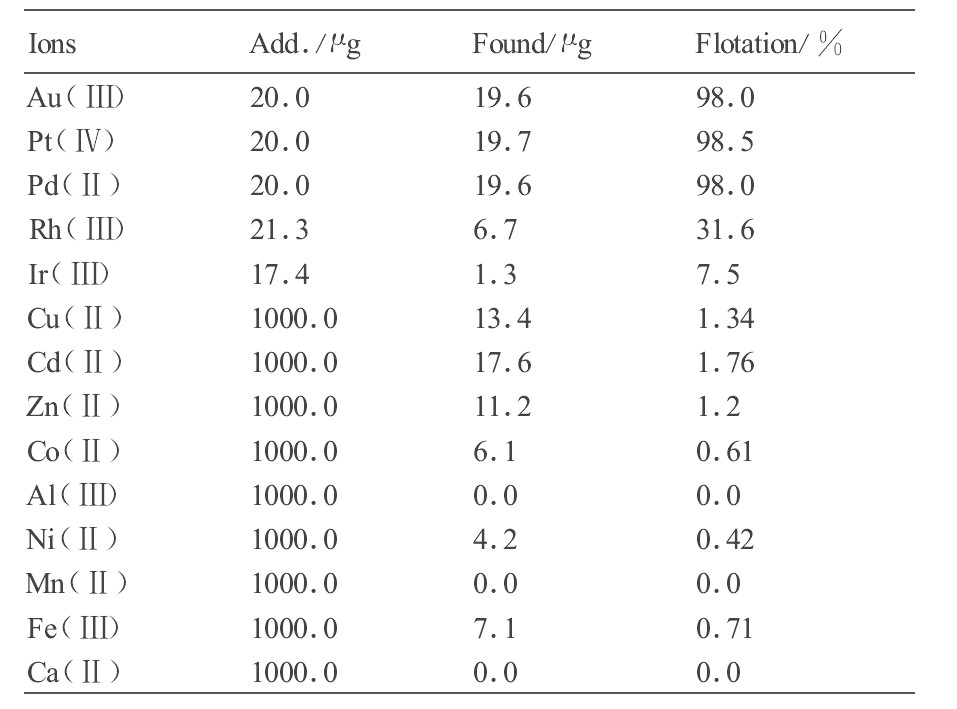
* Determined by ICP-AES
��1 �˹��ϳ����ķ���*
��2 ��Ʒ���������� (g��L-1, n=5) * ����ԭͼ
Table 2 Analytical results of food samples
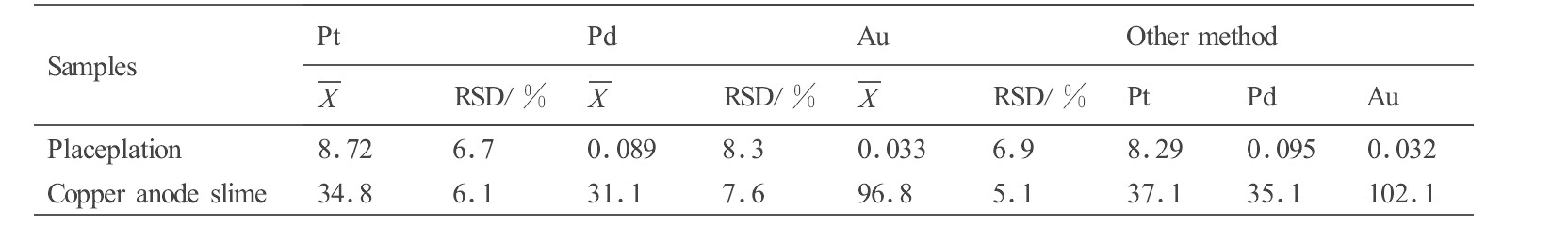
* Determined by fire assay
��2 ��Ʒ���������� (g��L-1, n=5) *
2.3 ��ѡ����̽��
������ʵ���֪, ������������ʱ�� (��) �� �� (��) �� �� (��) �ĸ�ѡ�ʺܵ�, ��˵��Au (��) ���������ӵĿɸ��Խϲ�, ���������Ӻ�Au (��) �ĸ�ѡ����������, ��ԭ������Au (��) �����������ӱȽ������������нϴ�����, ��ˮ�Ը�ǿ, ��˿ɸ�������; ����CTMACŨ�ȵ�����, Au (��) �ĸ�ѡ����֮����, ������ʵ������֪, ��CTMAC��NaBr����ͬʱ����ʱ, Au (��) ���ܱ���ѡ, ���������������ڸ�ѡ��ʵ����ʵ�Լ�Au (��) �����γ�����������˵����ѡ�ǻ������ӵ����γɵ�����, �ɴ˿��Ʋ�ĸ�ѡ���� (��Au (��) Ϊ��) ��:
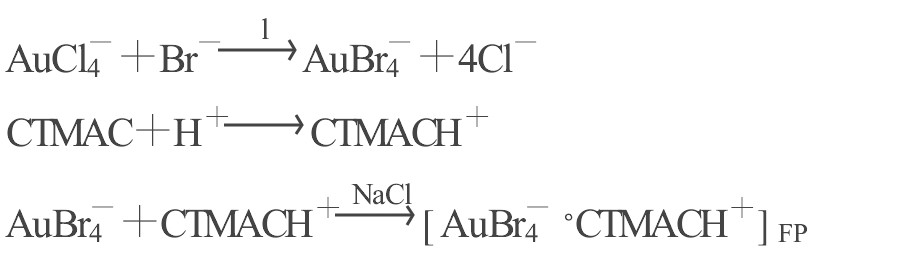
��ѡ�� (FP) �Dz�����ˮ��[AuBr-4��CTMAC+], �������ܶȵ�����ˮ����ܶ�, ���������ˮ���������ڷ��롣
NaCl���н�ǿ��ˮ������, ������ˮ���ӵ�����, ������н�ǿ����������, ������[AuBr-4��CTMAC+]�γɲ���ˮ������, ��֮����NaCl��, ��ˮ����ܶ�����, Ҳ������[AuBr-4��CTMAC+]������ˮ��ķ��롣
���ĵ���ϵ�� (��) �� �� (��) �� �� (��) ���������������õķ���Ч������Ϊ�����������ӷ�Ӧ�IJ�����, �� (��) �� �� (��) �� �� (��) ����Br-�γ��ȶ�������������, �����������������Br-�γ��������Ȼ����������ʽ����, ���������ӻ���CTMAC�γ����ӵ��ﲻ����ѡ��
3 �� ��
��һ����NaCl������, ���� �١� �����������������γ���������, ���������ӱ��������ʮ����������Ȼ�� (CTMAC) �γ����ӵ��︡����ˮ�����γɽ���������Һ-�����౻������ѡ, �Ҵ�������������Ӳ�����ѡ, �Ӷ�ʵ���˲��� �١� ���븴�ӻ�������Ķ�������; ����ü���Ⱦ��������B�� ��ȸ�̵���Ϊ�������ӵ���ϵ, ���ĵķ����հϵ�, �Ժ����IJⶨ���Ž�С, ��ʹ����������Ϊ��ϼ�Ҳ��������ʹ�õ����Ӷ����µ�ͭ�� �ӵȽ�������Ҳͬʱ����ѡ������, �������ȡ�ȷ������, �����ĺ��������dz���; ���������ڲ��� �١� ��ICP-AES�ȷ���ͬʱ�ⶨǰ�븴�ӻ���������ӵķ��롣
�����
[1] ������, �Լ���, ������.�Ȼ��ƴ������Ȼ�����-����B-ˮ��ϵ��ѡ����ҿ[J].�ҿ����, 2002, 21 (6) :117.
[2] ������, ��ΰ.�Ȼ��ƴ�����Ӧ���Ȼ���������B-ˮ��ϵ��ѡ������[J].2002, 21 (3) :31.
[3] ����ɽ, ���¹�.ʮ����������廯��������-�Ȼ�����ϵ��ѡ������ (��) [J].������ѧ, 2004, 32 (9) :118.
[4] ������, ������.�Ȼ��ƴ����µ⻯��-����B-ˮ��ϵ��ѡ������ (��) ���о�[J].����ʵ����, 2004, 21 (1) :73.
[5] ��ȫ��, ��ΰ, ����.�Ȼ���-�������-�廯ʮ������������ϵ��ѡ����п[J].������ѧ, 2001, 29 (2) :205.
[6] ��ȫ��, �Դ�ϼ, ��ΰ.�������-�ᾧ��-H2O��ϵ��ѡ������[J].����������, 2001, 20 (3) :37.
[7] ������, ������, ��ΪΥ.����80-�����-ˮ��-Һ��ϵ��ȡ�������ҿ[J].Ӧ�û�ѧ, 2001, 17 (2) :201.
[8] ������, ������, ��ΰ.����-�����-ˮҺ-Һ��ϵ��ȡ���벬���١�����ɵ��о�[J].������ѧ, 2001, 29 (8) :901.
[9] ������, ������.�Ȼ��ƴ����±���һ�⻯����ϵ��ȡ���벬���ٵ��о�[J].����������, 2001, 20 (3) :14.
[10] ��ȫ��, ������, ������, ��.����Ǯ�����µ⻯��-�ᾧ��-������ϵ��ȡ������[J].������ѧ, 1998, 26 (9) :1071.
[11] ������, ������, ��ΰ��.�����-�⻯��-��ȸʯ����ϵ�����[J].�ƽ�, 2002, 23 (6) :47.
[12] ����, ������, ������, ��.�����-�Ȼ�����-��ȸ����ϵ��ѡ���벬[J].�����, 2003, 24 (2) :16.
[1] ������, �Լ���, ������.�Ȼ��ƴ������Ȼ�����-����B-ˮ��ϵ��ѡ����ҿ[J].�ҿ����, 2002, 21 (6) :117.
[2] ������, ��ΰ.�Ȼ��ƴ�����Ӧ���Ȼ���������B-ˮ��ϵ��ѡ������[J].2002, 21 (3) :31.
[3] ����ɽ, ���¹�.ʮ����������廯��������-�Ȼ�����ϵ��ѡ������ (��) [J].������ѧ, 2004, 32 (9) :118.
[4] ������, ������.�Ȼ��ƴ����µ⻯��-����B-ˮ��ϵ��ѡ������ (��) ���о�[J].����ʵ����, 2004, 21 (1) :73.
[5] ��ȫ��, ��ΰ, ����.�Ȼ���-�������-�廯ʮ������������ϵ��ѡ����п[J].������ѧ, 2001, 29 (2) :205.
[6] ��ȫ��, �Դ�ϼ, ��ΰ.�������-�ᾧ��-H2O��ϵ��ѡ������[J].����������, 2001, 20 (3) :37.
[7] ������, ������, ��ΪΥ.����80-�����-ˮ��-Һ��ϵ��ȡ�������ҿ[J].Ӧ�û�ѧ, 2001, 17 (2) :201.
[8] ������, ������, ��ΰ.����-�����-ˮҺ-Һ��ϵ��ȡ���벬���١�����ɵ��о�[J].������ѧ, 2001, 29 (8) :901.
[9] ������, ������.�Ȼ��ƴ����±���һ�⻯����ϵ��ȡ���벬���ٵ��о�[J].����������, 2001, 20 (3) :14.
[10] ��ȫ��, ������, ������, ��.����Ǯ�����µ⻯��-�ᾧ��-������ϵ��ȡ������[J].������ѧ, 1998, 26 (9) :1071.
[11] ������, ������, ��ΰ��.�����-�⻯��-��ȸʯ����ϵ�����[J].�ƽ�, 2002, 23 (6) :47.
[12] ����, ������, ������, ��.�����-�Ȼ�����-��ȸ����ϵ��ѡ���벬[J].�����, 2003, 24 (2) :16.