ZrO2-Al2O3����������Ʊ�������Pd�����������������ܵ�Ӱ��
�ϲ���ѧӦ�û�ѧ�о���,�ϲ���ѧӦ�û�ѧ�о���,�ϲ���ѧӦ�û�ѧ�о���,������ϢӦ��ְҵ����ѧԺ �����ϲ�330031,�����ϲ�330031,�����ϲ�330031,�����ϲ�330043
ժ Ҫ��
��������������װ�ÿ�����ZrO2-Al2O3���������Ʊ�������Pd�����������������ܵ�Ӱ��, ������XRD, TPR, H2-TPD, NH3-TPD��H2�����ȼ����Դ��������˱������������, ����������Ʊ�������Pd�������������������нϴ��Ӱ��, ����շ����, �ܽ�-�������Ʊ��ĸ���������ǿ�˻������������������, ������Pd��ɢ�ȵ�����ʹ�������������, �Ӷ�������Pd���������Ե���ߡ�
�ؼ��ʣ�
ZrO2-Al2O3��������;��������;Pd������;�Ʊ�����;
��ͼ����ţ� TE624.55
����飺������ (E-mail: Luolaitao@163.com) ;
�ո����ڣ�2007-04-18
�����ߵ�ѧУ��ʿѧ�Ƶ�ר���о����� (20040403001);�������������л���;�ϲ���ѧ�������Ի���������Ŀ;
Effects of Preparation Methods of ZrO2-Al2O3 Mixed Supports on Properties of Palladium Based Catalysts for HDS
Abstract��
ZrO2-Al2O3 mixed supports were prepared by impregnation (I) and sol-gel (S) methods separately.Influences of preparation methods on properties of Pd based catalysts for thiophene hydrogenation desulfurization (HDS) were studied.Prepared samples were characterized by means of XRD, H2-TPD, H2-TPR and NH3-TPD.Comparing with Pd/ZrO2-Al2O3 (I) catalyst, Pd/ZrO2-Al2O3 (S) catalyst had a higher dispersion of palladium and stronger interaction between palladium and mixed supports and more acid sites, which presented an increasing driving-force toward the catalyzed conversion of thiophene.The methods prepared supporte affected the property of Pt based catalysts for HDS.
Keyword��
ZrO2-Al2O3 mixed support;hydrodesulfurization;palladium based catalyst;preparation methods;
Received�� 2007-04-18
ȫ������β�����ŷŵ�������к����ʶԻ�����������ص���Ⱦ, Ϊ��������������������������������Խ��Խ�ϸ������, ���, ʯ�����ƹ����е����������ѳ�Ϊʯ�ͻ�����ҵ����Ҫ�������ؿ��⡣ ���ڶ���ص���������, �������� (HDS) ��һ��ʵ���Ժ�ǿ��������, Ŀǰ���ڼ�������Ӧ�Ĵ�����Ҫ��Co (��Ni) -Moϵ�� ̼��� ����� �����Լ������ (��Pt, Pd��) ����
����Դ�������������Ҫ��Ӱ��, ������Ч�ظ��غͷ�ɢ�����, ��߹����������Ч�ʺͽ��ʹ����ɱ�, ���ҳ��������ֹ�ͬ�Դ���Ӧ�������á� ����������������֮���ǿ�����, ���¹����Pd��d-����ȱ��, �Ӷ��������л������ǿ������, ������Pd����������������������������
1 ʵ ��
1.1 ZrO2-Al2O3 (1��4 (Ħ����) ) ����������Ʊ�
��������շ� (IMP��) : ��5.000 g Al2O3 (203.1 m2��g-1) ������������ZrOCl2��8H2O��Һ (0.207 mol��L-1) 24 h, 393 K�����ҹ, 773 K����4 h��ZrO2-Al2O3 (I) �������塣
�ܽ�-������ (sol-gel��) : ��15.000 g Al (NO3) 3��9H2O��1.611 g ZrOCl2��8H2O��������ˮ���0.5 mol��L-1�Ļ����Һ, ����ˮ��5��1 (Ħ����) ������ˮ�Ҵ���һ�����ľ��Ҷ���-20000��ɢ��, ��293��303 K������ˮ���Ƶþ��ȵ��ܽ�, �ϻ�36 h�ð�ɫ����, ��������ո���, 773 K����4 h��ZrO2-Al2O3 (S) �������塣
1.2 �������Ʊ�
Pd/ZrO2-Al2O3�������õ�������շ��Ʊ��� ��1.000 g ZrO2-Al2O3 (I) ��ZrO2-Al2O3 (S) �����������PdCl2��Һ (0.156 mol��L-1) 24 h, 393 K�����ҹ, 773 K����4 h, �ֱ��Pd/ZrO2-Al2O3 (I) ��Pd/ZrO2-Al2O3 (S) ����, ������Pd����Ϊ2% (��������) ��
1.3 �������ԵIJⶨ
�������ԵIJⶨ�ڹ̶�������������װ���н��С� ��0.100 g���� (40��60Ŀ) װ�벻��ַ�Ӧ����, N2��ɨ0.5 h���л���H2, 573 K��ԭ3 h, ����Լ�������Ϊ̽�뷴Ӧ, ��H2����Ա����������뷴Ӧ���� ��Ӧ����Ϊ��ѹ�� ��Ӧ�¶�543��663 K�� ���/H2=0.0289/1 (Ħ����) , SV=15.46 mmol��h-1��g-1�� ��Ӧ2 h����ͨ������, GC102M����ɫ���Ƿ���, PEG-20000��, FID��⡣ �����Ļ����Է�Ӧ���ʳ���k��ʾ, k=-Fln (1-x) /W, ����FΪ������� (mmol��h-1) , WΪ���������� (g) , xΪ��Ե�ת���ʡ� ����Arrhenius����k=Aexp (-Ea/RT) , ��lnk��1/T��ͼ, ��ֱ��б�ʿ�����÷�Ӧ�ı��ۻ��Ea��
1.4 �����ı���
1.4.1 X�������� (XRD)
XRD���õ¹� (Bruker-AXS) ��˾D8 Advnce��תX����������, ����Cu K������, ������ѹ40 kV, ��������40 mA, ɨ������1 (��) ��min-1�� ����Scherrer��ʽ��������d=K��/B1/2cos��, ����KΪScherrer���� (0.89) ; dΪ���� (nm) ; B1/2Ϊ���� (�Ի��ȱ�ʾ) ; ��Ϊ�������; ��ΪX���߲��� (0.15406 nm) ��
1.4.2 �������»�ԭ (TPR)
���� (0.100 g) ��N2 (30 ml��min-1) ����5 K��min-1���������ʴ���������1073 K, ����������ƽֱ, ��������, �л���10%H2/N2����� (30 ml��min-1) , ��ͬ����������������1073 K, β���������ˮ�����TCD��⡣
1.4.3 H2-TPD��NH3-TPD
��H2����573 K������ (0.100 g) ��ԭ3 h, ��������, ��������H2 (NH3) ������, ��N2 (30 ml��min-1) ��ɨ������ƽֱ, ��5 K��min-1��������1073 K, ��H2 (NH3) -TPD��
1.4.4 ��ɢ�ȵIJⶨ
�����ķ�ɢ�Ȳ���H2��ѧ�������ⶨ�� ������ (0.100 g) װ��ʯӢ��, N2��ɨ0.5 h���л���H2, 573 K��������ԭ3 h����N2��ɨ2 h, ����423 K
1.4.5 BET����
��Ʒ��BET�����ڱ�������������������ST-2000�ȱ�����ⶨ���Ͻ���, N2Ϊ������, �����¶�Ϊ77 K��
2 ���������
2.1 ������XRD
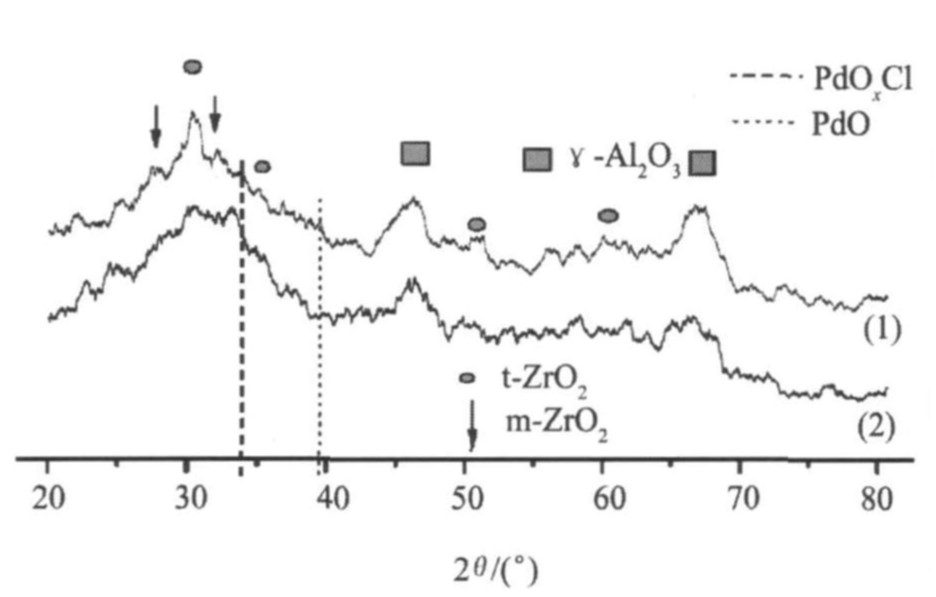
ͼ1������Pd��������XRDͼ�� ��ͼ�ɿ���, Pd/ZrO2-Al2O3 (I) ������XRDͼ�з�����PdO (39.9��) ��PdOxCl (33.8��) �������, PdOxCly��������PdCl2ΪPdԴ�Ʊ�Pd�������γɵ�
ͼ1 ������XRD��ͼ
Fig.1 XRD patterns of catalysts (1) Pd/ZrO2-Al2O3 (I) ; (2) Pd/ZrO2-Al2O3 (S)
2.2 �����Ʊ�������Pd��������ԭ���ܵ�Ӱ��
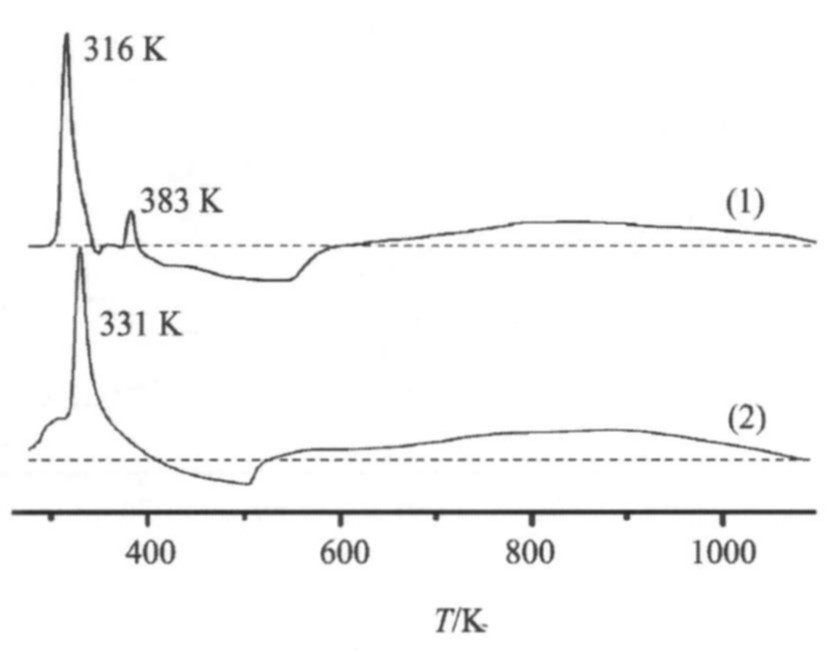
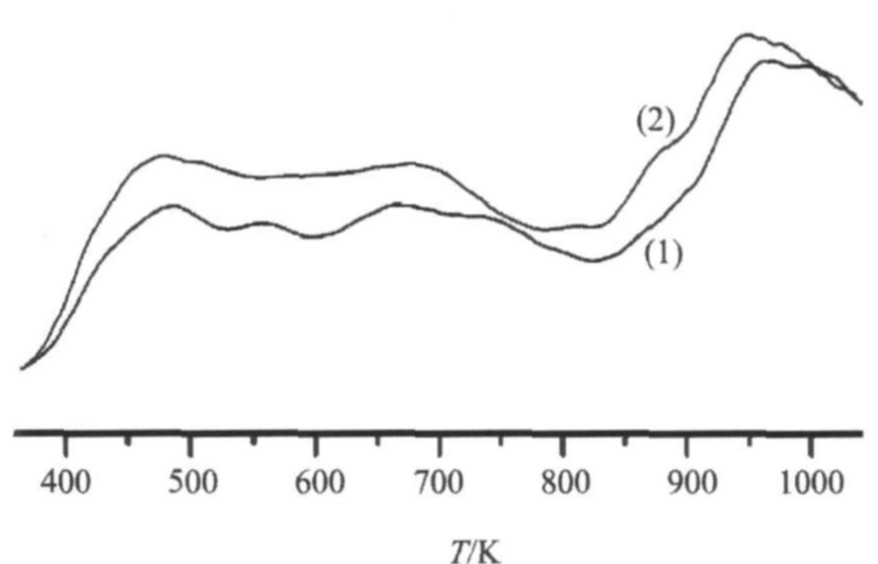
H2-TPR���о������������ ����������֮������õ���Ч����, ������TPR������ͼ2��ʾ�� 316��331 K���ֵĻ�ԭ��ֱ������Pd/ZrO2-Al2O3 (I) ��Pd/ZrO2-Al2O3 (S) ��������PdO�Ļ�ԭ, 383 K���ֵĻ�ԭ���������Pd/ZrO2-Al2O3 (I) ��������PdO�Ļ�ԭ�� ��Pd/ZrO2-Al2O3 (I) �������, Pd/ZrO2-Al2O3 (S) ��������PdO�Ļ�ԭ������·����ƶ�, ����Pd/ZrO2-Al2O3 (S) �����н��������������ý�ǿ�� Pd/ZrO2-Al2O3 (S) �����б���PdO�Ļ�ԭ�������Pd/ZrO2-Al2O3 (I) ������, ������ɢ��Pd/ZrO2-Al2O3 (S) ���������PdO�϶ࡣ ��Լ�������Ӧ��Ҫ���ڽ��������Ͻ���, �������Pd����Խ��Է�ӦԽ����, ������Ļ��Բⶨ���һ�¡�
������ZrO2����һ���Ļ�ԭ��, �仹ԭ�¶���1000 K����
ͼ2 H2��TPR��ͼ
Fig.2 H2-TPR profiles of catalysts (1) Pd/ZrO2-Al2O3 (I) ; (2) Pd/ZrO2-Al2O3 (S)
2.3 �����Ʊ�������Pd�������Ѹ����ܵ�Ӱ��
��Լ�������ӦΪ����̬��H2������̬����Է�Ӧ, H2�����������������ڷ�Ӧ�Ľ��С� ��1�г��˴�����H2��������Pd��ɢ��, ͨ��PdHx�ķֽ��¶�Ϊ363��393 K, Ϊ�˱���PdHx�ķֽ��Pd��ɢ�Ȳⶨ��Ӱ��, ����������
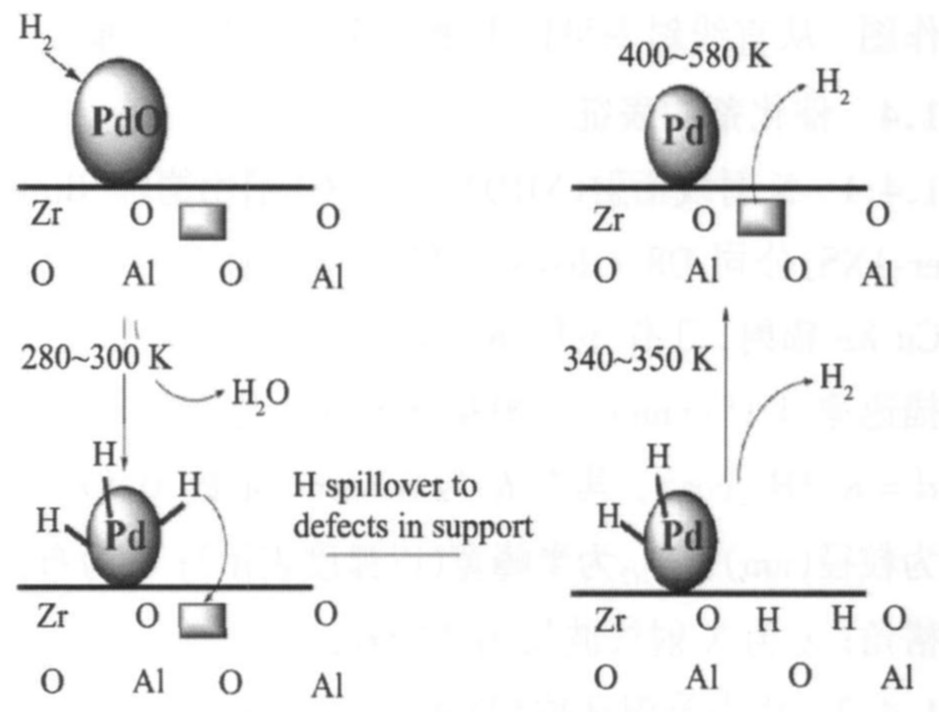
ͼ3 �������� ���غ��ͷŻ���
Fig.3 Mechanism of hydrogen spillover, storage and release from catalysts
��1 ������H2�������� Pd��ɢ�ȡ� ���ۻ��
Table 1H2adsorbed amount and dispersion and activation energy (Ea) of catalysts
| Catalysts | H2 adsorbed amount/ (10-5 mol��g-1) |
Pd dispersion (H/Pd) |
Activation energy/ (kJ��mol-1) |
Pd/ZrO2-Al2O3 (I) |
6.14 | 0.60 | 55.7 |
Pd/ZrO2-Al2O3 (S) |
7.78 | 0.76 | 52.9 |
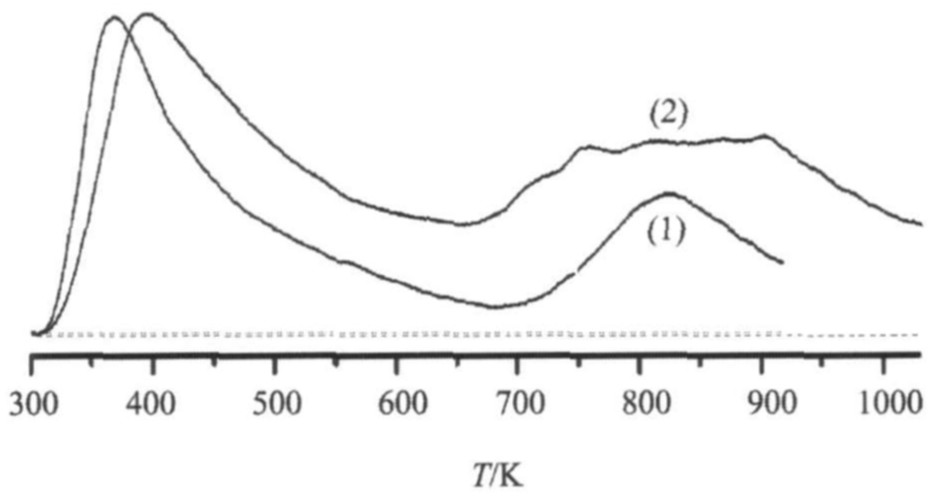
Pd/ZrO2-Al2O3 (I) ��Pd/ZrO2-Al2O3 (S) ������H2-TPD��ͼ4�� Pd/ZrO2-Al2O3���������ֵ��º��������Ѹ���, �ֱ�����ڽ���Pd������������ȱ��λ��������Ѹ��� ��Pd/ZrO2-Al2O3 (I) �������, Pd/ZrO2-Al2O3 (S) �����Ѹ����½ϸ��ҷ�����ϴ� ���º��·����Խ��, ��ӳ��Pd/ZrO2-Al2O3 (S) �����н���Pd�ķ�ɢ��Խ�������������ȱ��λԽ��, �Լ�������ӦԽ������ �ܽ�-�������ٽ���ZrO2��Al2O3�еķ�ɢ, ��ǿ��Zr�ĸ�����ЧӦ
ͼ4 H2��TPDͼ
Fig.4 H2-TPD profiles of catalysts
(1) Pd/ZrO2-Al2O3 (I) ; (2) Pd/ZrO2-Al2O3 (S)
2.4 �����Ʊ�������Pd���������Ե�Ӱ��
NH3-TPD�Ǽ��������Ե�һ�ֳ��÷����� ͼ5������Pd��������NH3-TPDͼ�� ��ͼ�пɿ���, Pd/ZrO2-Al3O3���������ֵ��º���NH3�Ѹ���, ������ (<523 K) ���Ѹ��岢��������������������NH3���Ѹ�, ����������NH4+ (NH3��H+����γ�NH4+) ��NH3���Ѹ�
ͼ5 NH3-TPD��ͼ
Fig.5 NH3-TPD profiles of catalysts
(1) Pd/ZrO2-Al2O3 (I) ; (2) Pd/ZrO2-Al2O3 (S)
2.5 ZrO2-Al2O3�����Ʊ�������Pd���������Ե�Ӱ��
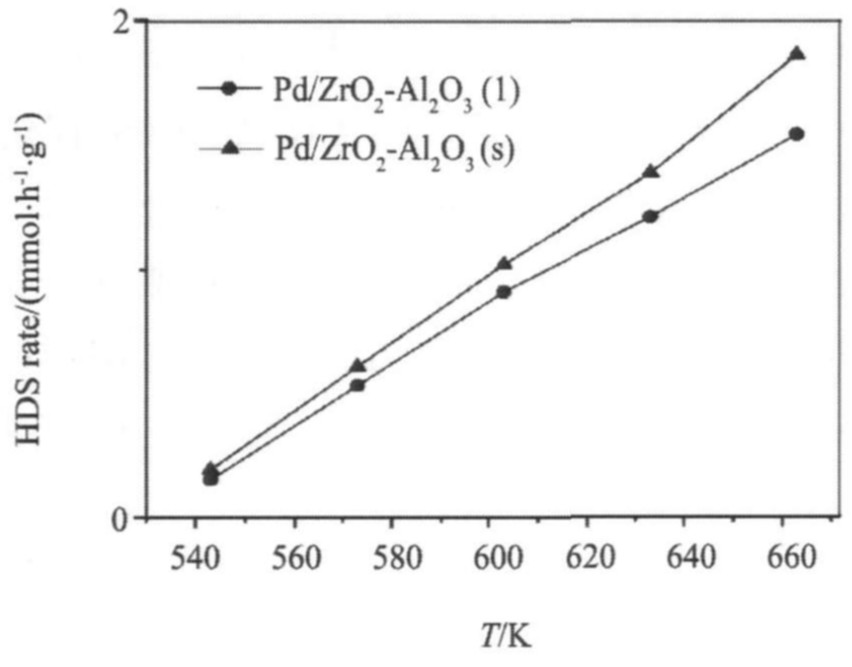
��������Լ�������Ӧ���Լ�ͼ6, ���ŷ�Ӧ�¶ȵ����ߴ����Ļ�����ߡ� ��ͼ6�ɿ���, ZrO2-Al2O3������Ʊ�������ͬ, Pd/ZrO2-Al2O3�����ļ����������Ҳ��ͬ, Pd/ZrO2-Al2O3 (S) ��������������Ա�Pd/ZrO2-Al2O3 (I) �����ߡ� ������ݱ���, Pd/ZrO2-Al2O3 (S) �����нϵ͵ı��ۻ��, ����
ͼ6 ��ͬ�����Ʊ�������Pd/ZrO2-Al2O3����HDS��Ӱ��
Fig.6 Effect of preparation methods of supports on HDS activity of Pd/ZrO2-Al2O3 catalysts
3 �� ��
��Pd/ZrO2-Al2O3 (I) �������, Pd/ZrO2-Al2O3 (S) �������нϸߵ���Լ���������ԡ� �ܽ�-�������Ʊ�ZrO2-Al2O3���������IMP��������ZrO2��Al2O3�еķ�ɢ, ���������ϵ�������ȱ��λ������, ��ǿ�˽��������������, �ٽ��˽���Pd�������ϵķ�ɢ, ʹPd�H2��������ǿ���������λ����, �����˱��ۻ��, ��������Pd���������Ļ��ԡ�
�����
[10] κ��÷, �����.CO2����CH4����ZrO2����Ni�������о�[J].�ߵ�ѧУ��ѧѧ��, 2002, 23:92.
[14] ��������.�����ԭ��[M].�Ϻ�:������ѧ������, 1997.
[15] �¹���, �ſ���, ������, ����.����Al2O3/ZrO2���Ϸ�����Ʊ�������[J].���Ͽ�ѧ�빤��, 2004, 12:20.
[16] ����, ������, �.����ZrO2������������ԭ��Ӱ��[J].ȼ�ϻ�ѧѧ��, 1990, 18:370.
[10] κ��÷, �����.CO2����CH4����ZrO2����Ni�������о�[J].�ߵ�ѧУ��ѧѧ��, 2002, 23:92.
[14] ��������.�����ԭ��[M].�Ϻ�:������ѧ������, 1997.
[15] �¹���, �ſ���, ������, ����.����Al2O3/ZrO2���Ϸ�����Ʊ�������[J].���Ͽ�ѧ�빤��, 2004, 12:20.
[16] ����, ������, �.����ZrO2������������ԭ��Ӱ��[J].ȼ�ϻ�ѧѧ��, 1990, 18:370.