DOI: 10.11817/j.ysxb.1004.0609.2021-36583
常压富氧浸出含锗氧化锌烟尘
朱应旭1,邓志敢1,魏 昶1,李衍林2,张 梅2,赵文丽1
(1. 昆明理工大学 冶金与能源工程学院,昆明 650093;
2. 云南驰宏锌锗股份有限公司,曲靖 655011)
摘 要:为提高含锗氧化锌烟尘中锗的浸出率,提出采用富氧常压浸出-中和工艺处理含锗氧化锌烟尘,通过调节合适的酸度控制烟尘中硅的浸出及氧的溶解,避免形成铁硅锗胶体造成锗的损失的同时控制溶液中Fe3+浓度便于烟尘中硫化物的溶出。结果表明:常压富氧条件下,在温度为90 ℃、液固比为7 mL/g、控制终点pH为0.3~0.7的条件下浸出4 h,锗浸出率为83%,较传统工艺条件下的锗浸出率提高13%。浸出渣的物相主要为硫酸铅和硫化锌以及二氧化硅,表面出现多孔、蓬松状结构。锗主要以硅酸盐态赋存,84.94%以该状态赋存的锗被浸出,占总锗的59.24%。浸出液中Fe3+浓度约为0.4 g/L,硅含量约为64.5 mg/L,实现了对Fe3+及Si的控制。采用含锗氧化锌烟尘对溶液进行中和还原,表明控制溶液温度为90 ℃,pH为3.0,反应1.5 h,可将溶液中Fe3+浓度控制在0.025 g/L内,满足后续的沉锗要求。
关键词:锗;氧化锌烟尘;常压富氧浸出
文章编号:1004-0609(2021)-04-0995-12 中图分类号:TF803.21 文献标志码:A
引文格式:朱应旭, 邓志敢, 魏 昶, 等. 常压富氧浸出含锗氧化锌烟尘[J]. 中国有色金属学报, 2021, 31(4): 995-1006. DOI: 10.11817/j.ysxb.1004.0609.2021-36583
ZHU Ying-xu, DENG Zhi-gan, WEI Chang, et al. Leaching germanium-containing zinc oxide dust by atmospheric oxygen enrichment[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(4): 995-1006. DOI: 10.11817/j.ysxb.1004.0609.2021-36583
锗被广泛应用于军事、红外、医药、催化、半导体、光纤等领域[1-2],随着高技术产业的发展,锗的需求量也越来越大。但自然界中几乎不存在独立的锗金属矿床,锗主要由伴生矿或二次资源的回收获得,常见锗伴生矿源有硫化铅锌矿和氧化铅锌矿以及煤矿和铜矿等[3-4]。在铅锌矿中,锗通常存在于硫化锌晶格或铁酸锌晶格中[5-6]。
目前,湿法炼锌广泛采用焙烧-浸出-电积工艺,焙烧过程中锗大部分存在于(Fe,Ge)2O4一类的铁酸盐固溶体[7],在中浸和弱酸浸出阶段基本不被浸出[8]。浸出渣经过火法工艺处理后[9],锗挥发与氧化锌烟尘一起被收集[10],得到含锗的副产物。此外,含锗的副产物还包括锌精炼渣等[11]。从锌冶炼系统中回收锗,主要包括两个过程[12]:从含锗的副产物中将锗浸出至溶液中;通过选择性的试剂将锗从溶液中分离并富集,包括萃取、树脂吸附以及化学沉淀等。其中在浸出过程中锗的浸出率决定着整个流程中锗回收率,Fe3+对锗的分离富集有着不利的影响[13-15],因此,在分离富集前应降低溶液中的Fe3+浓度。此外,浸出过程中锗可因水解、杂质离子吸附等原因进入至渣中,造成表观上锗浸出率下降。其中,锗与硅具有相近的共价半径和离子半径[16],易与铁形成共铁硅锗胶体沉淀造成锗损失[17],DUTRIZE等[5]证实弱酸渣中锗大部分以铁硅锗胶体形式存在。LIANG等[18]证实在高压酸浸中硅和锗可形成共沉淀造成锗的损失。
吴雪兰[19]分别采用SO2还原浸出工艺和热酸工艺处理锌浸出渣,但锗的浸出效果仅为70%;通过还原焙烧-磁选-锈蚀法从处理锌浸出渣[20-21],以及采用高压酸浸、草酸浸出[22-23]或酸碱选择性浸出工艺[24]处理锌精炼渣,均可达到较高的锗浸出率。王万坤[25]通过微波碱性焙烧-水溶工艺处理含锗氧化锌烟尘处理含锗氧化锌,锗浸出率达到了97.16%。目前,在实际生产中,普遍采用两段工艺从含锗氧化锌中回收锗。
以云南某企业通过两段浸出工艺(pH为2.5~3.0的弱酸浸出和高酸浸出)处理烟化炉所产出的含锗氧化锌烟尘为例,锗的浸出为70%左右。较低的浸出率造成了整个流程中锗回收率不高的问题。JIANG等[26]对锗在烟尘中的分布进行了研究,表明锗分布于氧化锌、硫化锌、方铅矿以及硅酸铅等,且在方铅矿中锗含量较高,锗的分布与铅和硫呈正相关关系,认为通过提供氧化剂将硫化铅、硫化锌等进行浸出可减少两者携带的锗的损失。弱酸阶段可将大部分氧化态的金属如锌、铁等浸出,但烟尘中硫化物的浸出则需要氧化剂的加入以及铁离子对氧进行传递,而氧的溶解度受温度和酸度的影 响[27],高温高酸不利于氧的溶解,低酸阶段加入氧化剂可能生成大量的Fe3+,不利于后续提锗工艺的进行,高酸阶段通入氧气,不利于氧的溶解的同时,矿浆中缺乏铁传递氧。此外,高酸阶段可将硅大量溶出,当硅含量较高的矿浆经过浓密加入至弱酸阶段时,在较高的pH条件下可形成锗硅胶沉淀,造成锗的损失。综上所述,依据湿法炼锌的主流程以及现有的工艺设备,本文作者采用常压富氧浸 出-中和工艺处理氧化锌烟尘,以氧气作为氧化剂并控制合适的酸度,控制硅的溶出的同时,以有利于氧的溶解以浸出部分硫化物,提高锗的浸出率,同时控制Fe3+浓度;在中和阶段采用含锗氧化锌烟尘对酸浸液进行中和还原,降低Fe3+以有利于后续提锗工艺的进行。
1 实验
1.1 实验方法及设备
将一定量的废电解液置于三口烧瓶中,在恒温水浴锅(金坛市大地自动化仪器厂,HH-S28s)内水浴加热,用电子天平(梅特勒―托利多仪器上海有限公司,E6001型)称取一定量的含锗氧化锌。待三口烧瓶中废电解液加热至所需温度后,将烟尘加入到三口烧瓶中。固定搅拌转速为400 r/min,同时通入富氧气体(昆明鹏翼达气体股份有限公司,80%O2(体积分数),20%N2(体积分数))后反应开始。反应结束够用真空泵(浙江台州求精真空泵有限公司,2XZ-2型)对矿浆进行过滤,得到滤液和浸出渣,用量筒量取滤液的体积,对滤液进行取样分析,采用重铬酸钾滴定法对滤液中Fe2+和Fe3+进行测定,用锗显色剂对滤液中锗着色后用紫外可见分光光度计(北京瑞丽分析仪器有限公司,UV-1801型)进行测定,浸出渣经过洗涤过滤后,置于真空干燥箱(上海一恒科学仪器有限公司,DZF-6090型)中,在70 ℃条件下恒温烘干后称重记录并送检。各元素浸出率(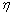 )以渣计,计算公式如下:
)以渣计,计算公式如下:
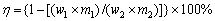 (1)
(1)
式中:η为浸出率;w1为浸出渣中元素含量,%;m1为浸出渣质量,g;w2为原料中元素含量,%;m2为实验中所用含锗氧化锌烟尘质量;g。
1.2 实验原料
实验中所用含锗氧化锌烟尘、废电解液均来自云南某湿法炼锌企业,其成分如表1和2所示。对含锗烟尘进行了物相分析和锗物相分析,物相分析和锗赋存状态如图1和表3所示。
由表1可知,含锗氧化锌烟尘中主要的有价金属锌含量达到了44.38%,锗含量分别达到了763.7 g/t,物料中铅含量为13.55%,铁含量分别为4.93%, 硫含量分别为7.13%,由于该烟尘是从烟化炉中产出,烟化炉处理锌浸渣时,常常配入二氧化硅进行造渣,因此烟尘中硅含量达到了2.78%(折算为二氧化硅)。废电解液为常规湿法炼锌过程常见的产物,由表2可知废电解液中硫酸浓度为151.62 g/L,同时含有锌、镁、锰等离子。
表1 含锗氧化锌烟尘主要化学成分
Table 1 Main chemical composition of germanium-containing zinc oxide dust (mass fraction, %)
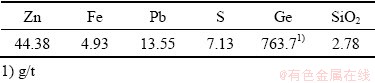
表2 废电解液主要化学成分
Table 2 Chemical composition of spent electrolyte (g/L)

2 结果与分析
2.1 氧化锌烟尘的含量
图1所示为含锗氧化锌烟尘XRD谱。表3所示为含锗氧化锌烟尘中锗的分布赋存。由图1可知,烟尘中主要为氧化锌,此外还含有硫化铅以及硫化锌。对于锗在氧化锌烟尘中的赋存,JIANG等[26]认为锗主要存在锌、铅的矿物中,特别是PbS中。但由表3可知,锗大部分赋存于硅酸盐中,比例达到了69.74%,这可能是由于锗的亲硅性使其易于赋存在硅酸盐中,约18.42%的锗赋存在一些金属形成的固溶体中,此外还有少量的锗以氧化态和硫化态的形式赋存。
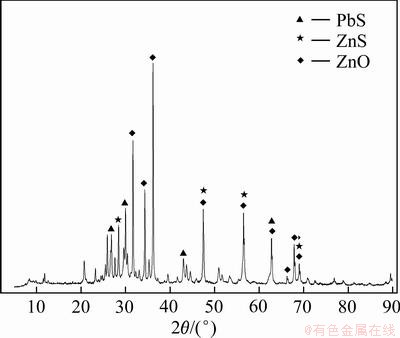
图1 含锗氧化锌烟尘XRD谱
Fig. 1 XRD pattern of germanium-containing zinc oxide dust
表3 锗的分布赋存
Table 3 Distribution of germanium

对含锗氧化锌烟尘进行形貌分析,其结果如图2所示。由图2可知,含锗氧化锌烟尘主要分为两种形貌,一种形貌以致密基体为主,表面粘附小颗粒,表面小颗粒间疏松多孔如图2(a)所示;另一种形貌主要是小颗粒聚集的松散结构如图2(b)所示。为进一步了解其组成,对氧化锌烟尘进行了EDS分析。图2中致密的球形颗粒(Part 1)表现出较强的Zn、Pb、O以及S的特征衍射峰,其中质量分数分别为25.44%、27.46%、16.06%、4.56%,结合王万坤等[28]的研究,可认为是以氧化锌包裹硫化铅为主的颗粒;细小颗粒(Part 2)表现出较强的Zn衍射峰,此外,还含有Pb、S及O的衍射峰,可能是氧化锌与硫化铅及硫化锌的混合物;致密部分(Part 3)衍射峰为Zn、O以及S的衍射峰,可能是硫化锌与氧化锌的混合物。图2中方形结构(Part 4)主要是硫化铅颗粒;球状结构(Part 5)衍射峰较为复杂,可能是ZnO、PbS及ZnS的混合颗粒;片状结构(Part 6)含有Zn、Pb、Si、O的衍射峰,可能是锌或铅的硅酸盐。
2.2 不同体系条件下氧化锌烟尘中金属的浸出率
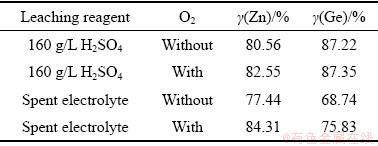
为探索在常压富氧条件下,能否有效提高锌、锗的浸出率,开展了探索实验,验证了在液固比为6 mL/g,在90 ℃条件下浸出时间为4 h,分别以浓度为160 g/L硫酸溶液为浸出剂与废电解液溶液作为浸出剂,在通氧与不通氧条件下的浸出效果,其结果如表4所示。
由表4可知,以配置的硫酸溶液作为浸出剂,锌浸出率由80.56%提升至82.55%,锗浸出率由87.22%提升至87.35%;以废电解液为浸出剂,锌浸出率由77.44%提升至84.41%,锗浸出率由68.74%提升至75.83%。同等条件下,采用配置的硫酸溶液浸出效果较采用废电解液浸出效果明显,这是由于废电解液中含有锌、镁、锰等离子,其黏度较配置硫酸溶液大,影响了浸出过程中的传质,造成了浸出效果的差异;通氧后的两个体系中的锌和锗浸出率均有提高,这是由于在常压富氧条件下,氧化氛围得到提高,有利于硫化物的浸出,且由于不通氧条件下废电解液体系中锌和锗浸出率较低,因此,该体系通氧后浸出效果对比较明显。此外,气体的通入可加强传质的进行,有利于反应的进行。
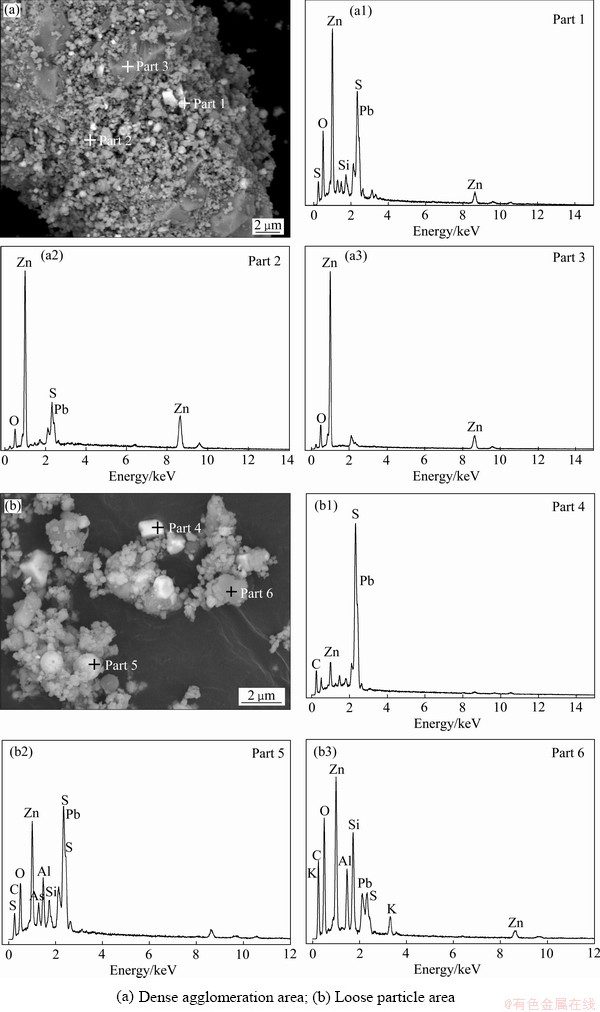
图2 含锗氧化锌烟尘SEM像和EDS谱
Fig. 2 SEM images((a), (b)) and EDS spectra((a1), (a2), (a3), (b1), (b2), (b3)) of germanium-containing zinc oxide dust
表4 不同体系中不同通氧条件下锌和锗的浸出结果
Table 4 Experimental leaching results of Zn and Ge in different system and oxygenation
2.3 各因素对浸出的影响
在2.2节中初步证实采用常压富氧工艺进行浸出能够有效提升锌和锗的浸出率,但在该工艺中,各因素对工艺的影响尚不明确。实际生产中通过时间、温度、液固比等控制浸出,当涉及到氧气或高温时,常常需要考虑到分压的大小。本节探讨了时间、温度、液固比以及氧分压对锌、锗浸出的影响。
采用富锗氧化锌烟尘与酸浓度为151.62 g/L的废电解液,在温度为90 ℃、液固比为7 mg/L条件下通氧进行实验。考察反应时间对锌、锗的浸出率如图3(a)所示。
由图3(a)可知,84%以上的锗在1 h内被浸出,且延长时间不能显著提高锗的浸出率,由于烟尘中主要物相为氧化锌,氧化锌烟尘酸溶反应剧烈,1 h内,80%以上的锌可被浸出,随后锌有缓慢上升的趋势,在浸出4 h后达到83.79%,延长时间有利于锌的浸出。这是由于烟尘中含有氧化锌与硫化锌烟尘混合的颗粒,受扩散控制,其反应速率较慢,颗粒中氧化锌需要较长时间才能被浸出,此外ZnS通过与Fe3+反应也能被溶出,表现为浸出率的缓慢上升。
采用富锗氧化锌烟尘与酸浓度为151.62 g/L的废电解液在90 ℃条件下通氧浸出4 h进行不同液固比条件下的实验,考察液固比对锌、锗的浸出效果如图3(b)所示。
由图3(b)可知,锌浸出率在液固比为6 mL/g时达到了84.14%,锗的浸出率在7 mL/g时达到了83.09%;当液固比大于7 mL/g,锌和锗浸出率趋于平缓。当酸的浓度一定时,液固比的选取决定着体系中酸的总量,包括参与反应的酸以及维持较大反应限度所需要的酸浓度,较大的液固比能够为反应体系提供足够的酸,较高的酸浓度可维持较大的反应限度,当溶液能够满足上述需要时,继续增加液固比无法提高锌和锗的浸出率。此外,由于可溶反应物的量是一定的,即酸的消耗量也是一定的,因此,体系中酸的总量决定着终点的酸度,当反应时间较长时,应控制合适的终点酸度,以保证硅在较长的时间内以及较低的酸度条件下不被浸。当液固比为5 mL/g、终点pH为0.81时,不能维持较大的反应限度;当液固比为8 mL/g、pH约为0时,终点的酸度较高;当液固比为7 mg/L时,体系可提供足够的酸进行反应,且可将矿浆中酸度控制在合理的水平。
采用一定量富锗氧化锌烟尘,选定液固比为7 mL/g,在不同温度下通氧4 h进行实验,温度对锌、锗的浸出效果如图3(c)所示。
由图3(c)可知,80 ℃时,锌浸出率约为83.18%,锗浸出率约为79.96%;随着温度的增加,锌浸出率变化不大,而锗浸出率在80~110 ℃间有上升趋势,为使锌和锗浸出率最大化,应选取较高的温度,且在较高的温度条件下,可减少因锗水解造成的损 失[18],但在实际生产中,考虑到因能耗及设备因素带来的成本问题,需要选取合适经济的温度。
采用氧化锌烟尘在,与酸浓度为151.62 g/L的废电解液在液固比为7 mL/g,温度为90 ℃的条件下通氧反应4 h,氧分压对锌、锗的浸出效果如图3(d)所示。
由图3(d)可知,锗在氧分压为0.021 MPa时的浸出率为80.78%;在氧分压为0.4 MPa时,浸出率为83.25%,在选取的氧压范围内,提高氧分压对锗浸出效果不明显;当氧分压为0~0.2 MPa时,锌浸出率无明显变化,维持在85.78%左右。这是因为Fe3+小于0.2 g/L,没有足够的Fe3+传递氧与硫化锌进行反应,当氧分压由0.2 MPa上升至0.3 MPa,锌浸出率由85.78%提高至97.43%。这是因为当氧分压大于等于0.3 MPa时,在控制的酸度和温度条件下,虽然溶液中仍然以Fe2+为主,但Fe3+上升并维持在1.4~1.5 g/L之间,有足够的Fe3+与硫化锌进行反应,即在控制的酸度条件下,氧压为0.3 MPa时即可达到较好的浸出效果。
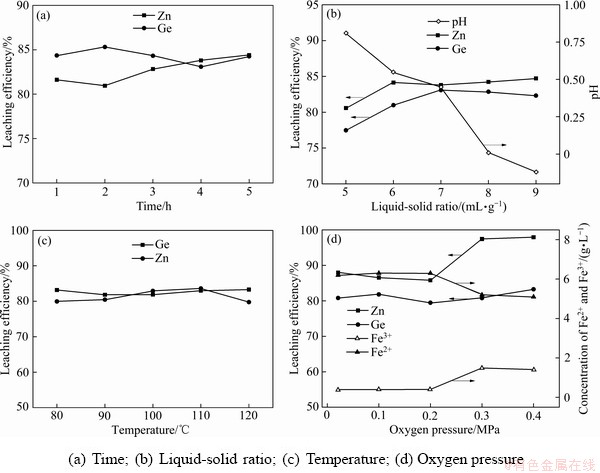
图3 各因素对锌浸出率的影响
Fig. 3 Effect of different experiment conditions on leaching efficiency
2.4 中和还原
在常压富氧条件下,按液固比为7 mL/g,温度为90 ℃条件下浸出4 h,进行了两组平行实验(实验1和实验2),其结果如表5和表6所示。
由表5和表6可知,两个实验中锌浸出率分别为83.79%、83.09%,锗浸出率分别为83.34%、82.33%,得到的酸浸液中铁元素主要为Fe2+,但仍然含有0.4 g/L的Fe3+,需降低Fe3+浓度便于后续提锗工艺的进行。此外,若采用单宁沉锗(pH约为3),需降低酸度,提高pH。
表5 平行实验锌和锗浸出率
Table 5 Result of parallel experiment of leaching efficiency of Zn and Ge

为降低溶液中Fe3+浓度和酸度,采用含锗氧化锌烟尘对上述两组实验(即实验1和实验2)所得滤液进行中和还原,控制温度为90 ℃、 pH为3.0 [29]、反应时间1.5 h,经过滤后中和滤液和中和渣,其中中和滤液成分如表7所示。
由表7可知,当中和pH控制在3.0附近时,溶液中锗并未水解而损失,且Fe3+浓度为0.025 g/L,达到了控制Fe3+浓度的目标。
表6 平行实验酸浸液pH、铁及锗含量
Table 6 pH and concentration of Fe and Ge in parallel experiment solution

2.5 浸出过程中硅的控制
对上述的实验所产出浸出渣的主要化学成分进行了分析,结果如表8所示。酸浸液成分如表9所示。
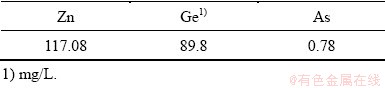
由表8可知,浸出渣中铅含量达到31.28%,主要为硫酸铅,较原料中铅含量富集了2.3倍,渣中含有17.24%的锌,6.2%的硅。由表9可知,中和后溶液中锌达到了117.08 g/L,锗达到了89.8 mg/L,此外还0.78 g/L的砷。实验中和前溶液中硅含量为64.5 mg/L,中和后溶液中硅含量达到了83.18 mg/L,表明在中和过程中部分硅溶解至溶液中,在整个过程中硅含量小于100 mg/L,小于传统工艺中120 mg/L的硅浓度,较低的硅浓度可有效减少锗铁硅胶体的形成,避免过多锗进入渣中。
表7 中和液中铁、锗浓度
Table 7 Concentration of iron and Ge ion in acid leaching liquid and neutralizing solution
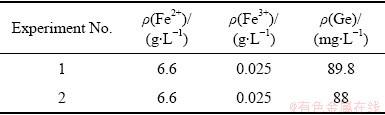
表8 酸浸渣主要成分
Table 8 Main chemical composition of acid leaching residue (mass fraction, %)
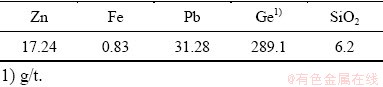
表9 中和溶液成分
Table 9 Concentration of Zn and Ge in neutralized solution (g/L)
2.6 酸度及铁的价态价态的变化
常压条件下,在液固比为7 mL/g、温度为90 ℃条件下通氧浸出4 h,铁的浸出率以及溶液中铁价态如图4所示。
由图4可知,70%以上的铁在1 h内被浸出,随着时间的延长,浸出率逐渐升高;3 h时,90%以上的铁被浸出。溶液中的铁大部分为Fe2+,在氧气的氧化氛围中逐渐被氧化为Fe3+,在3h时,约有0.4 g/L的Fe3+随后趋于平缓未见升高,其矿浆pH如图5所示,pH在1 h时上升至0.175,这是因为大量的金属溶解消耗酸,随后逐渐上升,到3 h时趋于平稳,在该pH条件下,Fe3+趋于平稳,实现了对铁价态的控制。
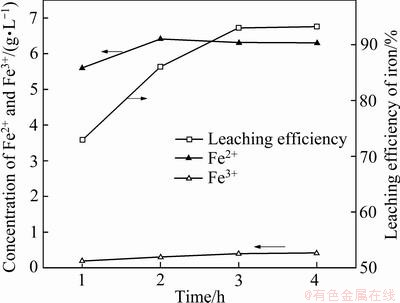
图4 不同时间时铁浸出率及铁价态的变化
Fig. 4 Change of leaching efficiency of iron and iron valence state with time
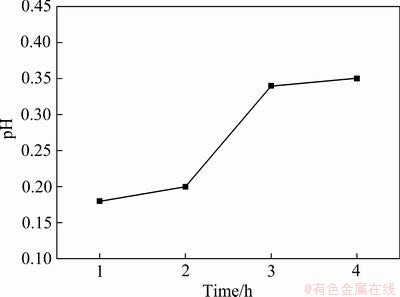
图5 pH随时间变化
Fig. 5 Change of pH with time
2.7 浸出过程中锗的物相变化
通过化学法对浸出渣进行了锗的赋存分布分析,锗的赋存状态如表10所示。根据原料和浸出渣中锗含量的变化,计算了各赋存状态中锗的浸出率以及各赋存状态下被浸出的锗占原料总锗的比例。
表10 浸出渣中锗的物相分布、各组分浸出率及被浸出锗的占比
Table 10 Distribution of germanium in residue and leaching efficiency and proportion of of leached germanium
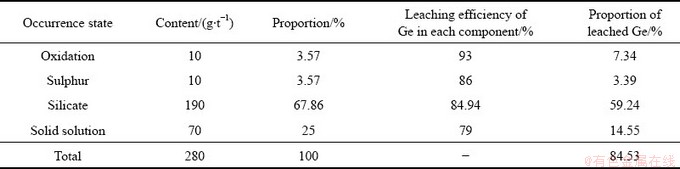
由表10可知,经过计算后,氧化态和硫化态的锗含量占比很小,但该赋存状态下锗浸出率分别达到了93%、86%,而以硅酸盐态赋存的锗含量为190 g/t,占比达到了68.86%;进过计算,该赋存状态下84.94%的锗被浸出,即原料中有59.34%的锗以硅酸盐状态被浸出。理论上该部分锗浸出率应当与硅浸出率相当,但实际上被浸出的硅很少,这是可能是因为锗主要存在于硅酸盐的边缘部分,边缘部分的锗含量远高于其他部分锗含量,DUTRIZE等[5]研究含锗弱酸渣时,观察到类似的锗分布。以固溶体状态存在的锗占比为25%,含量为70 g/t,以该赋存状态存在的锗约有79%被浸出,占原料总锗的14.55%。
2.8 浸出渣表征
对实验过程中产生的酸浸渣进行了物相分析和SEM-EDS分析,分别如图6和7所示。
由图6可知,经过常压富氧浸出后,酸浸渣主要成分为硫酸铅、硫化锌以及二氧化硅。由于较低的酸度下,二氧化硅较难浸出,由于含锗烟尘经过浸出后质量减小,二氧化硅含量升高,可被XRD检测到;在常压富氧浸出过程中,在控制的pH条件下,由于Fe3+浓度较低,含锗氧化锌烟尘中的硫化锌并不能完全反应进入到溶液中,因此浸出渣中含有一定量的硫化锌;浸出渣中未见硫化铅的衍射峰,出现了硫酸铅的衍射峰,这是由于在有氧存在的条件下,大部分硫化铅转化为硫酸铅,这有利于该部分硫化物中的锗浸出至溶液中[27]。硫化铅转化为硫酸铅,反应式如下所示:
PbS+H2SO4+0.5O2=PbSO4+S+H2O (2)
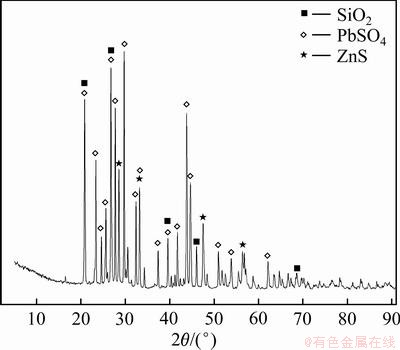
图6 酸浸渣的XRD谱
Fig. 6 XRD pattern of acid leaching residue
由图7可知,经过常压富氧浸出后,酸浸渣致密基体表面呈多孔结构,颗粒减少,出现蓬松状结构(Part 1),其成分较为复杂,含有S、Pb、Zn、Si等元素;出现的白色壳状物(Part 2)Zn、S特征衍射峰强烈,可推测是ZnS,结合原料中氧化锌与硫化锌混合形成的球形致密颗粒,可推测浸出过程中氧化锌部分被溶解留下了壳状的硫化锌结构,该部分氧化锌由于传质条件限制,需要较长时间才能浸出,宏观上表现为浸出率的略微上升。此外,还发现了致密颗粒状结构(见图7 中Part 3),含有较强的Pb及S的特征衍射峰,主要成分是PbS,浸出渣中仍有部分硫化铅未转化为硫酸铅。由于在该体系下应当有硫酸铅生成,但Part 3中主要为光滑状的颗粒,因此可能是硫化铅颗粒反应后,生成硫酸铅从表明脱离,留下未反应的硫化铅。
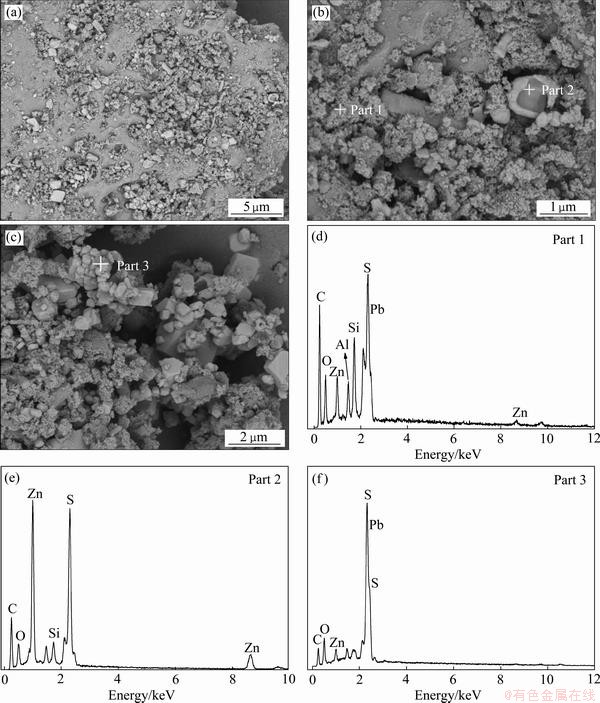
图7 浸出渣的SEM像和EDS谱
Fig. 7 SEM images and EDS spectra of acid leaching residue
3 结论
1) 在反应温度为90 ℃、浸出时间为4 h、液固比为7 mL/g条件下,采用常压富氧浸出处理氧化锌烟尘,可有效提高含锗氧化锌烟尘中锌和锗的浸出率,其浸出率在80%以上,溶液中硅浓度小于100 mg/L,远小于传统工艺中硅浓度。通过循环实验验证常压富氧浸出工艺的稳定性,经过多次循环,其锌浸出率稳定在83%左右,锗浸出率为83%,锗浸出率较现有工艺的70%提高了13%。
2) 对采用常压富氧浸出得到的酸浸液进行了中和,在温度为90 ℃、pH为3.0的条件下反应1.5 h,可将溶液中Fe3+浓度可降低至0.025 g/L以下,满足后续沉锗要求。
3) 浸出渣中锌含量较高,达到了17.24%,其主要物相为硫化锌,而铅含量达到了31.28%,其主要物相为硫酸铅,可作为炼铅的原料。
REFERENCES
[1] BEN D, ANTOON T, ROMANDICLGOR L. Germanium: From the first application of Czochralski crystal growth to large diameter dislocation-free wafers[J]. Materials Science in Semiconductor Processing, 2006, 9(4/5): 437-443.
[2] DASS D. Effects of surface passivation by hydrogen on the structural and electronic properties of a germanium nanowire: A sp3 tight binding study[J]. Applied Surface Science, 2019, 488: 404-417.
[3] 刘丽霞, 李文挺, 彭 军, 等. 粉煤灰中锗的高温火法二次富集工艺[J]. 中国有色金属学报, 2018, 28(1): 183-187.
LIU Li-xia, LI Wen-ting, PENG Jun, et al. Germanium enrichment from ash by second enrichment process at high temperature[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(1): 183-187.
[4] HOLL R, KLING M, SCHROLL E. Metallogenesis of germanium―A review[J]. Ore Geology Reviews, 2007, 30(3/4): 145-180.
[5] DUTRIZAC J E, CHEN T T, LONGTON R J. The mineralogical deportment of germanium in the clarksville electrolytic zinc plant of savage zinc[J]. Metallurgical and Materials Transaction, 1996(27): 567-576.
[6] 赵 汀, 王登红, 刘 超, 等. 中国锗矿成矿规律与开发利用现状[J]. 地质学报, 2019, 93(6): 1245-1251.
ZHAO Ting, WANG Deng-hong, LIU Chao, et al. Metallogenic and utilization status of Ge deposit in China[J]. Actageologica Sinica, 2019, 93(6): 1245-1251.
[7] 许绍全, 李素清. 硫化锌精矿工艺中稀散金属回收的新途径[J]. 有色金属(冶炼部分), 1990(1): 32-35.
XU Shao-quan, LI Su-qing. A new method for recovery of scattered metal from zinc sulfide concentrate process[J]. Nonferrous Metals(Extractive Metallurgy), 1990(1): 32-35.
[8] 刘中清, 唐谟堂, 鲁君乐, 等. 湿法炼锌中性浸出过程中锗的行为研究[J]. 湿法冶金, 2000, 19(2): 43-47.
LIU Zhong-qing, TANG Mo-tang, LU Jun-le, et al. Study on behavior of germanium during neutral leaching of zinc hydrometallurgy process[J]. Hydrometallurgy of China, 2000, 19(2): 43-47.
[9] 梅光贵, 王德润, 周敬元, 等. 湿法炼锌[M]. 长沙: 中南大学出版社, 2001.
MEI Guang-gui, WANG De-run, ZHOU Jing-yuan, et al. Zinc hydrometallurgy[M]. Changsha: Central South University Press, 2001.
[10] 王吉坤, 何蔼平. 现代锗冶金[M]. 北京: 冶金工业出版社, 2005.
WANG Ji-kun, HE Ai-ping. Modern germanium metallurgy[M]. Beijing: Metallurgical Industry Press, 2005.
[11] 刘付朋, 刘志宏, 李玉虎, 等. 锌粉置换镓锗渣硫酸浸出过程[J]. 中国有色金属学报, 2016, 26(4): 908-918.
LIU Fu-peng, LIU Zhi-hu, LI Yu-hu, et al. Sulfuric leaching process of zinc powder replacement residue containing gallium and germanium[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(4): 908-918.
[12] KUL M, TOPKAYA Y. Recovery of germanium and other valuable metals from zinc plant residues[J]. Hydrometallurgy, 2008, 92(3/4): 87-94.
[13] LIANG Duo-qiang, WANG Ji-kun, WANG Yun-hua, et al. Behavior of tannins in germanium recovery by tannin process[J]. Hydrometallurgy, 2008, 93: 140-142.
[14] MA Xi-hong, QIN Wen-qing, WU Xue-lan. Extraction of germanium(Ⅳ) from acid leaching solution with mixtures of P204 and TBP[J]. Journal of Central South University, 2013, 7(7): 1978-1984.
[15] ZHOU Tai-li, ZHONG Xiang, ZHENG Long-ao. Recovering In, Ge and Ga from zinc residues[J]. Journal of the Minerals, Metals and Materials Society, 1989, 41(6): 36-40.
[16] 章 明, 顾雪祥, 付绍洪, 等. 锗的地球化学性质与锗矿床[J]. 矿物岩石地球通报, 2003, 22(1): 82-87.
ZHANG Ming, GU Xue-xiang, FU Shao-hong, et al. A review of disperse element germanium[J]. Bulletin of Mineralogy, Petrology and Geochemistry, 2003, 22(1): 82-87
[17] WARDELL M P, DAVIDSON C F. Acid leaching extraction of Ga and Ge[J]. Journal of Metals, 1987, 39(6): 39-41.
[18] LIANG Duo-qiang, WANG Ji-kun, WANG Yun-hua. Difference in dissolution between germanium and zinc during the oxidative pressure leaching of sphalerite[J]. Hydrometallurgy, 2009, 95(1/2): 5-7.
[19] 吴雪兰. 从锌浸出渣中回收镓锗的研究[D]. 长沙: 中南大学, 2013.
WU Xue-lan. Recovery of gallium and germanium from zinc residue[D]. Changsha: Central South University, 2013.
[20] 黄柱成, 杨永斌, 蔡江松, 等. 浸锌渣综合利用新工艺及镓的富集行为[J]. 中南工业大学学报, 2002, 33(2): 133-136.
HUANG Zhu-cheng, YANG Yong-bin, CAI Jiang-song, et al. Comprehensive utilization of zinc-leaching residue and concentration mechanism of gallium[J]. Journal of Central South University of Technology, 2002, 33(2): 133-136.
[21] 李光辉, 董海刚, 姜 涛, 等. 锈蚀法从浸锌渣还原铁粉中分离镓锗的基础与应用[J]. 中国有色金属学报, 2004, 14(11): 1940-1945.
LI Guang-hui, DONG Hai-gang, JIANG Tao, et al. Fundamentals and applications of separating Ga and Ge from ferrous powder reduced from zinc leach residues by corrosion process[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(11): 1940-1945.
[22] 刘付朋, 刘志宏, 李玉虎, 等. 锌粉置换镓锗渣草酸浸出过程[J]. 中国有色金属学报, 2017, 27(10): 2154-2163.
LIU Fu-peng, LIU Zhi-hu, LI Yu-hu, et al. Oxalic acid leaching of zinc powder replacement residue containing gallium and germanium[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(10): 2154-2163.
[23] 刘付朋, 刘志宏, 李玉虎, 等. 锌粉置换镓锗渣高压酸浸的浸出机理[J]. 中国有色金属学报, 2014, 24(4): 1091-1098.
LIU Fu-peng, LIU Zhi-hu, LI Yu-hu, et al. Leaching mechanism of zinc powder replacement residue containing gallium and germanium by high pressure acid leaching[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(4): 1091-1098.
[24] RAO Shuai, WANG Dong-xing, LIU Zhi-qiang, et al. Selective extraction of zinc, gallium, and germanium from zinc refinery residue using two stage acid and alkaline leaching[J]. Hydrometallurgy, 2019, 183: 38-44.
[25] 王万坤. 微波焙烧含锗氧化锌烟尘回收锗的研究[D]. 昆明: 昆明理工大学, 2013.
WANG Wan-kun. Study on germanium recovery from zinc oxide dust containing germanium by microwave roasting[D]. Kunming: Kunming University of Science and Technology, 2013.
[26] JIANG Tao, ZHANG Tao, YE Feng-chun, et al. Occurrence state and sulfuric-acid leaching behavior of germanium in secondary zinc oxide[J]. Minerals Engineering, 2019, 137: 334-343.
[27] TROMANS D. Oxygen solubility modeling in inorganic solutions: concentration, temperature and pressure effects[J]. Hydrometallurgy, 1998, 50(3): 279-296.
[28] 王万坤, 王福春, 尹雨悦, 等. 氧化锌烟尘工艺矿物学研究[J]. 矿产保护与利用, 2018(4): 79-82.
WANG Wan-kun, WANG Fu-chun, YIN Yu-yue, et al. Study on the mineralogy of zinc oxide dust[J]. Conservation and Utilization of Mineral Resources, 2018(4): 79-82.
[29] 魏 昶, 李存兄. 锌提取冶金学[M]. 北京: 冶金工业出版社, 2013.
WEI Chang, LI Cun-xiong. Zinc extraction metallurgy[M]. Beijing: Metallurgical Industry Press, 2013.
Leaching germanium-containing zinc oxide dust by atmospheric oxygen enrichment
ZHU Ying-xu1, DENG Zhi-gan1, WEI Chang1, LI Yan-lin2, ZHANG Mei2, ZHAO Wen-li1
(1. Faculty of Metallurgy and Energy Engineering, Kunming University of Science and Technology, Kunming 650093, China;
2. Yun Nan ChiHong Zn & Ge Co., Ltd., Qujing 650011, China)
Abstract: The atmospheric oxygen enrichment leaching-neutralization process was proposed to deal with the dust. The acidity was controlled to reduce leaching of Si and dissolution of oxygen, avoiding the loss of Ge by iron gel-silica gel, controlling concentration of Fe3+ to leach sulfide. The results indicate that the germanium leaching efficiency can reach 83% under the condition of temperature 90 ℃, liquid-solid ratio 7 mL/g and pH 0.3-0.7 for 4 h. The phase of acid leaching residue contains zinc sulfate, lead sulfate and silicon dioxide, the surface appears porous and loose structure. Most of Ge occurs by silicate. The leaching efficiency of Ge in silicate reaches 84.94%, the proportion reaches 59.24% in all leached germanium. The concentration of ferric and silicon in acid leaching solution are controlled to 0.4 g/L and 64.5 mg/L, respectively. The dust is used to neutralize the acid solution. The neutralization experiment and cycle experiment verify, controlling solution pH in 3.0-3.5 and react for 1.5 h, the concentration of Fe3+ can reduce within 0.025 g/L, meeting the subsequent requirements for extract germanium.
Key words: germanium; zinc oxide dust; atmospheric oxygen enrichment leaching
Foundation item: Projects(51664030, 51804146, 51964029) supported by the National Natural Science Foundation of China; Project(2018YFC1900402) supported by the National Key Research and Development Plan Solid Waste Resources Special of China
Received date: 2020-06-18; Accepted date: 2020-10-12
Corresponding author: DENG Zhi-gan; Tel: +86-15925127947; E-mail: dengzhigan83@163.com
(编辑 李艳红)
基金项目:国家自然科学基金资助项目(51664030,51804146,51964029);国家重点研发计划固废资源化专项(2018YFC1900402)
收稿日期:2020-06-18;修订日期:2020-10-12
通信作者:邓志敢,讲师,博士;电话:15925127947;E-mail:dengzhigan83@163.com