文章编号:1004-0609(2012)02-0572-07
一氧化碳还原热解硫酸镁制备高纯氧化镁
张 萍1,冯雅丽1,李浩然2,田京雷1,汪 平1,刘欣伟1
(1. 北京科技大学 土木与环境学院,北京 100083;
2. 中国科学院 过程工程研究所 生化工程国家重点实验室,北京 100190)
摘 要:利用菱镁矿和工业纯硫酸制备七水硫酸镁,进一步脱水得到无水硫酸镁。以无水硫酸镁和CO气体为原料,经高温煅烧制备高纯氧化镁,考察硫酸镁粒径、CO气体流量、煅烧温度和煅烧时间对硫酸镁转化率的影响。通过单因素实验确定的最佳工艺条件为:粒径51.8 μm,CO气体流量30 mL/min,煅烧温度800 ℃,煅烧时间 2.0 h。样品氧化镁经X射线衍射和扫描电镜表征,纯度达到99%,其平均粒径为40nm,单分子表面为多孔蓬松状。经实验和动力学推导得到描述热解过程的经验方程,CO气体还原热解硫酸镁的动力学模型为收缩核动力学模型,热解表观活化能为234.055 kJ/mol,该模型表明热解过程中的控制步骤决定于氧化还原速率。
关键词:菱镁矿;硫酸镁;CO;高纯氧化镁;收缩核模型;煅烧
中图分类号:TQ132.2 文献标志码:A
Preparation of high-purity magnesia by
carbon monoxide reduction pyrolysis of magnesium sulfate
ZHANG Ping1, FENG Ya-li1, LI Hao-ran2, TIAN Jing-lei1, WANG Ping1, LIU Xin-wei1
(1. School of Civil and Environmental Engineering, University of Science and Technology Beijing,
Beijing 100083, China;
2. State Key Laboratory of Biochemical Engineering, Institute of Process Engineering,
Chinese Academy of Sciences, Beijing 100190, China)
Abstract: The magnesium sulfate heptahydrate prepared by magnesite and commercial sulfuric acid was dehydrated to prepare anhydrous magnesium sulfate. The high-purity magnesia was obtained by commercial magnesium sulfate and carbon monoxide. The influences of the particles diameter, gas flow, calcining temperature and time on the purity of prepared magnesium oxide were investigated. The optimum processing parameters of precipitation were obtained by single factor experiments, and the conditions were as follows: the grain diameter 51.8 μm, the carbon monoxide flow 30 mL/min, the calcining heat 800 ℃, the calcining time 2.0 h. The morphology of the magnesia was characterized by X-ray diffractometry (XRD) and scanning electron microscopy (SEM). The results indicate that sample particle has high purity to 99%, the average particle diameter is 40 nm. The single molecule surface with high specific surface area is porous and fluffy. By means of experiment and kinetic deduction, an empirical equation for the calcining process was established, and the apparent activation energy is 234.055 kJ/mol. The calcining process of magnesium sulfate can be simulated with a shrinking core model, which indicates that the control factor of the calcining process is the diffusion rate of reacting reagents in the redox process.
Key words: magnesite; magnesium sulfate; CO; high-purity magnesium oxide; shrinking core model; calcining
我国高纯氧化镁(w(MgO)≥98%)的产品薄弱,急需进行开发研究[1]。据近期资料报道,中国高纯氧化镁市场需求量近100 kt,而国内产量仅10 kt左右,缺口相当大。目前,我国除利用蛇纹石为原料外,还利用沿海制盐后卤水、青海水氯镁石、东北水镁石、菱苦土等原料制取高纯氧化镁产品[2-3]。
本文作者探索利用硫酸镁还原热解制备氧化镁的方法,将菱镁矿和硫酸来制备硫酸镁,并以硫酸镁和CO气体为原料制备高纯氧化镁[4-6]。该方法克服菱镁矿不易纯化的缺点,中间产物硫酸镁易纯化,更易制得高纯的氧化镁产品。利用该工艺制得的MgO粉体没有团聚现象,反应尾气SO2采用软锰矿吸收,获得高附加值的MnSO4产品。该工艺原料可采性好、流程短、操作简单、可控性强、能耗低。
1 实验
1.1 实验试剂、仪器和装置
试剂:菱镁矿、硫酸、CO气体。
仪器:坩埚炉、石英管、天平、X射线衍射仪(日本理学公司生产,D/max-γB型:Cu靶,λ为0.154 06 nm,管电压为40 kV,管电流为100 mA,衍射速度为 4 (°)/min,扫描范围2θ为10°~70°)、扫描电子显微镜(日立H-600型)。
实验装置如图1所示。

图1 实验装置图
Fig. 1 Schematic diagram of experimental set-up: 1―CO gas bottle; 2―Gas flowmeter; 3―Temperature controller; 4―Quartz tube; 5―Potoven; 6―SO2 absorption bottle; 7―Magnetic stirring apparatus; 8―CO2 absorption bottle; 9―CO gas collecting bottle
1.2 实验方法
1) 硫酸镁制备:将菱镁矿和硫酸在一定条件下反应,经冷却过滤、结晶生成七水硫酸镁 (w(MgSO4・7H2O)>99%),反应式如下:
MgCO3+H2SO4+6H2O→MgSO4・7H2O+CO2 ↑ (1)
2) 硫酸镁脱水:称取一定量的硫酸镁放入坩埚中,置于马弗炉内加热至600 ℃脱水2 h。根据硫酸镁脱水前后质量的变化,计算脱水率[7]。
为考察MgSO4・7H2O脱水过程的规律,利用TG-DSC测量脱水过程中能量和质量的变化。在加热过程中,随温度升高,样品逐步脱去结晶水,质量逐渐减少。样品与惰性参比物之间的能量差会随温度的变化而变化。对样品进行分析得出TG-DSC曲线,图2所示为600 ℃内MgSO4・7H2O脱水过程中的TG-DSC曲线。
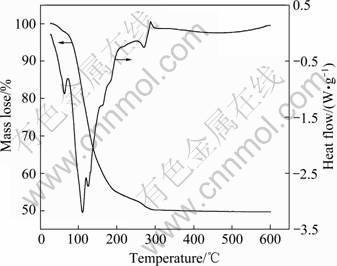
图2 七水硫酸镁加热分解过程TG-DSC曲线
Fig. 2 TG-DSC curves of magnesium sulfate heptahydrate pyrolysis process
3) CO气体与硫酸镁高温热解反应
将洁净的自制石英管置于马弗炉内烘干,并将脱水后的MgSO4放入其中,通CO气体,设定温度加热煅烧,反应式如下[8]。
主反应如下:
2MgSO4+CO→2MgO+SO2+CO2+SO3 (2)
副反应如下:
2CO+SO2→2CO2+S (3)
CO+H2O→CO2+H2 (4)
利用质量损失分析法得到不同条件下无水MgSO4分解率。这个步骤需注意样品的防潮性,防止未热解的硫酸镁吸潮影响实验结果的准确性,防潮性通过将样品放入干燥器来实现。
1.3 分析及表征
产物中MgO质量分数由日立原子吸收光谱仪进行测定。样品的晶体结构和微粒的大小、形貌,利用日本理学公司的D/max-γB型X射线衍射仪分析与日立H-600型扫描电子显微镜观察。
2 结果与讨论
2.1 粒径对硫酸镁转化率的影响
当CO气体流量为30 mL/min,煅烧温度800 ℃,煅烧时间2.0 h 时,粒径对MgSO4转化率的影响如图3所示(样品粒径均指指定粒径含量在98%以上)。由图3可知,粒径小于109 μm时,硫酸镁的热分解率随粒径的增大而增大,当粒径大于109 μm时,热分解率随粒径的增大而减小。在109 μm时,热分解率可达到最大值99%。
样品热解过程中,粒径大,颗粒比表面积小,颗粒之间相对传热面积小,传热性能差,热解过程同时受反应动力学速率与传热传质现象控制,样品分解率较小。本实验中样品粒径109~700 μm范围内,随着样品粒径减小,颗粒比表面积增大,颗粒之间相对传热面积变大,传热性能增强,传热系数变大,硫酸镁热分解率逐渐增大。当粒径小于109 μm时,样品堆积密度增大,传热性能降低,硫酸镁分解率出现下降趋势[9]。
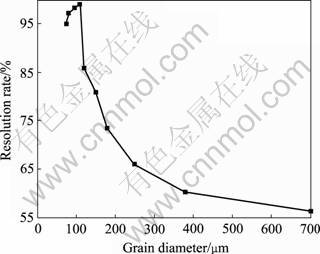
图3 粒径对硫酸镁转化率的影响
Fig. 3 Effect of grain diameter on magnesium sulfate resolution rate
2.2 CO气体流量对硫酸镁转化率的影响
当粒径为51.8 μm,煅烧温度800 ℃,煅烧时间2.0 h时,CO气体流量对MgSO4转化率的影响如图4所示。
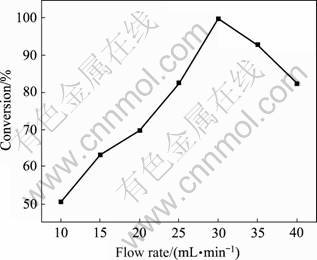
图4 CO气体流量对硫酸镁转化率的影响
Fig. 4 Effect of flow rate of CO on magnesium sulfate resolution conversion
从图4可以看出,MgSO4转化率随着CO气体流量的增加先增大后降低,在30 mL/min处达到最大值,转化率大于99%。
根据反应式(2)计算可知,当流量增大至最佳反应量30 mL/min之前,流量增大有利于该反应向右进行,达到平衡。但达到最佳反应流量后,流量增加导致冷气进入量增大,降低了反应体系的温度,导致MgSO4转化率降低。
2.3 煅烧温度对硫酸镁转化率的影响
当CO气体流量为30 mL/min,粒径51.8 μm,煅烧时间2.0 h时,煅烧温度对MgSO4转化率的影响如图5所示。
由图5可知,无水硫酸镁的分解率在600~800 ℃间,随温度的升高而增大。650 ℃时样品的分解率在6%左右,可见650 ℃是硫酸镁热分解的起始点。在600~700 ℃时,随温度的升高,分解率的增长减缓;在700~800 ℃时,分解率的增长速率提高;800 ℃时,分解率大于99%。由此确定热分解的最佳温度为800 ℃。
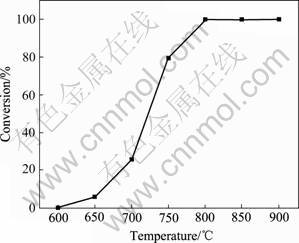
图5 煅烧温度对硫酸镁转化率的影响
Fig. 5 Effect of temperature on conversion of magnesium sulfate resolution
低于700 ℃时的热传递过程主要是热传导作用,分解速度慢。热量从样品的外部逐渐传递到内部,进而使其发生热解;温度高于700 ℃时,热辐射起主要作用,热量以射线的形式,对样品进行整体加热,使其热解[10]。
2.4 煅烧时间对硫酸镁转化率的影响
当CO气体流量为30 mL/min,粒径51.8 μm,煅烧温度800 ℃时,煅烧时间对MgSO4转化率的影响如图6所示。
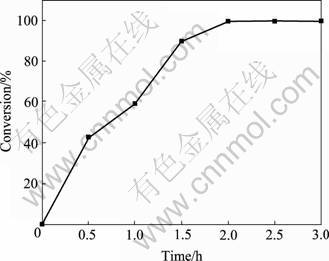
图6 煅烧时间对硫酸镁转化率的影响
Fig. 6 Effect of time on conversion of magnesium sulfate resolution
由实验可知,硫酸镁的分解率在恒定温度条件下,随着热解时间的增加,分解率逐步增高。根据焦耳定律,热量Q=I 2Rt,加热时间长,在温度相同的条件下,电流I相同,样品得到的热量Q会增大,从而样品分解率会增高。由计算和实验得出,热解时间为2.0 h时,无水硫酸镁完全热解。
2.5 样品表征
1) XRD表征
图7(b)所示为利用CO气体还原热解硫酸镁制备的MgO产品与纯MgO(JCPDS NO.4-082(a0=b0=c0= 4.213; α=β=γ=90°))XRD谱。两图基本相符,图7(b)中各个主峰尖锐,基底平滑,没有杂质峰。在 2θ= 43.04°时氧化镁的特征峰相对强度很高,说明其晶形完整[11]。
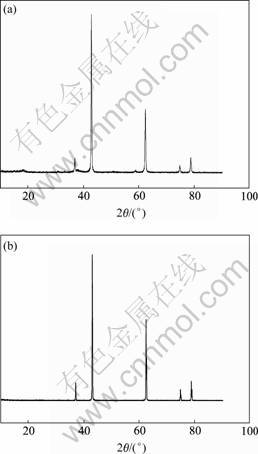
图7 化学纯氧化镁与自制氧化镁的XRD谱
Fig. 7 XRD patterns of chemical pure MgO(a) and self-made MgO(b)
2) SEM表征
图8所示为自制硫酸镁和热解产物氧化镁的SEM像。由图8可看出,自制硫酸镁大部分颗粒形状较规则,粒度小于20 μm的产品达到总产品的95.3%;产品氧化镁具细小的微晶结构,呈颗粒状,粒度分布较窄、分散性良好,其平均粒径约为40 nm与谢乐(Scherrer)公式计算的晶粒尺寸能很好的吻合。

图8 自制七水硫酸镁和自制氧化镁的SEM像
Fig. 8 SEM images of self-made MgSO4・7H2O(a) and MgO(b)
3) 纯度分析
表1所列为MgO纯度分析。由表1结果可知,氧化镁的纯度达到99.58%(大于高纯氧化镁纯度≥98%的标准),说明制得的氧化镁是高纯氧化镁。
表1 MgO纯度分析
Table 1 MgO purity analysis (mass fraction, %)

3 热解过程的动力学分析
3.1 固膜扩散过程中收缩核动力学模型
由实验观察得知,硫酸镁还原热解过程是硫酸镁外层先行分解产生氧化镁继而由外层向内层逐步扩散分解的过程,该反应遵循一般固体物质分解的动力学公式[12]:
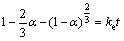 (5)
(5)
式中: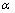 为转化率;t为反应时间;ke为扩散速度系数,
为转化率;t为反应时间;ke为扩散速度系数, 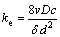 ;v为气体体积;D为扩散系数;δ为反应体系密度;d为固相颗粒直径;c为CO气体浓度。
;v为气体体积;D为扩散系数;δ为反应体系密度;d为固相颗粒直径;c为CO气体浓度。
该方程表示硫酸镁的转化率与煅烧时间的关系,又称收缩核模型[13]。将实验结果按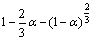 对时间t作图,其结果如图9所示。
对时间t作图,其结果如图9所示。
由图9可以看出,实验数据与“收缩核模型”基本符合,所得图形均近似直线,表明在任意温度下所得ke为常数,即ke是温度的函数。由此可以推断,硫酸镁被CO气体还原热解遵循收缩核动力学模型。
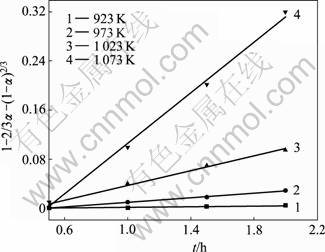
图9 不同温度下热解动力学曲线
Fig. 9 Pyrolysis dynamic curves at different temperatures
3.2 热解过程动力学分析
由图9可以求出不同温度下热解反应扩散速度系数ke,根据Arrhenius定理[14]:
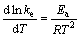 (6)
(6)
将式(6)积分便得到Arrhenius速度公式的积分形式:
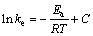 (7)
(7)
式中:Ea为表观活化能;T为热力学温度;R为摩尔气体常数;C为与温度无关的积分常数。
将不同温度时的ln ke对1/T作图,得到Arrhenius线形图,如图10所示。
由图10计算出活化能Ea=234.055 kJ/moL,该活化能较大,进一步说明该过程控制步骤是氧化还原反应,即反应速率由最慢的氧化还原反应速率决定。
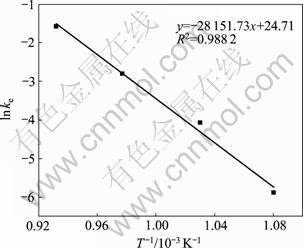
图10 ln ke―1/T 曲线
Fig. 10 ln ke―1/T curve
根据上述动力学研究,推断硫酸镁还原热解经历以下步骤,其示意图如图11所示。
1) CO气体通过围着MgSO4颗粒表面的气膜层扩散到MgSO4颗粒的外表面,即外扩散;
2) CO气体进一步通过MgSO4产物层的孔隙扩散到MgSO4-MgO之间的界面,即内扩散;
3) CO气体在MgSO4-MgO的固-固界面进行氧化还原反应,然后CO2和SO2等气体产物从反应界面上解吸;
4) 热解尾气通过MgO产物层的孔隙扩散到(内扩散) MgO产物层的外表面;
5) 热解产物气体通过MgSO4颗粒表面的气膜层扩散到尾气中。
其中,CO气体在MgSO4-MgO的固-固界面进行的氧化还原反应速率是整个反应的控制速率,即步骤
3)是决定步骤,改变这个阶段影响氧化还原速率条件,即随CO气体流量增大、煅烧温度升高、煅烧时间延长,氧化还原速率加快,将使整个反应中硫酸镁的转化率提高。
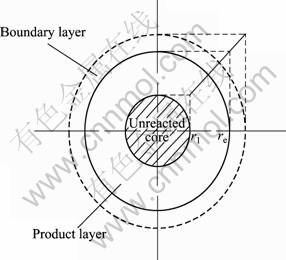
图11 颗粒的未反应收缩核模型
Fig. 11 Unreacted core shrinking model of particle
4 结论
1) 当粒径为51.8 μm,CO气体流量30 mL/min, 煅烧温度800 ℃,煅烧时间2.0 h时,硫酸镁的转化率最高且大于99%,说明CO气体能很好还原硫酸镁并生成高纯氧化镁。
2) CO气体还原热解硫酸镁的反应,符合“反应收缩核”模型: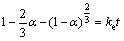 ,其表观活化能为234.055 kJ/moL,热解过程由CO气体在MgSO4- MgO的固-固界面进行的氧化还原反应控制。
,其表观活化能为234.055 kJ/moL,热解过程由CO气体在MgSO4- MgO的固-固界面进行的氧化还原反应控制。
3) 增大CO气体流量和增大粒径使硫酸镁的转化率先增大后减小;而提高煅烧温度和延长煅烧时间使硫酸镁的转化率先增大后保持不变。
REFERENCES
[1] 张京京, 冯雅丽, 李浩然. 硫酸镁直接热解制备氧化镁的研究[J]. 无机盐工业, 2010(5): 11-14.
ZHANG Jing-jing. FENG Ya-li, LI Hao-ran. Preparation of magnesia by solid phase direct decomposition of magnesium sulfate[J]. Inorganic Chemicals Industry, 2010(5): 11-14.
[2] 宋 彬, 杨保俊, 郝建文. 蛇纹石尾矿制备高纯氧化镁工艺条件的研究[J]. 合肥工业大学学报: 自然科学版, 2008, 31(1): 150-153.
SONG Bin, YANG Bao-jun, HAO Jian-wen. Preparation of high-purity magnesium oxide from serpentine[J]. Journal of Hefei University of Technology: Natural Science, 2008, 31(1): 150-153.
[3] 宋长友, 崔江丽. 高纯氧化镁的制备研究[J]. 化工矿物与加工, 2010, 12(2): 11-13.
SONG Chang-you, CUI Jiang-li. Preparation of high-purity magnesium oxide[J]. Industrial minerals& processing, 2010, 12(2): 11-13.
[4] 胡章文, 饶丹丹, 杨保俊. 高纯纳米氧化镁制备工艺研究[J]. 矿冶工程, 2006, 26(5): 69-70.
HU Zhang-wen, RAO Dan-dan, YANG Bao-jun. Preparation parameters of high-purity nanometer magnesium oxide[J]. Mining and Metallurgical Engineering, 2006, 26(5): 69-70.
[5] LI Fa-qiang, LING Bao-ping, MA Pei-hua. Manufacture of boron-free magnesia with high purity from residual brine[J]. Chinese Chemical Letters, 2004, 15(11): 1353-1356.
[6] MISHAKOW I V, BEDILO A F, RICHARDS R M. Nanocrystalline MgO as adehydrohalogenation catalyst[J]. J Catal, 2002, 206: 40-48.
[7] 胡章文, 王自友, 杨保俊. 高纯氧化镁制备工艺研究[J]. 安徽工程科技学院学报, 2004, 19(4): 18-21.
HU Zhang-wen, WANG Zi-you, YANG Bao-jun. Technological conditions for preparing high purity magnesium oxidie[J]. Journal of Anhui University of Technology and Science, 2004, 19(4): 18-21.
[8] 柴多里, 储志兵, 杨保俊. 工业硫酸镁制备高纯氧化镁的合成研究[J]. 广州化工, 2009, 37(3): 80-83.
CHAI Duo-li, CHU Zhi-bing, YANG Bao-jun. Research on preparation of high-purity MgO by commercial magnesium sulfate[J].Guangzhou Chemicals, 2009, 37(3): 80-83.
[9] 刘海刚, 王文侠. 硫酸镁热解制氧化镁工艺初探[J]. 化工矿物与加工, 2009(5): 15-17.
LIU Hai-gang, WANG Wen-xia. Primary research on production of magnesium oxide by pyrolysis of magnesium sulfate[J]. Industrial Minerals & Processing, 2009(5): 15-17.
[10] 胡庆福, 贺春宝, 卫冠亚. 镁化合物生产与应用[M]. 北京: 化学工业出版社, 2004: 71-75.
HU Qing-fu, HE Chun-bao, WEI Guan-ya. The production and applications of magnesium compound[M]. Beijing: Chemical Industry Press, 2004: 71-75.
[11] 罗森诺 W M, 哈特尼特 J P, 加尼 E N. 传热学应用手册[M]. 北京: 科学出版社, 2002: 463-470.
ROSENOER W M, HARTNETT J P, VERGANI E N. Thermodynamics application note [M]. Beijing: Science press, 2002: 463-470.
[12] 许 越. 化学反应动力学[M]. 北京: 化学工业出版社, 2005: 56-58.
XU Yue. Kinetics of chemical reaction[M]. Beijing: Chemical Industry Press, 2005: 56-58.
[13] YU Zhen-xing, WANG Er-de. Shell and shrinking core kinetics model of Mg-based hydrogen storage alloy[J]. Transactions of Nonferrous Metals Society of China, 2005, 15(2): 178-182.
[14] 刘文萍, 熊利芝, 彭治国. 超细氧化镁的直接沉淀法制备及其表征[J]. 吉首大学学报: 自然科学版, 2007, 28(2): 100-104.
LIU Wen-ping, XIONG Li-zhi, PENG Zhi-guo. Synthesis and characterization of superfine-MgO powders by direct precipitation methods[J]. Journal of Jishou University: Natural Sciences Edition, 2007, 28(2): 100-104.
(编辑 李艳红)
基金项目:国家高技术研究发展计划资助项目(2007AA05Z158);国家自然科学基金资助项目(20876160)
收稿日期:2010-07-28;修订日期:2010-12-28
通信作者:冯雅丽,教授,博士;电话:010-62311181;E-mail: ylfeng126@126.com