ЗвТұҪрАнВЫУл·Ҫ·ЁСРҫҝҪшХ№
АҙФҙЖЪҝҜЈәЦР№ъУРЙ«ҪрКфС§ұЁ2021ДкөЪ7ЖЪ
ВЫОДЧчХЯЈә№щС§Тж іВФ¶БЦ МпЗм»Ә НхЗЧГН
ОДХВТіВлЈә1891 - 1907
№ШјьҙКЈәЗвТұҪрЈ»ёЦМъТұҪрЈ»УРЙ«ҪрКфТұҪ𣻶юҙОЧКФҙАыУГЈ»ИИБҰС§Ј»¶ҜБҰС§
Key wordsЈәhydrogen metallurgy; extractive metallurgy of ferrous metals; extractive metallurgy of nonferrous metals; secondary resource utilization; thermodynamics; kinetics
ХӘ ТӘЈәТұҪрРРТөКЗОТ№ъЦШТӘөДҫӯјГЦ§іЕРРТөЈ¬ТІКЗЦчТӘөДМјЕЕ·ЕРРТөЎЈЗвТұҪрКЗөұЗ°ТұҪрБмУтөНМј·ўХ№өДЦШТӘ·ҪПтЈ¬ТСКЬөҪ№ъДЪНв№г·ә№ШЧўЎЈұҫОД¶ФЗвТұҪрјјКхФЪёЦМъТұҪрЎўУРЙ«ҪрКфТұҪрТФј°¶юҙОЧКФҙАыУГБмУтөД»щҙЎАнВЫСРҫҝЎў№ӨТХУҰУГСРҫҝҪшХ№ҪшРРБЛПөНіЧЫКцЎЈЧчОӘЖшМе»№ФӯјБЈ¬ФЪОВ¶ИҙуУЪ810 ЎжөДМхјюПВЈ¬ЗвЖш»№ФӯДЬБҰЗҝУЪТ»Сх»ҜМјЈ¬ЗТЗвЖшөД»№Фӯ·ҙУҰЛЩВКұИМј»№ФӯјБёЯ1өҪ2ёцКэБҝј¶ЎЈ»щУЪЗвТұҪрөДЦұҪУ»№ФӯБ¶МъјјКхТСҙҰУЪјјКхіЙКмЎўОИІҪ·ўХ№ҪЧ¶ОЈ¬ЖдУҰУГ°ьАЁөдРНөДMidrexЎўHYL-ўу№ӨТХЎўЕ·ЦЮөДULCOSЎўИрөдөДHYBRTЎўИХұҫөДCOURSE50ПоДҝТФј°ОТ№ъөДЦРҪъҝуТөөИЎЈЗвТұҪрФЪУРЙ«ҪрКфТұҪрТФј°¶юҙОЧКФҙАыУГБмУтөД·ўХ№ҙҰУЪ»щҙЎСРҫҝҪЧ¶ОЈ¬УРҙэҪшТ»ІҪјјКхН»ЖЖЎЈЗвЖшҙу№жДЈЎўөНіЙұҫЦЖұёТФј°ЗвТұҪр№эіМөДИИБҝЖҪәвКЗ·ўХ№ЗвТұҪрјјКхШҪҙэҪвҫцөД№ШјьОКМвЎЈ
Abstract: The metallurgy industry is a strong support for economic and a major carbon emission industry in China. Hydrogen metallurgy is regarded as a vibrant research branch in developing efficient metallurgical technologies with low-carbon emission at present. Therefore, hydrogen metallurgical technology has been concerned worldwide. In the present paper, the recent developments of theory researches and applications of hydrogen metallurgical technology in the fields of extractive metallurgy of ferrous metals and nonferrous metals, and secondary resources utilization are systematically reviewed. As a gaseous reducing agent, H2 possesses a stronger reduction capacity than CO at the temperature higher than 810 Ўж. And the reduction reaction rate of H2 is higher than that of carbon reducing agent with 1 to 2 orders of magnitude. The direct reduction iron making technology based on hydrogen metallurgy is in the stage of steady development, its application includes the typical processes Midrex and HYL-ўу, and some other new projects, such as EuropeЎҜs ULCOS, Sweden''''s HYBRT, JapanЎҜs COURSE50, and China''''s Zhongjin Mining. While the researches of hydrogen metallurgy in the fields of extractive metallurgy of nonferrous metals and secondary resource utilization are in theoretical study stage, and further technical breakthrough is in needed. The production of hydrogen with large scale and low cost and the thermal balance in hydrogen metallurgy process are the key problems to be solved in the future.
DOI: 10.11817/j.ysxb.1004.0609.2021-40038
№щС§ТжЈ¬іВФ¶БЦЈ¬МпЗм»ӘЈ¬НхЗЧГН
(ЦРДПҙуС§ ТұҪрУл»·ҫіС§ФәЈ¬іӨЙі 410083)
ХӘ ТӘЈәТұҪрРРТөКЗОТ№ъЦШТӘөДҫӯјГЦ§іЕРРТөЈ¬ТІКЗЦчТӘөДМјЕЕ·ЕРРТөЎЈЗвТұҪрКЗөұЗ°ТұҪрБмУтөНМј·ўХ№өДЦШТӘ·ҪПтЈ¬ТСКЬөҪ№ъДЪНв№г·ә№ШЧўЎЈұҫОД¶ФЗвТұҪрјјКхФЪёЦМъТұҪрЎўУРЙ«ҪрКфТұҪрТФј°¶юҙОЧКФҙАыУГБмУтөД»щҙЎАнВЫСРҫҝЎў№ӨТХУҰУГСРҫҝҪшХ№ҪшРРБЛПөНіЧЫКцЎЈЧчОӘЖшМе»№ФӯјБЈ¬ФЪОВ¶ИҙуУЪ810 ЎжөДМхјюПВЈ¬ЗвЖш»№ФӯДЬБҰЗҝУЪТ»Сх»ҜМјЈ¬ЗТЗвЖшөД»№Фӯ·ҙУҰЛЩВКұИМј»№ФӯјБёЯ1өҪ2ёцКэБҝј¶ЎЈ»щУЪЗвТұҪрөДЦұҪУ»№ФӯБ¶МъјјКхТСҙҰУЪјјКхіЙКмЎўОИІҪ·ўХ№ҪЧ¶ОЈ¬ЖдУҰУГ°ьАЁөдРНөДMidrexЎўHYL-ўу№ӨТХЎўЕ·ЦЮөДULCOSЎўИрөдөДHYBRTЎўИХұҫөДCOURSE50ПоДҝТФј°ОТ№ъөДЦРҪъҝуТөөИЎЈЗвТұҪрФЪУРЙ«ҪрКфТұҪрТФј°¶юҙОЧКФҙАыУГБмУтөД·ўХ№ҙҰУЪ»щҙЎСРҫҝҪЧ¶ОЈ¬УРҙэҪшТ»ІҪјјКхН»ЖЖЎЈЗвЖшҙу№жДЈЎўөНіЙұҫЦЖұёТФј°ЗвТұҪр№эіМөДИИБҝЖҪәвКЗ·ўХ№ЗвТұҪрјјКхШҪҙэҪвҫцөД№ШјьОКМвЎЈ
№ШјьҙКЈәЗвТұҪрЈ»ёЦМъТұҪрЈ»УРЙ«ҪрКфТұҪ𣻶юҙОЧКФҙАыУГЈ»ИИБҰС§Ј»¶ҜБҰС§
ОДХВұаәЕЈә1004-0609(2021)-07-1891-16ЎЎЎЎ ЦРНј·ЦАаәЕЈәTF19ЎЎЎЎ ОДПЧұкЦҫВлЈәA
ТэОДёсКҪЈә№щС§Тж, іВФ¶БЦ, МпЗм»Ә, өИ. ЗвТұҪрАнВЫУл·Ҫ·ЁСРҫҝҪшХ№[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2021, 31(7): 1891-1906. DOI: 10.11817/j.ysxb.1004.0609.2021-40038
GUO Xue-yi, CHEN Yuan-lin, TIAN Qing-hua, et al. Research progress on hydrogen metallurgy theory and method[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(7): 1891-1906. DOI: 10.11817/ j.ysxb.1004.0609.2021-40038
ЛжЧЕКАҪз№ӨТөөДҝмЛЩ·ўХ№Ј¬УЙМјЕЕ·ЕТэЖрөДОВКТР§УҰөИ»·ҫіОКМвИХТжН»іцЎЈТұҪрРРТөЧчОӘОТ№ъЦШТӘөДҫӯјГ·ўХ№Ц§іЕРРТөЈ¬Н¬КұЈ¬ТІКЗЦчТӘөДМјЕЕ·ЕРРТөЈ¬ОТ№ъёЦМъТұҪрДкМјЕЕ·ЕБҝі¬№э2.2ЎБ109 t CO2[1]ЎўУРЙ«ҪрКфТұҪрДкМјЕЕ·ЕТІёЯҙп3.0ЎБ109 t CO2[2]ЎЈФЪөұЗ°·ўХ№өНМјҫӯјГөДЖИЗРРОКЖПВЈ¬ШҪРиҝӘ·ўЗеҪаТұҪрјјКхЈ¬ұЈХПТұҪрРРТөөДҝЙіЦРш·ўХ№ЎЈЗвТұҪрЧчОӘВМЙ«ТұҪрРВјјКхЈ¬КЗөұЗ°ТұҪрБмУтөНМј·ўХ№өДЦШТӘ·ҪПтЈ¬ТСКЬөҪ№ъДЪНвҝЖСР№ӨЧчХЯ№г·ә№ШЧўЎЈ
1995ДкЈ¬EDELSON[3]МбіцБЛІЙУГH2ИЫИЪ»№ФӯБ¶МъөД№ӨТХЈ¬ІўЙкЗлБЛГА№ъЧЁАыЎЈОТ№ъРмҝпөПФәКҝФЪ1999Дкұұҫ©өЪ125ҙОПгЙҪҝЖС§»бТйөИС§Кх»бТйЙП¶аҙОМбіц·ўХ№H2ТұҪрөДі«ТйЈ¬ІўИПОӘҝЙНЁ№эПт·ҙУҰМеПөК©јУОпАніЎөД·Ҫ·ЁАҙКөПЦH2ТұҪр№эіМЗҝ»Ҝ[4]ЎЈЦЈЙЩІЁ[5]әНGERMESHUIZENөИ[6]¶ФУҰУГH2өДёЦМъТұҪрБчіМҪшРРБЛјјКхЎўҫӯјГЖАјЫЈ¬ИПОӘІЙУГ»щУЪәЛДЬөДH2МжҙъМјЧчОӘБ¶Мъ»№ФӯјБЈ¬ЙъІъіЙұҫМбёЯФј12.8%Ј¬ө«КЗЈ¬CO2ЕЕ·ЕБҝҝЙҪөөН63%ЎЈVOGLөИ[7]ИПОӘЈ¬H2ЦұҪУ»№ФӯБ¶МъөДДЬБҝПыәДУлҙ«НіёЯВҜБ¶МъПаөұЈ¬ФЪөзБҰіЙұҫөНәНМјЕЕ·ЕТӘЗуСПёсөДЗйҝцПВЈ¬H2ЦұҪУ»№ФӯБ¶Мъ№ӨТХФтҫЯУР№гА«З°ҫ°ЎЈ
21КАјНКЗЗвКұҙъЈ¬ЗвТұҪрТФЗвҙъМжМј»№ФӯЈ¬І»ө«МјЕЕ·ЕөНЈ¬¶шЗТ·ҙУҰЛЩ¶Иј«ҝм[8-9]ЎЈДҝЗ°Ј¬№ъДЪНвТұҪрБмУтҫщМбіцБЛЗвТұҪрөДХҪВФ№ж»®Ј¬°ьАЁЕ·ЦЮөДULCOSЎўИрөдөДHYBRTЎўИХұҫөДCOURSE50ПоДҝТФј°ОТ№ъөДЦРҪъҝуТөөИ[9]ЎЈTANGөИ[9]ЧЫКцБЛЗвТұҪрФЪ№ъДЪНвёЦМъТұҪрБмУтөДСР·ўҪшХ№Ј¬ІўМбіцБЛККәПОТ№ъөДЗвТұҪрВ·ПЯЎЈЛжЧЕЦЖЗвјјКхөД·ўХ№Ј¬ЗвТұҪрҪ«іЙОӘОҙАҙТұҪрРРТөРВөДҫәХщБмУт[10-11]ЎЈұҫОДҪ«¶ФЗвТұҪрјјКхФЪёЦМъТұҪрЎўУРЙ«ҪрКфТұҪрј°¶юҙОЧКФҙАыУГБмУтөД»щҙЎАнВЫСРҫҝЎў№ӨТХУҰУГСРҫҝҪшХ№ҪшРРПөНіЧЫКцЈ¬Іў¶ФЗвТұҪрјјКхОҙАҙ·ўХ№З°ҫ°ј°ШҪҙэҪвҫцөД№ШјьОКМвҪшРР·ЦОцЈ¬ОӘЗвТұҪрБмУтөДСРҫҝМṩІОҝјЎЈ
1 ёЦМъТұҪрБмУтЗвТұҪрСРҫҝҪшХ№
ҙ«НіёЯВҜБ¶Мъ№ӨТХЗҝБТТААөТұҪрҪ№Ј¬ДЬәДёЯЎўОЫИҫЦШЈ¬ОӘБЛ°ЪНСёЯВҜ№ӨТХөД№МУРИұөгЈ¬ҝӘ·ўЗеҪаөДёЦМъТұҪр№ӨТХЈ¬»щУЪЗвТұҪрөДБ¶МъјјКхУҰФЛ¶шЙъЎЈ·ўХ№ЗвТұҪрКЗБ¶МъјјКхөДТ»іЎёпГьЈ¬Ҫ«УРР§НЖ¶ҜёЦМъ№ӨТөөДҝЙіЦРш·ўХ№[12]ЎЈДҝЗ°Ј¬ёЦМъТұҪрБмУтөДЗвТұҪрСРҫҝЦчТӘ°ьАЁЖш»щЦұҪУ»№ФӯәНИЫИЪ»№Фӯ(јыұн1) [13-14]ЎЈ
1.1 H2»№ФӯМъСх»ҜОпөД»щҙЎСРҫҝ
ІЙУГҙҝH2ҙъМжМјЧчОӘБ¶Мъ»№ФӯјБКұЈ¬ІъОпОӘH2OЈ¬ұЬГвБЛМј»№ФӯІъЙъөДCO2Ј¬АнВЫЙПҝЙКөПЦОВКТЖшМеөДБгЕЕ·ЕЈ¬ОӘёЦМъТұҪрөДВМЙ«·ўХ№МṩБЛҝЙДЬЎЈТтҙЛЈ¬№ъДЪНв¶ФH2»№ФӯМъСх»ҜОпөДРРОӘј°»ъАнҪшРРБЛҙуБҝСРҫҝЎЈ
1.1.1 ИИБҰС§СРҫҝ
ДҝЗ°Ј¬Жш»щ»№ФӯБ¶МъЦчТӘІЙУГH2ЎўCO»мәПЖшМеЧчОӘ»№ФӯЖшЈ¬H2ЎўCO»№ФӯМъСх»ҜОпКұЈ¬ИИБҰС§ЖҪәвНјИзНј1ЛщКҫ[15-16]Ј¬»№Фӯ№эіМ·ЦОӘFe3O4ОИ¶ЁЗшЎўFeOОИ¶ЁЗшәНҪрКфМъОИ¶ЁЗшЎЈ·ҙУҰОВ¶ИРЎУЪ570 ЎжКұЈ¬МъСх»ҜОпөД»№ФӯАъіМОӘFe2O3ЎъFe3O4Ўъ FeЈ»·ҙУҰОВ¶ИҙуУЪ570 ЎжКұЈ¬МъСх»ҜОпөД»№ФӯАъіМФтОӘFe2O3ЎъFe3O4ЎъFeOЎъFeЎЈ
ұн1 ЗвЖшТұҪрФЪБ¶Мъ№ӨТХЦРөДУҰУГПЦЧҙ[13-14]
Table 1 Application status of hydrogen metallurgy in iron-making[13-14]

Нј1 H2ЎўCO»№ФӯМъСх»ҜОпЖҪәвНј[15-16]
Fig. 1 Equilibrium diagram of iron oxides reduced by H2, CO[15-16]
ФЪ·ҙУҰОВ¶ИРЎУЪ810 ЎжКұЈ¬CO»№ФӯЖҪәвЗъПЯО»УЪH2»№ФӯЖҪәвЗъПЯПВ·ҪЈ¬ПаН¬ОВ¶ИМхјюПВЈ¬»№ФӯМъСх»ҜОпЙъіЙҪрКфМъЛщРиCOЖҪәв·ЦС№РЎУЪH2Ј¬ұнГчҙЛОВ¶И·¶О§ДЪCO»№ФӯДЬБҰЗҝУЪH2Ј»¶ш·ҙУҰОВ¶ИҙуУЪ810 ЎжКұЈ¬ФтH2»№ФӯДЬБҰЗҝУЪCOЎЈУЙУЪКөјК·ҙУҰОВ¶ИТ»°гҙуУЪ810 ЎжЈ¬ТтҙЛЈ¬ІЙУГё»Зв»тҙҝЗв»№ФӯЖшМеҪшРРМъҝу»№ФӯФЪИИБҰС§ЙПҫЯУРТ»¶ЁөДУЕКЖЎЈ
1.1.2 ¶ҜБҰС§СРҫҝ
H2¶Ф№ММ¬МъСх»ҜОпөД»№Фӯ№эіМЈ¬ЦчТӘ°ьАЁТФПВ»·ҪЪ[17]Јә
ўЩ H2ҙУЖшБчІгПт№М-ЖшҪзГжА©ЙўІўұ»ҪзГжОьёҪЈ»
ўЪ ·ўЙъҪзГж»№Фӯ·ҙУҰЈ¬ЙъіЙЖшМеH2OәНПаУҰөД№ММеІъОпЈ»
ўЫ ЖшМеH2OҙУ·ҙУҰҪзГжНСёҪЈ»
ўЬ ЛжЧЕ·ҙУҰөДҪшРРЈ¬№ММеІъОпіЙәЛЎўЙъіӨЈ¬ІўРОіЙІъОпІгЈ¬H2OРиТӘҙ©№э№ММеІъОпІгҙУ·ҙУҰҪзГжПтЖшБчІгА©ЙўЈ¬»№Фӯ·ҙУҰЛЩВКИЎҫцУЪЛЩВКЧоөНөД»·ҪЪЎЈ
H2»№ФӯИЫИЪМъСх»ҜОпОӘЖш-Тә·ҙУҰ№эіМЈ¬ХыМе·ҙУҰЛЩВКФтЦчТӘУЙИэёц»·ҪЪҝШЦЖ[18]Јә
ўЩ ЖшПаЦРөДЦКБҝҙ«өЭЛЩВКЈ»
ўЪ Жш-ТәҪзГж·ҙУҰЛЩВКЈ»
ўЫ ТәПаЦРөДЦКБҝҙ«өЭЛЩВКЎЈ
ҪьДкАҙЈ¬Т»Р©№ШУЪH2»№ФӯМъСх»ҜОпөД¶ҜБҰС§СРҫҝҪб№ыИзұн2ЛщКҫЎЈ
1) H2»№ФӯМъСх»ҜОпөДУ°ПмТтЛШ
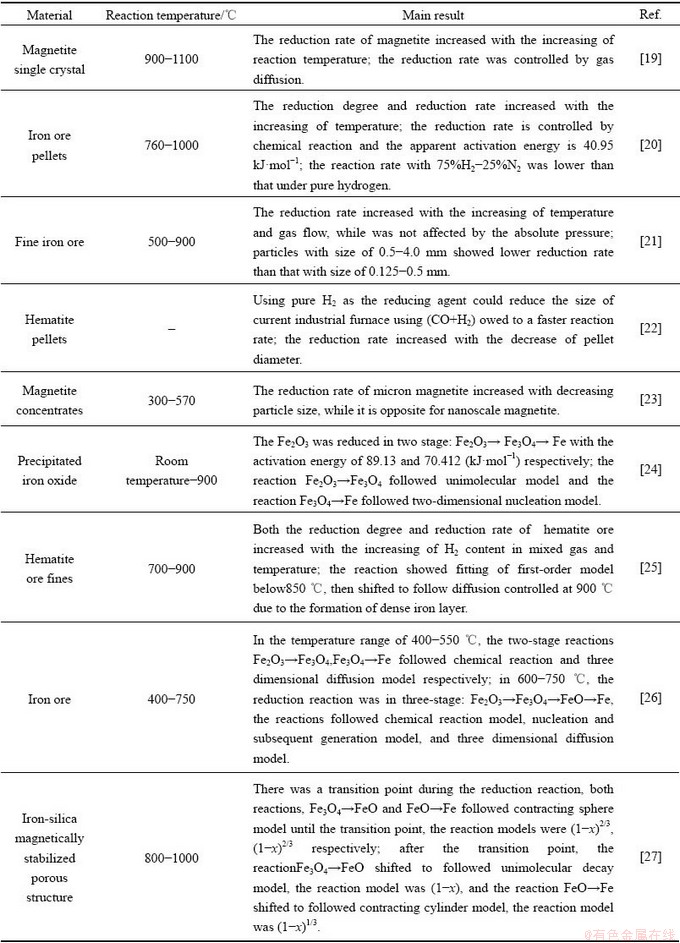
H2¶Ф№ММ¬МъҝуОпөД»№Фӯ·ҙУҰЛЩВККЬ¶а·ҪГжМхјюУ°ПмЈ¬ФЪ¶ҜБҰС§ЙПЈ¬МбёЯОВ¶ИУРАыУЪјУҝмH2А©Йўј°ҪзГж·ҙУҰЛЩВКЈ»ИИБҰС§ЙПЈ¬МъСх»ҜОп»№ФӯөДЧЬМе·ҙУҰ(Fe2O3+3H2(g)=2Fe+3H2O(g)Ј¬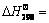 95.8 kJ/mol)КЗОьИИР§УҰЈ¬МбёЯОВ¶ИЈ¬ҝЙФцЗҝ·ҙУҰЗчКЖЎЈТтҙЛЈ¬Т»¶Ё·¶О§ДЪМбёЯОВ¶ИЈ¬УРАыУЪH2»№ФӯМъСх»ҜОпЈ¬ХвУлОДПЧСРҫҝҪб№ыТ»ЦВ[19-21]ЎЈ
95.8 kJ/mol)КЗОьИИР§УҰЈ¬МбёЯОВ¶ИЈ¬ҝЙФцЗҝ·ҙУҰЗчКЖЎЈТтҙЛЈ¬Т»¶Ё·¶О§ДЪМбёЯОВ¶ИЈ¬УРАыУЪH2»№ФӯМъСх»ҜОпЈ¬ХвУлОДПЧСРҫҝҪб№ыТ»ЦВ[19-21]ЎЈ
І»Н¬ҝуОпБЈ¶ИөјЦВ·ҙУҰ№эіМЛЩВКҝШЦЖ»·ҪЪөДІоТмЈ¬ТІУ°ПмH2¶ФМъҝуОпөД»№Фӯ·ҙУҰЛЩВКЎЈHABERMANNөИ[21]МбіцЈ¬ЛжЧЕіаМъҝуБЈ¶ИФцҙуЈ¬H2»№Фӯ·ҙУҰЛЩВКҪөөНЈ¬ЧоЦХ»№ФӯВКФт»щұҫІ»ұдЎЈCOSTAөИ[22]¶ФКъВҜДЪH2ЦұҪУ»№ФӯМъҝуЗтНЕҪшРРБЛДЈДв·ЦОцЈ¬ТІИПОӘФЪЧоУЕ·ҙУҰОВ¶И800 ЎжМхјюПВЈ¬ЗтНЕБЈҫ¶ФҪРЎ»№Фӯ·ҙУҰЛЩВКФҪҝмЎЈTEPLOV[23]ФтИПОӘЈ¬¶ФУЪОўГЧј¶ҙЕМъҝ󣬻№ФӯЛЩВКЛжБЈ¶ИјхРЎПФЦшМбёЯЈ¬¶шДЙГЧј¶ҙЕМъҝу»№ФӯЛЩВКФтЛжБЈ¶ИјхРЎПФЦшҪөөНЎЈҙЛНвЈ¬ЖшМеС№БҰЎўМъСх»ҜОпҝЧП¶ВКөИТтЛШ¶ФH2»№Фӯ·ҙУҰТІУРУ°Пм[17]ЎЈ
2) H2»№ФӯМъСх»ҜОпөД¶ҜБҰС§»ъЦЖ
¶ФУЪH2»№ФӯМъСх»ҜОпөД·ҙУҰ¶ҜБҰС§»ъЦЖЈ¬№ъДЪНвСРҫҝХЯМбіцБЛІ»Н¬өДКэС§ДЈРНЎЈSPREITZERөИ[17]ИПОӘЈ¬H2¶Ф№ММ¬МъСх»ҜОпөД»№Фӯ№эіМ·ыәПОҙ·ҙУҰәЛДЈРНЈ¬·ҙУҰЛЩВКЦчТӘУЙНвА©ЙўЎўДЪА©ЙўЎў»ҜС§·ҙУҰҝШЦЖЎЈУЙУЪМъСх»ҜОпөД»№ФӯКЗ·ЦІҪҪшРРЈ¬ЗТІ»Н¬ОВ¶И·¶О§ДЪ·ҙУҰАъіМІ»Н¬Ј¬ТтҙЛЈ¬І»Н¬ОВ¶ИМхјюПВH2»№ФӯМъСх»ҜОпөД¶ҜБҰС§»ъЦЖҙжФЪІоТм[24-27]ЎЈИзіВвЩ[26]МбіцЈ¬H2»№ФӯМъСх»ҜОпЈ¬ФЪ400~550 Ўж·¶О§ДЪЈ¬өЪТ»ҪЧ¶О·ўЙъ»№Фӯ·ҙУҰFe2O3Ўъ Fe3O4Ј¬·ыәП»ҜС§·ҙУҰДЈРНЈ¬өЪ¶юҪЧ¶О·ўЙъ»№Фӯ·ҙУҰFe3O4ЎъFeЈ¬·ыәПИэО¬А©ЙўДЈРНЈ»ФЪ600~750 Ўж·¶О§ДЪЈ¬өЪТ»ҪЧ¶О·ўЙъ»№Фӯ·ҙУҰFe2O3ЎъFe3O4Ј¬·ыәП»ҜС§·ҙУҰДЈРНЈ¬өЪ¶юҪЧ¶ОФт·ўЙъ»№Фӯ·ҙУҰFe3O4Ўъ FeOЈ¬·ыәПЛж»ъіЙәЛәНЛжәуЙъіӨДЈРНЈ¬өЪИэҪЧ¶О·ўЙъ»№Фӯ·ҙУҰFeOЎъFeЈ¬·ыәПИэО¬А©ЙўДЈРНЎЈ
ФЪҙу¶аКэМхјюПВЈ¬H2¶ФМъСх»ҜОпөДИЫИЪ»№Фӯ·ҙУҰЛЩВКФт·ЗіЈҝмЈ¬·ҙУҰЛЩВКЦчТӘКЬЖшМеІгЦРөДҙ«ЦКЛЩВКҝШЦЖ[28]ЎЈNAGASAKAөИ[18]МбіцЈ¬ФЪ1673 KМхјюПВЈ¬H2¶ФҙҝМъСх»ҜОпИЫМеөД»№Фӯ·ҙУҰКЗ№ШУЪH2·ЦС№өДТ»ј¶·ҙУҰЈ¬ЖдЛЩВКәҜКэҝЙұнКҫОӘЈә
r=ka[H2]ЎӨ(p(H2)-p(H2O)/KH)
КҪЦРЈәЛЩВКіЈКэka[H2]= 1.6ЎБ10-6Ј»KHОӘЖшМеЦРH2OУлH2өД·ЦС№ұИp(H2O)/p(H2)ЎЈ
І»Н¬ФьПөЦРЈ¬H2¶ФИЫИЪМъСх»ҜОпөД»№Фӯ·ҙУҰЛЩВКТІҙжФЪІоТмЈ¬ФЪТ»¶Ё·¶О§ДЪЛжЧЕФьЦРCaOә¬БҝФцјУЈ¬·ҙУҰЛЩВКМбёЯЈ¬¶шSiO2ә¬БҝФцјУЈ¬·ҙУҰЛЩВКФтҪөөН[18]ЎЈ
І»Н¬СРҫҝХЯ¶ФУЪH2»№ФӯМъСх»ҜОп¶ҜБҰС§»ъЦЖөДСРҫҝҪб№ыҙжФЪТ»¶ЁІоТмЈ¬ЦчТӘФӯТтКЗІЙУГөД·ҙУҰМхјю(ИзОВ¶И)ТФј°МъҝуФӯБПіЙ·ЦЎўРОМ¬ҙжФЪІоТмЎЈXUөИ[29]әНWANGөИ[30]НЁ№эКөСйЦӨГчБЛҝуОпЦЦАа(әЦМъҝуЎўіаМъҝуЎўцЬЧҙіаМъҝу)ЎўМъҝуіЙ·Ц¶ФМъҝуЦРМъСх»ҜОпөД»№ФӯЛЩВКУРПФЦшУ°ПмЎЈ
1.1.3 H2ЧчОӘЖш»щ»№ФӯјБөДУЕКЖ
ИИБҰС§СРҫҝұнГчЈ¬ФЪ·ҙУҰОВ¶ИҙуУЪ810 ЎжКұЈ¬H2¶ФМъСх»ҜОпөД»№ФӯДЬБҰЗҝУЪCOЎЈҙУ¶ҜБҰС§ҪЗ¶ИҝҙЈ¬ФЪПаН¬ОВ¶ИМхјюПВЈ¬H2-H2OөД»ҘА©ЙўПөКэ(1000 KКұ7.330 cm2/s)ҙуУЪCO-CO2өД»ҘА©ЙўПөКэ(1000 KКұ1.342 cm2/s)Ј¬ТтҙЛЈ¬H2ұИCOёьИЭТЧПтМъҝуҝЕБЈ»тЗтНЕДЪІҝА©ЙўЈ¬¶Ф№ММ¬МъСх»ҜОпөД»№ФӯЛЩВКТІёьҝм[31]ЎЈ
ұн2 №ШУЪH2»№ФӯМъСх»ҜОпөД¶ҜБҰС§СРҫҝҪб№ы[19-27]
Table 2 Results of kinetic study on reducing of iron oxides by hydrogen[19-27]
TATEOөИ[32]әНHIDEKIөИ[33]ІЙУГCO-H2»мәП»№ФӯЖшМе»№ФӯМъСх»ҜОпұнГчЈ¬ФЪОВ¶ИОӘ1093 KМхјюПВЈ¬ЛжЧЕГәЖшЦРH2ә¬БҝөДФцјУЈ¬»№Фӯ·ҙУҰұн№ЫЛЩВКіЈКэҫщПФЦшФцҙуЈ¬ІЙУГCOЎўH2-CO»мәПЖш(Ме»эұИ1:1)ј°H2ОӘ»№ФӯјБКұөДұн№ЫЛЩВКіЈКэ·ЦұрОӘ8.6Ўў15.0әН33.0 mol/(sЎӨm3ЎӨatm)ЎЈZUOөИ[34]ТІЦӨГчБЛЈ¬ІЙУГCO-H2»мәПЖшМе»№ФӯМъСх»ҜҝуЗтНЕКұЈ¬МбёЯ»№ФӯЖшМеЦРH2ә¬БҝЈ¬ҝЙПФЦшМбёЯЖшМеөДУРР§А©ЙўПөКэәН·ҙУҰЛЩВКіЈКэЎЈ
ФЪИЫИЪЧҙМ¬Ј¬H2»№ФӯМъСх»ҜОпөД·ҙУҰЛЩВКіЈКэТІұИ№ММ¬CЎўИЫҪвМ¬[C]әНCOҫщёЯ1өҪ2ёцКэБҝј¶Ј¬ТтҙЛЈ¬H2КЗёЯР§өДБ¶Мъ»№ФӯјБ[18]ЎЈ
1.2 ё»ЗвЖш»щЦұҪУ»№ФӯБ¶МъјјКхСРҫҝ
Жш»щЦұҪУ»№ФӯКЗФЪөНУЪМъҝуКҜИЫөгөДОВ¶ИПВЈ¬ІЙУГ»№ФӯЖшМеҪ«МъСх»ҜОп»№ФӯіЙёЯЖ·О»ҪрКфМъөД·Ҫ·ЁЈ¬УЙУЪЦұҪУ»№ФӯМъНССх№эіМЦРРОіЙРн¶аОўҝЧЈ¬ФЪПФОўҫөПВ№ЫҝҙЧҙЛЖәЈГаЈ¬УЦіЖОӘәЈГаМъЎЈДҝЗ°Ј¬Жш»щЦұҪУ»№ФӯБ¶МъТСРОіЙ№ӨТө»ҜУҰУГЈ¬№жДЈЧоҙуөДMidrex№ӨТХДкІъәЈГаМъҙпөҪ4500НтtЈ¬ІЙУГөД»№ФӯЖшМеОӘә¬H2әНCOөДё»Зв»мәПЖшМеЈ¬ТтҙЛЈ¬Жш»щЦұҪУ»№ФӯКЗТ»ЦЦ»щУЪЗвТұҪрөДБ¶МъјјКхЎЈё»ЗвЖш»щЦұҪУ»№ФӯБчіМЙъІъөДәЈГаМъФјХјКАҪзәЈГаМъЧЬІъБҝ75%Ј¬ЦчТӘ°ьАЁКъВҜ№ӨТХЎўБч»ҜҙІ№ӨТХөИЈ¬ЖдЦРЈ¬»щУЪКъВҜ·ЁөДMidrex№ӨТХЎўHYL-ўу№ӨТХКЗЧоіЙ№ҰөДБҪЦЦё»ЗвЖш»щЦұҪУ»№Фӯ№ӨТХ[35]ЎЈ
1.2.1 Жш»щКъВҜ·Ё
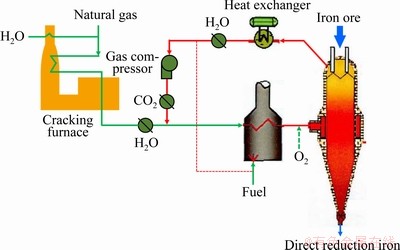
1) Midrex№ӨТХЈ¬УЙMidrex№«ЛҫҝӘ·ўіЙ№ҰЈ¬БчіМИзНј2ЛщКҫ[36]ЎЈҪ«МъҝуСх»ҜЗтНЕ»тҝйҝуФӯБПҙУВҜ¶ҘјУИлЈ¬ҙУКъВҜЦРІҝНЁИлё»ЗвИИ»№ФӯЖшЈ¬ВҜБПУлИИ·зөДДжПтФЛ¶ҜЦРұ»ИИ»№ФӯЖшјУИИ»№ФӯіЙәЈГаМъЎЈё»Зв»№ФӯЖшУЙМмИ»ЖшҫӯҙЯ»ҜБС»ҜЦЖИЎЈ¬БС»ҜјБОӘВҜ¶ҘГәЖшЎЈВҜ¶ҘГәЖшҫӯПҙөУәуІҝ·ЦУлТ»¶ЁұИАэМмИ»Жш»мәПҫӯҙЯ»ҜБС»Ҝ·ҙУҰЧӘ»ҜіЙ»№ФӯЖшЈ¬КЈУаІҝ·ЦФтУлМмИ»Жш»мәПУГЧчИИДЬ№©УҰЈ¬ҙЯ»ҜБС»Ҝ·ҙУҰЦчТӘ°ь АЁ[35, 37-39]Јә
CH4+CO2Ўъ2CO+2H2 (1)
CH4+H2OЎъCO+3H2 (2)
ІъЙъөДё»Зв»№ФӯЖшЦРЈ¬V(H2)/V(CO)ЎЦ1.5Ј¬ОВ¶ИОӘ850~900 Ўж[35, 37-39]ЎЈMidrex№ӨТХ»№ФӯЖшЦРH2ә¬БҝҪПөНЈ¬КъВҜЦР»№ФӯЖшәНМъҝуКҜөД·ҙУҰұнПЦОӘ·ЕИИР§УҰ[40]ЎЈ

Нј2 Midrex№ӨТХБчіМКҫТвНј[36]
Fig. 2 Process diagram of Midrex[36]
Midrex№ӨТХҝЙ»сөГЧоУЕМъҪрКф»ҜВКҙп100%Ј¬ө«ІъБҝҙу·щҪөөНЈ¬МъҪрКф»ҜВКФјОӘ96%КұКЗЧоУЕЙъІъМхјюЈ¬ФцјУ»№ФӯЖшМеөДCOұИАэҝЙТФМбёЯІъБҝ[41]ЎЈ¶ФMidrex№ӨТХКъВҜөДДЈДвСРҫҝұнГчЈ¬ФЪКъВҜ7.0 mЙо¶ИТФПВЈ¬ЛжЧЕ»№ФӯЖшЙПРРЈ¬H2Ме»э·ЦКэСёЛЩјхЙЩЈ¬¶шCOМе»э·ЦКэұд»ҜәЬРЎЈ¬ЦұЦБ2.0 mЙо¶ИТФЙПCOөДМе»э·ЦКэІЕПФЦшҪөөНЈ¬МъҝуФӯБПФЪВҜДЪФЛРРФј2.0 mјҙҝЙНкИ«ұдіЙёЎКПМеСх»ҜСЗМъ[42]ЎЈGHADIөИ[43]ФтМбіцЈәіаМъҝуФЪMidrexКъВҜ»№ФӯЗшЙПІҝНкИ«ЧӘұдОӘҙЕМъҝуЈ¬ФЛРРөҪЦРІҝКұұ»»№ФӯОӘ·ҪМъҝуЈ¬ФЪВҜөЧІҝКұ·ҪМъҝуІЕұ»»№ФӯОӘәЈГаМъЈ»ІЙУГЛ«ЖшМеЕзЧмЈ¬ҝЙМбёЯМъҝу»№ФӯВКЈ¬ГҝЙъІъ1 tәЈГаМъҝЙјхЙЩH2УГБҝ100 m3ЎЈ
2) HYL-ўу№ӨТХЈ¬УЙД«ОчёзHylsa№«ЛҫҝӘ·ўЈ¬№ӨТХБчіМИзНј3ЛщКҫ[36]ЎЈHYL-ўу№ӨТХК№УГЗтНЕҝу»тМмИ»ҝйҝуОӘФӯБПЈ¬ФӯБПФЪФӨИИ¶ОДЪУлЙПЙэөДё»Зв»№ФӯЖшЧчУГЈ¬СёЛЩЙэОВНкіЙФӨИИЈ¬ЛжЧЕОВ¶ИөДЙэёЯЈ¬ҝуКҜөД»№Фӯ·ҙУҰЦрҪҘјУЛЩЈ¬РОіЙәЈГаМъЎЈё»Зв»№ФӯЖшІЙУГМмИ»ЖшОӘФӯБПЈ¬Л®ХфЖыОӘБС»ҜјБЈ¬ҫӯҙЯ»ҜБС»Ҝ·ҙУҰЦЖИЎ[35, 37-39]Јә
CH4+H2OЎъCO+3H2 (3)
ё»Зв»№ФӯЖшЦРV(H2)/V(CO)=5~6Ј¬ОВ¶ИёЯҙп 930 Ўж[35, 37-39]ЎЈёГ№ӨТХ»№ФӯЖшЦРH2ә¬БҝҪПMidrex№ӨТХёЯЈ¬КъВҜЦР»№Фӯ·ҙУҰФтұнПЦОӘОьИИР§УҰЈ¬ТтҙЛ¶ФИлВҜ»№ФӯЖшОВ¶ИТӘЗуҪПёЯ[40]ЎЈ
¶шәуЈ¬Hylsa№«ЛҫУЦ»щУЪHYL-ўу№ӨТХҝӘ·ўБЛHYL-ZR№ӨТХЈ¬ёГ№ӨТХҝЙТФЦұҪУК№УГҪ№ВҜГәЖшЎўГәЦЖЖшөИё»ЗвЖшМеЈ¬ОӘё»ГәИұЖшөДөШЗш·ўХ№Жш»щЦұҪУ»№Фӯ№ӨТХҝӘұЩБЛРВВ·ҫ¶ЎЈ
УлMidrex№ӨТХПаұИЈ¬ІЙУГV(H2)/V(CO)=1өДГәЦЖЖшЙъІъ1 tәЈГаМъІъЖ·Ј¬»№ФӯЖшПыәДБҝФцјУФј100 m3Ј¬¶шДЬБҝАыУГВКМбёЯФј3.3%[35]ЎЈЦЬУеЙъөИ[44]ИПОӘЈ¬ЦР№ъөДДЬФҙҪб№№ККәП·ўХ№ТФГәЖшОӘЖшФҙөДЖш»щЦұҪУ»№ФӯБ¶Мъ№ӨТХЈ¬ІўМбіцБЛПЦУРГәЖш»ҜЙиұёУлHYLКъВҜҪбәПөД№ӨТХ·Ҫ°ёЎЈНхХЧІЕ[37]¶ФГәЦЖЖш-HYLЦұҪУ»№Фӯ№ӨТХҪшРРБЛПөНіСРҫҝЈ¬Ҫб№ыұнГчЈәІЙУГH2ә¬Бҝ30%~75%өДГәЦЖәПіЙЖшЈ¬»№Фӯ·ҙУҰ2 hДЪЈ¬МъҝуЗтНЕҪрКф»ҜВКҫщҝЙҙп95%ЧуУТЈ»»№ФӯЖшЦРH2ә¬БҝФцјУУРАыУЪ»№Фӯ·ҙУҰөДҪшРРЈ¬ө«H2ә¬БҝҙпөҪ50%әуЈ¬H2¶Ф»№Фӯ·ҙУҰөДФцЗҝЧчУГЦрҪҘјхИхЎЈ
Нј3 HYL-ўу№ӨТХБчіМКҫТвНј[36]
Fig. 3 The process diagram of HYL-ўу[36]
1.2.2 Жш»щБч»ҜҙІ·Ё
»щУЪБч»ҜҙІ·ЁөДЦұҪУ»№ФӯБ¶Мъ№ӨТХЦчТӘУРFinmetәНCircored№ӨТХЈ¬Finmet№ӨТХУЙОҜДЪИрАӯOrinoco Iron№«ЛҫәН°ВөШАыSiemens VAI Metals Technologies№«ЛҫБӘәПҝӘ·ўІўФЛУӘ[14]ЎЈCircored№ӨТХУЙOutotec№«ЛҫҝӘ·ўЈ¬ІЙУГМмИ»ЖшЦШХыІъЙъөДH2ЧчОӘ»№ФӯЖшМе[14]ЎЈПаУЪКъВҜ·ЁЈ¬»щУЪБч»ҜҙІ·ЁөДЦұҪУ»№ФӯМъЙъІъ№жДЈҪПРЎЎЈБч»ҜҙІ·ЁҝЙЦұҪУІЙУГМъҝу·ЫФӯБПЈ¬ФЪёЯОВ»№ФӯЖшБчЦРҪшРР»№ФӯЈ¬·ҙУҰЛЩ¶ИҝмЈ¬АнВЫЙПКЗЖш»щ·ЁЦРЧоәПАнөД№ӨТХ·Ҫ·ЁЎЈө«ЙъІъКөјщЦРЈ¬К№ОпБПҙҰУЪБч»ҜМ¬ЛщРиөДЖшМеБчБҝФ¶ҙуУЪАнВЫ»№ФӯЛщРиөДЖшБҝЈ¬ФміЙ»№ФӯЖшАыУГВКј«өНЈ¬ЖшМеСӯ»·ДЬәДёЯЈ»ЖдҙОЈ¬Ў°К§БчЎұөИЙъІъОКМвДСТФҪвҫцЈ¬Чи°ӯБЛБч»ҜҙІ·ЁөДҪшТ»ІҪ·ўХ№[35]ЎЈ
1.2.3 ё»ЗвЖш»щЦұҪУ»№ФӯБ¶МъјјКхРВ·ўХ№
2004ДкЈ¬АҙЧФЕ·ЦЮ15ёц№ъјТөД48ёцЖуТөЎўЧйЦҜБӘәПЖф¶ҜБЛULCOS(Ultra-low CO2 Steelmaking)ПоДҝЈ¬ІўМбіцБЛ»щУЪЗвТұҪрөДёЦМъТұҪрВ·ПЯЈ¬НЁ№эөзҪвЛ®ІъЗвЈ¬№©ёшЦұҪУ»№ФӯКъВҜЈ¬№ӨТХВ·ПЯИзНј4ЛщКҫ[45]ЎЈёГПоДҝЗвТұҪрјјКхөДН»ЖЖЈ¬ҝЙК№ёЦМъТұБ¶МјЕЕ·ЕҙУ1850 kgCO2/tҙЦёЦҪөөН84%ЦБ300 kgCO2/tҙЦёЦ[45]ЎЈ
2008ДкЈ¬ИХұҫЖф¶ҜБЛҙҙРВРФБ¶Мъ№ӨТХјјКхҝӘ·ўПоДҝ(COURSE50)Ј¬СРҫҝДЪИЭ°ьАЁH2»№ФӯБ¶МъјјКхҝӘ·ўЈ¬МбёЯH2»№ФӯР§УҰ[46-47]ЎЈДҝЗ°Ј¬СРҫҝИЛФұФЪ12 m3өДКФСйёЯВҜЙПҪшРРБЛ¶аҙОКФСйЈ¬¶ФҙөИлH2ҙшАҙөДУ°Пмј°CO2јхЕЕР§№ыөИҪшРРБЛСйЦӨЈ¬И·БўБЛH2»№ФӯР§№ыЧоҙу»ҜөД№ӨТХМхјюЎЈCOURSE50ПоДҝјЖ»®ФЪ2030ДкН¶ИлФЛРРЈ¬ҙЛәуҪ«ҝӘХ№ёЦМъі§НвІҝ№©ЗвјјКхөДҝӘ·ўЈ¬ЧоЦХКөПЦЎ°БгМјёЦЎұДҝұк[47]ЎЈ
2017ДкЈ¬ИрөдёЦМъ№«ЛҫЎўLKABМъҝуКҜ№«ЛҫәНVattenfallөзБҰ№«ЛҫБӘәПіЙБўБЛәПЧКЖуТөЈ¬ЦјФЪНЖ¶ҜHYBRIT(Hydrogen breakthrough ironmaking tech- nology)ПоДҝЈ¬ҝӘ·ў»щУЪH2ЦұҪУ»№ФӯөДБ¶МъјјКхЈ¬Мжҙъҙ«НіөДҪ№МҝәНМмИ»ЖшЈ¬јхЙЩИрөдёЦМъРРТөМјЕЕ·Е[48]ЎЈҫӯ№АЛгЈ¬ІЙУГҙҝH2»№ФӯЈ¬ҝјВЗјдҪУМјЕЕ·ЕБҝЈ¬ҝЙҪөөНЦБ53 kgCO2/tҙЦёЦ[7]ЎЈHYBRITПоДҝјЖ»®УЪ2018ЎӘ2024ДкҪшРРЦРКФКФСйЈ¬2025ЎӘ2035ДкҪЁБўH2ЦұҪУ»№ФӯБ¶МъКҫ·¶і§Ј¬ІўТАНРРВҪЁөДH2ҙўҙжЙиК©Ј¬өҪ2045ДкКөПЦОЮ»ҜКҜДЬФҙБ¶МъөДДҝұк[48]ЎЈ
2019ДкЈ¬өВ№ъөЩЙӯҝЛВІІ®јҜНЕУлТә»ҜҝХЖш№«ЛҫБӘәПЈ¬ХэКҪЖф¶ҜБЛёЯВҜH2Б¶МъКФСйЈ¬ІўјЖ»®ҙУ2022ДкҝӘКјЈ¬¶ЕТБЛ№ұӨөШЗшЖдЛыёЯВҜҫщК№УГH2ҪшРРёЦМъТұБ¶Ј¬ҝЙК№ЙъІъ№эіМЦРCO2ЕЕ·ЕБҝҪөөН20%[47]ЎЈ
2019Дк10ФВЈ¬ОТ№ъЙҪОчЦРҪъҝуТөДкІъ30НтtЗвЖшЦұ»№Б¶МъПоДҝөчКФН¶ІъЈ¬ёГПоДҝХл¶Ф№ъДЪЎ°ё»ГәИұЖшЎұөДЧКФҙМШөгЈ¬ЧФЦчСР·ўБЛЎ°Ҫ№ВҜГәЖшёЙЦШХы»№ФӯЖшЎұ№ӨТХЈ¬Н»ЖЖБЛЖш»щКъВҜЦұҪУ»№ФӯјјКхФЪОТ№ъІъТө»ҜөДЖҝҫұЈ¬CO2ЕЕ·ЕБҝұИҙ«НіёЯВҜБ¶МъҪөөН31.7%[49]ЎЈ
УЙҙЛҝЙјыЈ¬ё»ЗвЖш»щЦұҪУ»№ФӯБ¶МъТСҫӯҪшИлјјКхіЙКмЎўОИІҪ·ўХ№өДҪЧ¶ОЈ¬ІўХэФЪПтҙҝЗвЖшЦұҪУ»№ФӯөД·ҪПт·ўХ№ЎЈ

Нј4 »щУЪЗвТұҪрөДёЦМъТұҪрВ·ПЯ[45]
Fig. 4 Iron and steel making route based on hydrogen metallurgy[42]
1.3 ё»ЗвИЫИЪ»№ФӯБ¶МъјјКхСРҫҝ
1995ДкЈ¬EDELSON[3]МбіцБЛІЙУГH2ИЫИЪ»№ФӯМъҝуЦЖұёМъЛ®өД№ӨТХЈ¬ёГ№ӨТХҪ«МъҝуФӯБПәНЦъИЫјБҙУВҜ¶ҘјУИлЈ¬ҙУ»№ФӯВҜЦРЙПІҝЎўЦРПВІҝ·ЦұрНЁИлO2әН№эБҝөДH2Ј¬ВҜБППВВд№эіМЦРКЧПИНЁ№эУЙ№эБҝH2УлO2ИјЙХІъЙъөД»рСжЗшұ»НкИ«ИЫ»ҜЈ¬И»әуИЫМеНЁ№э»№ФӯЗшұ»H2»№ФӯЈ¬ЧоәуИЫМеФЪ»№ФӯВҜөЧІҝКөПЦФьМъ·ЦАлЎЈҙУВҜ¶ҘҪ«ОІЖш»ШКХЈ¬ІўАыУГОІЖшУаИИ¶ФH2әНO2ҪшРРФӨИИЎЈ
УЙУЪҙҝH2ИЫИЪ»№ФӯБ¶МъИФҙжФЪ¶МЖЪДЪДСТФКөПЦҙу№жДЈЎўөНіЙұҫЦЖЗвөДОКМвЈ¬ҪьДкАҙЈ¬ЙПәЈҙуС§МбіцМъФЎМј-ЗвёҙҙөИЫИЪ»№Фӯ№ӨТХВ·ПЯЈ¬Жд»щұҫВ·ПЯКЗФЪИЫИЪ»№Фӯ·ҙУҰЦРТФH2ОӘЦчТӘ»№ФӯјБЎўТФМјОӘЦчТӘИјБПЈ¬ҙпөҪҪөөНДЬәДәНCO2ЕЕ·ЕөДДҝұк[50]ЎЈМј-ЗвИЫИЪ»№Фӯ№ӨТХЦчТӘ»щУЪТФПВФӯАн[5]ЎЈ
»№ФӯЈә
Fe2O3+3H2(g)=2Fe+3H2O(g) (4)
№©ИИЈә
2C+O2(g)=2CO(g) (5)
ЦЖЗвЈә
CO(g)+H2O(g)=H2(g)+CO2(g) (6)
АнВЫјЖЛгұнГчЈ¬ІЙУГH2»№Фӯіц1molFeПыәДөДИИБҝҪцОӘМј»№ФӯөДОе·ЦЦ®Т»Ј¬ЗТ·ҙУҰОВ¶ИҙпөҪ1400 ЎжКұЈ¬»№ФӯЛЩВКұИCOёЯ2ёцКэБҝј¶Ј¬ТтҙЛЈ¬ФЪИЫИЪЧҙМ¬ПВІЙУГH2»№ФӯМъҝуҫЯУРЛЩ¶ИҝмЎўДЬәДәНCO2ЕЕ·ЕҫщҪПөНөДУЕКЖ[51]ЎЈ
ДЯПюГчөИ[52]ҪшРРБЛМј-ЗвИЫИЪ»№ФӯМъҝуөДКөСйСРҫҝЈ¬Ҫб№ыұнГчЈәјё·ЦЦУЦ®ДЪҝЙНкіЙҫшҙуІҝ·ЦМъСх»ҜОпөД»№ФӯЈ¬ЗТЦХФьTFeҝЙҙпөҪ1%ТФПВЈ»Мј-ЗвИЫИЪ»№Фӯ·ҙУҰОӘТ»ј¶·ҙУҰЈ¬ЛжЧЕ·ҙУҰҪшРРЈ¬»№ФӯЛЩВКҪөөНЈ¬·ҙУҰЛЩВКҝШЦЖ»·ҪЪЧӘұдОӘМъСх»ҜОпөДА©ЙўЎЈ
ІЬіҜХжөИ[53]¶ФІЙУГH2ИЎҙъМјҪшРРИЫИЪ»№ФӯБ¶МъөДҝЙРРРФҪшРРБЛСРҫҝЈ¬ИПОӘЈә»щУЪПЦУРөДИЫИЪ»№Фӯ№ӨТХЈ¬ПтИЫБ¶ВҜЕзҙөH2Ј¬НЁ№эјхЙЩЕзГәБҝІўФцјУH2ЕзҙөБҝЈ¬К№n(C):n(O)РЎУЪ1Ј¬ҝЙҙпөҪҪөөН»№ФӯЗшЛщРиИИёәәЙөДДҝөДЈ»МъҝуИЫИЪ»№ФӯөД¶ЦМъДЬәДЛжn(H2)/n(H2+C)МбёЯ¶шҪөөНЈ¬И«МјИЫИЪ»№ФӯөДАнВЫ¶ЦМъДЬәДҙп4ЎБ106 kJЈ¬¶шИ«H2ИЫИЪ»№ФӯАнВЫ¶ЦМъДЬәДҪцОӘФј0.8ЎБ106kJЈ¬¶ЦМъАнВЫәДЗвБҝОӘ980 m3ЎЈ
ХЕІЁ[50]Хл¶ФМъФЎМј-ЗвёҙҙөИЫИЪ»№ФӯМъҝу№ӨТХЈ¬СРҫҝҪЁБўБЛ·ҙУҰЖч¶ҜБҰС§ДЈРНЈ¬ИПОӘТэИлH2әу»№ФӯР§№ыУЕУЪҙҝМј»№ФӯЈ¬¶шФЪәПККұИАэПВөДМј-Зв»мәП»№ФӯУЦУЕУЪҙҝH2»№ФӯЈ»МбёЯn(C):n(H2)ұИАэЈ¬УРАыУЪМбёЯІъДЬЈ¬¶шЛжЧЕH2БҝөДФцјУЈ¬ФьЦРМъә¬БҝҪөөНЈ»Мј-Зв»мәП»№ФӯТФј°ҙҝМјЎўҙҝH2»№Фӯ·ҙУҰЛЩВКіЈКэ·ЦұрОӘ2.34 g-Fe/(cm2ЎӨmin)Ўў1.7~1.85 g-Fe/ (cm2ЎӨmin)Ўў2.05 g-Fe/(cm2ЎӨmin)Ј¬әПККөДn(C):n(H2)ұИАэОӘ0.5:1~1.2:1ЎЈ
2 УРЙ«ҪрКфТұҪрБмУтЗвТұҪрСРҫҝҪшХ№
2.1 УРЙ«ҪрКфТұҪрБмУт·ўХ№ЗвТұҪрөДҝЙРРРФ
ОТ№ъУРЙ«ҪрКф№ӨТө·ўХ№СёЛЩЈ¬ЧФ2002ДкТФАҙОТ№ъУРЙ«ҪрКфІъБҝБ¬Рш17ДкҫУКАҪзөЪТ»[54]ЎЈИ»¶шЈ¬ОТ№ъУРЙ«ҪрКфТұҪрОӘёЯОЫИҫІъТөЈ¬ГҝДкІъЙъҙуБҝОВКТР§УҰЖшМеЎЈТтҙЛЈ¬·ўХ№ЗвТұҪрјјКх¶ФОТ№ъУРЙ«ҪрКфТұҪрІъТөЙэј¶ТвТеЦШҙуЎЈ
ёщҫЭИИБҰС§ФӯАнЈ¬ҪрКфСх»ҜОпЙъіЙјӘІјЛ№ЧФУЙДЬ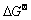 (MeO)ҙуУЪЛ®ЙъіЙЧФУЙДЬ
(MeO)ҙуУЪЛ®ЙъіЙЧФУЙДЬ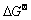 (H2O)КұЈ¬ёГҪрКфСх»ҜОпҝЙұ»H2»№ФӯЎЈҙУEllinghamНј[55] (јыНј5)ҝЙЦӘЈ¬ФЪТ»¶ЁОВ¶ИМхјюПВЈ¬ЗҰЎўОэЎўНӯЎўДшЎўоЬөИ¶аЦЦҪрКф¶ФУҰСх»ҜОп
(H2O)КұЈ¬ёГҪрКфСх»ҜОпҝЙұ»H2»№ФӯЎЈҙУEllinghamНј[55] (јыНј5)ҝЙЦӘЈ¬ФЪТ»¶ЁОВ¶ИМхјюПВЈ¬ЗҰЎўОэЎўНӯЎўДшЎўоЬөИ¶аЦЦҪрКф¶ФУҰСх»ҜОп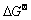 (MeO)ёЯУЪ
(MeO)ёЯУЪ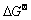 (H2O)Ј¬ҫЯУРH2»№ФӯөДҝЙРРРФЎЈ¶шЗТЈ¬өНОВМхјюПВЈ¬
(H2O)Ј¬ҫЯУРH2»№ФӯөДҝЙРРРФЎЈ¶шЗТЈ¬өНОВМхјюПВЈ¬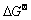 (H2O)РЎУЪУЙМјЙъіЙCO2өД
(H2O)РЎУЪУЙМјЙъіЙCO2өД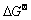 (CO2)Ј¬јҙH2»№ФӯДЬБҰЗҝУЪМјЈ¬ҫЯұёМжҙъМј»№ФӯјБөДЗұДЬЎЈ
(CO2)Ј¬јҙH2»№ФӯДЬБҰЗҝУЪМјЈ¬ҫЯұёМжҙъМј»№ФӯјБөДЗұДЬЎЈ
ҪьДкАҙЈ¬ФЪ·ўХ№ВМЙ«ТұҪрөДРОКЖЗэ¶ҜПВЈ¬ЗвТұҪрФЪУРЙ«ҪрКфТұҪрБмУтТІФҪАҙФҪКЬ№ШЧўЈ¬МШұрКЗУлёЦМъТұҪрПа№Ш¶ИҪПёЯөДДшЎўоСөИТұҪрРРТөЎЈ
2.2 ДшТұҪр
»щУЪЧЫәПАыУГё»ЗвҪ№ВҜГәЖшҪөөНәмНБДшҝуТұБ¶ДЬәДөДЙиПлЈ¬В¬ҪЬ[56]ІЙУГҪ№ВҜГәЖшЦчТӘіЙ·ЦH2ЧчОӘ»№ФӯјБЈ¬ҪшРРБЛәмНБДшҝу»№ФӯұәЙХ-ҙЕСЎЦЖұёДшМъөДСРҫҝЈ¬Ҫб№ыұнГчЈәДшЎўМъ»ШКХВКҫщЛж»№Фӯ№эіМH2·ЦС№Фцҙу¶шМбёЯЈ¬ФЪЧЬЖшЛЩОӘ200 L/hЎў»№ФӯОВ¶И800 ЎжЎў»№ФӯКұјд220 minЎўБтЛбДЖМнјУБҝ20%Ўў»№ФӯІъОпДҘҝуКұјд10 minЎўҙЕіЎЗҝ¶И0.156 TөДУЕ»ҜМхјюПВЈ¬ҝЙ»сөГДшЖ·О»5.64%ЎўДш»ШКХВК83.59%өДДшМъІъЖ·ЎЈ¶ЎЦҫ№гөИ[57-58]¶ФH2»№ФӯәмНБДшҝу№эіМҪшРРБЛПкПё·ЦОцЈ¬·ўПЦФЪРЎУЪ600 Ўж өДөНОВМхјюПВЈ¬ДшЎўМъөДҪрКф»ҜВКЛжОВ¶ИЙэёЯіКПЦМбёЯөДЗчКЖЈ»КөСйЛщІЙИЎөДЗвЖшЕЁ¶И(20%~100%)ј°ҝуОпБЈ¶И(0.15~0.83 mm)Мхјю¶ФДшЎўМъҪрКф»ҜВКөДУ°ПмІўІ»ПФЦшЈ»¶Фә¬Ni 0.82%ЎўFe 9.67%ЎўMgO 31.49%өД№иГҫРНәмНБДшҝуЈ¬ФЪОВ¶И600 ЎжЎў»№ФӯКұјд90 minј°H2ЕЁ¶И(Ме»э·ЦКэ)60%өДМхјюПВЈ¬ДшЎўМъҪрКф»ҜВК·ЦұрОӘ88%Ўў46%Ј¬ЖдЦРҙуІҝ·ЦМъСх»ҜОпұ»»№ФӯОӘөНјЫСх»ҜОпЈ¬јМРшМбёЯ»№ФӯОВ¶ИЈ¬ФтәмНБДшҝуЦРОЮ¶ЁРНГҫ№иЛбСОНЁ№эЦШҪбҫ§ЙъіЙЦВГЬөДГҫйПйӯКҜПа(Mg2SiO4)Ј¬°ьёІДшЎўМъСх»ҜОпЈ¬Чи°ӯБЛNiЎўFeөДҪшТ»ІҪ»№ФӯЎЈ

Нј5 EllinghamНј[55]
Fig. 5 Ellingham diagram[55]
¶ФУЪH2»№ФӯДшЎўМъСх»ҜОпөД¶ҜБҰС§Ј¬ХЕәЈЕаөИ[59]ИПОӘЈәFe2O3-NiOМеПөФЪH2Жш·ХПВ»№Фӯ№эіМөД·ҙУҰ»ъАнәҜКэОӘ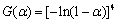 (
(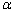 ОӘ·ҙУҰ·ЦКэ)Ј¬·ҙУҰ№эіМ·ыәПЛж»ъіЙәЛәНЛжәуЙъіӨДЈРНЈ¬МеПөЦРFe2O3ә¬БҝФҪёЯЈ¬·ҙУҰ»о»ҜДЬФҪёЯЈ»·ҙУҰ№эіМЦРЈ¬NiOұ»УЕПИ»№ФӯЈ¬ЙъіЙөДNiҝЙЧчОӘҙЯ»ҜјБҙЩҪшFe2O3өД»№ФӯЎЈ
ОӘ·ҙУҰ·ЦКэ)Ј¬·ҙУҰ№эіМ·ыәПЛж»ъіЙәЛәНЛжәуЙъіӨДЈРНЈ¬МеПөЦРFe2O3ә¬БҝФҪёЯЈ¬·ҙУҰ»о»ҜДЬФҪёЯЈ»·ҙУҰ№эіМЦРЈ¬NiOұ»УЕПИ»№ФӯЈ¬ЙъіЙөДNiҝЙЧчОӘҙЯ»ҜјБҙЩҪшFe2O3өД»№ФӯЎЈ
УРСРҫҝХЯНЁ№эІЙУГДЖСОМнјУјБЗҝ»ҜH2¶ФәмНБДшҝуөД»№Фӯ№эіМЈ¬ІўИЎөГБЛБјәГөДР§№ыЎЈLUөИ[60]СРҫҝБЛБтЛбДЖ¶ФЗҝ»ҜH2»№ФӯәмНБДшҝуөДЧчУГЈ¬ФЪ0%~20%өДМнјУ·¶О§ДЪЈ¬ФцјУБтЛбДЖМнјУБҝҝЙМбёЯІъЖ·ДшЖ·О»Ул»ШКХВКЈ¬Na+әН ұ»ОьёҪФЪәмНБДшҝуұнГжЈ¬јУҝмБЛҪзГж·ҙУҰЛЩВКЈ»Н¬КұЈ¬БтЛбДЖұ»H2»№ФӯРОіЙFe-S№МИЬМеЈ¬јУЛЩБЛХыёц·ҙУҰөДҙ«ЦК№эіМЈ¬ҙЩҪшДшМъҪрКфҝЕБЈөДҙ«ЦКәНҫЫјҜіӨҙуЎЈёЯҪрМОөИ[61]ИПОӘЈ¬ұәЙХ№эіМЦРМјЛбДЖҝЙҙЩҪшәмНБДшҝуДшЎўМъСх»ҜОпөДКН·ЕЈ¬УРАыУЪҪшТ»ІҪ»№ФӯЈ¬»№ФӯІъОпЦРДшЦчТӘТФМъОӘФШМеЈ¬ІўТФFe-NiРОКҪЙъіЙЎЈ
ұ»ОьёҪФЪәмНБДшҝуұнГжЈ¬јУҝмБЛҪзГж·ҙУҰЛЩВКЈ»Н¬КұЈ¬БтЛбДЖұ»H2»№ФӯРОіЙFe-S№МИЬМеЈ¬јУЛЩБЛХыёц·ҙУҰөДҙ«ЦК№эіМЈ¬ҙЩҪшДшМъҪрКфҝЕБЈөДҙ«ЦКәНҫЫјҜіӨҙуЎЈёЯҪрМОөИ[61]ИПОӘЈ¬ұәЙХ№эіМЦРМјЛбДЖҝЙҙЩҪшәмНБДшҝуДшЎўМъСх»ҜОпөДКН·ЕЈ¬УРАыУЪҪшТ»ІҪ»№ФӯЈ¬»№ФӯІъОпЦРДшЦчТӘТФМъОӘФШМеЈ¬ІўТФFe-NiРОКҪЙъіЙЎЈ
2.3 оСТұҪр
LIөИ[62-63]ІЙУГH2ЎўCO»мәПЖшМеЈ¬¶Ф·°оСҙЕМъҝуЗтНЕҪшРР»№ФӯЈ¬Іў·ЦОц·ҙУҰ№эіМөД¶ҜБҰС§Ј¬·ўПЦЈәЛжЧЕ»№ФӯОВ¶ИЎўV(H2)/V(CO)ұИАэөДЙэёЯТФј°ЗтНЕБЈҫ¶јхРЎЈ¬ҪрКфЧЬ»№ФӯВКіКЙэёЯЗчКЖЈ»»№Фӯ·ҙУҰұнГж»о»ҜДЬОӘ60.78 kJ/molЈ¬·ҙУҰ№эіМіхКјҪЧ¶ОУЙұнГж»ҜС§·ҙУҰҝШЦЖЈ¬Д©ОІҪЧ¶ОФтУЙ»ҜС§·ҙУҰУлДЪА©Йў»·ҪЪБӘәПҝШЦЖЈ»¶Фә¬FeO 26.25%ЎўTiO2 9.26%ЎўV2O5 0.62%ЎўCr2O3 1.48%өД·°оСҙЕМъҝуЈ¬ІЙУГұәЙХ-ё»ЗвЖш»щЦұҪУ»№Фӯ-ИЫИЪ·ЦАл№ӨТХЈ¬ҪшРРМъЎўоСЎў·°ЎўёхҪрКфөДМбИЎЈ»ФЪұәЙХОВ¶И1200 ЎжЎўұәЙХКұјд15 minЎў»№ФӯОВ¶И1050 ЎжЎўV(H2)/V(CO)ОӘ2.5Ўў»№ФӯКұјд30 minЎўИЫИЪОВ¶И1580 ЎжЎўИЫИЪ·ЦАлКұјд30 minөДУЕ»ҜМхјюПВЈ¬»сөГМъЎўоСЎў·°Ўўёх»ШКХВК·ЦұрҙпөҪ97.9%Ўў89.8%Ўў96.7%Ўў97.8%ЎЈ
SARGEANTөИ[64-65]ҪшРРБЛH2»№ФӯоСМъҝуөДКөСйСРҫҝЈ¬Ҫб№ыЦӨГчЈ¬оСМъҝу»№Фӯ№эіМЦР·ўЙъБЛТФПВ·ҙУҰЈә
FeTiO3+H2(g)=Fe+TiO2+H2O(g) (7)
Іў·ўПЦЈ¬H2ЕЁ¶И¶ФоСМъҝуөД»№ФӯҫЯУРПФЦшУ°ПмЈ¬1000 ЎжМхјюПВ»№ФӯоСМъҝуЈ¬·ҙУҰіхКјөД1 hКұјдДЪЈ¬өНH2С№БҰПВ»№Фӯ·ҙУҰЛЩВКёьёЯЈ¬ЛжЧЕ·ҙУҰөДҪшРРЈ¬ФтРиТӘМбёЯH2С№БҰІЕДЬұЈіЦУліхКјПаөұөД»№Фӯ·ҙУҰЛЩВКЎЈ
ZHAGNөИ[66]ІЙУГH2ёЁЦъГҫИИ»№ФӯTiO2ЦЖұёБЛоСҪрКф·ЫД©ЎЈУЙУЪоС¶ФСхҫЯУРј«ЗҝөДЗЧәНБҰЈ¬MgДСТФЦұҪУ»№ФӯTiO2Ј¬¶шёЯОВМхјюПВTi-H-O№МИЬМеОИ¶ЁРФөНУЪTi-O№МИЬМеЈ¬ТтҙЛЈ¬ҝЙІЙУГH2Жш·ХФцЗҝMgУлTi-O·ҙУҰөДИИБҰС§Зэ¶ҜБҰЈ¬НЁ№эГҫөДҪшТ»ІҪНССхЧчУГЈ¬»сөГоСҪрКф·ЫД©ЎЈ
2.4 ЖдЛыУРЙ«ҪрКфТұҪр
ЗвТұҪрјјКхТІұ»УҰУГУЪОЩЎўовҪрКф·ЫД©өДЦЖұёЎЈZHUөИ[67]ІЙУГH2¶Фә¬ЙйОЩСх»ҜОпҪшРР»№ФӯЈ¬ЦЖұёОЩҪрКф·ЫД©Ј¬ФЪ800 ЎжМхјюПВ»№Фӯ3 hЈ¬ЧоЦХҝЙ»сөГW-1%AsёҙәПДЙГЧ·ЫД©ЎЈKANGөИ[68]СРҫҝБЛH2·Цұр»№ФӯҙҝWO3әНWO3-NiOМеПөөД¶ҜБҰС§Ј¬Ҫб№ыұнГчЈәH2¶ФҙҝWO3өД»№Фӯ·ҙУҰ»о»ҜДЬОӘ94.6~117.4 kJ/molЈ¬¶ш¶ФWO3-NiOМеПөЦРWO3ЎўNiOөД»№Фӯ·ҙУҰ»о»ҜДЬ·ЦұрОӘ87.4 kJ/molЎў79.4 kJ/molЈ»»мәПОпМеПөЦРЈ¬·ҙУҰЙъіЙөДNiҝЙҙЩҪшH2¶ФWO3өД»№ФӯЎЈ
ZHANGөИ[69]ІЙУГH2¶ФMoO2·ЫД©ҪшРР»№ФӯЈ¬ІўМнјУі¬Пёов·ЫД©ЧчОӘіЙәЛјБЈ¬іЙ№ҰЦЖұёБЛДЙГЧов·ЫД©ЎЈH2¶ФMoO2өД»№Фӯ·ҙУҰЛЩВККЬұнГж»ҜС§·ҙУҰҝШЦЖЈ¬»о»ҜДЬОӘ54.89~62.23 kJ/molЈ¬ФЪ»№Фӯ№эіМЦРМнјУ0.1%NaClЈ¬·ҙУҰ»о»ҜДЬМбёЯЦБ67.05~73.76 kJ/molЈ¬ТтҙЛЈ¬ККБҝМнјУNaClҝЙПЮЦЖ·ҙУҰЙъіЙөДовҝЕБЈіӨҙуЈ¬ҙУ¶ш»сөГОўПёҝЕБЈөДов·ЫД©[70]ЎЈ
ЗвТұҪрјјКхФЪУРЙ«ҪрКфТұҪрБмУтөДСРҫҝДҝЗ°ИФҙҰУЪКөСйКТСРҫҝҪЧ¶ОЈ¬¶шЗТҪцХл¶ФСх»ҜҝуОпөДТұҪр№эіМЎЈҪ«ЗвТұҪрјјКхУҰУГУЪУРЙ«ҪрКфБт»ҜҝуЧКФҙөДТұҪр№эіМЈ¬ИзёЯЗҰФьЎўМаСхөД»№ФӯИЫБ¶Ј¬ИФИ»ҫЯУРәЬҙуөД·ўХ№ЗұБҰЎЈ
3 ¶юҙОЧКФҙАыУГБмУтЗвТұҪрСРҫҝҪшХ№
ДҝЗ°Ј¬ЗвТұҪрјјКхФЪУРЙ«ҪрКф¶юҙОЧКФҙАыУГБмУтөДУҰУГТІТСУРОДПЧұЁөАЎЈ
ХЕ»іО°[71]ІЙУГМј-ЗвёҙәП»№Фӯ¶ФНӯФьҪшРРЖ¶»ҜЈ¬СРҫҝұнГчЈәФЪ»№ФӯёДРФ№эіМЦРЈ¬НӯФьНССхБҝәН»№ФӯЛЩВКЛж»№ФӯЖшМеЦРH2ә¬БҝөДФцјУ¶шМбёЯЈ¬COәНH2ЧојСМе»эұИОӘV(CO):V(H2)=1:2Ј»ИЫИЪ»№Фӯ№эіМөД№М-Тә-ЖшИэПа·ҙУҰЦчТӘ°ьАЁТФПВ»·ҪЪЈә
1) ТФH2әНCOОӘәЛРДөДЖшЕЭРОіЙІўіӨҙуЈ»
2) H2әНCOНЁ№эЖшПаұЯҪзІгА©ЙўөҪФь-ЖшҪзГжЈ»
3) ИЫФьЦРFe3+ПтФь-ЖшҪзГжЗЁТЖЈ»
4) ФЪФь-ЖшҪзГжҙҰЈ¬»№ФӯЖшМеҪ«Fe3O4(Fe3+)»№ФӯіЙFeO(Fe2+)әНH2OЈ»
5) Fe2+ПтИЫФьДЪІҝЗЁТЖЈ»
6) ЖшЕЭЙПЙэ№эіМЦРЈ¬УОАлМ¬өДМјУлH2O·ўЙъ·ҙУҰЈ¬ЙъІъCOәНH2ЎЈ
јЖЛгҪб№ыұнГчЈ¬ИЫИЪНӯФьөДМј-ЗвёҙәП»№Фӯ·ҙУҰОӘТ»ј¶·ҙУҰЈ¬ұн№Ы»о»ҜДЬОӘ58.8 kJ/mol[71]ЎЈНЁ№э·ЦОцИЫИЪ»№ФӯНӯФь№эіМНӯәНМъөД·ЦІјЧҙМ¬·ўПЦЈ¬ЕзҙөH2ҝЙОӘұщНӯҝЕБЈөДЕцЧІҫЫјҜМṩУРАыМхјю[72]ЎЈ
EBINөИ[73]ІЙУГH2»№ФӯёЁЦъИИҪвјјКхҙУZn-C·ПЖъөзіШөДөзј«ІДБПЦР»ШКХРҝЈ¬ФЪ950 ЎжөД»№ФӯИИҪвМхјюПВЈ¬Рҝ»ШКХВКҙпөҪ99.8%Ј¬НЁ№э·ЦОцИПОӘЈәФЪёГ·ҙУҰМхјюПВЈ¬H2¶ФөзіШәЪ·ЫөД»№ФӯКЗЦчТӘ·ҙУҰЈ¬МјИИ»№ФӯОӘҙОТӘ·ҙУҰЎЈ
ё¶»ФБъөИ[74]ІЙУГМъФЎМј-Зв»мәП»№Фӯ№ӨТХ¶ФІ»РвёЦ·ЫіҫЦРөДёхҪшРР»ШКХЈ¬ТІ»сөГБЛҪПәГөДР§№ыЈ¬Ҫб№ыұнГчЈ¬өЧҙөH2ҝЙПФЦшјУҝмә¬ёхОпБПөД»№ФӯҪшіМЎЈ
4 ·ўХ№ЗвТұҪрШҪҙэҪвҫцөД№ШјьОКМв
4.1 H2өДҙу№жДЈЎўөНіЙұҫЦЖұё
ТұҪр№ӨТөКфУЪЧКФҙЎўДЬФҙГЬјҜРНРРТөЈ¬ТӘ·ўХ№ЗвТұҪрјјКхЈ¬КЧПИРиТӘҪвҫцҙуИЭБҝЎўөНіЙұҫЦЖЗвөДОКМвЎЈТФёЦМъТұҪрОӘАэЈ¬ІЙУГҙҝH2ИЫИЪ»№ФӯБ¶МъјјКхЈ¬¶ЦМъАнВЫәДЗвБҝёЯҙп980 m3[53]ЎЈТтҙЛЈ¬·ўХ№ЗвТұҪрРиТӘұЈЦӨH2өДҙу№жДЈЎўөНіЙұҫЦЖұёЎЈҙЛНвЈ¬ҫЎ№ЬФЪД©¶ЛАыУГ»·ҪЪЈ¬H2ұ»ИПОӘКЗТ»ЦЦЗеҪаөДДЬФҙәН»№ФӯјБЈ¬ө«КЗЦЖЗв№эіМөДЗеҪаЦёКэКЗКөПЦХыёцРРТөЗеҪаЙъІъөД№ШјьЎЈДҝЗ°Ј¬ұИҪПіЙКмөДөзҪвЛ®ЎўГәҪ№Жш»ҜЎўМмИ»ЖшБСҪвөИЦЖЗвјјКхЙъІъіЙұҫҪПёЯЈ¬ЗТҫщТААөҙ«НіДЬФҙЈ¬Иұ·ҰҝЙіЦРшРФ[10]ЎЈ
ЛжЧЕҙ«НіДЬФҙ¶МИұОКМвөДИХТжН»іцЈ¬»щУЪМ«СфДЬөДРВРНЦЖЗвјјКхЈ¬Из№вҙЯ»ҜЎў№вөзҪвЎўИИҪвЦЖЗвЈ¬ТСФҪАҙФҪКЬ№ъДЪНвСРҫҝХЯ№ШЧўЈ¬ІўТСИЎөГҙуБҝСРҫҝіЙ№ы[75]ЎЈACARөИ[76-77]ҙУҫӯјГРФЎўјјКхҝЙРРРФЎў»·ҫіУ°ПмөИ·ҪГж¶ФІ»Н¬өДЦЖЗвјјКхҪшРРҝЙіЦРшРФ·ЦОцИПОӘЈ¬ІЙУГМ«СфДЬөДИИҪвЦЖЗвКЗ»щУЪПЦҙжөзНшЛ®ҪвЦЖЗвТФНвЧоҫЯҝЙіЦРшРФөДЦЖЗвјјКхЈ¬ө«ИФРиН»ЖЖҙу№жДЈУҰУГөДјјКхХП°ӯЎЈ
4.2 H2»№Фӯ№эіМИИБҝЖҪәв
H2ЦұҪУ»№Фӯ№эіМЈ¬ТФМъСх»ҜОп»№ФӯОӘАэЈә
3Fe2O3+H2(g)=2Fe3O4+H2O(g),
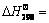 -12.1 kJ/mol (8)
-12.1 kJ/mol (8)
Fe3O4+H2(g)=3FeO+H2O(g), 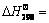 164.0 kJ/mol (9)
164.0 kJ/mol (9)
FeO+H2(g)=Fe+H2O(g), 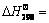 135.6 kJ/mol (10)
135.6 kJ/mol (10)
ЧЬ·ҙУҰЈә
Fe2O3+ 3H2(g)=2Fe+3H2O(g),
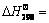 95.8 kJ/mol (11)
95.8 kJ/mol (11)
Хыёц»№Фӯ·ҙУҰ№эіМұнПЦОӘЗҝБТөДОьИИР§УҰЈ¬өјЦВҙҝH2»№ФӯМеПөИИБҝЖҪәвРиЗвБҝФ¶ҙуУЪ»ҜС§ЖҪәвРиЗвБҝЈ¬ВҜДЪ»ҜС§ДЬәНОпАнДЬІ»ЖҘЕдЈ¬РлҪвҫц»№Фӯ№эіМөДИИБҝЖҪәвОКМвЈ¬ТФО¬іЦОИ¶ЁөД·ҙУҰОВ¶ИЎЈ
ҙ«НіКъВҜH2АыУГВКөНЈ¬ВҜ¶ҘЖшөД»№ФӯКЖҪПёЯЎЈАоВ·Т¶[78]әН°ЧГч»ӘөИ[79]НЁ№эДЈДв·ЦОцЈ¬ЙијЖБЛҙөСхКъВҜЈ¬ИјЙХІҝ·ЦОҙ·ҙУҰөДH2Ј¬АыУГИјЙХИИ¶ФЙПІҝАдВҜБПҪшРРФӨИИЈ¬ҝЙК№H2УГБҝұИҙ«НіКъВҜјхЙЩ22.08%ЎўH2АыУГВКМбёЯ33.43%ЎЈТтҙЛЈ¬ЗвТұҪр№эіМЈ¬ІЙУГH2ОӘ»№ФӯјБөДН¬КұИјЙХ№эКЈөДH2І№ідИИБҝЈ¬О¬іЦ·ҙУҰИИБҝЖҪәвЈ¬КЗМбёЯ·ҙУҰР§ВКЈ¬ҪөөНЙъІъіЙұҫөДҝЙРР·Ҫ·ЁЎЈ
5 ҪбУп
1) ЧчОӘЖшМе»№ФӯјБЈ¬ФЪОВ¶ИҙуУЪ810 ЎжөДМхјюПВЈ¬H2¶ФМъСх»ҜОпөД»№ФӯДЬБҰЗҝУЪCOЈ¬ЗТH2өД»№Фӯ·ҙУҰЛЩВКұИМј»№ФӯјБёЯ1өҪ2ёцКэБҝј¶ЎЈТтҙЛЈ¬H2КЗёЯР§ЎўЗеҪаөДБ¶Мъ»№ФӯјБЎЈ
2) ё»ЗвЖш»щЦұҪУ»№ФӯБ¶МъјјКхҙҰУЪјјКхіЙКмЎўОИІҪ·ўХ№өДҪЧ¶ОЎЈMidrexәНHYL-ўу№ӨТХКЗөдРНөД»щУЪЗвТұҪрөДЦұҪУ»№ФӯБ¶Мъ№ӨТХЈ¬ДҝЗ°Ј¬№ъДЪНвТұҪрБмУтҫщФЪ·ўХ№»щУЪЗвТұҪрөДЦұҪУ»№ФӯБ¶МъјјКхЈ¬ИзЕ·ЦЮөДULCOSЎўИрөдөДHYBRTЎўИХұҫөДCOURSE50ПоДҝТФј°ОТ№ъөДЦРҪъҝуТөөИЎЈH2ИЫИЪ»№ФӯБ¶МъјјКхҙҰУЪКөСйКТСРҫҝҪЧ¶ОЎЈ
3) ЗвТұҪрјјКхФЪДшЎўоСЎўОЩЎўовөИУРЙ«ҪрКфТұҪрј°¶юҙОЧКФҙАыУГБмУтөДУҰУГТСФҪАҙФҪКЬ№ШЧўЈ¬ө«ДҝЗ°ҙҰУЪКөСйКТСРҫҝҪЧ¶ОЈ¬УРҙэҪшТ»ІҪөДјјКхН»ЖЖЎЈ
4) УЙУЪЗвТұҪрәДЗвБҝҙуЈ¬ТтҙЛЈ¬·ўХ№ЗвТұҪрРлН»ЖЖH2өДҙу№жДЈЎўөНіЙұҫЎўҝЙіЦРшЦЖұёјјКхЎЈH2ЦұҪУ»№Фӯ№эіМОӘОьИИР§УҰЈ¬»№РлҪвҫцИИБҝЖҪәвОКМвЈ¬ТФО¬іЦОИ¶ЁөД·ҙУҰ№эіМЎЈ
REFERENCES
[1] LIN Bo-qiang, WU Rong-xin. Designing energy policy based on dynamic change in energy and carbon dioxide emission performance of ChinaЎҜs iron and steel industry[J]. Journal of Cleaner Production, 2020, 256: 1-14.
[2] іВ РЗ. ЦР№ъУРЙ«ҪрКф№ӨТөИ«ТӘЛШМјЕЕ·ЕР§ВКУлМјЕЕ·ЕјЁР§СРҫҝ[D]. ПГГЕ: ПГГЕҙуС§, 2017.
CHEN Xing. Research of total-factor carbon emission efficiency and carbon emission performance in ChinaЎҜs non-ferrous metals industry[D]. Xiamen: Xiamen University, 2017
[3] EDELSON J. Method for reducing particulate iron ore to molten iron with hydrogen as reductant. American, 5464464[P]. 1999-11-07.
[4] РмҝпөП, ҪҜ№ъІэ. ЦР№ъёЦМъ№ӨТөөДПЦЧҙәН·ўХ№[J].ЦР№ъ№ӨіМҝЖС§, 2000, 2(7): 1-8.
XU Kuang-di, JIANG Guo-chang. Present situations and development of Chinese iron and steel industry[J]. Engineering Science, 2000, 2(7): 1-8.
[5] ЦЈЙЩІЁ. ЗвТұҪр»щҙЎСРҫҝј°РВ№ӨТХМҪЛч[J]. ЦР№ъТұҪр, 2012, 22(7): 1-6.
ZHENG Shao-bo. Basic research on hydrogen metallurgy and new ironmaking idea-process[J]. China Metallurgy, 2012, 22(7): 1-6.
[6] GERMESHUIZEN L M, BLOM P W E. A techno-economic evaluation of the use of hydrogen in a steel production process, utilizing nuclear process heat[J]. International Journal of Hydrogen Energy, 2013, 38(25): 10671-10682.
[7] VOGL V, AHMAN M, NILSSON L J. Assessment of hydrogen direct reduction for fossil-free steelmaking[J]. Journal of Cleaner Production, 2018, 203: 736-745.
[8] ёЙ УВ. 21КАјНКЗЎ°ЗвЎұөДКұҙъ[EB/OL]. [2019-09-20]. http://www.sohu.com/a/238747317_655347.
GAN Yong. The 21th Century is the Age of Hydrogen[EB/OL]. [2019-09-20]. http://www.sohu.com/a/238747317_655347.
[9] TANG Jue, CHU Man-sheng, LI Feng, et al. Development and progress on hydrogen metallurgy[J]. International Journal of Minerals, Metallurgy and Materials, 2020, 27(6): 713-723.
[10] ХЕЕеАј, ЦЈ Аи. №ӨТөЦЖЗвјјКхј°ҫӯјГРФ·ЦОц[J]. ЙҪОч»Ҝ№Ө, 2014, 34(5): 54-56.
ZHANG Pei-lan, ZHENG Li. Several industrial hydrogen production technology and economic analysis[J]. Shanxi Chemical Industry, 2014, 34(5): 54-56.
[11] DAWOOD F, ANDA M, SHAFIULLAH G M. Hydrogen production for energy: An overview[J]. International Journal of Hydrogen Energy, 2020, 45(7): 3847-3869.
[12] НхМ«СЧ, НхЙЩБў, ёЯіЙББ. КФВЫЗвТұҪр№ӨіМС§[J]. °°ёЦјјКх, 2005(1): 4-8.
WANG Tai-yan, WANG Shao-li, GAO Cheng-liang. Exploratory discussion on hydrogen metallurgical engineering[J]. Angang Technology, 2005(1): 4-8.
[13] ХЕёЈГч, ІЬіҜХж, Рм »Ф. Жш»щКъВҜЦұҪУ»№ФӯјјКхөД·ўХ№ПЦЧҙУлХ№Ны[J]. ёЦМъ, 2014, 49(3): 1-10.
ZHANG Fu-ming. CAO Chao-zhen, XU Hui. Current status and prospects of gas-based shaft furnace direct reduction technology[J]. Irom and Steel, 2014, 49(3): 1-10.
[14] SCHENK J L. Recent status of fluidized bed technologies for producing iron input materials for steelmaking[J]. Particuology, 2011, 9(1): 14-23.
[15] ZHOU Shi-wei, WEI Yong-gang, ZHANG Shuo-yao. Reduction of copper smelting slag using waste cooking oil[J]. Journal of Cleaner Production, 2019, 236: 1-5.
[16] ёрҝЎАс. Жш»щЦұҪУ»№ФӯКъВҜВҜДЪРРОӘУлВҜРН№ШПөСРҫҝ[D]. ЗШ»Көә: СаЙҪҙуС§, 2014.
GE Jun-li. The research on relationship of furnace profile and behavior in gas-based direct reduction shaft[D]. Qinhuangdao: Yanshan University, 2014.
[17] SPREITZER D, SCHENK J. Reduction of iron oxides with hydrogenЎӘA review[J]. Steel Research International, 2019, 90(10): 201900108.
[18] NAGASAKA T, HINA M, BAN-YA S. Interfacial kinetics of hydrogen with liquid slag containing iron oxide[J]. Metall and Materi Trans B, 2000, 31(5): 945-955.
[19] BAHAGAT M, KHEDR M H. Reduction kinetics, magnetic behavior and morphological changes during reduction of magnetite single crystal[J]. Materials Science and Engineering B, 2007, 138(3): 251-258.
[20] BAI Ming-hua, LONG Hu, REN Su-bo, et al. Reduction behavior and kinetics of iron ore pellets under H2-N2 atmosphere[J]. ISIJ International, 2018, 58(6): 1034-1041.
[21] HABERMANN A, WINTER F, HOFBAUER H, et al. An experimental study on the kinetics of fluidized bed iron ore reduction[J]. ISIJ International, 2000, 40(10): 935-942.
[22] COSTA A R, WAGNER D, PATISSON F. Modelling a new, low CO2 emissions, hydrogen steelmaking process[J]. Journal of Cleaner Production, 2013, 46: 27-35.
[23] TEPLOV O A. Kinetics of the low temperature hydrogen reduction of magnetite concentrates[J]. Russian Metallurgy (Metally), 2012(1): 8-21.
[24] LIN H Y, CHEN Y W, LI C. The mechanism of reduction of iron oxide by hydrogen[J]. Thermochimica Acta, 2003, 400(1/2): 61-67.
[25] WEI Zheng, ZHANG Jing, QIN Bao-ping, et al. Reduction kinetics of hematite ore fines with H2 in a rotary drum reactor[J]. Powder Technology, 2018, 332: 18-26.
[26] іВ вЩ. Жш»щ»№ФӯСх»ҜМъ¶ҜБҰС§»ъАнСРҫҝ[D]. ҙуБ¬: ҙуБ¬Ан№ӨҙуС§, 2011.
CHEN Geng. The kinetics of the gas-based reduction of iron oxide[D]. Dalian: Dalian University of Technology, 2011.
[27] BARDE A A, KLAUSNER J F, MEI R. Solid state reaction kinetics of iron oxide reduction using hydrogen as a reducing agent[J]. International Journal of Hydrogen Energy, 2016, 41(24): 10103-10119.
[28] HAYASHI S, IGUCHI Y. Hydrogen reduction of liquid iron oxide fines in gas-conveyed systems[J]. ISIJ International, 1994, 34(7): 555-561.
[29] XU Run-sheng, DAI Bo-wen, WANG Wei, et al. Effect of iron ore type on the thermal behaviour and kinetics of coal-iron ore briquettes during coking[J]. Fuel Processing Technology, 2018, 173: 11-20.
[30] WANG H T, SOHN H Y. Effect of CaO and SiO2 on swelling and iron whisker formation during reduction of iron oxide compact[J]. Ironmaking & Steelmaking, 2011, 38(6): 447-452.
[31] ЧЮЧЪКч, Нх іј. ИЫИЪ»№ФӯБ¶Мъ№ӨТХөДГәЖшё»ЗвёДЦКФӨ»№Фӯ[J]. ёЦМъ, 2007, 42(8): 17-20.
ZOU Zong-shu, WANG Chen. On hydrogen-enriching gas reform for pre-reduction in smelting reduction iron-making process[J]. Iron and Steel, 2007, 42(8): 17-20.
[32] TATEO U, TSUNEHISA N, HIDEKI O, et al. Effective use of hydrogen in gaseous reduction of iron ore agglomerates with H2-CO[J]. Journal of Iron and Steel Research International, 2009, 16(2): 1179-1184.
[33] HIDEKI O, TOSHINARI Y, TATEO U. Effect of water-gas shift reaction on reduction of iron oxide powder packed bed with H2-CO mixtures[J]. ISIJ International, 2003, 43(10): 1502-1511.
[34] ZUO Hai-bin, WANG Cong, DONG Jie-ji. Reduction kinetics of iron oxide pellets with H2 and CO mixtures[J]. International Journal of Minerals, Metallurgy and Materials, 2015, 22(7): 688-696.
[35] ТЧБиФЖ. МъҝуЗтНЕ»мәПЖшМеЖш»щЦұҪУ»№Фӯ»щҙЎСРҫҝ[D]. іӨЙі: ЦРДПҙуС§, 2013.
YI Ling-yun. Fundamental research on gas-based direct reduction of iron ore pellets with carbon monoxide and hydrogen mixtures[D]. Changsha: Central South University, 3013.
[36] Бх Бъ. ЗвЖшЦұҪУ»№ФӯКъВҜ»№Фӯ¶ОДЪОВ¶ИіЎј°БчіЎСР ҫҝ[D]. ЗШ»Көә: СаЙҪҙуС§, 2016.
Liu Long. Research on temperature field and flow field in the hydrogen direct reduction shaft furnace reduction[D]. Qinhuangdao: Yanshan University, 2016.
[37] НхХЧІЕ. Сх»ҜЗтНЕЖш»щКъВҜЦұҪУ»№ФӯөД»щҙЎСРҫҝ[D]. ЙтСф: ¶«ұұҙуС§, 2009.
WANG Zhao-cai. Fundamental study on direct reduction of oxidized pellets by gas-based shaft furnace[D]. Shenyang: Northeastern University, 2009.
[38] ХЕёЈГч, ІЬіҜХж, Рм »Ф. Жш»щКъВҜЦұҪУ»№ФӯјјКхөД·ўХ№ПЦЧҙУлХ№Ны[J]. ёЦМъ, 2014, 49(3): 1-10.
ZHANG Fu-ming, CAO Chao-zhen, XU Hui. Current status and prospects of gas-based shaft furnace direct reduction technology[J]. Iron and Steel, 2014, 49(3): 1-10.
[39] ¶ӯ Фҫ, ЗЗРЗРЗ, БхёД»», өИ. Жш»щЦұҪУ»№ФӯМъ№ӨТХ»№ФӯЖшСРҫҝПЦЧҙ[J]. ДЬФҙУлҪЪДЬ, 2016(3): 1-4.
DONG Yue, QIAO Xing-xing, LIU Gai-huan, et al. Research situation of reduction gas used in gas-based direct reduction iron technology[J]. Energy and Energy Conservation, 2016(3): 1-4.
[40] ВАҪЁі¬. Жш»щЦұҪУ»№ФӯКъВҜДЪ»№Фӯ№эіМөДСРҫҝУл·ЦОц[D]. ЗШ»Көә: СаЙҪҙуС§, 2017.
LЁ№ Jian-chao. Research and analysis on the reduction process of gas-based direction shaft furnace[D]. Qinhuangdao: Yanshan University, 2017.
[41] PARISI D R, LABORDE M A. Modeling of counter current moving bed gas-solid reactor used in direct reduction of iron ore[J]. Chemical Engineering Journal, 2004, 104(1/3): 35-43.
[42] Рм »Ф, ЧЮЧЪКч, ЦЬУеЙъ, өИ. КъВҜЙъІъЦұҪУ»№ФӯМъ№эіМөДКэЦөДЈДв[J]. ІДБПУлТұҪрС§ұЁ, 2009, 8(1): 7-11.
XU Hui, ZOU Zong-shu, ZHOU Yu-sheng, et al. Preliminary numerical simulation of shaft furnaceprocess for DRI production[J]. Journal of Materials and Metallurgy, 2009, 8(1): 7-11.
[43] GHADI A Z, VALIPOUR M S, BIGLARI M. CFD simulation of two-phase gas-particle flow in the Midrex shaft furnace: The effect of twin gas injection system on the performance of the reactor[J]. International Journal of Hydrogen Energy, 2017, 42(1): 103-118.
[44] ЦЬУеЙъ, З® кН, ЖлФЁәй, өИ. ГәЦЖЖшЙъІъЦұҪУ»№ФӯМъөДБӘәП№ӨТХ·Ҫ°ё[J]. ёЦМъ, 2012, 47(11): 27-35.
ZHOU Yu-sheng, QIAN hui, QI Yuan-hong, et al. Scheme of direct reduction iron production combined with coal gasification[J]. Iron and Steel, 2012, 47(11): 27-35.
[45] QUADER M A, AHMED S, DAWAL S Z. Present needs, recent progress and future trends of energy-efficient Ultra-Low Carbon Dioxide (CO2) Steelmaking (ULCOS) program[J]. Renewable Sustainable Energy Rev., 2016, 55: 537-549.
[46] И« ИЩ. COURSE50Б¶Мъ№ӨТХСР·ўҪшХ№[N]. КАҪзҪрКфөјұЁ, 2016-05-17(B03).
QUAN Rong. Research progress of COURSE50 ironmaking technology[N]. World Metals, 2016-05-17(B03).
[47] ХЕҫ©Жј. Уөұ§ЗвҫӯјГКұҙъИ«ЗтЗвТұҪрјјКхСР·ўББөг·ЧіК[N]. КАҪзҪрКфөјұЁ, 2019-11-26(F01).
ZHANG Jing-ping. Many breakthroughs on hydrometallurgy technology in the era of hydrogen economy[N]. World Metals, 2019-11-26(F01).
[48] KARAKAYA E, NUUR C, ASSBRING L. Potential transitions in the iron and steel industry in Sweden: Towards a hydrogen-based future?[J]. Journal of Cleaner Production, 2018, 195: 651-663.
[49] ЦРҪъТұҪрҝЖјјУРПЮ№«Лҫ. ЙҪОчЦРҪъҝуТөДкІъ30Нт¶ЦЗвЖшЦұ»№МъПоДҝјҙҪ«Н¶Іъ[EB/OL]. [2019-09-20]. http://www.zjthky.com/view.asp?id=274.
Zhongjin Metallurgical Technology Co. LTD. A project with annual output of 300 thousand tons of DRI by hydrogen reduction will be put into production in Shanxi Zhongjin Mining[EB/OL]. [2019-09-20]. http://www.zjthky.com/ view.asp?id=274.
[50] ХЕ ІЁ. МъФЎМј-ЗвёҙәПҙөЦХ»№Фӯ·ҙУҰ¶ҜБҰС§СРҫҝ[D]. ЙПәЈ: ЙПәЈҙуС§, 2011.
ZHANG Bo. Study on end-reduction kinetics of iron ore in a bath reactor with H2-C mixed reduction agents[D]. Shanghai: Shanghai University, 2011.
[51] ЦЈЙЩІЁ, әй РВ, РмҪЁВЧ, өИ. C-H2ВМЙ«ёЯР§МъҝуИЫМ¬»№ФӯјјКх№№Пл[C]// 2006Дк·ЗёЯВҜБ¶МъДк»бВЫОДјҜ. ЙтСф: ЦР№ъҪрКфС§»б, 2006: 117-123.
ZHENG Shao-bo, HONG Xin, XU Jian-lun, et al. Technical conception on green and efficient molten reduction of iron ore with C-H2mixed reduction agents[C]// Proceeding of the 2006 Annual Conference on Non-blast Furnace Ironmaking. Shenyang: The Chinese Society for Metals, 2006: 117-123.
[52] ДЯПюГч, Вж БХ, СоЙӯБъ, өИ. Зв-МјИЫИЪ»№ФӯКөСйКТКФСйСРҫҝ[C]// 2008Дк·ЗёЯВҜБ¶МъДк»бОДјҜ. СУјӘ: ЦР№ъҪрКфС§»б, 2008: 310-315.
NI Xiao-ming, LUO Lin, YANG Sen-long, et al. Experiment study on smelting reduction with carbon and bottom-blowing hydrogen[C]// Proceeding of the 2008 Annual Conference on Non-blast Furnace Ironmaking. Yanji: The Chinese Society for Metals, 2008: 315-320.
[53] ІЬіҜХж, №щЕаГс, ХФ Еж, өИ. ёЯОВИЫМ¬ЗвТұҪрјјКхСРҫҝ[J]. ёЦМъ·°оС, 2009, 30(1): 1-6.
CAO Chao-zhen, GUO Pei-min, ZHAO Pei, et al. Study on high temperature smelting hydrogen metallurgy[J]. Iron Steel Vanadium Titanium, 2009, 30(1): 1-6.
[54] №щС§Тж, МпЗм»Ә, Бх УҪ, өИ. УРЙ«ҪрКфЧКФҙСӯ»·СРҫҝУҰУГҪшХ№[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2019, 29(9): 1859-1901.
GUO Xue-yi, TIAN Qing-hua, LIU Yong, et al. Progress in research and application ofnon-ferrous metal resources recycling[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(9): 1859-1901.
[55] HASEGAWA M. Treatise on process metallurgy: Chapter 3.3-ellingham diagram[M]. Stockholm, Sweden: Royal Institute of Technology, 2014.
[56] В¬ ҪЬ. БтЛбДЖ¶ФәмНБДшҝуФЪЗвЖшәНјЧНйЖш·ХПВөД»№ФӯРФСРҫҝ[D]. М«Фӯ: М«ФӯАн№ӨҙуС§, 2013.
LU Jie. The reducibility research of sodium sulphate on the hydrogen and methane reduction process of nickel laterite ore[D]. Taiyuan: Taiyuan University of Technology, 2013.
[57] ¶ЎЦҫ№г. №иГҫРНәмНБДшҝуЖш»щ№МПа»№ФӯөДСРҫҝ[D]. АҘГч: АҘГчАн№ӨҙуС§, 2017.
DING Zhi-guang. Study on gas-based solid phase reduction of garnieritic laterite ore[D]. Kunming: Kunming University of Technology, 2017.
[58] ¶ЎЦҫ№г, Ао І©, ОәУАёХ. ЗвЖшЧчУГПВ№иГҫРНәмНБДшҝуөДөНОВ»№ФӯМШРФ[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2018, 28(8): 1669-1675.
DING Zhi-guang, LI Bo, WEI Yong-gang. Reduction characteristic of garnieritic laterite ore using hydrogen at low temperature[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(8): 1669-1675.
[59] ХЕәЈЕа, Ао І©, ¶ЎЦҫ№г, өИ. ·ЗөИОВМхјюПВЗвЖш»№ФӯFe2O3-NiOЦЖұёДшМъәПҪрөД·ҙУҰ¶ҜБҰС§[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2017, 27(1): 171-177.
ZHANG Hai-pei, LI Bo, DING Zhi-guang, et al. Reduction kinetics of Fe2O3-NiO composites for production of Fe/Ni alloy using hydrogen under non-isothermal conditions[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(1): 171-177.
[60] LU Jie, LIU Shou-jun, SHANGGUAN Ju, et al. The effect of sodium sulphate on the hydrogen reduction process of nickel laterite ore[J]. Minerals Engineering, 2013, 49: 154-164.
[61] ёЯҪрМО, ХЕСХНҘ, іВЕаоЪ, өИ. әмНБДшҝуё»јҜДшәНМъөДұәЙХЎўЗвЖш»№ФӯәНҙЕСЎ·ЦАл[J]. ұұҫ©ҝЖјјҙуѧѧұЁ, 2013, 35(10): 1289-1296.
GAO Jin-tao, ZHANG Yan-ting, CHEN Pei-yu, et al. Enrichment of Ni and Fe from nickel laterite by calcination, hydrogen reduction and magnetic separation[J]. Journal of University of Science and Technology Beijing, 2013, 35(10): 1289-1296.
[62] LI Wei, FU Gui-qin, CHU Man-sheng, et al. Reduction behavior and mechanism of Hongge vanadium titanomagnetite pellets by gas mixture of H2 and CO[J]. Journal of Iron and Steel Research, Internationa, 2017, 24(1): 34-42.
[63] LI Wei, FU Gui-qin, CHU Man-sheng, et al. An effective and cleaner process to recovery iron, titanium, vanadium, and chromium from Hongge vanadium titanomagnetite with hydrogen-rich gases[J]. Ironmaking & Steelmaking, 2020, 1743-2812. DOI: 10.1080/03019233.2020.1721955.
[64] SARGEANT H M, ABERNETHY F A J, BARBER S J, et al. Hydrogen reduction of ilmenite: Towards an in situ resource utilization demonstration on the surface of the Moon[J]. Planetary and Space Science, 2020, 180: 104751.
[65] SARGEANT H M, ABERNETHY F A J, ANAND M, et al. Feasibility studies for hydrogen reduction of ilmenite in a static system for use as an ISRU demonstration on the lunar surface[J]. Planetary and Space Science, 2020, 180: 104759.
[66] ZHANGY, FANGZ Z, XIA Y, et al. Hydrogen assisted magnesiothermic reduction of TiO2[J]. Chemical Engineering Journal, 2017, 308: 299-310.
[67] ZHU Hong-bo, TAN Dun-qiang, LI Ya-lei, et al. Refining mechanisms of arsenic in the hydrogen reduction processof tungsten oxide[J]. Advanced Powder Technology, 2015, 26(3): 1013-1020.
[68] KANG H, JEONG Y K, OH S T. Hydrogen reduction behavior and microstructural characteristics of WO3 and WO3-NiO powders[J]. International Journal of Refractory Metals & Hard Materials, 2019, 80: 69-72.
[69] ZHANG Yong, JIAO Shu-qiang, CHOU Kuo-Chih, et al. Size-controlled synthesis of Mo powders via hydrogen reduction of MoO2 powders with the assistance of Mo nuclei[J]. International Journal of Hydrogen Energy, 2020, 45(3): 1435-1443.
[70] SUN Guo-dong, WANG Kai-fei, JI Xin-peng, et al. Preparation of ultrafine/nano Mo particles via NaCl-assisted hydrogen reduction of different-sized MoO2 powders[J]. International Journal of Refractory Metals & Hard Materials, 2019, 80: 243-252.
[71] ХЕ»іО°. »щУЪЦұБчөзіЎәНМј-ЗвёҙәП»№ФӯёДРФөДНӯФьЖ¶»Ҝ№эіМөДКөСйСРҫҝ[D]. ЙПәЈ: ЙПәЈҙуС§, 2014.
ZHANG Huai-wei. Study of copper slag cleaning process based on DC electric field and C-H2 mixed reduction[D]. Shanghai: Shanghai University, 2014.
[72] QU Guo-rui, WEI Yong-gang, LI Bo, et al. Distribution of copper and iron components with hydrogen reduction of copper slag[J]. Journal of Alloys and Compounds, 2020, 824: 1-9.
[73] EBIN B, PETRANIKOVA M, STEENARI B M, et al. Investigation of zinc recovery by hydrogen reduction assisted pyrolysisof alkaline and zinc-carbon battery waste[J]. Waste Management, 2017, 68: 508-517.
[74] ё¶»ФБъ, ЕЈ Л§, іВОДұт, өИ. ә¬ёхОпБПМъФЎМјЗв»№ФӯөДКөСйСРҫҝ[J]. №эіМ№ӨіМС§ұЁ, 2013, 13(2): 246-249.
FU Hui-long, NIU Shuai, CHEN Wen-bin, et al. Experimental study on reduction of Cr-containing materials in iron bath with C and H2[J]. The Chinese Journal of Process Engineering, 2013, 13(2): 246-249.
[75] LIU G, SHENG Y, AGER J W, et al. Research advances towards large-scale solar hydrogen production from water[J]. Energy Chem, 2019, 1(2): 1-41.
[76] ACAR C, BESKESE A, TEMUR G T. Sustainability analysis of different hydrogen production options using hesitant fuzzy AHP[J]. International Journal of Hydrogen Energy, 2018, 43(39): 18059-18076.
[77] ACAR C, DINCER I. Review and evaluation of hydrogen production options for better environment[J]. Journal of Cleaner Production, 2019, 218: 835-849.
[78] АоВ·Т¶. ЦұҪУ»№ФӯКъВҜЗвЖшАыУГВКј°ВҜДЪОВ¶ИіЎСРҫҝ[D]. ЗШ»Көә: СаЙҪҙуС§, 2016.
LI Lu-ye. Research on hydrogen utilization in DR shaft furnace and temperature field[J]. Qinhuangdao: Yanshan University, 2016.
[79] °ЧГч»Ә, АоВ·Т¶, Рм ҝн, өИ. ЦұҪУ»№ФӯКъВҜЗвЖшАыУГВКөДКэЦө·ЦОцј°УЕ»Ҝ[J]. СаЙҪҙуѧѧұЁ, 2016, 40(6): 481-486.
BAI Ming-hua, LI Lu-ye, XU Kuan, et al. Numerical analysis and optimization on hydrogen utilization in DR shaft furnace[J]. Journal of Yanshan University, 2016, 40(6): 481-486.
GUO Xue-yi, CHEN Yuan-lin, TIAN Qing-hua, WANG Qin-meng
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: The metallurgy industry is a strong support for economic and a major carbon emission industry in China. Hydrogen metallurgy is regarded as a vibrant research branch in developing efficient metallurgical technologies with low-carbon emission at present. Therefore, hydrogen metallurgical technology has been concerned worldwide. In the present paper, the recent developments of theory researches and applications of hydrogen metallurgical technology in the fields of extractive metallurgy of ferrous metals and nonferrous metals, and secondary resources utilization are systematically reviewed. As a gaseous reducing agent, H2 possesses a stronger reduction capacity than CO at the temperature higher than 810 Ўж. And the reduction reaction rate of H2 is higher than that of carbon reducing agent with 1 to 2 orders of magnitude. The direct reduction iron making technology based on hydrogen metallurgy is in the stage of steady development, its application includes the typical processes Midrex and HYL-ўу, and some other new projects, such as EuropeЎҜs ULCOS, Sweden's HYBRT, JapanЎҜs COURSE50, and China's Zhongjin Mining. While the researches of hydrogen metallurgy in the fields of extractive metallurgy of nonferrous metals and secondary resource utilization are in theoretical study stage, and further technical breakthrough is in needed. The production of hydrogen with large scale and low cost and the thermal balance in hydrogen metallurgy process are the key problems to be solved in the future.
Key words: hydrogen metallurgy; extractive metallurgy of ferrous metals; extractive metallurgy of nonferrous metals; secondary resource utilization; thermodynamics; kinetics
Foundation item: Project(2019YFC1907400) supported by the National Key Research and Development Program of China; Projects (51904351, 51620105013) supported by the National Natural Science Foundation of China; Project(2019SK2061) supported by the Key Research and Development Program of Hunan Province, China; Project(2020CX028) supported by the Innovation Driven Program of Central South University, China
Received date: 2020-08-25; Accepted date: 2020-11-06
Corresponding author: WANG Qin-meng; Tel: +86-13574812541; E-mail: qmwang@csu.edu.cn
(ұајӯ әОС§·ж)
»щҪрПоДҝЈә№ъјТЦШөгСР·ўјЖ»®ЧКЦъПоДҝ(2019YFC1907400)Ј»№ъјТЧФИ»ҝЖС§»щҪрЧКЦъПоДҝ(51904351,51620105013)Ј»әюДПКЎЦШөгБмУтСР·ўјЖ»®ЧКЦъПоДҝ(2019SK2061)Ј¬ЦРДПҙуС§ҙҙРВЗэ¶ҜПоДҝ(2020CX028)
КХёеИХЖЪЈә2020-08-25Ј»РЮ¶©ИХЖЪЈә2020-11-06
НЁРЕЧчХЯЈәНхЗЧГНЈ¬ёұҪМКЪЈ¬І©КҝЈ»өз»°Јә13574812541Ј»E-mailЈәqmwang@csu.edu.cn

