文章编号:1004-0609(2012)08-2276-07
以Mn3O4为前驱体制备
尖晶石型LiMn2O4及其性能
王英平1,王先友1,隗小山2,魏启亮1,杨秀康1,杨顺毅1,舒洪波1,白艳松1,吴 强1
(1. 湘潭大学 化学学院 环境友好化学与应用教育部重点实验室,湘潭 411105;
2. 湖南石油化工职业技术学院,岳阳 414012)
摘 要:采用改进的固相反应法合成了高性能的锂离子电池正极材料LiMn2O4。首先,以廉价的MnSO4为原料,通过水解-氧化法制备纳米级Mn3O4前驱体;然后,将Mn3O4和Li2CO3混合均匀,在750 ℃固相反应20 h,得到尖晶石型LiMn2O4。用X射线衍射(XRD)和扫描电镜(SEM)对Mn3O4前驱体和LiMn2O4样品进行表征,用充放电测试和循环伏安技术对LiMn2O4样品进行电化学性能研究。结果表明:所制备的LiMn2O4具有完整的尖晶石型结构,且晶体粒子分布均匀。所制备的LiMn2O4材料在3.0~4.4 V之间,室温(25 ℃)下,在0.2C倍率下首次放电比容量为130.6 mA・h/g;在0.5C倍率下首次放电比容量为127.1 mA・h/g,30次循环后,容量仍有109.5 mA・h/g,且样品具有较好的高温性能。
关键词:锂离子电池;正极材料;尖晶石LiMn2O4;水解-氧化法;Mn3O4前驱体
中图分类号:TM 912 文献标志码:A
Preparation process and performance of spinel LiMn2O4 using Mn3O4 as precursor
WAGN Ying-ping1, WANG Xian-you1, KUI Xiao-shan2, WEI Qi-liang1, YANG Xiu-kang1,
YANG Shun-yi1, SHU Hong-bo1, BAI Yan-song1, WU Qiang1
(1. School of Chemistry, Key Laboratory of Environmentally Friendly Chemistry and Applications,
Ministry of Education, Xiangtan University, Xiangtan 411105, China;
2. Hunan Petrochemical Vocational Technology College, Yueyang 414012, China)
Abstract: LiMn2O4 with high-performance for the application of lithium-ion batteries was successfully synthesized by a modified solid phase reaction route. First, the precursor Mn3O4 was prepared by a hydrolyzation -oxidation method using cheap MnSO4 as Mn source. Then, the as-prepared precursor Mn3O4 and Li2CO3 were mixed homogeneously and calcined at 750 ℃ for 20 h to obtain spinel LiMn2O4. The properties of samples were characterized by XRD and SEM, charge-discharge tests and cyclic voltammetry. The results show that the as-prepared LiMn2O4 has spine structure and exhibits uniform particle size distribution. The initial discharge capacities of the as-prepared LiMn2O4 are as high as 130.9 mA・h/g at 0.2C and 127.1 mA・h/g at 0.5C in the voltage range of 3.0-4.4 V at 25 ℃, especially, the discharge capacity at 30th cycle still keep to be 109.5 mA・h/g at 0.5C. Besides, the as-prepared LiMn2O4 presents good high temperature performance.
Key words: lithium ion battery; cathode material; spinel LiMn2O4; hydrolyzation-oxidation method; Mn3O4 precursor
相比镍氢、镍镉和铅酸电池,锂离子二次电池具有无记忆效应、能量密度高、工作电压高、循环寿命长的优势,是性能卓越的新一代绿色环保、可再生的化学能源[1-2]。正极材料是制造锂离子电池的关键材料之一。目前,商业化锂离子电池正极材料主要有LiCoO2、尖晶石型LiMn2O4和LiFePO4,其中尖晶石型LiMn2O4材料具有原材料丰富、价格便宜、无毒、无污染、安全性好等优点,被认为是最具有发展潜力的锂离子动力电池正极材料之一[3-6]。研究表明[7-8],电极材料的电化学性能与材料结构的完整性、粒径大小和粒度分布以及形貌等物理化学性能密切相关,而其物理化学性能则主要取决于它们的合成方法。尖晶石型LiMn2O4材料的合成方法大体上可以分为两大类:固相合成和湿化学合成。其中固相法是制备锰酸锂材料的传统方法,具有工艺简单、制备条件容易控制和易于工业化生产等优点,因而被广泛采用[9]。
传统固相法多采用电解MnO2(EMD)为锰源制备LiMn2O4,但是EMD晶体结构为γ-MnO2,颗粒分布不均匀,且含有杂质如Na+和SO42-等,杂质的存在通常会增大LiMn2O4的电化学阻抗,且导致储能过程中的可逆容量衰减加剧[10-11]。近年来,科学家们考虑用锰的其他氧化物作为锰源来制备尖晶石型LiMn2O4,如Mn2O3[12-13]、Mn3O4[14]和γ-MnOOH[15]等。其中Mn3O4是一种很重要的多功能氧化物,广泛应用于催化、磁性材料以及空气净化等领域[16],目前,其在锂离子电池正极材料中的应用受到了极大的关注。PU等[17]通过控制结晶法制备了Mn3O4前驱体,并以Mn3O4前驱体为锰源,制备了尖晶石型LiMn2O4材料,发现其具有较好的电化学性能,首次放电比容量为128 mA・h/g,但该方法的工艺条件控制较苛刻,难以工业化生产。PARK等[18]用超声波法制备了纳米级Mn3O4,并与LiOH混合,制备了纳米级的LiMn2O4,超声波法虽然操作简单,但是大规模化生产尚待努力。本文作者改进Mn3O4的制备工艺路线,以廉价MnSO4为原料,提出用水解-氧化法合成Mn3O4前驱体,并与Li2CO3混合,通过固相反应合成尖晶石型LiMn2O4,并对所合成材料的结构特性和电化学性能进行研究。
1 实验
1.1 前驱体Mn3O4材料的制备
硫酸锰在氨性介质中水解沉淀:称取一定量的硫酸锰溶解于100 mL蒸馏水中,在60 ℃的水浴中搅拌,逐滴加入浓氨水,调节pH=9.5左右,得到Mn(OH)2沉淀,冷却后抽滤,反复洗涤,直至滤液中检测不到SO42-。
Mn(OH)2氧化制备Mn3O4前驱体:将上述滤饼放入烧杯中,加入100 mL蒸馏水,置于50 ℃的水浴锅中,搅拌,加入45 mL乙醇作为分散剂;逐滴加入适量的10%H2O2溶液,控制滴加速度,并不断搅拌至H2O2加完即止,冷却后抽滤,洗涤,干燥(在120 ℃干燥箱中,时间为6 h),即得Mn3O4前驱体。
1.2 尖晶石型LiMn2O4的制备
按n(Li):n(Mn)=1:2称取一定量的Li2CO3和制备的Mn3O4前驱体,置于研钵中,加入乙醇,将原料调制成为流变相,研磨混合均匀。待乙醇完全挥发后,将样品装入坩埚中,然后置于马弗炉内,以5 ℃/min的速率,升温至750 ℃,焙烧20 h,自然冷却至室温,即得尖晶石型LiMn2O4材料,标记为S-1。作为对比,以EMD为锰源,Li2CO3为锂源,在同样条件下反应得到尖晶石型LiMn2O4材料,标记为S-2。
1.3 材料结构与形貌的表征测试
采用日本理学D/max-3C型X射线衍射仪(XRD)对样品进行物相分析,使用Cu Kα靶,λ=0.154 056 nm,石墨单色器,管电流100 mA,管电压50 kV,扫描角度为10°~80°(2θ)。用日本JEOL公司JSM-5600LV型扫描电子显微镜(SEM)观察样品的粒径和形貌。
1.4 材料的电化学性能测试
以NMP为溶剂,将LiMn2O4、乙炔黑、石墨和PVDF按质量比80:5:5:10混合均匀成正极浆液,涂覆在铝箔上,120 ℃真空干燥12 h。以Celgard2400聚丙烯多孔膜为隔膜,1 mol/L LiPF6的碳酸乙烯酯(EC)和二乙基碳酸酯(DEC)混合液(V(EC):V(DEC)=1:1,韩国三星公司)为电解液,金属锂片为负极,在充满氩气的手套箱内组装成扣式电池。在深圳新威尔电子有限公司生产的NEWARE电池测试系统进行充放电性能测试,电压测试范围为3.0~4.4 V;在上海辰华仪器公司生产的CHI660电化学工作站进行循环伏安测试,循环伏安测试电压范围为3.0~4.4 V,扫速为0.05 mV/s。
2 结果与讨论
2.1 前驱体Mn3O4材料的物相分析
通过水解-氧化法制备Mn3O4前驱体,其反应原理如下:
MnSO4+2NH3・H2O=Mn(OH)2↓+(NH4)2SO4
3Mn(OH)2+H2O2=Mn3O4+4H2O
图1所示为Mn3O4样品的XRD谱。从图1中可看出,制备的Mn3O4样品的各衍射峰位置与标准图谱(JCPDS#80-0382)中各峰的位置基本吻合,为四方晶系结构,其中5个强峰的位置、晶面指数和半峰宽分别为2θ=18.014°,(101),d=0.486 nm;2θ=29.072°,(112),d=0.307 nm;2θ=32.546°,(103),d=0.275 nm;2θ=36.279°,(211),d=0.247 nm;2θ=60.029°,(224),d=0.154 nm。各衍射峰的d值和相对强度与标准卡片(JCPDS#80-0382)的数据基本一致,证明产物为Mn3O4。表1所列为所制备的Mn3O4样品及标准谱的晶格常数,Mn3O4样品的参数值略小于标准参数值,但差别不大,在误差范围内。此外,从图谱上可以看到,Mn3O4样品的衍射峰尖锐,说明Mn3O4样品的结晶度高。图2所示为制备的Mn3O4样品的SEM像。从图2中可以看出,通过水解-氧化两步法所制备的Mn3O4前驱体颗粒分布均匀,且颗粒较小,为纳米级。纳米级的前驱体粒子可以与Li2CO3充分接触,混合均匀,使固相反应进行得更充分,从而形成粒径分布均匀的LiMn2O4。

图1 Mn3O4样品的XRD谱
Fig. 1 XRD patterns of Mn3O4 sample
表1 Mn3O4样品的晶格常数
Table 1 Lattice parameters of Mn3O4 sample


图2 Mn3O4样品的SEM像
Fig. 2 SEM image of Mn3O4 sample
2.2 LiMn2O4样品的结构和形貌分析
图3所示为LiMn2O4的XRD谱。从图3中可以看出,LiMn2O4样品的衍射峰均与尖晶石型LiMn2O4的标准图谱(JCPDS#88-1749)的衍射峰完全吻合,没有出现任何其它杂质峰,表明材料具有结晶完整的尖晶石结构,属于Fd3m面心立方结构。尖晶石结构的LiMn2O4是以氧原子的立方堆积为骨架,其中Li+占据四面体的8a位置,Mn4+占据八面体的16d位置,在立方晶胞间隔的像限中形成四面体簇。空的八面体16c位形成了1个近似三维结构的共边八面体位,所以[Mn2]O4阵列被认为是密堆积的主体框架结构,其中四面体晶格8d、48f和八面体晶格16c共面而构成互通的三维离子通道[19]。从图3中还可以看出,样品S-1的衍射峰比较尖锐,而样品S-2的衍射峰较为宽泛,说明制备的LiMn2O4样品S-1具有较高的结晶度,结晶度越高,材料的循环性能就越好。表2所列为基于5个强峰(111)、(311)、(400)、(511)和(440)计算出的LiMn2O4的晶格常数。由表2可知,用Mn3O4为锰源制备的LiMn2O4样品S-1和用EMD为锰源制备的LiMn2O4样品S-2的晶格常数均与标准值相接近,且样品S-1的晶格常数比样品S-2的略有增大。尖晶石型LiMn2O4具有三维隧道,适于锂离子在充放电过程中的脱嵌,当晶格常数a较大时,三维隧道相应增大,锂离子脱嵌更容易,因而样品S-1的电化学性能更好。
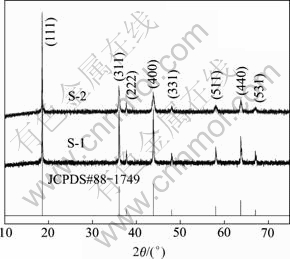
图3 LiMn2O4样品的XRD谱
Fig. 3 XRD patterns of LiMn2O4 samples
表2 LiMn2O4样品的晶格常数
Table 2 Lattice parameters of LiMn2O4 samples obtained by Rietveld refinement

LiMn2O4样品的SEM像如图4所示。由图4可以看出,LiMn2O4具有典型的立方结构,且样品的颗粒均较小。以Mn3O4为锰源制备的LiMn2O4样品S-1晶体颗粒分布均匀、粒径均一,且粒子的形貌清晰、规则,晶界明显,无软团聚现象。而以EMD为锰源制备的LiMn2O4样品S-2,颗粒不均匀,有团聚现象出现,粒径分布范围较广。这是由于样品S-1所采用的锰源Mn3O4前驱体颗粒大小一致,且分散均匀,易于和锂源充分混合均匀,形成颗粒分布均匀的LiMn2O4材料。因此,以氧化-还原法制备的Mn3O4为前驱体制备LiMn2O4在很大程度上改善了其产品颗粒分布的均匀性。

图4 LiMn2O4样品的SEM像
Fig. 4 SEM images of LiMn2O4 samples: (a) S-1; (b) S-2
2.3 样品的电化学性能分析
图5所示为LiMn2O4样品在0.2C倍率下的首次充放电曲线。从图5中可见,样品S-1和S-2的首次充放电曲线均有两个明显的充放电平台,表明锂的脱嵌是分两步进行的[20-21],主要是由于在LiMn2O4 的正尖晶石型结构中,占据8a位置的Li+首先一部分从四面体的8a位置嵌入(或脱出),此时克服的是Li+之间的相互作用力,然后另一部分Li+从四面体余下的8a位置嵌入(或脱出),每个嵌入(或脱出)Li+将受到相邻4个Li+的相互作用,它们之间的相互作用导致能量的分裂,所以锂的嵌入和脱出各出现两个稳定的电压平台。在0.2C倍率下,以Mn3O4为锰源制备的样品S-1的首次充电的平台为4.02 V和4.15 V,放电平台为3.97 V和4.11 V,首次放比电容量高达130.6 mA・h/g,而以EMD为锰源制备的样品S-2的首次充电平台为4.00 V和4.17 V,放电平台为3.93 V和4.09 V,首次放电比容量为119.0 mA・h/g。相比而言,样品S-1不仅具有较高的首次放电比容量,且放电电压较高,放电平台更为平坦。

图5 LiMn2O4样品在0.2C倍率下首次充放电曲线
Fig. 5 Initial charge-discharge curves of LiMn2O4 samples at 0.2C
LiMn2O4样品的循环性能如图6所示。在室温(25 ℃)下,样品S-1和S-2在不同倍率(0.5C、1C、2C)下的循环性能如图6(a)、(b)和(c)所示。从图6(a)、(b)和(c)中可以看出,在0.5C、1C和2C倍率下,样品S-1的首次放电比容量分别为127.1、124.0和105.1 mA・h/g,30次循环之后为109.5、99.0和82.1 mA・h/g,100次循环之后,比容量仍有96.2、86.9和75.5 mA・h/g;样品S-2的首次放电比容量分别为119.3、105.3和95.9 mA・h/g,30次循环之后为80.9、71.7和65.9 mA・h/g。图6(d)所示为LiMn2O4样品在1C倍率下的高温(55 ℃)循环性能曲线。由图6(d)可知,在55 ℃时,1C倍率下,样品S-1的首次放电容量为120.7 mA・h/g,100次循环之后,容量仍有74.7 mA・h/g;而样品S-2的首次放电容量为102.3 mA・h/g,100次循环之后,容量只有39.6 mA・h/g。由此可见,样品S-1在常温下具有较高的首次放电比容量、较好的倍率性能和循环稳定性,在高温下,同样具有良好的循环稳定性。这是由于样品S-1结晶度高,颗粒分布较均匀。如果正极材料粉体的粒度分布不均匀,在进行充放电循环时,容易造成小颗粒过放,以及大颗粒局部成分不均匀造成较大内应力,从而致使电池的容量衰减[22]。因此,以Mn3O4为锰源制备的LiMn2O4样品S-1在很大程度上提高了锂离子电池的循环稳定性。

图6 不同放电倍率下样品的循环性能
Fig. 6 Cycle performance of samples at different discharge rates: (a) 0.5C, 25 ℃; (b) 1C, 25 ℃; (c) 2C, 25 ℃; (d) 1C, 55 ℃
图7所示为LiMn2O4样品在电压为3.0~4.4 V,扫描速率为0.05 mV/s时的伏安曲线。从图7中可以看到,在扫描电压范围内,LiMn2O4样品均有两个明显的氧化还原峰。样品S-1的氧化峰电位分别为4.18和4.05 V,还原峰电位分别为4.07和3.94 V,两对氧化峰与还原峰间的电位差均为0.11 V;样品S-2的氧化峰电位分别为4.19和4.07 V,还原峰电位分别为4.05和3.92 V,两对氧化峰与还原峰间的电位差为别为0.14和0.15 V。样品S-1的两对氧化还原峰和样品S-2的两对氧化还原峰之间的电位差相差不大,由此可知,用Mn3O4为锰源制备的LiMn2O4样品S-1和用EMD为锰源制备的LiMn2O4样品S-2具有相同的脱嵌锂机理,锂离子的脱出和嵌入是分两步进行的,即[23]
LiMn2O4?Li1-xMn2O4+xLi++xe (x<0.5)
Li1-xMn2O4?LiMn2O4+(1-x)Li++(1-x)e (x>0.5)
从图7中还可以看出,样品S-1的氧化还原峰较样品S-2的尖锐。通过对样品S-1和S-2曲线所包围的面积进行积分,可以发现样品S-1的氧化峰面积和还原峰面积基本相当;而样品S-2氧化峰的面积大于还原峰的面积,表明样品S-1具有较高的充放电效率,这主要是由于样品S-1的晶体粒子分布均匀,粒径较小,锂离子的扩散路径短,扩散阻力小。
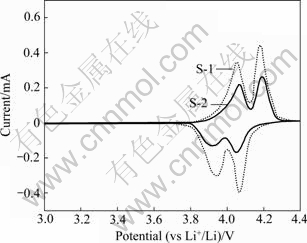
图7 样品在0.05 mV/s扫描速度下的循环伏安曲线
Fig. 7 Cyclic voltammograms of samples at scan rate of 0.05 mV/s
3 结论
1) 与传统固相法制备的LiMn2O4材料相比,采用改进固相法合成的LiMn2O4具有较高的结晶度,且晶体颗粒分布均匀、粒径均一。
2) 在室温时,改进固相法制备的LiMn2O4材料表现出具有较高的首次放电容量、较好的循环性能和良好的倍率性能,在0.5C倍率下首次放电比容量为127.1 mA・h/g,100次循环之后,容量仍有96.2 mA・h/g;在1C倍率下首次放电容量为124.0 mA・h/g,100次循环后容量为86.9 mA・h/g。高温(55 ℃)下,该材料仍然具有较好的电化学性能,在1C倍率下首次放电比容量为120.7 mA・h/g。
3) 与传统固相法制备的LiMn2O4材料相比,采用改进固相法制备的LiMn2O4材料不仅具有较好的形貌,且放电电压较高,放电平台更为平坦,电化学性能明显提高。
REFERENCES
[1] TARASCON J M, ARMAND M. Issues and challenges facing rechargeable lithium batteries[J]. Nature, 2001, 414(6861): 359-367.
[2] 李 荣, 陈昌国, 梁国明, 余丹梅. 锂离子电池正极材料LixMn2O4电子结构的量子化学DV-Xα研究[J]. 中国有色金属学报, 2004, 14(5): 865-870.
LI Rong, CHEN Chang-guo, LIANG Guo-ming, YU Dan-mei. Quantum chemical DV-Xα study on electronic structure of electrode material LixMn2O4 for lithium ion battery[J]. The Chinese Journal of Nonferrous Metals Society, 2004, 14(5): 865-870.
[3] FERGUS J W. Recent developments in cathode materials for lithium ion batteries[J]. Journal of Power Sources, 2010, 195(4): 939-954.
[4] KANG H K, AHN W, LEE S G, HAN K S, SONG J H, KWON O H, KANG E Y. Eutectic self-mixing method for the preparation of LiMn2O4 without any artificial mixing procedures[J]. Journal of Power Sources, 2006, 163(1): 166-172.
[5] 王先友, 易四勇, 肖 琼. 大容量锰酸锂动力电池的研制[J]. 湘潭大学自然科学学报, 2009, 31(2): 99-103.
WANG Xian-you, YI Si-yong, XIAO Qiong. The design and manufacture of high capacity Li-ion power battery with LiMn2O4 cathode[J]. Natural Science Journal of Xiangtan University, 2009, 31(2): 99-103.
[6] CHEN Ze-hua, HUANG Ke-long, LIU Su-qin, WANG Hai-yan. Preparation and characterization of spinel LiMn2O4 nanorods as lithium-ion battery cathodes[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(12): 2309-2313.
[7] CABANA J, VALDES SOLIS T, PALACIN M R, ORO SOLE J, FUERTES A, MARBAN G, FUERTES A B. Enhanced high rate performance of LiMn2O4 spinel nanoparticles synthesized by a hard-template route[J]. Journal of Power Sources, 2007, 166(2): 492-498.
[8] MOHAN RAO M, LIEBENOW C, JAYALAKSHMI M, WULFF H, GUTH U, SCHOLZ F. High-temperature combustion synthesis and electrochemical characterization of LiNiO2, LiCoO2 and LiMn2O4 for lithium-ion secondary batteries[J]. Journal of Solid State Electrochemistry, 2001, 5(5): 348-354.
[9] 蒋庆来, 胡国荣, 彭忠东, 杜 柯, 刘业翔. 二氧化锰原料对固相法制备尖晶石锰酸锂性能的影响[J]. 功能材料, 2010, 41(9): 1485-1489.
JIANG Qing-lai, HU Guo-rong, PENG Zhong-dong, DU Ke, LIU Ye-xiang. Influence of MnO2 materials on performance of spinel LiMn2O4 prepared by solid state method[J]. Journal of Functional Materials, 2010, 41(9): 1485-1489.
[10] GUO Hua-jun, LI Qi-hou, HE Fang-yong, LI Xin-hai, WANG Zhi-xing, PENG Wen-jie. The role of sulfate ions coming from source materials on the properties of Li1.05Mn2O4 cathode for lithium ion batteries[J]. Materials Chemistry and Physics, 2010, 124(2/3): 922-926.
[11] GUO Hua-jun, LI Xiang-qun, HE Fang-yong, LI Xin-hai, WANG Zhi-xing, PENG Wen-jie. Effects of sodium substitution on properties of LiMn2O4 cathode for lithium ion batteries[J]. Transactions Nonferrous Metals Society of China, 2010, 20(6): 1043-1048.
[12] JU S H, KIM D Y, JO E B, KANG Y C. LiMn2O4 powers prepared from nano-sized manganese oxide powders[J]. Journal of the Ceramic Society of Japan, 2007, 115(4): 241-244.
[13] 何向明, 蒲薇华, 蔡 砚, 姜长印, 万春荣, 夏定国. 基于控制结晶法制备的锂离子电池正极材料球形锰酸锂[J]. 中国有色金属学报, 2005, 15(9): 1390-1395.
HE Xiang-ming, PU Wei-hua, CAI Yan, JIANG Chang-yin, WAN Chun-rong, XIA Ding-guo. Preparation of spherical LiMn2O4 for Li-ion batteries based on controlled crystallization[J]. The Chinese Journal of Nonferrous Metals Society of China, 2005, 15(9): 1390-1395.
[14] LEE K S, MYUNG S T, BANG H J, CHUNG S, SUN Y K. Co-precipitation synthesis of spherical Li1.05M0.05Mn1.9O4 (M=Ni, Mg, Al) spinel and its application for lithium secondary battery cathode[J]. Electrochimica Acta, 2007, 52(16): 5201-5206.
[15] BAO Shu-juan, LI Chang-ming, LI Hu-lin, LUONG H T. Morphology and electrochemistry of LiMn2O4 optimized by using different Mn-sources[J]. Journal of Power Sources, 2007, 164(2): 885-889.
[16] BERBENNI V, MARINI A. Solid state synthesis of lithiated manganese oxides from mechanically activated Li2CO3-Mn3O4 mixtures[J]. Journal of Analytical and Applied Pyrolysis, 2003, 70(2): 437-456.
[17] PU Wei-hua, HE Xiang-ming, ZHANG Guo-yun, JIANG Chang-yin, WAN Chun-rong, ZHANG Shi-chao. Preparation of spherical spinel LiMn2O4 cathode material for lithium ion batteries[J]. Key Engineering Materials, 2007, 336/338: 477-480.
[18] PARK J P, KIM S K, PARK J Y, HWANG C H, CHOI M H, KIM J E, OK K Mi, KWAK H Y, SHIM Il-W. Syntheses of Mn3O4 and LiMn2O4 nanoparticles by a simple sonochemical method[J]. Materials Letters, 2009, 63(26): 2201-2204.
[19] 朱彦荣, 夏继才, 伊廷锋, 岳彩波, 诸荣孙, 贾志刚. 温度对LiMn2O4正极材料嵌锂动力学的影响[J]. 电池工业, 2010, 15(4): 202-204.
ZHU Yan-rong, XIA Ji-cai, YI Ting-feng, YUE Cai-bo, ZHU Rong-sun, JIA Zhi-gang. Effect of temperature on kinetics of lithium ion insertion for Li-ion battery positive electrode material[J]. Chinese Battery Industry, 2010, 15(4): 202-204.
[20] YI Ting-feng, HAO Chun-li, YUE Cai-bo, ZHU Rong-sun, SHU Jie. A literature review and test: Structure and physicochemical properties of spinel LiMn2O4 synthesized by different temperatures for lithium ion battery[J]. Synthetic Metals, 2009, 159(13): 1255-1260.
[21] 薛 云, 陈 野, 张密林. 锰酸锂的制备及其在中性电解液中的电容性能[J]. 硅酸盐学报, 2006, 34(12): 1528-1531.
XUE Yun, CHEN Ye, ZHANG Mi-lin. Preparation and capacitive performance of lithium manganate in neutral electrolyte solutions[J]. Journal of the Chinese Ceramic Society, 2006, 34(12): 1528-1531.
[22] 李智敏, 罗 发, 苏晓磊, 朱冬梅, 周万城. LiMn2O4正极材料的合成及电化学性能[J]. 稀有金属材料与工程, 2007, 36(8): 1382-1385.
LI Zhi-min, LUO Fa, SU Xiao-lei, ZHU Dong-mei, ZHOU Wan-cheng. Synthesis and electrochemical properties of LiMn2O4 cathode material[J]. Rare Metal Materials and Engineering, 2007, 36(8): 1382-1385.
[23] 蔡 羽, 朱金娥, 李董轩, 赵胜利. 螯合剂量和锂锰比对尖晶石LiMn2O4性能的影响[J]. 热加工工艺, 2009, 38(16): 59-62.
CAI Yu, ZHU Jin-e, LI Dong-xuan, ZHAO Sheng-li. Effect of chelator content and Li/Mn ratio on properties of spinel LiMn2O4[J]. Hot Working Technology, 2009, 38(16): 59-62.
(编辑 李艳红)
基金项目:国家自然科学基金资助项目(20871101);科技部科技计划项目(2009GJD20021);湖南省科技厅计划项目(2010WK4007);湖南省科技计划项目(2010TC2004);湖南省自然科学市州联合基金重点资助项目(09JJ8001)
收稿日期:2011-07-15;修订日期:2011-11-25
通信作者:王先友,教授,博士;电话:0731-8293061;E-mail: wxianyou@yahoo.com