文章编号:1004-0609(2008)09-1721-06
锂离子电池Li(Ni3/8Co3/8Mn2/8)O2层状正极材料的
制备与电化学性能
胡传跃,郭 军,汪形艳
(湖南人文科技学院 化学与材料科学系,娄底 417000)
摘 要:采用液相共沉淀方法合成锂离子电池用Li(Ni3/8Co3/8Mn2/8)O2正极材料,以XRD、SEM、原子吸收光谱法和电池充放电循环测试方法表征Li(Ni3/8Co3/8Mn2/8)O2粉末的结构和性能。结果表明:900 ℃焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2粉末样品具有较好的综合电化学性能和良好的六角层状结构,阳离子混合度小,六角晶格有序性高,颗粒为由小晶粒结合而成的多晶体,平均粒径约为4.5 mm,I003/I104为1.25,R值为0.48,首次放电容量为172.9 mA・h/g(2.8~4.5 V, 0.1C倍率),0.2C倍率循环20次后电容量为首次循环放电容量的96.1%。
关键词:锂离子电池;正极材料;氢氧化物共沉淀;电化学性能
中图分类号:TQ 137.12;O 646.2 文献标识码:A
Synthesis and electrochemical properties of layered Li(Ni3/8Co3/8Mn2/8)O2 cathode material for lithium ion batteries
HU Chuan-yue, GUO Jun, WANG Xing-yan
(Department of Chemistry and Material Science, Hunan Institute of Humanities, Science and Technology,
Loudi 417000, China)
Abstract: The layered Li(Ni3/8Co3/8Mn2/8)O2 cathode material for lithium ion batteries was synthesized by hydroxide co-precipitation method. The structure and electrochemical properties of Li(Ni3/8Co3/8Mn2/8)O2 were characterized by X-ray diffractometry, scanning electron microscopy, atomic absorption spectroscopy, and galvanostatic charge-discharge cycling. The results show that Li(Ni3/8Co3/8Mn2/8)O2 powder sample synthesized at 900 ℃ for 10 h reveals good intergration electrochemical properties and well-ordered hexagonal layered structure with low cation mixing. The value of I003/I104 is 1.25. The value of R is 0.48. The particles with 4.5 mm size can be identified from SEM observations. The initial discharge capacity of the Li[Ni1/3Co1/3Mn1/3]O2 cathode is 172.9 mA・h/g in the voltage range of 2.8?4.5 V at 30 ℃ and 1C, and the initial capacity maintains 96.1% after 20 charge-discharge cycles at 0.2C.
Key words: lithium ion batteries; cathode material; hydroxide co-precipitation; electrochemical performance
LiCoO2具有低的不可逆容量损失和良好的循环性能,被广泛应用于商品化锂离子电池中。由于LiCoO2价格昂贵、实际容量不高,近年来,研究者们一直在探索LiCoO2的替代材料,如层状LiNiO2,尖晶石型LiMn2O4和橄榄石型LiFePO4。研究发现,化学计量组成的LiNiO2的合成困难,在电化学循环过程中容易发生结构降解[1?2],LiMn2O4因Jahn-Teller效应而导致容量衰减率严重[3?4],LiFePO4虽然具有良好的热稳定性、但电子阻抗大、使得LiFePO4的高倍率性能欠佳[5?8]。因此,人们开始注意Ni-Co-Mn三元系列过渡金属氧化物的在锂离子电池中的应用。
LIU等[9]首次报道了LiNi1?x?yCoxMnyO2(0<x<0.5,0<y<0.5)的镍钴锰三元过渡金属复合氧化物。作为锂离子电池正极材料,该复合氧化物综合了LiCoO2的良好循环性能、LiNiO2的高比容量和LiMn2O4的高安全 性,存在明显的协同效应,形成共熔体系。人们对镍钴锰三元过渡金属的各种配比进行了大量研究,如Li(Ni0.6Co0.2Mn0.2)O2[10]、Li(Ni1/3Co1/3Mn1/3)O2[11?17]和不同元素掺杂的Li(Ni1/3Co1/3Mn1/3)O2?zFz[18],Li(Ni0.333- Co0.333Mn0.29Al0.04)O2?zFz[19],Al-与Fe-掺杂的Li(Ni1/3- Co1/3Mn1/3)O2[20],Al2O3包覆的Li(Ni1/3Co1/3Mn1/3)O2[21],Li[Ni0.4Co0.2Mn(0.4?x)Mgx]O2?yFy[22]及LiNi0.8Co0.1Mn0.1- O2[23]等。
目前,关于镍钴锰三元正极材料的研究主要集中在材料的合成及电化学性能与结构的关系上,高密度、粒径分布均匀的球形LiNi1?x?yCoxMnyO2化合物的制备已成为研究热点。如何在保证其电化学性能的情况下,提高振实密度是LiNi1?x?yCoxMnyO2材料规模生产应用的关键。本文作者拟采用氢氧化物共沉淀法制备(Ni3/8Co1/8Mn3/8)(OH)2前驱体,然后与LiOH固相反应合成Li(Ni3/8Co3/8Mn2/8)O2材料,考察焙烧温度与焙烧时间对Li(Ni3/8Co3/8Mn2/8)O2的结构和性能的影响。
1 实验
1.1 实验仪器与实验原料
实验仪器如下:PHS?3C数字酸度计(上海鹏顺科学仪器有限公司);DZ?2BC型真空干燥箱(天津市泰斯特仪器有限公司);SGQ管式高温气氛炉(湘潭市中山仪器厂);FA2004型电子天平(上海良平仪器仪表有限公司);超级净化手套箱(米开罗那(中国)有限公司);BK?6016A/2 mA可充电电池性能检测设备(广州蓝奇电子实业有限公司)。
实验原料如下:NiSO4?6H2O(AR,天津市科密欧化学试剂有限公司);CoSO4?7H2O(AR,湖南湘中化学试剂有限公司);MnSO4?H2O(AR,天津市科密欧化学试剂有限公司);LiOH?H2O(AR,湖南湘中化学试剂有限公司);NaOH(AR,湖南汇虹试剂有限公司);NH3?H2O(湖南省株洲市化学工业研究所)。
1.2 实验方法
按化学计量比n(Ni)?n(Co)?n(Mn)=3?3?2将一定量的NiSO4・6H2O、CoSO4・7H2O和MnSO4・H2O混合,配制成2 mol/L混合溶液,然后加入一定量的NH3・H2O和2 mol/L的NaOH溶液,调节pH=11~12,在60 ℃和氮气气氛下,搅拌12 h制得前驱体沉淀。将前驱体过滤、洗涤、真空100 ℃干燥12 h,再与过量8%的LiOH・H2O(过量的锂盐用于补偿高温煅烧过程中损失的锂)混合,以行星式球磨机将其混合均匀,最后进行高温焙烧。焙烧制度如下:将混合粉末置于空气气氛中,以2 ℃/min速率升温至480 ℃、保温5 h,然后继续升温750~950 ℃、保温8~15 h,合成LiNi3/8Co3/8Mn2/8O2正极材料粉末。
物相分析采用Y?2000A型X射线衍射(XRD)分析仪(丹东奥龙射线仪器有限公司),30 kV,20 mA,步宽0.02?,扫描速度4 (?)/min,扫描范围(2θ)为10?~80?。
将活性材料、导电碳黑和PVDF粘结剂按质量比90.5?3.5?6.0混合制备电极。在氩气气氛的手套操作箱中,将活性电极、锂箔(负极)、隔膜和电解液1 mol/L LiPF6乙烯基碳酸酯(EC)-二甲基碳酸酯(DMC)-乙基甲基碳酸酯(EMC) (1?1?1,质量比)组装成R2025型扣式电池,进行电化学性能测试。采用可充电电池性能检测设备(BK?6016A/2,广州蓝奇电子实业有限公司)进行充放电循环测试,循环条件为:16 mA/g,2.8~4.5 V (vs Li/Li+),25 ℃。
2 结果与讨论
2.1 焙烧温度对材料相结构与电化学性能的影响
以氢氧化物共沉淀过程制备的棕色粉末(Ni1/3Co1/3Mn1/3)(OH)2前驱体,前驱体中过渡金属离子计量比采用原子吸收光谱分析。结果表明,n(Ni)?n(Co)? n(Mn)比为3?3?2。图1所示为不同温度焙烧10 h制备的Li(Ni3/8Co3/8Mn2/8)O2粉末的XRD谱。由图1可以看出, 前驱体的XRD谱中,2θ = 19?左右存在一个较强衍射峰,这是过渡金属Ni、Co和Mn氢氧化物产生的衍射峰,表明形成(Ni3/8Co3/8Mn2/8)- (OH)2共沉淀。与JCPDS卡片中α-NaFeO2标准衍射峰比较,结果表明:所有Li(Ni3/8Co3/8Mn2/8)O2粉末的衍射峰均与α-NaFeO2衍射峰完全对应,表明合成的样品具有典型的α-NaFeO2结构,属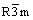 空间群和六方晶系。由XRD曲线中可以观察到明显的(006)/(102)和(018)/(110)分裂峰,表明合成的材料为具有层状结构的Li(Ni3/8Co3/8Mn2/8)O2活性材料。
空间群和六方晶系。由XRD曲线中可以观察到明显的(006)/(102)和(018)/(110)分裂峰,表明合成的材料为具有层状结构的Li(Ni3/8Co3/8Mn2/8)O2活性材料。
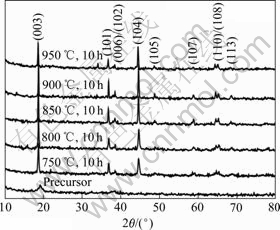
图1 不同温度10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的XRD谱
Fig.1 XRD patterns of Li(Ni3/8Co3/8Mn2/8)O2 synthesized at various temperatures for 10 h
部分研究者[24]以I003/I104的峰强度比表征镍钴锰三元过渡金属锂离子电池层状正极材料结构中阳离子的混合程度。当I003/I104>1.2时,则阳离子混合度小,材料层状结构良好。计算结果表明,当焙烧温度分别为750、800、850、900和950 ℃,反应时间为10 h时,Li(Ni3/8Co3/8Mn2/8)O2粉末样品中I003/I104比值依次为1.66、1.35、1.31、1.25和0.95。这说明除了950 ℃条件以外,在其余温度下均获得层状结构良好、阳离子混合度小的Li(Ni3/8Co3/8Mn2/8)O2样品。另外,有研究者以R因子(R = I102+I006)/I101)表征六角晶格的有序性,R数值愈小,则六角晶格有序性愈好[19, 24]。计算结果表明,焙烧温度分别为750、800、850、900和950 ℃时,Li(Ni3/8Co3/8Mn2/8)O2样品结构中R数值依次为0.38、0.59、0.53、0.48、0.68,表明在900 ℃和750 ℃合成的Li(Ni3/8Co3/8Mn2/8)O2样品具有较小的R因子,即样品结构具有较好的六角晶格有序性。
为了进一步研究合成条件对Li(Ni3/8Co3/8Mn2/8)O2的电化学性能的影响,实验中在室温、2.8~4.5 V (vs Li/Li+)电压范围,以16 mA/g的电流密度对测试电池进行充放电循环。图2所示为不同温度焙烧10 h制备的Li(Ni3/8Co3/8Mn2/8)O2的首次充放电曲线,首次循环后的交流阻抗图谱如图3所示,首次放电容量,放电效率和交流阻抗数据如表1所示。

图2 不同温度合成的Li(Ni3/8Co3/8Mn2/8)O2的0.1C倍率时的首次循环充放电曲线
Fig.2 Initial charge-discharge profiles of Li(Ni3/8Co3/8- Mn2/8)O2 synthesized at different temperatures and 0.1C

图3 不同温度焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的首次循环后的交流阻抗谱
Fig.3 Impedance patterns of Li(Ni3/8Co3/8Mn2/8)O2 powder synthesized at various temperatures for 10 h
表1 不同温度焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2材料首次循环放电容量和交流阻抗值
Table 1 Initial discharge capacity and impedance of Li(Ni3/8- Co3/8Mn2/8)O2 synthesized at various temperatures for 10 h
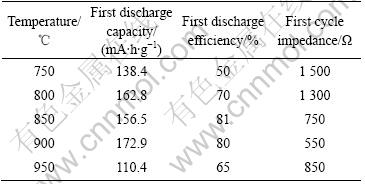
由图2可以看出,所有样品的充放电曲线平滑且单调。充电过程中,电池电压迅速升至3.75 V,然后保持在3.75~3.95 V之间,直到充电容量达到约100 mA・h/g后继续充电。由于在这电压范围内发生Ni2+/Ni4+氧化还原反应,电池的电压线性增加到4.5 V。由图2和表1的数据可知,在900 ℃焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2具有较高的首次放电容量(172.9 mA・h/g)和较高的首次放电效率(80%)。
图3所示为不同温度焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的首次循环后的交流阻抗谱。由图3可以看出,仅800 ℃合成的样品具有两个明显的半圆,其余样品的两个半圆因界面反应与电化学反应的频率区间重叠而成一个半圆。由图3和表1的数据可知,900 ℃焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的总交流阻抗(包括界面反应阻抗和电化学反应阻抗)最小,为550 Ω。
图4所示为不同温度烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的0.2C倍率循环寿命曲线。在750、800、850、900和950 ℃焙烧10 h合成的样品循环20次后,其放电比容量依次为105.1、130.5、141.0、166.2和97.5 mA・h/g,分别为首次放电容量的75.9%、80.2%、90.1%、96.1%和88.3%。
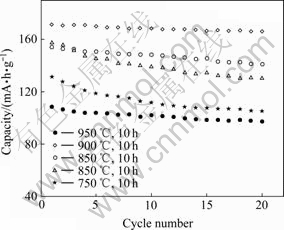
图4 不同温度焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的0.2C倍率循环寿命曲线
Fig.4 Discharge capacities as function of cycle number of Li(Ni3/8Co3/8Mn2/8)O2 (2.8?4.5 V) synthesized at different temperatures at 0.2C
根据以上结果讨论,900 ℃焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2具有较好的层状的结构与电化学性能。
2.2 反应时间对材料相结构与电化学性能的影响
图5所示900 ℃不同焙烧时间合成的Li(Ni3/8- Co3/8Mn2/8)O2的XRD谱。由图可知,焙烧8、10和15 h合成的Li(Ni3/8Co3/8Mn2/8)O2的XRD谱中存在(006)/(102)和(018)/(110)分裂峰,说明粉末样品具有较好的层状结构。900 ℃分别焙烧8、10和15 h合成的Li(Ni3/8Co3/8Mn2/8)O2的I003/I104值依次为1.55、1.25、1.20,R因子依次为0.36、0.48、0.72。其中I003/I104值大于或等于1.20,表明3个Li(Ni3/8Co3/8Mn2/8)O2样品具有较好的层状结构、阳离子混合度小,这与存在(006)/(102)和(018)/(110)分裂双峰的事实一致,焙烧8和10 h合成的样品的R值较小,六角晶格有序性更好。
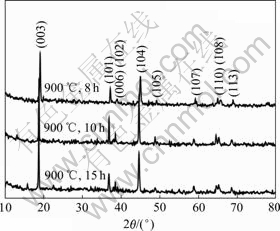
图5 900 ℃不同焙烧时间合成的Li(Ni3/8Co3/8Mn2/8)O2的XRD谱
Fig.5 XRD patterns of Li(Ni3/8Co3/8Mn2/8)O2 synthesized at 900 ℃ for different times
图6所示为900 ℃焙烧不同时间合成的Li(Ni3/8Co3/8Mn2/8)O2的首次充放电容量曲线,首次循环后的交流阻抗图谱如图7所示,首次放电容量、放电效率和交流阻抗数据如表2所示。结果表明,对焙烧8、10和15 h合成的3个Li(Ni3/8Co3/8Mn2/8)O2样品而言,900 ℃焙烧10 h合成的样品具有较低的充电电压平台和较高的放电电压平台、较高的放电容量(172.9 mA・h/g)和较低的交流阻抗(550 Ω)。而焙烧15 h合成的样品虽然放电效率高(99.6%),但放电容量较低(仅132.8 mA・h/g)、并且交流阻抗值高达1 300 Ω,表明锂离子的固相扩散和电化学反应所需的活化能较高。
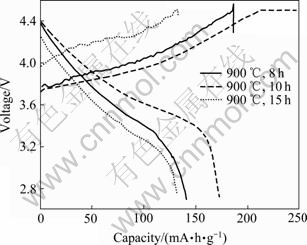
图6 900 ℃不同时间合成的Li(Ni3/8Co3/8Mn2/8)O2的0.1C倍率首次循环充放电曲线
Fig.6 Initial charge-discharge profiles of Li(Ni3/8Co3/8- Mn2/8)O2 synthesized at 900℃ for different times (2.8?4.5 V) at 0.1C
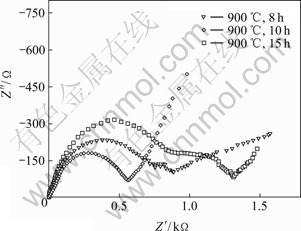
图7 900 ℃不同焙烧时间合成的Li(Ni3/8Co3/8Mn2/8)O2的首次循环后的交流阻抗谱
Fig.7 Impedance patterns of Li(Ni3/8Co3/8Mn2/8)O2 synthesized at 900 ℃ for different times
表2 900 ℃不同焙烧时间合成的Li(Ni3/8Co3/8Mn2/8)O2的首次循环放电容量与交流阻抗(0.1C)
Table 2 Initial discharge capacity and impedance of Li(Ni3/8Co3/8Mn2/8)O2 synthesized at 900 ℃ for different times
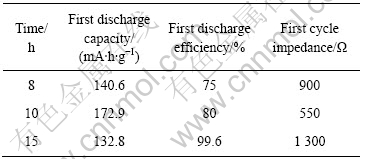
图8所示为900 ℃焙烧不同时间合成的Li(Ni3/8- Co3/8Mn2/8)O2的0.2C倍率循环寿命曲线。由图8可以看出,焙烧8、10和15 h合成的Li(Ni3/8Co3/8- Mn2/8)O2以0.2C倍率循环20次后的放电比容量依次为120.5、166.2和106.5 mA・h/g,分别为首次放电容量的85.7%、96.1%和80.2%,说明Li(Ni3/8Co3/8- Mn2/8)O2的循环性能开始随着焙烧时间的增加而升高,但焙烧时间达到15 h以上后样品的循环性能开始下降。
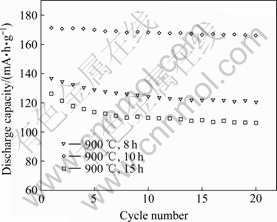
图8 900 ℃不同焙烧时间合成的Li(Ni3/8Co3/8Mn2/8)O2材料0.2C倍率循环寿命曲线
Fig.8 Discharge capacities as function of cycle number of Li(Ni3/8Co3/8Mn2/8)O2 synthesized at 900℃ for different times (2.8?4.5 V) at 0.2C
根据以上结果讨论可知,在900 ℃焙烧10 h制备的Li(Ni3/8Co3/8Mn2/8)O2具有较好的综合电化学性能和良好的层状结构,阳离子混合度小。
图9所示为900 ℃焙烧10 h后合成的Li(Ni3/8Co3/8Mn2/8)O2的SEM形貌。由图可以看出,合成的Li(Ni3/8Co3/8Mn2/8)O2粉末样品的平均粒径约为4.5 mm,由小晶粒附着而成的多晶体,并存在小晶粒的团聚现象。
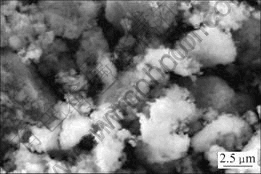
图9 900 ℃焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的SEM形貌
Fig.9 SEM image of Li(Ni3/8Co3/8Mn2/8)O2 synthesized at 900 ℃ for 10 h
3 结论
1) 900 ℃焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2的I003/I104比值为1.25, R值为0.48,首次放电容量为172.9 mA・h/g(2.8~4.5 V, 0.1C倍率),首次充放电容量效率为80%,首次循环后的交流阻抗值为550 Ω,0.2C倍率循环20次后,放电容量为166.2 mA・h/g(为首次放电容量的96.1%)。
2) 900 ℃焙烧10 h合成的Li(Ni3/8Co3/8Mn2/8)O2粉末具有较好的综合电化学性能和良好的层状结构、阳离子混合度小,六角晶格有序性高。由其SEM形貌可以看出,合成的Li(Ni3/8Co3/8Mn2/8)O2粉末是由小晶粒结合而成的多晶,平均粒径为约4.5 mm。
REFERENCES
[1] MOLENDA J, WILK P, MARZEC J. Structural, electrical and electrochemical properties of LiNiO2[J]. Solid State Ionic, 2002,146(1/2): 73?79.
[2] LEE K K, YOON W S, KIM K B, LEE K Y, HONG S T. Thermal behavior and the decomposition mechanism of electrochemically delithiated Li1?xNiO2[J]. J Power Sources, 2001, 97/98: 321?325.
[3] CHUNG K Y, KIM K B. Ivestigations into capacity fading as a result of a Jahn-Teller distortion in 4 V LiMn2O4 thin film electrodes[J]. Electrochimica Acta, 2004, 4(20)9: 3327?3337.
[4] TU J, ZHAO X B, XIE J, CAO G S, ZHUNAG D G, ZHU T J, TU J P. Enhanced low voltage cycling stability of LiMn2O4 cathode by ZnO coating for lithium ion batteries[J]. J Alloys and Compounds, 2007, 432: 313?317.
[5] KIM H S, CHO B W, CHO W L. Cycling performance of LiFePO4 cathode material for lithium secondary batteries[J]. J Power Sources, 2004, 132(1/2): 235?239.
[6] MELIGRANA G, GERBALDI C, TUEL A, BODOARDO S, PENAZZI N. Hydrothermal synthesis of high surface LiFePO4 powders as cathode for Li-ion cells[J]. J Power Sources, 2006, 160(1): 516?522.
[7] LIU H, LI C, ZHANG H P, FU L J, WU Y P, WU H Q. Kinetic study on LiFePO4/C nanocomposites synthesized by solid state technique[J]. J Power Sources, 2006, 159(1): 717?720.
[8] CHO D, PRASHANT I, KUMTA N. Surfactant based sol-gel approach to nanostructured LiFePO4 for high rate Li-ion batteries[J]. J Power Sources, 2007, 163(2): 1064?1069.
[9] LIU Z L, YU A S, LEE J Y. Synthesis and characterization of LiNi1?x?yCoxMnyO2 as the cathode materials of secondary lithium batteries[J]. J Power Sources, 1999, 81/82: 416?419.
[10] ZHANG Y, CAO H, ZHANG J, XIA B J. Synthesis of LiNi0.6Co0.2Mn0.2O2 cathode material by a carbonate co-precipitation method and its electrochemical characterization[J]. Solid State Ionics, 2006, 177(37/38): 3303?3307.
[11] MYUN S T, LEE M H, KOMABA S C, KUMAGAI N, SUN Y K. Hydrothermal synthesis of layered Li[Ni1/3Co1/3Mn1/3]O2 as positive electrode material for lithium secondary battery[J]. Eelectrochimica Acta, 2005, 50(24): 4800?4806.
[12] YU X Y, HU G M, PENG Z D, XIAO, LIU Y X. Synthesis and electrochemical characterization of layered Li[Ni1/3Co1/3Mn1/3]O2 cathode material for Li-ion batteries[J]. Trans nonferrous Met Soc China, 2005, 15(6): 1425?1428.
[13] CHO A H, SHIOSAKI Y, NOGUCHI H. Preparation and characterization of layered Li[Ni1/3Co1/3Mn1/3]O2 as cathode material by an oxalate co-precipitation method[J]. J Power Sources, 2006, 159(2): 1322?1327.
[14] NAOAKI Y, TSUTOMU O. Electrochemical behaviors of Li[Ni1/3Co1/3Mn1/3]O2 in lithium batteries at elevated temperature[J]. J Power Sources, 2005, 146(1/2): 636?639.
[15] LEE M H, KANG Y J, MYUNG S T, SUN Y K. Synthetic optimization of Li[Ni1/3Co1/3Mn1/3]O2 via co-precipitation[J]. Eelectrochimica Acta, 2004, 50(4): 939?948.
[16] LUO Xu-fang, WANG Xian-you, LIAO Li, WANG Xi-min, GAMBOA S, SEBASTIAN P J. Effects of synthesis conditions on the structural and electrochemical properties of layered Li[Ni1/3Co1/3Mn1/3]O2 cathode material via the hydroxide co-precipitation method LIB SCITECH[J]. J Power Sources, 2006, 161(1): 601?605.
[17] 刘智敏, 胡国荣, 方正升, 张新龙, 刘业翔. 超声喷雾热分解制备锂离子电池正极材料LiNi1/3Co1/3Mn1/3O2及表征[J]. 无机材料学报, 2007, 22(4): 637?641.
LIU Zhi-min, HU Guo-rong, FANG Zheng-sheng, ZHANG Xin-long, LIU Ye-xiang. Synthesis and characterization of LiNi1/3Co1/3Mn1/3O2 as a cathode material for lithium batteries by ultrasonic spray pyrolysis[J]. Journal of Inorganic Materials, 2007, 22(4): 637?641.
[18] HE Yu-shi, PEI Li, LIAO Xiao-zhen, MA Zi-feng. Synthesis of Li[Ni1/3Co1/3Mn1/3]O2?zFz cathode material from oxalate precursors for lithium ion battery[J]. J Fluorine Chemistry, 2007, 128(1): 139?143.
[19] LIAO Li, WANG Xiang-you, LUO Xu-fang, WANG Xi-ming, GAMBOA S, SEBASTIAN P J. Synthesis and electrochemical properties of layered Li[Ni0.333Co0.333Mn0.293Al0.04]O2?zFz cathode materials prepared by the sol-gel method[J]. J Power Sources, 2006, 160(1): 657?661.
[20] LIU Dao-tan, WANG Zhao-xiang, CHEN Li-quan. Comparison of structure and electrochemistry of Al- and Fe-doped LiNi1/3Co1/3Mn1/3O2[J]. Electrochimica Acta, 2006, 51(20): 4199?4203.
[21] KIM Y, KIM H S, MARGIN S W. Synthesis and electrochemical characteristics of Al2O3-coated LiNi1/3Co1/3Mn1/3O2 cathode materials for lithium ion batteries[J]. Electrochimica Acta, 2006(52): 1316?1322.
[22] SHIN H S, SHIN D, SUN Y K. Improvement of electrochemical properties of Li[Ni0.4Co0.2Mn(0.4?x)Mgx]O2?yFy cathode materials at high voltage region[J]. Electrochimica Acta, 2006, 52: 1477?1482.
[23] 王希敏, 王先友, 易四勇, 曹俊琪. 层状锂离子电池正极材料LiNi0.8Co0.1Mn0.1O2的制备及性能工巧匠[J]. 过程工程学报, 2007, 7(4): 817?821.
WANG Xi-min, WANG Xian-you, YI Si-yong, CAO Jun-qi. Synthesis and characteristics of layered LiNi0.8Co0.1Mn0.1O2 cathode material for lithium rechargeable batteries[J]. The Chinese Journal of Process Engineering, 2007, 7(4): 817?821.
[24] LI De-cheng, TAKAHISA M, ZHANG Lian-qi, MASAKI Y, HIDEYUKI N. Effect of synthesis method on the electrochemical performance of LiNi1/3Co1/3Mn1/3O2[J]. J Power Sources, 2004, 132(1): 150?155.
基金项目:湖南省自然科学基金项目(07JJ6082)
收稿日期:2008-01-21;修订日期:2008-06-18
通讯作者:胡传跃,讲师,博士;电话:0738-8325065;E-mail: huchuanyue@vip. sina. com
(编辑 龙怀中)