DOI: 10.11817/j.issn.1672-7207.2016.02.007
�����������Ʊ������ѻ����ܲ���
����1������2������Ƽ1������Ԫ1��������1
(1. ���ϴ�ѧ ��ѧ����ѧԺ������ ��ɳ��410083��
2. ���Ĵ�ѧ ��Ȼ��ת���ص�ʵ���ң����� ������750021)
ժҪ��Ϊ����Ч���������ѻ����ϵľ��͡��ṹ�������ɱ������һ�ֿ�ֱ���Ʊ��������������ѻ���Ʒ���·���������ĥ����������ĩ��ϡ���Ṥ�մ������ȫ��ת��Ϊ�����������װ����䳤�ȡ����Ⱥͺ�ȷֱ�Ϊ50~100��5~20��2~5 nm���о���������������������װ��������Ͼ��нϺõ�����Ӵ洢���ܡ�ͨ����ĥ�����ս��������մ��������ɻ�þ���˫�������Ķ������������������д��(50~80 nm)��Ӧ���ž���һ���������֮��ļ�϶��С��(3~20 nm)���Ӧ�������ӱ����ϵĶ������⣬����õĶ�ṹ�Ķ����������ײ�Ʒ��ʾ���ϸߵĹ�����ԡ�
�ؼ��ʣ���������ĥ���ѻ����ײ��ϣ����ܣ����
��ͼ����ţ�TM912.9 ���ױ�־�룺A ���±�ţ�1672-7207(2016)02-0401-07
Synthesis of titanium-based nanostructures from ilmenite
TAO Tao1, LI Peng2, HU Huiping1, CHEN Qiyuan1, YIN Zhoulan1
(1.School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Natural Gas Conversion, Ningxia University, Yinchuan 750021, China)
Abstract: It was found that a new method could be good for producing high quality titanium based nanomaterials to effectively control its morphology, structure and cost. Ball milling and acid solution treatment of natural ilmenite result in the products of TiO2 nanorods. The lengths, width and thickness of the nanorods are 50-100, 5-20 and 2-5 nm, respectively. The results show that the nanorods exhibit a good electrochemical performance when they are used as an anode material for the lithium-ion batteries. A method which includes ball milling, annealing and acid leaching to obtain porous TiO2 from ilmenite has been demonstrated. The porous products show a bimodal pore size distribution. The typical range of big pores (50-80 nm) is attributed to the spaces between nanoparticles in aggregates, and the typical range centered at 3-20 nm corresponds to holes within nanoparticles. The obtained porous TiO2 shows an excellent photocatalytic activity.
Key words: ilmenite; ball milling; titanium based nanomaterials; energy storage; photocatalysis
�����ѻ��������������������ܺ㷺����;�����ܸ���������Ա������[1-5]�����ѱ��ɹ���Ӧ���ڸ�����������������ӵ�غ�̫���ܵ��[6-7]�������ѻ����ϵĵ��Ӵ������ܡ�����������ﻯ����ǿ�ҵ��������侧��ṹ����������ò���ṹ��������Ϊ��Ч���������ѻ����ϵľ��ͺͽṹ��JUNG��[8-14]���Բ��ö��ֲ�ͬ��������ѧ���ֶΣ���ģ�巨��ˮ�Ⱥ��ܼ��ȷ����������Ը�ʴ���ܽ�-��������ԭ�Ӳ���������������Ĥ���������ȡ���Ȼ��Щ�������Ʊ������ѻ����Ϸ��涼���и��Ե����ƣ������Ǵ��ڹ�ͬ��ȱ�㣬���Ʊ������������̺�ԭ���ϳɱ�̫�ߣ���ˣ����������������ʵ�����������е�Ӧ�á�FeTiO3(������)Ϊ��Ȼ����������Դ���������ۡ����������ḻ���ŵ㣬��һ�ִ�϶����Ϊ2.54~2.58 eV�;������Դ����Եİ뵼�壬���������Ʊ��ѻ�����[15-19]����Ҫ�ֲ���������(����)��������(�Ĵ�����)��������(�����ͼ��ô�)������(ӡ�ȡ��й���Խ��) ŷ��(����˹��Ų��)�ͷ���(�ϷǺ�Īɣ�ȿ�)������2004��2008����г�����[16]�����������ԼΪ6.8��108 t����۸�Ϊ80~100��Ԫ/t������(3.5~4.0)��108 t�������ѡ��й��Ĵ���֦��������������״��Ƭ״����ʽ�ֲ��ڴ��������֮��������У�Ϊ���͵���������ء����⣬������������ɽ����Ų���Ŀ������ա�����˹��������ɽ�������������ݵ���ɽ�ͼ��ô�����˵İ����º��ȡ���ֱ��������Ȼ���������Ʊ������ѻ����ϣ�����ܻἫ��ؽ��������ѻ����ϵ������ɱ�����ˣ��ɷ�չ�¹��ջ��¼�������Ȼ������ֱ����ȡ���ײ��ϡ�������������Ȼ������Ϊԭ�ϣ�ͨ����ȷ�����Ʊ����գ����ڷֱ��ö�����������ѺͶ����������װ���Ʒ����������Ʒ�Ľṹ�����ܡ�
1 ʵ��
1.1 ԭ��
�������ɰĴ������ۺϽ��ʯ����˾(Consolidated Rutile Ltd., Australia������Ϊ99%)�ṩ���仯ѧ�ɷ�(��������)Ϊ��TiO2 49.6%, Fe(����) 35.1% (FeO 32.8%, Fe2O3 13.7%), Al2O3 0.47%, Cr2O3 0.25%, SiO2 0.45%������̿��Ӣ��BDH��ѧ�Լ�����˾�ṩ��
�������������Ʊ������ѻ����ϵĹ����У����õĹ������������ĥԤ���������ջ�ѧʪ���ȴ�����
1.2 ��ĥ
��Լ10 g����������4��ֱ��Ϊ25.4 mm�IJ������һ��װ����ĥ������ĥ����ĥʱ��Ϊ150 h����������Ϊ100 kPa �����ת��Ϊ160 r/min��������ĥ���̾��ڴ����ĸ��������½��У�������ˮƽ�����45��[8]��
1.3 TiO2���װ����Ʊ�
��1 g��������ĥ�ۻ���2 mol/L����������Һ(100 mL)�У���120 ���¼���2 h��ֹͣ���Ⱥ�ͨ�������ռ�������Ʒ������õ���Ʒ������ϴ�Ӻ��ں����к�ɣ�����¶�Ϊ90 �棬ʱ��Ϊ4 h����1 g��Һ������������ĥ�����õ���Ʒ���ܽ���4 mol/L������Һ��(100 mL)��ʱ��Ϊ4 h���ܽ��¶�Ϊ90 �档��Ӧ��ɺ�ͨ�������ռ�������Ʒ���������õ�����Ʒ����ϴ�Ӻ�ת���������к�ɣ����ʱ��Ϊ4 h���¶�Ϊ90 �档���е���Һ��������ͨ����ԡʵ�֣����ȹ��̰����Ž��裬�������ʺ㶨Ϊ800 r/min��
1.4 ���TiO2���������Ʊ�
�������Ϲ��մ����������Ʊ���״�ṹ�����������Ѳ�Ʒ���������հ��մ�����������Ⱥ�˳�ɾ����Ϊ��ĥԤ������̼�Ȼ�ԭ�������ܽ�Ϳ����б���4�����裺1) ��ĥ����4��ֱ��Ϊ25.4 mm�IJ��������6 g���ҵ�������ͻ���̿�Ļ����һ����ĥ��������е������������̿��������Ϊ4:1����ĥ����������������ͬ��2) ̼�Ȼ�ԭ��2 g��ĥ�������ˮƽ��ʽ¯�к���������´����¼��ȵ�1 000 �棬ʱ��ԼΪ30 min��������1 000 ���º���1 h��ֹͣ���Ⱥ�����Ʒ��Ȼ��ȴ������(���������)��3) �ܽ⣺����ԭ���պ����Ʒ(1 g)�ܽ���4 mol/L������Һ(100 mL)�У��ܽ��¶�Ϊ90 �棬ʱ��Ϊ4 h�������ܽ���̰����Ž���(800 r/min)���ܽ���ɺ�ͨ�������ռ�������Ʒ���������õ�����Ʒ����ϴ�Ӻ�ת���������к�ɣ�����¶�Ϊ90 �棬ʱ��Ϊ4 h��4) ���գ�����ɺ����Ʒ���ڹ�ʽ¯�С��������պ�600 ���±���2 h��
�ο�����[20-23]�����˲��ϱ��������ܲ���(���������ӵ��)��ȫ���̡�
2 ���������
2.1 �����������װ�
��ĥ������۾�����������������������������ò���������Եı仯��ͼ1��ʾΪ������ͨ����ĥ������������������������õ���Ʒ��ɨ��羵��Ƭ����羵��Ƭ����ͼ1(a)��֪�����������õIJ�Ʒ��òΪ���װ�״�ṹ����Щ���װ��ֲ����ܼ����䳤��Ϊ50~100 nm������Ϊ5~20 nm�����Ϊ2~5 nm����Ʒ��TEM������Ƭ��һ��֤ʵ��������
��״�ṹ������ò(ͼ1(b)��ͼ1(c))����Ӧ��ѡ����������ͼ֤�������װ��������ڽ��ʯ�͡�ͼ1(d)��ʾΪ�������װ��ֲ��ĸ߷ֱ���TEM��Ƭ��ͼ1(d)�еľ�����������������ʾ�����װ�2�����ھ����ļ��Ϊ0.33 nm��

ͼ1 ������ͨ����ĥ��������������������������Ʒ��ɨ��羵��Ƭ����羵��Ƭ
Fig. 1 SEM and TEM images of samples obtained by milled, alkali treated and acid leached ilmenite
ͼ2��ʾΪ���װ���Ʒ��XRD�ס���ͼ2��֪����ƷXRD����嶼��Ӧ���ķ����ʯ���������(JCPDS��01-076-1939)��֤ʵ��ͨ����ĥ�����������������մ�����Ȼ������ԭ�Ϻɻ�ô������ʯ�Ͷ������ѵ������װ���Ʒ��
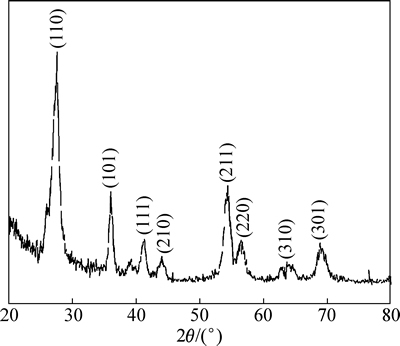
ͼ2 ������ͨ����ĥ����������������������������õ���Ʒ��X��������
Fig. 2 XRD patterns of products obtained from milled,alkali treated and acid leached ilmenite
��ĥ����ɽ���������ķ�Ӧ��ܣ��ӿ���������������Һ�е��ܽ��ٶȡ���ϴ����������ȥ�������е����ʣ��Ӷ���߲�Ʒ�Ĵ��ȡ�������������ȫ���ܽ����������������ɲ��ȶ����ε��м��࣬�м�������ˮ�Ⲣ���������Ķ������Ѿ��ˣ���Щ���˻����½ᾧ���۳��������γɶ����������װ���Ʒ����ˣ�������Ϊ������õĶ����������װ���Ʒ���γɻ������ܽ⡪ˮ�⡪����������
ͼ3(a)��ʾΪ�����������װ���Ϊ����ӵ�ظ���ʱ��ѭ���������ߡ���ͼ3(a)��֪����Ʒ��ѭ���������������Դ���1��������ԭ�� (1.81 V/1.91 V)�����ͼ��ֱ��ӦLi+�ڻ��Բ���TiO2��Ƕ���Ƕ���ķ�Ӧ��ͼ3(b)��ʾΪ�����������װ��缫��33.6 mA/g�����ܶȺ͵�ѹɨ�贰��1~3 V�µ�ѭ����������ͼ����ͼ3(b)��֪�����״ηŵ������Ϊ249.9 mA��h/g����������Ϊ157.5 mA��h/g��������������ʧ��92.0 mA��h/g�� ����100��ѭ����, �����������121.0 mA��h/g�����⣬�����Ч����ѭ�������г�ǰ6 �����������98%���ϣ�˵���缫��Ӧ���нϺõĿ����ԡ�ͼ3(c)��ʾΪ�䱶�����ܵIJ��Խ������ͼ3(c)��֪���������ܶȴ�168.0 mA/g������3.36 A/gʱ�����������Լ127.0 mA��h/g��Ϊ52.0 mA��h/g��˵���ϵ͵ĵ����ܶȿɻ�ø��ߵķŵ������������������ڽ�С�ĵ��������ڸ���Ļ���
���ϲ��봢�ܷ�Ӧ���������ܶȴ�33.6 mA/g���� 1.68 A/gʱ����30��ѭ����ı�������˥��Լ16 mA��h/g(��ͼ3(d))��ͼ3(e)��ʾΪ��ҵ�������ѿ���������������װ�100��ѭ���ĺ�����ŵ����ߡ���ͼ3(e)��֪�����װ�����������������ҵ����Ʒ�����װ��ϸߵ�����Ӵ洢���ܿ��ܹ���������صĽṹ������ ��Ϊ���װ�״�ṹ��������߲��ϱ����ĵ������������̵缫���ϳ�ŵ����������ӵĴ���·�������ҿ�ʹ���Һ��缫���ϳ�ֽӴ���

ͼ3 �����������װ��绯ѧ����
Fig. 3 Electrochemical properties of rutile TiO2 nanorods
2.2 ���������������
������ͻ���̿�Ļ����ͨ����ĥ�����ա����ܺ�����������4����������õIJ�Ʒ��TEM����Ƭ��ͼ4��ʾ����ͼ4(a)��֪����Ʒ�ľ�������С��100 nm����������Ӧ�ĵ�������(SADP)ͼ��ͼ4(b)��ʾ����һ��֤ʵ�˻�õIJ�ƷΪ���ʯ�͵Ķ������ѡ�ͼ4(c)��ͼ4(d)��ʾΪ����������TEM��Ƭ����ͼ4(c)��ͼ4(d)�ɼ�����ͷ����ʾ������Ϊ�����ϱ�������������ϲ���������С�ס�������ѡ������ĵ�������ͼ(��ͼ4(d)�еIJ����ͼ)������羵��Ƭ�е���Щ���������Ǵ�Խ�����������ҿĺ�ȵIJ�ͬ���ܵ��¶Աȶȵı仯����ˮƽ��ƫб���Ƶľ�����ֱ�Ϊ0.23 nm��0.28 nm�����Ӧ����Ϊ{200}��{101}��
ͼ5(a)��ʾΪ���TiO2��Ʒ�Ŀ��ֲ�ͼ����ͼ5(a)��֪����Ʒ�Ŀ�����˫��������TEM(��ͼ4��ʾ)�Ľ������С��(2~20 nm)��Ҫ�ֲ��ڿ������ڲ��ͱ��棬���(25~150 nm)��Ҫ�ֲ��ھۺ���һ���С����֮��ļ�϶�����궨������֪�����TiO2��ƷXRD��(��ͼ5(b)��ʾ)�б�����������������ʯTiO2�ı�ͼ�� (JCPDS file no. 01-077-0440)��ȫ�Ǻϣ���û�г������Ե��������ʵ�����壬˵����Ʒ�ǵ�һ��TiO2�ࡣ
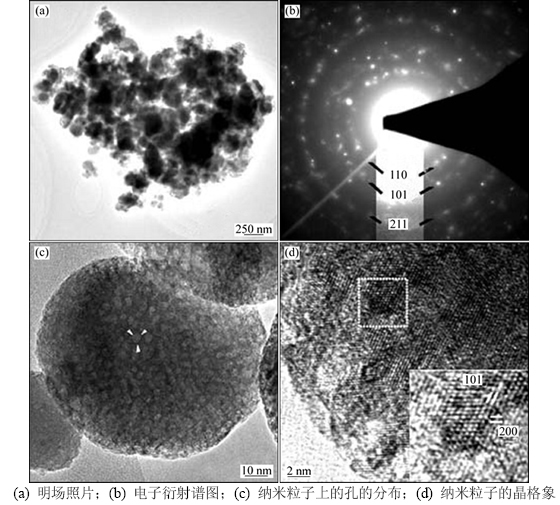
ͼ4 ����õĶ����Ʒ����羵��Ƭ
Fig. 4 TEM images of obtained porous samples
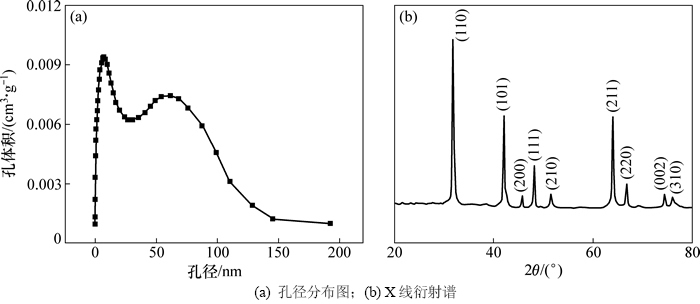
ͼ5 ����Ϳ�״�ṹ�Ķ������Ѳ�Ʒ�Ŀ��ֲ�ͼ��X��������
Fig. 5 Pore size distribution and XRD pattern of obtained rutile porous TiO2 products
��������ĥ���պ�ת��Ϊ�������Ѻ����Ļ�����ϲ��ᆳ����������������ʿɱ���ȥ���Ӷ���ö�ṹ�Ķ������Ѳ�Ʒ��������ʱ��϶�ʱ��������Ļ�ԭ�̶Ƚϵͣ������ʵ�������С��������������������γ�С�ף�������ʱ��ϳ�ʱ��������Ļ�ԭ�̶Ƚϸߣ������ʵ������ϴ������γɴ�ף�������ʱ������ʱ�������2�������������ʣ�������Ʒ�;���˫����������Ȼ���ܴ��ڶ�������Ӱ���Ķ������Ѳ�Ʒ�����ɣ�����ĥ��̼�Ȼ�ԭ����������еĸ��ֹ���������
ͼ6��ʾΪ��ṹ�Ľ��ʯ��TiO2����������ҵ���ʯ��TiO2��ĩ�������������������Խ����ÿ��ʵ���е���̼��Ϊ1 mg����ͼ6��֪����ҵ��������(������ֱ����100 nm���ȱ������130 m2/g)�Ͷ�ṹ�Ķ��������ڽ�����ʼ�Ĺ����ղ����ֱ�Ϊ360 nm��458 nm������ҵ��Ʒ�ڿɼ�������(�����ˣ�400 nm) û���κι����գ�����ṹ�IJ����ڽ����������������Դ��ں����������������������Ƕ�ײ����д��ڵ�ȱ�ݻ�������ʹ�����ڶ������ѵĵ��������ʴ��䷢��Ǩ��������ġ��ڴ���320 nm��������ڽ�ǿ�Ĺ����գ�˵����������Ѳ��Ͽ����ڿɼ����������һ���Ĺ�����ԣ������Ѿ���Խ�����о��ķ��롣��������Ѳ�Ʒ����ҵ�������ѵĹ�����ܵIJ��Խ��֤ʵ�˿�״�ṹ�Ķ������ѿ��л��ﱽ�ӵ��������Ը�����ҵ�������ѵ����ʣ��ҿ�״�ṹ�Ķ��������ܹ�����Һ�����е��л�̼��˵����ṹ�Ľ��ʯ�Ͷ��������нϸߵĹ�����ܣ���ϸߵĹ�����ܿ���������ò�������[24]��
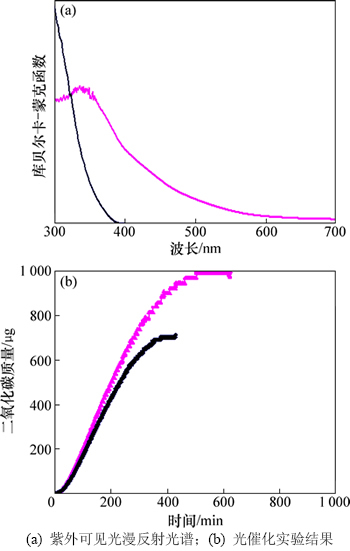
ͼ6 ����ɼ���������������ʵ�����Ա�
Fig. 6 UV-Vis diffuse reflectance spectra and results of photocatalytic tests
3 ����
1) ����Ȼ������Ϊԭ�ϣ����������Ϲ��������õ��˽ṹ��ͬ�������ѻ���Ʒ��
2) ͨ����ĥ����ϴ����������Դ���Ȼ����������ȡ�����Ľ��ʯ�Ͷ��������������������8 h��ȡ�ij���Ϊ50~100 nm������Ϊ5~20 nm�ͺ��Ϊ2~5 nm�����װ��������õĽᾧ�ԣ�����ö����������װ���Ϊ����ӵ�ظ���ʱ���нϺ�����Ӵ洢���ܡ�
3) �����۷ḻ��������ͻ���̿Ϊԭ�ϣ��������µ����Ϲ���(��ĥ�����ա����ܺ�����)������˴���������������ѿ�������ͨ�����ƹ�����������ʵ�ֲ�Ʒ���ĵ��ڡ�������Խ����������ṹ�Ľ��ʯ�Ͷ������Ѿ��н�ǿ�Ĺ����պ�����ܣ�����ߵ����ܿ��ܹ�����������Ķ�ṹ��
�ο����ף�
[1] CHEN X B, MAO S S. Titanium dioxide nanomaterials: synthesis, properties, modifications, and applications[J]. Chemical Reviews, 2007, 107(7): 2891-2959.
[2] CHEN Z H, BELHAROUAK I, SUN Y K, et al. Titanium-based anode materials for safe lithium-ion batteries[J]. Advanced Functional Materials, 2013, 23(8): 959-969.
[3] ROY P, BERGER S, SCHMUKI P. TiO2 nanotubes: synthesis and applications[J]. Angewandte Chemie International Edition, 2011, 50(13): 2904-2939.
[4] LIU Jiehua, LIU Xuewei. Two-dimensional nanoarchitectures for lithium storage[J]. Advanced Materials, 2012, 24(30): 4097-4111.
[5]  F, TALIN A A. Electrical contacts to one-and two-dimensional nanomaterials[J]. Nature Nanotechnology, 2011, 6(12): 773-783.
F, TALIN A A. Electrical contacts to one-and two-dimensional nanomaterials[J]. Nature Nanotechnology, 2011, 6(12): 773-783.
[6] YANG Z G, CHOI D W, KERISIT S, et al. Nanostructures and lithium electrochemical reactivity of lithium titanites and titanium oxides: a review[J]. Journal of Power Sources, 2009, 192(2): 588-598.
[7] ZHU Guannan, WANG Yonggang, XIA Yaoyong. Ti-based compounds as anode materials for Li-ion batteries[J]. Energy & Environmental Science, 2012, 5(5): 6652-6667.
[8] JUNG J H, KOBAYASHI H, VAN BOMMEL K J C, et al. Creation of novel helical ribbon and double-layered nanotube TiO2 structures using an organogel template[J]. Chemistry of Materials, 2002, 14(4): 1445-1447.
[9] TSAI M C, CHANG J C, SHEU H S, et al. Lithium ion intercalation performance of porous laminal titanium dioxides synthesized by sol-gel process[J]. Chemistry of Materials, 2009, 21(3): 499-505.
[10] GONG D, GRIMES C A, VARGHESE O K, et al. Titanium oxide nanotube arrays prepared by anodic oxidation[J]. Journal of Materials Research, 2001, 16(12): 3331-3334.
[11] PRADHAN S K, REUCROFT P J, YANG F Q, et al. Growth of TiO2 nanorods by metalorganic chemical vapor deposition[J]. Journal of Crystal Growth, 2003, 256(1/2): 83-88.
[12] KASUGA T, HIRAMATSU M, HOSON A, et al. Titania nanotubes prepared by chemical processing[J]. Advanced Materials, 1999, 11(15): 1307-1311.
[13] ARMSTRONG A R, ARMSTRONG G, CANALES J, et al. TiO2-B nanowires[J]. Angewandte Chemie International Edition, 2004, 43(17): 2286-2288.
[14] CHUNG C C, CHUNG T W, YANG T C K. Rapid synthesis of titania nanowires by microwave-assisted hydrothermal treatments[J]. Industrial and Engineering Chemistry Research, 2008, 47(7): 2301-2307.
[15] WELHAM N J. A parametric study of the mechanically activated carbothermic reduction of ilmenite[J]. Minerals Engineering, 1996, 9(12): 1189-1200.
[16] LI Chun, LIANG Bin, CHEN Sengpin. Combined milling�Cdissolution of Panzhihua ilmenite in sulfuric acid[J]. Hydrometallurgy, 2006, 82(1/2): 93-99.
[17] GINLEY D S, BUTLER M A. The photoelectrolysis of water using iron titanate anodes[J]. Journal of Applied Physics, 1977, 48(5): 2019-2021.
[18] ZHOU F, KOTRU S, PANDEY R K. Nonlinear current�Cvoltage characteristics of ilmenite�Chematite ceramic[J]. Materials Letters, 2003, 57(13/14): 2104-2109.
[19] MCDONALD P F, PARASIRIS A, PANDEY R K, et al. Paramagnetic resonance and susceptibility of ilmenite, FeTiO3 crystal[J]. Journal of Applied Physics, 1991, 69(2): 1104-1107.
[20] TAO T, GLUSHENKOV A M, CHEN Q Y, et al. Porous TiO2 with a controllable bimodal pore size distribution from natural ilmenite[J]. Cryst Eng Comm, 2011, 13(5): 1322-1327.
[21] TAO Tao, CHEN Ying, ZHOU Dan, et al. Expanding the applications of the ilmenite mineral to the preparation of nanostructures: TiO2 nanorods and their photocatalytic properties in the degradation of oxalic acid[J]. Chemistry: A European Journal, 2013, 19(3): 1091-1096.
[22] TAO Tao, CHEN Ying. Direct synthesis of rutile TiO2 nanorods with improved electrochemical lithium ion storage properties[J]. Materials Letters, 2013, 98: 112-115.
[23] TAO T, GLUSHENKOV A M, RAHMAN M M, et al. Electrochemical reactivity of ilmenite FeTiO3, its nanostructures and oxide-carbon nanocomposites with lithium[J]. Electrochimica Acta, 2013, 108: 127-134.
[24] ISKANDAR F, NANDIYANTO A B D, YUN K M, et al. Enhanced photocatalytic performance of brookite TiO2 macroporous particles prepared by spray drying with colloidal templating[J]. Advanced Materials, 2007, 19(10): 1408-1412.
(�༭ ����ΰ)
�ո����ڣ�2015-02-27�������ڣ�2015-04-26
������Ŀ(Foundation item)��������Ȼ��ѧ����������Ŀ(NZ15004)�����ϴ�ѧ��ʿ�����������Ŀ(109004)��������Ȼ��ѧ����������Ŀ(51174231)(Project (NZ15004) supported by the Natural Science Foundation of Ningxia; Project (109004) supported by the Postdoctoral Science Foundation of Central South University; Project (51174231) supported by the National Natural Science Foundation of China)
ͨ�����ߣ�����Ƽ����ʿ�����ڣ�����ʪ��ұ�߷��ӻ�ѧ���о���E-mail��phuhuiping@126.com