文章编号:1004-0609(2009)04-0760-06
白铜合金废料综合回收工艺
徐源来1, 2,徐盛明2,徐 刚2,池汝安1
(1. 清华大学 核能与新能源技术研究院,北京 100084;
2. 武汉工程大学 湖北省新型反应器绿色化学工艺重点实验室,武汉 430074)
摘 要:采用粉碎白铜合金废料→酸浸出→N902萃取分离出铜离子→P204萃取分离出锌离子→水相中剩余硫酸镍溶液工艺回收白铜合金废料中的有色金属。经实验得到较优回收工艺条件是将初步机械粉碎的白铜合金投入硫酸溶液中反应,得到浸出液;使用铜特效萃取剂N902首先分离出浸出液中的铜离子。结果表明,萃取剂N902对铜具有较好的选择性。在相比为1:1、pH值为0.57、N902的体积浓度为50%,混合时间为90 s的条件下,铜的萃取率达到99.36%。使用2 mol/L的硫酸进行反萃操作,平衡时间仅为30 s,反萃回收率达到99.68%;使用萃取剂P204萃取分离后续水相溶液中的锌离子,在相比为2?1、pH值为2.93、P204体积浓度为40%的条件下,混合时间为1 min,经5级萃取后锌离子的萃取率为99.73%,且几乎不萃取水相中的镍,选择性分离效果好。使用1 mol/L的硫酸反萃,经40 s混合后,反萃达平衡,富锌有机相的反萃率为100%。整条工艺完成了铜、镍和锌3种主要离子间的分离,得到硫酸铜、硫酸锌和硫酸镍3种产品。
关键词:回收;白铜合金;N902;P204;萃取
中图分类号:TF 805.2 文献标识码: A
Comprehensive recovery of copper-nickel alloy scrap
XU Yuan-lai1, 2, XU Sheng-ming2, XU Gang2, CHI Ru-an1
(1. Institute of Nuclear and New Energy Technology, Tsinghua University, Beijing 102201, China;
2. Hubei Key Laboratory Novel Reactor and Green Chemical Technology, Wuhan Institute of Technology,Wuhan 430073, China)
Abstract: In order to recover nonferrous metals in copper-nickel alloy scrap, a corresponding technology was adopted as follows crushing copper-nickel alloy scrap→leaching the sample with sulfuric acid→extracting copper ion with N902→extracting zinc ion with P204→getting nickelous sulfate solution. Based on the experiments, the operation fators were optimized as follows. At first, the leaching solution is obtained after putting copper-nickel alloy scrap into sulfuric acid solution. Second, extractant N902 is utilized to extract copper in the leaching solution and has good selectivity to copper. The extraction rate of copper can reach 99.36% at the room temperature when the phase ratio, pH value, N902 concentration and mixing time are 1?1, 0.57, 50% and 90 s, respectively. The stripping rate of copper is 99.68% by using 2 mol/L sulfuric acid solution after 30 s. Finally, the extraction rate of zinc can reach 99.73% at the room temperature by five-stage extraction when the pH value, phase ratio, P204 concentration and mixing time are 2.93, 2?1, 40% and 60 s, respectively. At the same time, there is no nickel extracted due to the fine selectivity of the extractant. If stripped with 1 mol/L H2SO4, 100% zinc in the organic phase can be stripped during 40 s. All the above results indicate significantly that the copper, nickle and zinc can be separated successfully by this technology and the three products of copper sulfate, zinc sulfate and nickelous sulfate are finally obtained.
Key words: recycling; copper-nickel alloy; N902; P204; solvent extraction
由于白铜合金材料具有优良的力学性能,已被广泛应用于精密仪器、医疗器械、通讯工业和卫生工程中的各种零件和弹性元件及日用品等,故每年都有大量的白铜合金废料产生[1]。作为铜镍锌等有色金属的重要二次资源,如何经济有效地利用回收其中有用的成分,在当今集约型发展的社会条件下显得尤为重要[2]。现阶段白铜合金回收一般采用火法冶金和湿法冶金方法,但火法冶金得到的产品仍旧是合金混合物,并未将各种金属完全地分离开,力学性能不高,产品附加值小[3-5]。湿法冶金技术则克服了以上缺点,能将各种金属完全地分离开来,回收价值高[6-9]。相对各种湿法金属分离和纯化技术而言,溶剂萃取[10-11]具有平衡速度快、分离效果好、处理能力大、金属回收率高以及操作容易实现自动控制等特点,金属溶剂萃取的应用领域越来越广泛,它不仅成为分离、纯化金属的一种手段,而且逐步深入到废杂金属回收和含金属废水处理等领域。
目前,镍在我国属于紧缺资源而铜工业正面临严重的资源危机,要确保有色金属工业的可持续发展和矿产资源的可持续开采,回收各种二次金属资源是有色金属工业发展主要的、必然的选择,对我国经济的发展具有战略的、全局性的意义。目前,浙江某公司每月能回收约200 t白铜合金碎屑,按当前市场价值和处理(1 a按300 d计算)量来计算,每年可创造千万元的经济价值。在产生可观经济效益的同时,还能消除污染、节约资源,促进有色金属工业的可持续发展。本文作者试图寻求一条回收效率高、经济合理、且环境友好的白铜合金废料的回收工艺。
1 实验
1.1 材料
使用了X-荧光半定量分析法分析原料白铜合金废料的成分(见表1)。
表1 白铜合金边料成分分析结果
Table 1 Analytical results of main elements in copper-nickel alloy scrap(mass fraction, %)
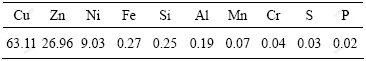
1.2 原理
目前市场上流行多种铜的特效萃取剂,如LIX系列、Cyanex系列和Kelex系列等。相对于这些萃取剂而言,实验所选用的萃取剂N902,虽然萃取铜的pH值范围和萃取容量相对较小,但它的价格相对便宜,适合大规模的工业化生产。实验结果表明:N902对铜具有很强的选择性,且反萃性能优良,有利于实现产业化[12-13]。
目前市场上还没有对锌选择性好、负载量大的特效锌萃取剂。锌萃取研究多是在碱性条件下进行的,而在酸性溶液中,国内外锌的萃取以P204为主。
对P204而言,一定条件下, 两种金属萃取平衡的pH值差越大,就越容易被分离。在硫酸介质中萃取的pH1/2的顺序为:Fe3+<Zn2+<Cu2+<Ca2+<Co2+<Mg2+<Ni2+。
由此可看出,通过调节pH值来萃取分离锌和镍的操作应该是合理的。考虑到萃取剂P204价格便宜,性能优良,故采用它来萃取合金浸出液中的锌。实验证明,在酸性体系中,此选择经济可行 [14-15]。
1.3 方法
白铜合金废料在硫酸溶液通入氧气条件下浸出,过滤后得到浸出液,浸出液经N902萃取铜、P204萃取锌,剩余液中为硫酸镍溶液。采用硫酸反萃经两次萃取后的负载有机相,分别得到硫酸铜和硫酸锌溶液。
2 结果与讨论
2.1 白铜合金废料的浸出
将白铜合金废料投入8 mol/L的硫酸中,在通入氧气条件下,搅拌并加热恒温至80 ℃,加入适量30%过氧化氢水溶液,约8 h后,合金能完全浸出。得到的浸出液成分如表2所列。该浸出液pH值为0.01(由pH计测得,下同)为酸性环境。
表2 浸出液的成分
Table 2 Component of leaching solution (g?L-1)
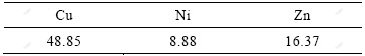
2.2 浸出液中铜与锌镍的萃取分离
2.2.1 水相pH值对N902萃取铜的影响
萃取剂N902为酸性萃取剂,在萃取过程中会产生大量的H+,且浸出过程是在硫酸过量的条件下进行的,因此浸出液也具有一定的酸度,故考察酸度对萃取铜的影响。实验固定萃取剂浓度、混合时间及相比分别于不同的水相酸度,考察萃取剂对铜的萃取效果。实验结果如图1所示。
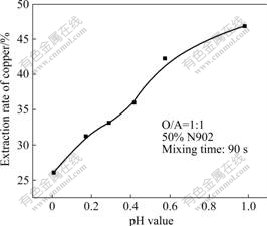
图1 水相pH值对N902萃取铜的影响
Fig.1 Effect of pH value on extraction rate of N902
从图1可以看出,水相pH值对N902萃取的影响较大,随着水相pH值的增加,N902的萃取率上升,因此需要调节浸出液的酸度。同时也可以看出,萃取率随pH值的升高而增大,当pH值为0.4~0.6时,单级萃取率可达35%以上。考虑到若将浸出液的pH值调得过高,将会消耗过多的NaOH,增加成本,因此萃取操作中水相pH值固定为0.57。
2.2.2 混合时间对N902萃取铜的影响
在萃取生产操作中,混合时间是一个重要指标,为此分别考查不同混合时间对铜萃取率的影响,实验结果如图2所示。
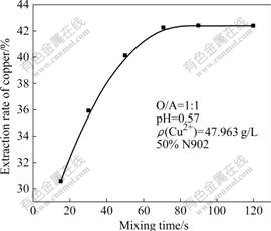
图2 混合时间对铜萃取率的影响
Fig.2 Effect of mixing time on extraction rate of copper
由图2可以看出,在该萃取条件下,混合90 s后,萃取即可达到平衡。这说明采用50%体积浓度的N902萃取合金浸出液中的铜,平衡时间短,有利于在工业上实现该操作。
2.2.3 萃取剂N902对铜的选择性
虽然N902是一种针对铜离子的萃取剂,但仍需考察在确定的水相溶液pH值下,该萃取剂对铜离子是否有较好的选择性。
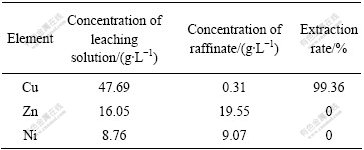
表3所列为经九级萃取操作后水相溶液中3种主要离子的浓度。对比萃取操作前后浸出液中3种离子的浓度可以看出,铜的萃取率达到99%以上,而其它元素几乎不被萃取,仍保留在浸出液中,这样铜与其它元素则能达到良好的分离效果。由此可见,采用N902萃取回收白铜合金中的铜是可行的。
表3 萃取剂N902对铜的选择实验结果
Table 3 Result of selectivity of N902 for copper
2.2.4 萃取剂N902对铜的萃取级数及效果的影响
萃取级数是萃取实现工业化需要考虑的重要因素之一,本实验考察了在pH值为0.57、相比为1?1、混合时间为90 s、N902体积浓度为50%的条件下萃取剂萃取级数对铜离子萃取率的影响,如图3所示。
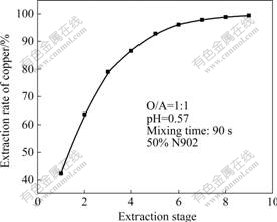
图3 N902萃取铜的萃取级数对萃取率的影响
Fig.3 Effect of extraction stage of N902 on extraction rate of copper
由图3看出,经过九级萃取后,铜离子的萃取率达到99.356%,而镍和锌基本不被萃取,这说明N902可以使溶液中的铜、镍和锌达到基本的分离。
2.2.5 反萃实验
1) 反萃平衡时间
使用2 mol/L的硫酸溶液反萃N902的负铜有机相,考察反萃平衡时间。图4所示为混合时间对铜反萃的影响。由图4可以看出,当反萃混合时间达到 30 s后,反萃基本达到平衡。由此可见,该有机相反萃是一个快速过程,有利于在工业上实现。后续的反萃操作混合时间均为50 s,以保证反应完全平衡。
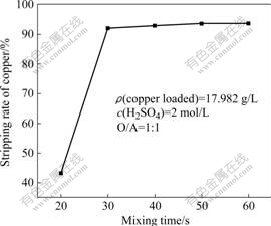
图4 混合时间对铜的反萃的影响
Fig.4 Effect of mixing time on stripping rate of copper
2) 反萃级数
为了反萃负载有机相中的铜,采用多级反萃铜工艺,实验结果如表4所列。
表4 负载有机相反萃铜的实验结果
Table 4 Stripping result of copper from copper loaded N902
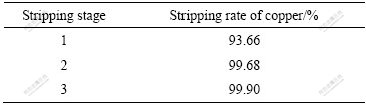
由表4可见,在相比为1?1、混合时间为50 s、硫酸浓度为2 mol/L的条件下,经过3级反萃能洗出负铜有机相中99.90%的铜,反萃酸耗和反萃液残酸浓度均较低,有利于铜的后续回收。
经过萃取剂N902九级萃取操作后,浸出液中的铜离子浓度为0.307 1 g/L、镍离子浓度为9.285 5 g/L、锌离子浓度为18.58 g/L,该溶液用于后续锌的萃取。
2.3 浸出液中锌与镍的萃取分离
由于P204为酸性萃取剂,在萃取过程中有机相置换出的H+会使萃余液酸度降低,萃取能力减弱。为使萃取时水相的终点pH值升高,一般需要在萃取过程中加入适量的碱或石灰乳来调节,或在萃取前用碱来对有机相进行皂化。若将这两种方法用于工业生产,由计算可知,所需的碱将会是大量的,无形间提高了回收成本。同时,使用皂化后的有机相,将会产生大量严重污染环境的含氮废水,加大后续处理的难度。故为了降低萃取锌生产时的成本,实验使用的P204均未经皂化,且萃取过程中没有调节水相的pH值。实验证明该方法也能获得较好的萃取效果。
2.3.1 水相pH值对P204萃取锌的影响
由于使用的为酸性萃取剂,在萃取过程中萃余液的酸度会发生变化,因此萃取前水相溶液的pH值对锌的萃取率有较大的影响。在混合时间为1 min、相比为2?1和有机相为40%(体积比)P204(未皂化)+磺化煤油的固定条件下,得到不同酸度下锌离子的萃取率,如图5所示。
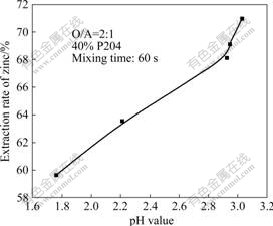
图5 水相pH值对 P204萃取锌的影响
Fig.5 Effect of pH value on extraction rate of P204 for zinc
由图5可知,当pH值达到2.8后,萃取率有一个直线上升的正比趋势,故将后续实验的pH值定为2.94,其对应的锌离子的单级萃取率为69.13。
2.3.2 混合时间对P204萃取锌的影响
有机相是40%的P204加60%的磺化煤油,水相是N902的九级萃后液且pH值为2.93,在室温、相比A?O=2?1的条件下,考察不同混合时间对锌离子萃取效果的影响,其结果如图6所示。
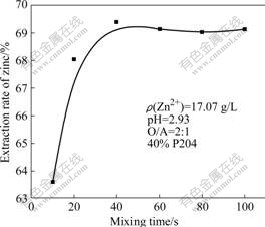
图6 混合时间对锌萃取率的影响
Fig.6 Effect of mixing time on extraction rate of zinc
由图6可以看出,混合时间达到40 s后,萃取即能平衡。在后续的实验中,为保证萃取过程完全平衡,混合时间均固定为1 min。
2.3.3 萃取剂P204对锌的选择性萃取和萃取级数
由实验知,当水相pH值为2~3时,溶液中的镍离子完全不被有机相萃取,萃取剂选择性好,这使得浸出液中的锌离子与镍离子能够得到有效的分离。
在工业中,一般的单级萃取很难满足生产的要求,故多采用多级逆流萃取。虽然根据萃取分配常数能
计算出实验所需要的萃取级数,但由于溶液的酸度pH值会在萃取过程中发生改变,所对应的分配常数就相应改变,这样准确地计算出级数较困难,需通过实验研究确定。在室温、水相pH=2.93、O/A=2?1、40%体积浓度的P204、混合时间为1 min的条件下,考察了萃取剂P204对锌离子的萃取效果,萃取级数与萃取率关系如图7所示。
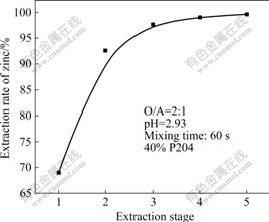
图7 P204萃取锌的萃取级数对萃取率的影响
Fig.7 Effect of extraction stage of P204 on extraction rate for zinc
由图7可知,经五级萃取后,萃取率就可达到99.73%,且镍不被萃取,能达到分离要求,利于工业化生产的实现。
2.3.4 反萃实验
1) 反萃平衡时间
使用1 mol/L的硫酸溶液反萃负锌有机相,考察反萃平衡时间。图8所示为混合时间对锌反萃的影响。由图8可知,当混合时间达到40 s后,反萃基本达到平衡,反萃平衡时间短,有利于工业生产。
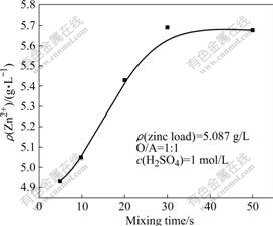
图8 混合时间对锌反萃的影响
Fig.8 Effect of mixing time on stripping rate of zinc
2) 反萃级数
在O/A=1?1、混合时间为40 s、硫酸浓度为1 mol/L 的条件下进行反萃,结果如表5所列。
表5 负载有机相反萃锌的实验结果
Table 5 Stripping results of zinc from zinc loaded P204

由表5可知,反萃级数为4级时,负锌有机相中锌离子的反萃率能达到100%,且锌反萃液残酸浓度较低,有利于锌的后续处理。
3 结论
1) 在通入氧气的条件下,白铜合金废料在8 mol/L的硫酸中搅拌并加热恒温至80 ℃,再加入适量的30%过氧化氢水溶液,反应约8 h后,白铜合金能完全浸出。
2) 萃取剂N902对铜具有较好的选择性。在相比为1?1、pH值为0.57、N902的体积浓度为50%、混合时间为90 s的条件下,铜的萃取率达到99.36%。采用2 mol/L的硫酸进行反萃,平衡时间仅为30 s,萃取回收率可达到99.68%。
3) P204在相比为2?1、pH值为2.93、体积浓度40%的条件下混合1 min,经5级萃取后,锌的萃取率为99.73%,完全不萃取水相中的镍。采用1 mol/L的硫酸溶液反萃,40 s后混合达平衡,负锌有机相中的锌离子回收率为100%。在此过程中,未对P204进行皂化,以及未对反应过程中产生的酸进行中和,整个过程中无含氮废水产生,对环境友好。
4) 萃余液中剩余的为硫酸镍溶液。本工艺基本完成了3种主要离子间的分离,平衡时间短、萃取回收率高、生产成本低、环保,适用于工业化生产。
REFERENCES
[1] 雷 霆. 眼镜绞链用白铜精密异型材生产工艺[J]. 材料科学与工艺, 2000, 8(2): 51-54.
LEI Ting. Manufacturing technology of copper-nickel precise share-wire used for glasses hinge[J]. Material Science & Technology, 2000, 8(2): 51-54.
[2] 严 逊. 白铜边料湿法再生过程中镍、锌的分离[J]. 金属再生, 1990(3): 24-29.
YAN Xun. The separation of Nickel and zinc during hydrometallurgy recovery process of copper-nickel alloy scrap[J]. Metal Recovery, 1990(3): 24-29.
[3] BRANDES M, MILLS M J. Static recovery in titanium alloys at lower temperatures[J]. Materials Science and Engineering A, 2004, 387/389: 570-575.
[4] LUO L, MIYAZAKI T, SHIBAYAMA A. A novel process for recovery of tungsten and vanadium from a leach solution of tungsten alloy scrap[J]. Minerals Engineering, 2003, 16(7): 665-670.
[5] RABAH M A. Recovery of aluminium, nickel-copper alloys and salts from spent fluorescent lamps[J]. Waste Management, 2004, 24(2): 119-126.
[6] RODRIGUEZ-TORRES I, VALENTIN G, CHANEL S, LAPICQUE F. Recovery of zinc and nickel from electrogalvanisation sludges using glycine solutions[J]. Electrochimica Acta, 2000, 46(2/3): 279-287.
[7] JHA M K, KUMAR V, SINGH R J. Review of hydrometallurgical recovery of zinc from industrial wastes[J]. Resources, Conservation and Recycling, 2001, 33(1): 1-22.
[8] de SOUZA C C B M, TEN?RIO J A S. Simultaneous recovery of zinc and manganese dioxide from household alkaline batteries through hydrometallurgical processing[J]. Journal of Power Sources, 2004, 136(1): 191-196.
[9] SADEQH S M , BAFGHI M S, MORADKHANI D, OJAQHI L M. A review on hydrometallurgical extraction and recovery of cadmium from various resources[J]. Minerals Engineering, 2007, 20(3): 211-220.
[10] 杨佼庸, 刘大星. 萃取[M]. 北京: 冶金工业出版社, 1988.
YANG Jiao-yong, LIU Da-xing. Extraction[M]. Beijing: Metallurgical Industry Press, 1988.
[11] 朱 屯. 萃取与离子交换[M]. 北京: 冶金工业出版社, 2005.
ZHU Tun. Extraction and ion-exchange[M]. Beijing: Metallurgical Industry Press, 2005.
[12] PENG Cui, ZHU Guo-cai, CHI Ru-an. Recovery of copper from leaching solution of copper smelting ash[J]. The Chinese Journal of Process Engineering, 2007, 7(2): 273-277.
[13] CHMIELEWSKI A G, URBANSKI T S, MIGDAL W. Separation technologies for metals recovery from industrial wastes[J]. Hydrometallurgy, 1997, 45(3): 333-344.
[14] 杨大锦, 谢 刚, 王吉坤, 彭建蓉. 硫酸锌溶液的萃取工艺研究[J]. 有色金属(冶炼部分), 2006(2): 9-13.
YANG Da-jin, XIE Gang, WANG Ji-kun, PENG Jian-rong. Study on solvent extraction of zinc sulfate solution[J]. Nonferrous Metals (Extractive Metallurgy), 2006(2): 9-13.
[15] 兰兴华. 锌溶剂萃取进展[J]. 世界有色金属, 2004(8): 28-31.
LAN Xing-hua. Development of zine solvent extraction[J]. World Nonferrous Metal, 2004(8): 28-31.
基金项目:国家自然科学基金资助项目(50674060;20601016;50734005);国家重点基础研究发展计划资助项目(2007CB613506)
收稿日期:2008-02-27;修订日期:2008-12-15
通讯作者:徐盛明,副教授,博士;电话:010-89796082;E-mail: smxu@tsinghua.edu.cn
(编辑 李艳红)