文章编号:1004-0609(2015)-05-1220-07
Mg-1.0Ca合金微弧氧化膜在模拟体液中的腐蚀降解行为
张荣发1,张勇强 2, 3,张淑芳1,郭世柏2,刘 洋1,向军淮1
(1. 江西科技师范大学 材料与机电学院,南昌 330013;
2. 湖南科技大学 机电工程学院,湘潭 411201;
3. 浙江盾安轻合金科技有限公司,诸暨 311835)
摘 要:在含植酸钠和碳酸钙的碱性溶液中,采用微弧氧化技术在Mg-1.0Ca合金表面制备钙磷盐涂层。采用扫描电镜、能谱仪和X射线衍射仪分析氧化膜的表面形貌、成分和相组成;通过析氢试验、表面观察法以及浸泡腐蚀失重法分析比较镁钙合金氧化前后在模拟体液中的腐蚀降解行为。结果表明:微弧氧化能显著降低Mg-1.0Ca合金的腐蚀降解速率;浸泡后氧化试样表面钙含量明显增加,表明氧化膜具有很好的生物活性。
关键词:镁钙合金;微弧氧化;钙磷涂层;腐蚀降解
中图分类号:TG174 文献标志码:A
Corrosion degradation behaviors of micro arc oxidation coatings on Mg-1.0Ca alloys in simulated body fluid
ZHANG Rong-fa1, ZHANG Yong-qiang2,3, ZHANG Shu-fang1, GUO Shi-bo2, LIU Yang1, XIANG Jun-huai1
(1. School of Materials and Electromechanics,
Jiangxi Science and Technology Normal University, Nanchang 330013, China;
2. College of Electromechanical Engineering, Hunan University of Science and Technology, Xiangtan 411201, China;
3. Zhejiang Dunan Light Alloy Technology Co., Ltd., Zhuji 311835, China)
Abstract: The calcium phosphate coatings were prepared by micro arc oxidation (MAO) technique on Mg-1.0Ca alloys in an alkaline solution containing sodium phytate and calcium carbonate. The surface morphology, chemical compositions and phase structure were characterized by scanning electron microscopy (SEM), energy dispersive spectrometry (EDS) and X-ray diffractometry (XRD). The corrosion degradation behavior of Mg-1.0Ca alloys before and after MAO treatment in a simulated body fluid (SBF) were compared through the hydrogen evolution test, surface observation method and immersion corrosion weight loss method. The results demonstrate that MAO treatment can significantly reduce the corrosion degradation rate of Mg-1.0Ca alloys. After immersion in SBF, the calcium content of the MAO samples increases significantly, indicating that the obtained micro arc coatings achieve excellent bioactivity.
Key words: Mg-Ca alloy; micro arc oxidation; calcium phosphate coating; corrosion degradation
镁合金具有弹性模量低、密度与人骨接近以及可体内降解等优点,成为可降解生物材料研究的热点[1-4]。近年来研究发现,镁合金具有抗菌性能[5-6]。但镁合金在体液中腐蚀降解速度过快,在组织愈合前失去其机械完整性[7]。因此,改善镁合金本身的耐蚀性并研究其腐蚀降解行为成为镁合金在医用植入材料领域的关键。
微弧氧化是一种有效的表面处理技术,能提高镁合金的耐蚀性和生物相容性。由于天然骨由有机基质和无机钙磷组成[8],因此,筛选能使生成的微弧氧化膜富含钙磷的电解质成为近年来制备生物涂层研究的重点。张勇强等[9]系统地对比了CaCO3、Ca(OH)2、Ca(CH3COO)2和Ca(H2PO4)2对氧化膜性能的影响,发现CaCO3能显著增加微弧氧化膜的厚度,改善氧化膜的微孔均匀性,增大孔间距,并能改变氧化膜的组成,从而降低氧化膜的腐蚀降解速率。
目前,微弧氧化使用的含磷电解质主要为无机磷酸盐如磷酸钠,但其氧化膜耐蚀性较差,在含氯化钠溶液中腐蚀速率达2 mm/y[10]。另外,从仿生角度看,有机-无机复合涂层无疑更近似于天然骨组织成分,促进周围骨形成[11]。在以上理论指导下,张勇强等[9]已将常用作食品添加剂的有机磷酸盐-植酸钠用作镁合金微弧氧化电解质[9]。植酸(Phytic acid)亦称环己六醇六磷酸酯,主要以钙镁复盐(植酸钙镁)的形式广泛存在于植物种子内,也存在于动物有核红细胞内。植酸分子具有能同金属配合的24个氧原子、12个羟基和6个磷酸基,可迅速与Ca2+,Mg2+,Fe2+和Zn2+等离子结合形成植酸盐沉淀[12]。植酸的毒性小于食盐的,属天然营养品。植酸钠是植酸的盐类衍生物,比植酸有着更广的应用范围。本文作者在前期研究基础上,以植酸钠和CaCO3为微弧氧化的主要电解质,在Mg-1.0Ca合金表面制备钙磷盐涂层,采用在模拟体液中浸泡实验,评价氧化膜的体外腐蚀降解行为。
1 实验
使用Mg-1.0Ca合金,理论成分为99.0% Mg和1.0% Ca(质量分数),试样规格为d 50 mm×10 mm的圆柱状。分别采用180~1000号的水砂纸由粗到细逐级打磨,然后经蒸馏水清洗、无水乙醇擦洗、热风吹干后,置入干燥器中待用。使用的电解液为3 g/L氢氧化钠、15 g/L植酸钠和5 g/L CaCO3。采用国产MAOI-50C微弧氧化电源,使用单(正)脉冲恒流控制,电参数如下:电流密度为40 mA/cm2,占空比为35%,频率为2000 Hz,氧化时间为5 min。
腐蚀介质为模拟体液,溶液组成如下[2]:8 g/L NaCl、0.4 g/L KCl、0.14 g/L CaCl2、0.35 g/L NaHCO3、1.0 g/L C6H12O6、0.2 g/L MgSO4・7H2O、0.1 g/L KH2PO4・H2O、0.06 g/L Na2HPO4・7H2O。根据ASTM G31-72浸泡实验标准[13],溶液体积与试样的表面积比为30 mL:1 cm2,模拟体液保持37℃恒温。采用排水集氢气法测量镁合金在模拟体液中的析氢腐蚀速率,实验方法参照文献[14]。使用BP211D分析天平(精度0.01 mg)称量浸泡前、后干燥试样的质量,通过式(1)计算出试样的腐蚀速度:
γ=M/(St) (1)
式中:M为腐蚀质量损失(g);S为试样的原始面积(cm2);t为浸泡时间(d)。
为避免因浸泡液中离子浓度变化对实验的影响,每隔两天更换模拟体液。采用PHS-3C酸度计测量溶液的pH值,用ΣIGMA FE扫描电子显微镜(Scanning electron microscope, SEM)观察氧化膜的表面形貌,用X射线能谱仪(Energy dispersive spectrometer, EDS)检测膜层的成分,采用D8 ADVANCE型X射线衍射(X-ray diffraction, XRD)仪分析氧化膜的物相组成。
2 结果与分析
2.1 微弧氧化膜的形貌及物相分析
微弧氧化膜的表面与截面形貌如图1所示。由图1(a)可知,微弧氧化膜表面微孔分布均匀,微孔孔径约为1.5~2.5 μm,微孔孔隙尺寸约为3~5 μm。氧化膜中含C 8.76%(摩尔分数,下同)、O 53.77%、Na 3.01%、Mg 24.57%、P 9.29%和 Ca 0.61%。由图1(b)可知,氧化膜层中有许多孔洞分布,尤其是在疏松层,是由火花放电形成,但孔洞没有贯穿整个膜层与基体接触。膜层厚度达到20 μm,其中疏松层约15 μm,致密层约5 μm。

图1 Mg-1.0Ca微弧氧化膜的表面与截面形貌
Fig. 1 Surface (a) and cross-section (b) morphologies of MAO coatings on Mg-1.0Ca alloys
图2所示为微弧氧化膜的XRD谱。由图2可知,微弧氧化试样除含有基体的Mg峰外,还包括MgO、CaHPO4、MgCO3・3H2O和(Ca,Mg)CO3相,说明植酸钠和碳酸钙均参与了微弧氧化膜的形成,P、Ca生物活性元素被成功地引入到氧化膜层中。

图2 Mg-1.0Ca合金微弧氧化膜的XRD谱
Fig. 2 XRD pattern of MAO coatings formed on Mg-1.0Ca alloys
2.2 模拟体液中析氢试验与pH值测定
将Mg-1.0Ca合金基体和微弧氧化处理后的试样浸泡在模拟体液中,每天定时记录各组试样产生的氢气量。Mg-1.0Ca合金基体在模拟体液中浸泡5 d的析氢量见图3。由图3可知,浸泡第一天析出氢气5.1 mL,第二天析出3.6 mL,平均每天析出氢气3.9 mL。
Mg-1.0Ca合金微弧氧化试样浸泡15 d的析氢量如图4所示。由图4可知,微弧氧化试样浸泡前3 d,没有氢气析出,而从第4 d开始,析出少量氢气,约为0.05 mL;随着浸泡时间延长,析出量逐渐增多,当浸泡到11 d时,析氢量为1.8 mL;随着浸泡时间的延长,析氢量逐渐减少,每天析出量在0.9 mL左右波动。由此可知,微弧氧化膜的保护作用,使得镁合金腐蚀降解速率缓慢,同时由于膜层溶解与钙磷盐的沉积同时发生,沉积的物质会填塞住一些腐蚀的通道,所以腐蚀速率逐渐下降。
Mg-1.0Ca合金微弧氧化膜浸泡期间,浸泡液pH值的变化如图5所示。
由图5可知,在浸泡前3 d,溶液的pH值基本保持不变。从第4 d开始,浸泡液pH值缓慢上升;溶液pH值在第5 d超过8,浸泡10 d后,上升趋势逐渐缓慢。浸泡液pH值的变化与镁合金在含氯离子溶液环境的发生阴极反应生成的OH-密切相关,同时浸泡液中pH值的变化趋势与图5中析氢量变化趋势相吻合。因此,浸泡液pH值随时间的变化趋势反映出了镁合金微弧氧化膜在模拟体液中腐蚀降解速率的变化。
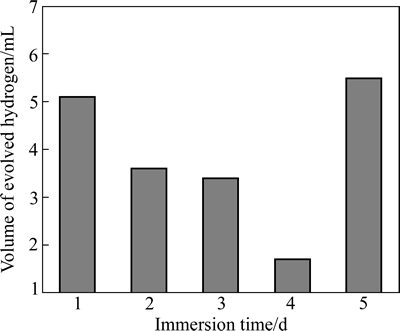
图3 Mg-1.0Ca合金基体在模拟体液中浸泡5 d的析氢量
Fig. 3 Hydrogen evolution volumes of Mg-10Ca alloy substrate after immersion in SBF for 5 d

图4 微弧氧化试样在模拟体液中浸泡15 d的析氢量
Fig. 4 Hydrogen evolution volumes of MAO treated samples after immersion in SBF for 15 d

图5 浸泡溶液的pH值与浸泡时间的关系
Fig. 5 Relationship between pH value of SBF and immersion time
2.3 试样在模拟体液中浸泡情况
将Mg-1.0Ca合金基体与微弧氧化膜试样浸入模拟体液中,发现基体表面很快有气泡溢出,并且浸泡一段时间后,表面出现黑色的斑点,失去金属光泽,并在气泡溢出位置有蚀坑出现。浸泡5 d后,基体与氧化后的试样在模拟体液中浸泡后的照片如图6所示。

图6 Mg-1.0Ca合金基体与微弧氧化试样在模拟体液中浸泡5 d后的照片
Fig. 6 Pictures of Mg-1.0Ca alloy substrate (a) and MAO treated sample (b) after immersion in SBF for 5 d
由图6(a)可知,基体试样浸泡5 d后,发生了严重的腐蚀,表面已经形成许多点蚀坑,同时表面生成了很多絮状物质。由图6(b)可知,经微弧氧化处理的镁合金在模拟体液中浸泡5 d,随膜层颜色较最初的灰白色暗淡,出现了细小的纹路,但表面没有肉眼可见的点蚀坑。可能由于微弧氧化膜层对镁合金的保护作用,腐蚀性阴离子还没有透过膜层与基体接触形成微电偶,因此没有形成腐蚀坑。
Mg-1.0Ca合金基体与微弧氧化后的试样在模拟体液中浸泡不同时间后的质量变化如图7所示。
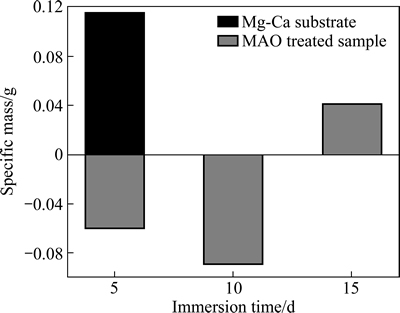
图7 基体与微弧氧化试样在模拟体液中的腐蚀质量损失柱状图
Fig. 7 Histogram showing corrosion mass loss of substrate and MAO treated samples after immersion in SBF
由图7可知,Mg-1.0Ca合金基体在模拟体液中浸泡5 d后,质量增加0.1157 g;而微弧氧化试样浸泡5 d和10 d质量损失分别为0.06和0.089 g,随着浸泡时间的延长,质量损失逐渐增加,质量损失速率分别为γ5=0.6 mg/(cm2・d)和γ10=0.045 mg/(cm2・d)。当浸泡15 d后,试样出现质量增加现象,质量增加0.0415 g。
图8所示为微弧氧化后的试样在模拟体液中浸泡不同时间后的表面形貌。由图8(a)可知,微弧氧化膜浸泡5 d后,表面出现突起或颗粒物质,但没有出现裂纹和腐蚀坑。由图8(b)可知,试样浸泡10 d后,表面微孔减小,出现了微裂纹,同时,涂层表面覆盖有白色乳状物质。由图8(c)可知,试样浸泡15 d后,表面局部区域出现了白色物质。
微弧氧化试样在模拟体液中浸泡不同时间的成分见表1。氧化试样在模拟体液中浸泡后,浸泡不同时间以及试样不同区域的化学成分是不一样的。浸泡前氧化膜中含钙仅为0.61%,浸泡后试样表面的钙含量明显增加(见表1),表明氧化试样具有较好的生物活性。

图8 氧化试样在模拟体液中浸泡不同时间后的表面形貌
Fig. 8 Surface morphologies of MAO treated samples after immersion in SBF for different times
表1 氧化试样在模拟体液中浸泡不同时间后的化学成分
Table 1 Chemical composition of MAO treated samples after immersion in SBF for different times
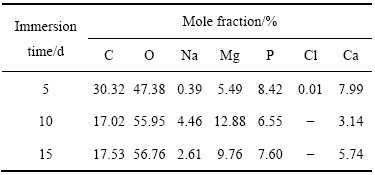
图9所示为镁钙合金氧化后的试样在模拟体液中浸泡不同时间的XRD谱。由图9可知,微弧氧化试样浸泡5 d后,表面成分主要为MgO、Mg(OH)2、(Ca,Mg)CO3、CaHPO4,说明微弧氧化膜在人体模拟体液环境生成了含P和Ca的物质。随着浸泡时间的延长,CaHPO4、(Ca,Mg)CO3和Mg(OH)2的峰值逐渐加强,说明这些物质逐渐增多。

图9 微弧氧化膜在模拟体液中浸泡不同时间后的XRD谱
Fig. 9 XRD patterns of MAO coatings after immersion in SBF for different times
3 讨论
由图1可知,氧化膜中含 9.29%的磷,表明植酸钠参与了氧化膜的形成。由于植酸钠属螯合物,而氧化膜中存在CaHPO4(见图2),可能是微弧氧化时,由于火花放电使试样表面的瞬时温度高于1000 ℃[15],在此条件下植酸钠发生水解反应,生成肌醇和磷酸氢二钠,水解反应方程式为[16]
Na12C6H6O24P6+H2O→C6H12O6+6Na2HPO4 (2)
磷酸氢根和钙离子反应,生成CaHPO4:
HPO4-+Ca2+→CaHPO4 (3)
当镁合金浸泡在腐蚀介质中,其腐蚀过程属于电化学过程,总反应方程式如下[13]:
Mg+2H2O→Mg(OH)2+H2↑ (4)
如果忽略可能有不稳定中间产物的形成,上述总反应方程可由分为以下两个反应:
阳极反应,
Mg→Mg2++2e (5)
阴极反应,
2H2O+2e→H2↑+2OH- (6)
由镁的总反应机理可知,镁合金浸泡在模拟体液中会不断产生氢气与镁离子的沉积,导致溶液pH上升,腐蚀越严重,pH上升越快,因此,通过收集浸泡期间产生的氢气与测量浸泡液pH的变化,可推测镁合金微弧氧化膜在模拟体液中腐蚀降解变化趋势。因此,由图3~5可知,微弧氧化后试样在模拟体液中析氢速率变慢,溶液pH值缓慢上升,说明微弧氧化能明显提高镁钙合金的耐蚀性,这也被图6所证实。
由图7可知,镁钙合金基体浸泡5 d后质量增加,而氧化试样浸泡5 d和10 d质量损失,浸泡15 d开始质量增加。经微弧氧化处理的试样,腐蚀前期,微弧氧化膜层的疏松层在含氯离子的模拟体液中发生溶解,导致质量损失。但由于有氧化膜致密层的保护,整个材料的腐蚀降解速率缓慢。另外,在模拟体液中,氧化膜的溶解和钙磷盐的沉积同时发生,沉积的物质也会填塞住一些腐蚀的通道,所以腐蚀速率逐渐下降。随着浸泡时间的延长,腐蚀过程中形成较多的腐蚀产物,沉积在表面或者填塞在腐蚀通道,导致试样质量增加。
由图9可知,在模拟体液中浸泡后,试样表面的钙和磷含量增加,一方面表明在浸泡过程中,钙磷盐的沉积过程是存在的,这与图8的结果一致;另一方面也说明,微弧氧化后的试样具有较好的生物活性。
4 结论
1) 在含植酸钠和碳酸钙的碱性溶液中,制备的微弧氧化膜为典型的多孔结构,主要由MgO、CaHPO4、MgCO3・3H2O、(Ca,Mg)CO3构成,植酸钠和CaCO3均参与了氧化膜的形成。
2) 镁合金基体在模拟体液中浸泡5 d后,质量增加,而微弧氧化试样浸泡5 d和10 d后质量损失,但浸泡15 d开始质量增加,表明在模拟体液中,氧化膜的溶解和钙磷盐的沉积同时进行。
3) 析氢试验和表面观察法结果表明:微弧氧化处理显著降低了镁合金的腐蚀降解速率;随着浸泡时间延长,腐蚀降解速率逐渐降低。
4) 在模拟体液中浸泡后,氧化样品表面的钙含量明显增加,表明氧化膜具有很好的生物活性。
REFERENCES
[1] SHADANBAZ S, DIAS G J. Calcium phosphate coatings on magnesium alloys for biomedical applications: A review[J]. Acta Biomaterialia, 2012, 8(1): 20-30.
[2] SONG G L. Control of biodegradation of biocompatible magnesium alloys[J]. Corrosion Science, 2007, 49(4): 1696-1701.
[3] ZHANG C Y, ZENG R C, LIU C L, GAO J C. Comparison of calcium phosphate coatings on Mg-Al and Mg-Ca alloys and their corrosion behavior in Hank’s solution[J]. Surface & Coatings Technology, 2010, 204(21/22): 3636-3640.
[4] 袁广银, 张 佳, 丁文江. 可降解医用镁基生物材料的研究进展[J]. 中国材料进展, 2011, 30(2): 44-50.
YUANG Guang-yin, ZHANG Jia, DING Wen-jiang. Research progress of Mg-based alloys as degradable biomedical materials[J]. Materials China, 2011, 30(2): 44-50.
[5] ROBINSON D A, GRIFFITH R W, SHECHTMAN D, EVANS R B, CONZEMIUS M G. In vitro antibacterial properties of magnesium metal against escherichia coli, pseudomonas aeruginosa and staphylococcus aureus[J]. Acta Biomaterialia, 2010, 6(5): 1869-1877.
[6] REN L, LIN X, TAN L L, YANG K. Effect of surface coating on antibacterial behavior of magnesium based metals[J]. Materials Letters, 2011, 65: 3509-3511.
[7] 黄晶晶, 杨 柯. 镁合金的生物医用研究[J]. 材料导报, 2006, 20(4): 67-69.
HUANG Jing-jing, YANG Ke. Research on magnesium alloy for bio-medical applications[J]. Materials Review, 2006, 20(4): 67-69.
[8] YU C C, CHANG J J, LEE Y H, LIN Y C, WU M H, YANG M C, CHIEN C T. Electrospun scaffolds composing of alginate, chitosan, collagen and hydroxyapatite for applying in bone tissue engineering[J]. Materials Letters, 2013, 93: 133-136.
[9] 张勇强, 郭世柏, 张荣发, 张淑芳, 姚灵菊, 谢辛玲. 含钙电解质对Mg-1.0Ca合金微弧氧化膜性能的影响[J]. 中国有色金属学报, 2013, 23(4): 1027-1033.
ZHANG Yong-qiang, GUO Shi-bo, ZHANG Rong-fa, ZHANG Shu-fang, YAO Ling-ju, XIE Xin-ling. Effects of calcium-containing electrolytes on property of anodic coatings obtained by micro arc oxidation on Mg-1.0Ca alloys[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(4): 1027-1033.
[10] DURDU S, AYTAC A, USTA M. Characterization and corrosion behavior of ceramic coating on magnesium by micro-arc oxidation[J]. Journal of Alloys and Compounds, 2011, 509: 8601-8606.
[11] 谢加兵, 徐祝军. 钛植入材料表面生物化改性研究进展[J]. 国际骨科学杂质, 2012, 33(1): 52-54.
XIE Jia-bing, XU Zhu-jun. Research progress in surface biological modification of titanium implant materials[J]. International Journal of Orthopaedics, 2012, 33(1): 52-54.
[12] CREA F, STEFANO C D, MILEA D, SAMMARTANO S. Formation and stability of phytate complexes in solution[J]. Coordination Chemistry Reviews, 2008, 252(10/11): 1108-1120.
[13] ASTM G31―72. Standard practice for laboratory immersion corrosion testing of metals. Annual Book of ASTM standards[S]. Philadelphia, Pennsylvania, USA:American socity for Testing and Materials, 2004.
[14] 张 佳, 宗 阳, 袁广银, 常建卫, 付鹏怀, 丁文江. 新型医用Mg-Nd-Zn-Zr镁合金在模拟体液中的降解行为[J]. 中国有色金属学报, 2010, 20(10): 1989-1997.
ZHANG Jia, ZONG Yang, YUAN Guang-yin, CHANG Jian-wei, FU Peng-huai, DING Wen-jiang. Degradable behavior of new-type medical Mg-Nd-Zn-Zr magnesium alloy in simulated body fluid[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(10): 1989-1997.
[15] XUE W B. Features of film growth during plasma anodizing of Al 2024/SiC metal matrix composite[J]. Applied Surface Science, 2006, 252: 6195-6200.
[16] 戴传波, 李建桥, 赵岩涛. 由植酸钠制取肌醇的水解反应动力学方程[J]. 农业机械学报, 2007, 38(10): 73-76.
DAI Chuan-bo, LI Jian-qiao, ZHAO Yan-tao. Study on reactive kinetics for preparation of inositol from the hydrolysis of sodium phytate[J]. Transactions of the Chinese Society of Agricultural Machinery, 2007, 38(10): 73-76.
(编辑 龙怀中)
基金项目:国家自然科学基金资助项目(51061007);江西省自然科学基金资助项目(20132BAB206011);江西省生物医药分子及检测仪器工程中心资助项目(311)
收稿日期:2014-02-10;修订日期:2015-02-10
通信作者:向军淮,教授,博士;电话:0791-83801423; E-mail: xiangjunhuai@163.com