H2O2����H4SiW12O40/SiO2��������л�Ⱦ�ϵ��о�
��Դ�ڿ���ϡ�н���2014���6��
�������ߣ��ܹ��� ��־Զ ���S �봫�� ��ˮ��
����ҳ�룺1073 - 1079
�ؼ��ʣ�������;����;SiO2;���;����;
ժ Ҫ�������ܽ�-��������Keggin��H4Si W12O40������Si O2��,����30%H2O2��Һ�����������,�Ƶ�H4Si W12O40/Si O2/H2O2�����,�ֱ����ø���Ҷ�任��������ǣ�FT-IR����X�������䣨XRD���Ըù�������б�������,�������H4Si W12O40�߶ȷ�ɢ��Si O2��,���Ҿ���H2O2��Һ�����Ĺ������935.2 cm-1������һ�������Ĺ��������շ�,����������ữ��������շ��һ�¡�����,���м���ģ���ˮ��Һ�ںڰ������µ�����-�Ѹ�ƽ��ʵ��,���������30 min�ﵽ����-�Ѹ�ƽ��,���Ż���ʵ��ѡ���ںڰ��½���30 min�Դﵽ����-�Ѹ�ƽ�⡣���ŶԼ��ȵij�ʼŨ�ȡ���Һp H�Լ��������������Ż���ʵ�鷢��,�ڼ��ȳ�ʼŨ��Ϊ15 mg��L-1,��Һp HΪ1.0,����������Ϊ6 g��L-1���Ż������,�⽵��3.0 h,���ȵĽ����ʴﵽ99.0%,H4Si W12O40/Si O2/H2O2������������Һ�Ĺ��̷���һ������ѧ��Ӧ����;��H4Si W12O40/Si O2/H2O2�Լ��ϡ���ȸʯ�̡��Ǽ���������B�ͼ�������нϸߵĹ������,�����ʴ�87.5%100.0%��
������ʱ��: 2014-02-24 08:50
ϡ�н��� 2014,38(06),1073-1079 DOI:10.13373/j.cnki.cjrm.2014.06.022
�ܹ��� ��־Զ ���S �봫�� ��ˮ��
����ʦ��ѧԺ��ѧ����ѧԺϡ�н�����ѧ����ʡЭͬ��������
������ѧ��ѧ����ѧԺ
�����ܽ�-��������Keggin��H4Si W12O40������Si O2��, ����30%H2O2��Һ�����������, �Ƶ�H4Si W12O40/Si O2/H2O2�����, �ֱ����ø���Ҷ�任��������� (FT-IR) ��X�������� (XRD) �Ըù�������б�������, �������H4Si W12O40�߶ȷ�ɢ��Si O2��, ���Ҿ���H2O2��Һ�����Ĺ������935.2 cm-1������һ�������Ĺ��������շ�, ����������ữ��������շ��һ�¡�����, ���м���ģ���ˮ��Һ�ںڰ������µ�����-�Ѹ�ƽ��ʵ��, ���������30 min�ﵽ����-�Ѹ�ƽ��, ���Ż���ʵ��ѡ���ںڰ��½���30 min�Դﵽ����-�Ѹ�ƽ�⡣���ŶԼ��ȵij�ʼŨ�ȡ���Һp H�Լ��������������Ż���ʵ�鷢��, �ڼ��ȳ�ʼŨ��Ϊ15 mg��L-1, ��Һp HΪ1.0, ����������Ϊ6 g��L-1���Ż������, �⽵��3.0 h, ���ȵĽ����ʴﵽ99.0%, H4Si W12O40/Si O2/H2O2������������Һ�Ĺ��̷���һ������ѧ��Ӧ����;��H4Si W12O40/Si O2/H2O2�Լ��ϡ���ȸʯ�̡��Ǽ���������B�ͼ�������нϸߵĹ������, �����ʴ�87.5%~100.0%��
��ͼ����ţ� O643.32;X703
����飺�ܹ��� (1989-) , ��, ������������, ѧʿ, �о�����:Ӧ�û�ѧ;E-mail:18772305667@163.com;;��ˮ��, ����;�绰:15629597607;E-mail:yangshuijin@163.com;
�ո����ڣ�2013-08-16
����������Ȼ��ѧ������Ŀ (21273065);����ʡ�ص�ʵ���ҿ��Ż�����Ŀ (KL2013M08);����ʦ��ѧԺ2012��У����ѧ�����´�ҵѵ���ƻ���Ŀ (2012017) ����;
Zhou Guohui Yang Zhiyuan Yang Yun Feng Chuanqi Yang Shuijin
Hubei Collaborative Innovation Center for Rare Metal Chemistry, College of Chemistry and Chemical Engineering, Hubei Normal University
College of Chemistry and Chemical Engineering, Hubei University
Abstract��
The Keggin-type H4 Si W12O40was loaded on the surface of Si O2 with sol-gel method, and sensitized by 30% H2O2 solution, then the photocatalyst was characterized using Fourier transform infrared ( FT-IR) spectrometer, X-ray diffraction ( XRD) . The results showed that H4 Si W12O40was highly dispersed on the Si O2, and the sensitized photocatalyst appeared a weak absorption peak at935. 2 cm- 1, which was in agreement with the absorption peak of peroxy compound. The adsorption-desorption equilibrium experiment of methyl orange waste water in dark condition showed that the process reached an equilibrium at 30 min, so stirring for 30 min in the dark was selected for the optimization experiment. Then, the photocatalytic degradation of methyl orange by H4 Si W12O40/ Si O2/ H2O2 under simulated natural light irradiation was investigated. At the same time, influences of the initial methyl orange concentration, the solution p H and the catalyst dosage on the photocatalytic degradation rate of methyl orange were also examined. The results demonstra-ted that when the initial concentration of methyl orange was 15 mg��L- 1, catalyst dosage was 6 g��L- 1and the p H was 1. 0, the degradation ratio of methyl orange was as high as 99. 0% after simulated natural light irradiation for 3. 0 h. The reaction of photocatalysis for methyl orange could be expressed as first-order kinetic model. The photodegradation of methyl violet, malachite green, methylene blue, rhodamine B and methyl red were also tested, and the degradation rate of dyes could reach 87. 5% ~ 100. 0%.
Keyword��
H4SiW12O40; methyl orange; SiO2; photocatalytic; degradation;
Received�� 2013-08-16
�л�Ⱦ�Ϸ�ˮ���Ϊ���㻯����, ����ż��������ռ80%����, ��Ũ�ȸ�, ���ﶾ�Դ�, ����ʹ�ô�ͳ�����オ�ⷨ���д���, ���Ⱦ�Ϸ�ˮ������������һ���д�����Ļ�������[1,2]�����ἰ�����������νж������ (POM) , ����Ϊ��ˮ���������ĸ����������ֱ��㷺�о�[3,4,5,6,7]���Ӷ��ἰ������������ص����ԡ�����ԡ���Ӧ����һ�͡���Һ�ࡱ��Ϊ���ص�, �ڴ������ܵ���ע[8]��������ԭ����ԭ�ӵĸ����ȿɰ��Ӷ��� (��) ��Ϊ5��:Keggin��, Dawson��, Waugh��, Anderson��, Silverton�͡���̬�Ӷ��� (��) �����ڵ��Ӷ������Ӽ����һ���Ŀ�϶, ��Ӧ���ӿɱ����յ������ڲ�, ʹ���Ӷ��� (��) �����Ũ��Һ���Ƶ������ṹ����������, ��Ӧ���ӵ���ɢ, �����ӵ���������, ʹ�÷�Ӧ��������Һ�н���һ�������ֽ��ڹ�������Һ֮���Ũ��Һ, ��Ϊ��Һ�ࡣͨ��ˮ���Ըߵ��Ӷ��ἰ���������γɼ�Һ��, �����ڴ�Ч�ʵ�����[9]��
���� (��) ������������н��ܡ���Ч����ѡ���ԡ��������������ơ���������ǿ���ܰ���Ⱦ�ﳹ�����������Ⱦ���ŵ㡣��Щ��Ϊ���� (��) ��Ϊ����������л���Ⱦ���Ӧ�ÿ����˹�����ǰ��[10]��Ȼ��, �Ӷ��᱾��������ˮ���������л��ܼ�, ��Ȼ��ʾ�˻��Ըߡ�ѡ���ԺúͲ��������º͵��ŵ�, ���Ǵ��������������͡������豸�Ӵ����ķ���ͻ������ѵȱˡ������������о����ȵ㼯���ڷǾ���������о�, ��Ҫ�����ڹ����� (��) �����������ʹ��������ʹ���3�����档
����Si O2���бȱ������, �ṹ�������ص�, ����Sol-Gel���Ʊ��Ķ������踺�ض���������νṹ���ȶ�, ��������, �Ǹ��ض������������������塣���ô�����δ�ı����������δ���������������մ������, ����һ�ּ����۵ļ�����ʹ���������Ӧ�ķ�Χ�������õ�Ӧ�ü�ֵ�����IJ���H2O2��H4Si W12O40/Si O2���д����[11,12], �����������ڹ⽵����ȵ��л�Ⱦ�ϵĹ������[13]��
1 ʵ��
1.1 �Լ�������
����������, ������, 30%H2O2��Һ, ����, ����, ��ȸʯ��, �Ǽ���, ����B�ͼ����Ϊ��������H4Si W12O40����, ʵ����ˮ��Ϊȥ����ˮ��
��ĩ���������D8 ADVANCE��X���������� (XRD, Bruker AXS����) , ��ͭ��K��1����, �ڹܵ���40 m A, �ܵ�ѹ40 k V�������²ⶨ, ɨ�跶Χ2��Ϊ5��~70��;����Ҷ�任������� (FT-IR) ��������Nicolet 5700�ͺ������������� (�����������˾��, KBrѹƬ��) ����;����ɼ�����������U-3010������ɼ������� (��ʽ�����) ���ԡ�
1.2 �����H4Si W12O40/Si O2/H2O2���Ʊ�
�ο�����[14-15]�����ܽ�-�������Ʊ�H4Si W12O40/Si O2����2 g H4Si W12O40�ܽ���26 mlˮ��, �������ԼΪ:2.5��1.0������������������������Һ�μӵ�H4Si W12O40��Һ�С�������, 45, 80���·ֱ����1, 1, 2 h������������45������¸���16.0 h, 90������¸���3.5 h�����ø�������90�����ˮϴ����ҺΪ���ԡ�Ȼ��, ���ڸ�����ʽ¯�н��л��
Ϊ���H4Si W12O40/Si O2�Կɼ���Ĺ������, ��30%H2O2��Һ�Դ���H4Si W12O40/Si O2��������������������������:��1 g H4Si W12O40/Si O2����15 ml 30%H2O2��Һ, Ȼ����20min����, ����, �������������ɡ������������������:H4Si W12O40/Si O2/H2O2��
1.3 ���������ȵIJ���
�ⷴӦװ�����ơ�500 ml�IJ�������������ʯӢ��Ϊ����, 500 W��믵� (�Ͼ��㽭���繤��) ��Ϊģ����Ȼ��Ĺ�Դ, ���ǿ��Ϊ1200��mol��m-2��s-1��������ͨ��ѭ��ˮ��ά��������Ӧ��������״̬����һ�����Ĵ����ͼ�����Һ���뵽�ⷴӦ����, ��ӦҺ�����������170 ml, ��ϡ���������������Һ, ������Һ��p Hֵ������Һ��������30 min, �Դﵽ�������л�Ⱦ�ϵ�����-�Ѹ�ƽ��, Ȼ�ƽ��й⽵��ʵ�顣��ÿ��һ����ʱ��, ȡ��Լ3.5 ml���ϲ���Һ, �������ĺ�, ͨ������ɼ������Dzⶨ������ȡ������� (DC) ͨ���¹�ʽ����:
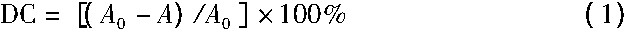
ʽ��A0�ǹ���ǰ�����������, A�ǹ���һ��ʱ������������ȡ�
2 ���������
2.1 �����ı���
����H4Si W12O40, H4Si W12O40/Si O2��H4Si W12O40/Si O2/H2O2�ĺ������ͼʾ��ͼ1����ʵ����H4Si W12O40�������ͼ��֪, 780 cm-1�� (W-O-W) , 925 cm-1�� (Si-O) ��982 cm-1�� (W=O) ��H4Si W12O40��Keggin�ṹ�������塣1624 cm-1Ϊˮ�����������շ�, �Ӷ�֤������ˮ�Ĵ��ڡ���H4Si W12O40��Si O2�������Ժ�, ��Щ�����巢���˸ı�, ����, Si O2�ı���OH���շ� (1074 cm-1) ���Եı��, �� (W=O) �ͦ� (Si-O) �ֱ�Ǩ��Ϊ1074, 931 cm-1���ɴ�˵��, ������Si O2�����ϵ�H4Si W12O40�Ծ���Keggin�ṹ, Ҳ֤����H4Si W12O40��Si O2�����ǻ�����ǿ�Ļ�ѧ����, ���Ǽ������������á�H4Si W12O40/Si O2/H2O2�Ĺ�����H4Si W12O40/Si O2����, ����, ���Կ�����935.2 cm-1������һ�������Ĺ��������շ�, ����������ữ��������շ��һ��[16,17]����ͼ1������֪, H4Si W12O40/Si O2��H4Si W12O40/Si O2/H2O2���Ӷ�����Ȼ��������Keggin�ṹ��ͬʱ, Ҳ�����Ӷ������������֮����ڽ�ǿ������á�
ͼ1 H4Si W12O40 (1) , H4Si W12O40/Si O2 (2) ��H4Si W12O40/Si O2/H2O2 (3) �ĺ������ͼFig.1 FT-IR spectra of H4Si W12O40/Si O2 (1) , H4Si W12O40/Si O2 (2) and H4Si W12O40/Si O2/H2O2 (3)
ͼ2ΪH4Si W12O40��H4Si W12O40/Si O2��XRDͼ����ͼ2��Ʒ��XRDͼ������֪, ��H4Si W12O40��8.15��, 10.23��, 20.85��, 23.25��, 25.65��, 28.05��, 34.71���37.80����ֽ�ǿ�������, �кܺõľ���, ����H4Si W12O4��Keggin�ṹ������H4Si W12O40/Si O2��XRD��ͼ��, ֻ������һ����ǿ�����ķ� (2��=24.15��) , �������Ե�H4Si W12O40�����������, ����H4Si W12O40/Si O2�ʵ��͵�����̬���ɴ˱���, H4Si W12O40�߶ȷ�ɢ��Si O2�����ϡ�
ͼ2 H4Si W12O40 (1) ��H4Si W12O40/Si O2 (2) ��XRDͼFig.2XRD patterns of H4Si W12O40 (1) and H4Si W12O40/Si O2 (2)
2.2 �����ڰ�����������-�Ѹ�ƽ�����
H4Si W12O40/Si O2/H2O2�����ڰ�����������-�Ѹ�ƽ��ʵ������ͼ3����ͼ3��֪, ��30 min���������ʱ��仯��б�����Դ���30 min֮��ı仯, ����30 min֮������Թ�ϵ, ��̽���Ķ���ѧ��ϵһ��, �ʿ�֪��30 min֮������-�Ѹ��Ѵﵽƽ��, ��Ҫ�ǹ�����������á�
2.3 ���ȳ�ʼŨ���Ż�
����Һp HΪ2.5, ��������Ϊ4 g��L-1 (ģ����Һ���170 ml, ����������Һ�����ͬ) ��������, �Լ��ȳ�ʼŨ�ȵ��Ż������ͼ4��ʾ����ͼ4��֪, �����ȳ�ʼŨ�ȵ�����, ������������, �ﵽһ��ֵ���ֿ�ʼ�½�, ��������һ�����Ĵ�������Һ�����������йء���ͼ3��֪, �ڹ����3.0 hʱ, ��ʼŨ��Ϊ15 mg��L-1�Ľ��������, ��˼��ȳ�ʼŨ��ѡ��15 mg��L-1��Ϊ���ʡ�
2.4 ���������Ż�
�ڼ��ȳ�ʼŨ���Ż�Ϊ15 mg��L-1, ������Һp HΪ2.5��������, �Դ��������ڹ�߽����е�Ӱ�����̽��, ʵ������ͼ5��
ͼ3 H4Si W12O40/Si O2/H2O2�����ڰ������������Ѹ�ƽ��ʵ��̽��Fig.3Results of adsorption and desorption for H4Si W12O40/Si O2/H2O2in dark
ͼ4 Ⱦ�ϵij�ʼŨ�ȶԹ⽵���Ӱ��Fig.4 Effect of initial dye concentration on photocatalytic ac-tivity of catalyst
��ͼ5��֪, �������������, �⽵��Ч�����ӡ��ڹ⽵��3.0 h, ��������Ϊ6 g��L-1ʱ, Ⱦ�ϼ�����ȫ�����⡣���, ����������ѡ��Ϊ6 g��L-1��
2.5 p H�Ż�
�ڼ��ȳ�ʼŨ��Ϊ15 mg��L-1, ����������Ϊ6 g��L-1��������, �����Һp HΪ3.8, �ڴ˻������о���Һp H�Ը���ϵ��Ӱ��, ʵ����ʾ��ͼ6��
ͼ5 �����������Թ⽵���Ӱ��Fig.5Effect of catalyst dosage on photocatalytic activity of catalyst
ͼ6 ��ӦҺp H�Թ⽵���Ӱ��Fig.6 Effect of solution p H on photocatalytic activity of catalyst
��ͼ6��֪, ��p H��Сʱ, �������Ч�����, ���������ΪH4Si W12O40�ڴ������½�Ϊ�ȶ�������, ��Һp HΪ1.0��Ϊ��õ�������
2.6 ����������ԱȽ�
�ڼ��ȳ�ʼŨ��Ϊ15 mg��L-1, ����������Ϊ6 g��L-1����Һp HΪ1.0��������, �о��˸���δ������δ����δ�������������������Ч��, �����ͼ7��ʾ��
��ͼ7��֪, ������������, ����3.0 h, H4Si W12O40���������ȵĽ�����Ϊ3.7%, H4Si W12O40/Si O2���������ȵĽ�����Ϊ42.6%, H2O2����H4Si W12O40/Si O2�����, H4Si W12O40/Si O2/H2O2���������ȵĽ����ʿɴ�99.0%�����ͬʱ, ��30%H2O2ϡ��1000��, Ȼ��ȡ1 ml����Һ���뵽170 ml�ļ��ȷ�ӦҺ��, ���Ż��������й������ʵ��, ������Ϊ9.7%, �ʿɱ����ڱ�ʵ��ķ�Ӧ��, ��������H2O2�Թ�������ú�С���ɴ˿ɼ�, H2O2����H4Si W12O40/Si O2�����, H4Si W12O40/Si O2/H2O2���������ȵĽ�������������H4Si W12O40��δ��H2O2������H4Si W12O40/Si O2�������������ʵ����, �ӹ�ҵ���ϵ�ʵ�ʳ���������ΪH4Si W12O40/Si O2/H2O2��Ϊһ�ֹ�����ǿ��е�, �������õ�Ӧ��ǰ����
ͼ7 H4Si W12O40, H4Si W12O40/Si O2��H4Si W12O40/Si O2/H2O2����������ȵ�̽��Fig.7Results of methyl orange degradation by H4Si W12O40, H4Si W12O40/Si O2and H4Si W12O40/Si O2/H2O2
2.7 �����������ȶ���ѧ����
�ڼ��ȳ�ʼŨ��Ϊ15 mg��L-1, ����������Ϊ6 g��L-1����Һp HΪ1��������, ��H4Si W12O40/Si O2/H2O2�����⽵����ȵĶ���ѧ�������о�, �����ͼ8��ʾ;ͼ��c0Ϊ������Һ�ij�ʼŨ��, cΪ�������ijһʱ�̵���ҺŨ�ȡ���ͼ8���Կ���ln (c0/c) ��ʱ��t���кܺõ����Թ�ϵ, �Ӷ�˵��������������ҺΪһ������ѧ��Ӧ����Langmuir-Hinshelwoodһ����Ӧ��ʽ��֪, ln (c0/c) =K��t����ø������µĹ⽵����ϵķ�Ӧ���ʳ��� (K) Ϊ1.553 h-1, �����Թ�ϵΪ0.9960��
ͼ8 ln (c0/c) ��ʱ��Ĺ�ϵFig.8 Relation of ln (c0/c) and time
ͼ9 H4Si W12O40/Si O2/H2O2�⽵�ⲻͬȾ�ϵ�̽��Fig.9 Light catalyst degradation of different dyes by H4Si W12O40/Si O2/H2O2
2.8 H4Si W12O40/Si O2/H2O2�⽵�ⲻͬȾ�ϵ�̽��
�ڼ��ȳ�ʼŨ��Ϊ15 mg��L-1, ����������Ϊ6 g��L-1����Һp HΪ1.0��������, �о��˴���H4Si W12O40/Si O2/H2O2�Բ�ͬȾ�ϵĹ������Ч��, �����ͼ9��ʾ��
��ͼ9���Է���, H4Si W12O40/Si O2/H2O2�Լ��ϡ���ȸʯ�̡��Ǽ���������B�ͼ�������нϸߵĹ⽵�����, ������Ϊ87.5%~100.0%�����, �ô����кܹ��������, �������õ�Ӧ��ǰ����
2.9 H4Si W12O40/Si O2/H2O2�벻ͬ�������ԶԱ�
H4Si W12O40/Si O2/H2O2��Y2O3-Bi2O3, Co����Zn O, Ag/Fe2O3-Ti O2�����Ĵ�Ч�����ڱ�1��
ͨ����1���ݱȽ�, H4Si W12O40/Si O2/H2O2�Ĺ��������Ա�Y2O3-Bi2O3, Co����Zn O, Ag/Fe2O3-Ti O2����Ҫ��, ˵��H4Si W12O40/Si O2/H2O2�Լ��Ⱦ������õĹ��������ԡ�
2.1 0 H4Si W12O40/Si O2/H2O2�������ظ�����
�ڼ��ȳ�ʼŨ��Ϊ15 mg��L-1, ��Һp HΪ1.0, ����������Ϊ6 g��L-1, ������3 h���Ż������, ̽���˴���H4Si W12O40/Si O2/H2O2���ظ��������ܡ����⽵�ⷴӦ�����Ժ�, ���������, ���¶�Ϊ100���¸���2 h, ��������H2O2���д�������������һ�η�Ӧ���������ظ����ý����ͼ10��
��ͼ10��֪, ����ʹ��4��, �ô����Ĺ��������ȵĽ����ʷֱ�Ϊ99.0%, 95.2%, 96.6%��88.7%, ���������Բ�û��̫��仯����Ҳ˵��, ���������������ڽ�ǿ�Ļ�ѧ����, ʹ��ʱ�����������, ��ʾ��ṹ���нϺõ��ȶ��ԡ�
3 ����
ͨ���ܽ�-��������H4Si W12O40������Si O2��, ����H2O2��Һ��������, ���������ģ����Ȼ���µĴ�����, �Ʊ�H4Si W12O40/Si O2/H2O2����������Ըô����⽵����ȵ�Ӱ�����ؽ�����̽��, �ڼ���Ϊ15 mg��L-1, ��Һp HΪ1.0, ����������Ϊ6 g��L-1���Ż������, �⽵��3.0 h, ���ȵĽ����ʴﵽ99.0%��H4Si W12O40/Si O2/H2O2�����������������ҺΪһ������ѧ��Ӧ����H4Si W12O40/Si O2/H2O2�Լ��ϡ���ȸʯ�̡��Ǽ���������B�ͼ�������нϸߵĹ������, �����ʴ�87.5%~100.0%��
ͼ1 0 H4Si W12O40/Si O2/H2O2�������ظ�ʹ��̽��Fig.10 Results of repeated use for H4Si W12O40/Si O2/H2O2
��1 H4Si W12O40/Si O2/H2O2�벻ͬ�������ԶԱ�Table 1 Comparison of catalytic activity between H4Si W12O40/Si O2/H2O2and other catalysts ����ԭͼ
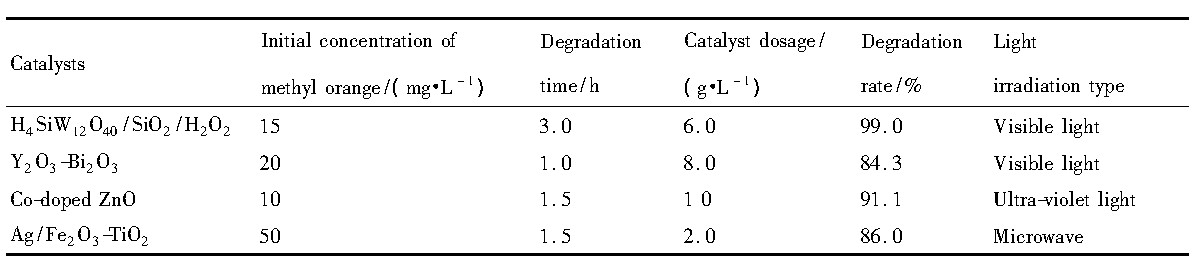
��1 H4Si W12O40/Si O2/H2O2�벻ͬ�������ԶԱ�Table 1 Comparison of catalytic activity between H4Si W12O40/Si O2/H2O2and other catalysts
���ʵ��������, ����H2O2����H4Si W12O40/Si O2�����Թ��������ȡ����ϡ���ȸʯ�̡��Ǽ���������B�ͼ�������нϺõĻ���, ��ģ����Ⱦ��Ĵ���ȡ���˽Ϻõ�Ч��, �������õ�Ӧ��ǰ����
�����

