���±�ţ�1004-0609(2010)05-0891-07
Mg-Zn-Ca��Ԫþ�Ͻ�������ϵĸ�ʴ��Ϊ
ŷ����1���� ��1���� ��1�������1, 2������ɽ3
(1. ���ϴ�ѧ ��ĩұ������ص�ʵ���ң���ɳ 410083��
2. ���ϴ�ѧ ����ҽԺ����ɳ 410008��
3. ���ϴ�ѧ ����ҽѧԺ����ɳ 410013)
ժ Ҫ����Zn��CaΪ�Ͻ���Ԫ���������ڽ�ע���Ʊ�3��Ca�����ֱ�Ϊ1%��2%��3%��Mg-Zn-Ca��Ԫþ�Ͻ�����ɽ�����ϣ�����3��þ�Ͻ���Hankģ����Һ�е�������ʧ��ʴ���绯ѧ��ʴ��Ϊ�����о����Բ�ͬ��ʴʱ��ĺϽ������ò�Լ��Ͻ���֯����ɷֽ��з��������������þ�Ͻ�ĸ�ʴ�Ǵ�þ����ĵ�ʴ��ʼ�ģ���Ca��Ϊ1%��þ�Ͻ���ֳ����õĿ���ʴ���ܣ��Ͻ���Mg2Ca��ķֲ�����Ӱ��Ͻ����ʴ���ܣ��Ͻ�����Mg2Ca��ĺ������źϽ���Ca���������Ӷ����ӣ����ºϽ�Ŀ���ʴ���ܱ�
�ؼ��ʣ�Mg-Zn-Ca�Ͻ�Hank��Һ���绯ѧ��ʴ��Mg2Ca�ࣻ���オ��
��ͼ����ţ�TG146.23���� ���ױ�־�룺A
Corrosion behaviours of ternary Mg-Zn-Ca alloy biomaterials
OUYANG Chun1, LEI Ting1, WANG Li1, LI Nian-feng1, 2, ZHOU Le-shan3
(1. State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China;
2. Xiangya Hospital, Central South University, Changsha 410008, China;
3. Xiangya School of Medicine, Central South University, Changsha 410013, China)
Abstract: With elements of Zn and Ca as alloy components, three kinds of degradable ternary Mg-Zn-Ca alloys with Ca contents of 1%, 2% and 3%(mass fraction), respectively, were fabricated by melting and casting. The mass loss measurement and electrochemical corrosion technique were employed to study their corrosion behaviours in Hank��s simulated body fluid. The results based on the SEM morphology observation and analyses of structures and phases show that the corrosion of Mg alloy begins from pitting corrosion at Mg matrix. The ternary alloy with 1% Ca shows an enhanced corrosion resistance, and the existence and distribution of Mg2Ca phase in alloy significantly affect its corrosion-resisting performance. The content of Mg2Ca phase in alloy increases with the increase of Ca content, leading to a poor corrosion resistance for alloy.
Key words: Mg-Zn-Ca alloy; Hank solution; electrochemical corrosion; Mg2Ca phase; biodegradation
��������þ��þ�Ͻ���Ϊ��������������ܵ�Խ��Խ��Ĺ�ע��þ��һ�����ʽ����������������Ĥ������ܶ�[1-2]�͵���ģ��[3]������[4]�����������Ժõ��ŵ㡣��Ŀǰ�ٴ����ձ���õ��ѺϽ𡢲���ֵȽ���ֲ�������ȣ�þ�Ͻ���������ᣬ����ģ�����ӽӽ���������֯������Ӧ���ڵ�[5]���ŵ㣬������Ϊ��������þ�����ܹ�ͨ���³´�л��ȫ�ų�����[6]����ˣ�þ��þ�Ͻ���ΪӲ��֯�����Ϻ���Ѫ��֧�ܲ������ٴ�ҽѧӦ���Ͼ��й�����ǰ����
þ�ı��缫��λΪ-2.34 V����ѧ���ʼ�Ϊ���ã������Ľ���þ�ڽ����м�������ʴ����ˣ�ͨ�����úϽ�����ǿþ����ʴ���ܡ�Ŀǰ������ҽ��þ�Ͻ���о���Ҫ������þ���Ͻ��þϡ��Mg-RE�Ͻ�ϵ�С�WITTE��[7]�Ƚ���AZ31��AZ91��WE43��LAE422��4��þ�Ͻ���ֲ���ڶ������ڵĸ�ʴ�����ص����֯��þֲ����ķ�Ӧ������þ�Ͻ���бȿɽ���ۺ�����õĹ���֯�����Ժ���֯�յ����ܡ���Щþ�Ͻ�����Ni��Al��Zr�ȺϽ�Ԫ������ǿþ��������ʴ�ԡ��������о�����ָ����ЩԪ�ؾ����°��ԡ��������Լ���ϸ�������Զ���[8-9]����ˣ��������и���ϸ�����Ժ�ϸ�������Ե�����þ������ɽ������ղ��Ͼ�����Ҫ��ҽ���ٴ�Ӧ�ü�ֵ����ǰ�������������ҹ�ѧ��ҲΪ�˿�չ�˹㷺���о���SONG[10]�о������ڴ�þ������ZnԪ���ܹ����������Ͻ�ĸ�ʴ�ٶȣ��Ժ�Znþ�Ͻ�����MnԪ�غ�Ͻ�ĸ�ʴ���������ܹ������������ҳϵ�[11]�о��˴�þ��þпϵ�кϽ��ڷ�����Һ�еĸ�ʴ��Ϊ�����ӽ� ��[12]�۲�þ�ƺϽ������ϸ��������Ӱ�죬����þ�ƺϽ����Һû�б��ֳ�ϸ���������ã����ֳ����õ�ϸ�������ԡ�
�ڴˣ�����������Ӫ��Ԫ��Zn��Ca��Ϊ�Ͻ���Ԫ���Ʊ�Mg-Zn-Ca ��Ԫþ�Ͻ����У�Zn������Mg�γ�MgZn�࣬���й���ǿ����ʱЧǿ����˫�����ã�Ca�ܹ�������Ĺ���������ȼ���ã�ͬʱϸ���Ͻ���֯�ľ������γ�Mg2Ca��[13-14]���Ӷ����þ��ǿ�Ⱥ����ԡ�������Ԫþ�Ͻ���Hankģ����Һ�е�������ʧ��ʴ���绯ѧ��ʴ��Ϊ�����о���ͨ���Բ�ͬ��ʴʱ��Ͻ������ò�Ĺ۲��Լ��Ͻ���֯����ɷֵķ�����̽����Ԫþ�Ͻ���ģ����Һ�еĸ�ʴ������
1 ʵ��
1.1 �Ͻ���Ʊ�
�Դ���Ϊ99.99%��þ����п���Լ�����Ϊ99.8%�ĸ�мΪԭ�ϡ����������þ������ʯī�����У�������գ�ͨ��CO2��SF6�����������������700~ 800 �����10~20 min����þ��ȫ���ۻ������������п��ԭ�ϣ��趨�����¶�Ϊ750 �棬��������25~45 min���ڱ��������³���ע��Ԥ����200 ��Ľ���ģ���У�������ֱ��Ϊ50 mm�ĺϽ�
������Ʒ�����и�Ƴ�14 mm��5 mm��Բ���������顣
1.2 ������ʧ��ʴ
��3�ֺϽ�ı�����ɰֽ��ĥ�⻬���ڱ�ͪ��Һ
�г������10 min��������������ʢ��100 mL Hankģ����Һ��ĥ��ƿ��(Hankģ����Һ�����[13]��NaC l8.0 g/L��KCl 0.4 g/L��CaCl2 0.14 g/L��NaHCO3 0.35 g/L��D-C6H6O6 0.35 g/L��MgSO4?7H2O 0.2 g/L��KH2PO4 0.1 g/L��Na2HPO4?12H2O 60 mg/L����50 mmol/LϡHCl��(CH2OH)3CNH2����pHֵΪ7.2~7.4)��(37��1)����£�9 d��ȡ����Ȼ����20%�����1%��������Һ�����2 min����ȥ��������ĸ�ʴ������ֱ��ڱ�ͪ�;ƾ��г�����ϴ10 min�����¸�����ھ���Ϊ0.1 mg�ĵ�����ƽ�ϳ������ظ����ϲ��轫ÿ�ֺϽ���Ʒ����3��ƽ�����顣
��ʴ���ʸ��ݹ�ʽv=��m/(At)����[15]�����У���mΪ��ʴǰ������Ʒ��������ʧ��AΪ�Ͻ����ǰ�ļ��������tΪ����ʱ�䡣
1.3 �绯ѧ��ʴ
��3�ֺϽ�ֱ�¶һ������Ϊ�����棬����������֬�ܷⲢ����һ�����ߣ��Ա�¶�ĺϽ��������ɰֽ��ĥ��ͱ�ͪ���������������缫��ϵ��������Ϊ�����缫���αȵ缫���ñ��ʹ��缫������Ϊ���ŵ�³��ëϸ�ܵĶ˿ھ������������缫���棬�Լ�С��Һ���裬��˿��Ϊ�Ե缫����CHI660C�绯ѧ����վ�Ͻ��е绯ѧ��ʴ���ԡ��ڿ�·��λ��-200~200 mV���䣬��5 mV/s��������ɨ�������ƶ����ߡ�
1.4 �������
��DMAX3C��X����������(XRD)���кϽ���Ʒ�ijɷַ�������HITACHI S-650��ɨ��������� (SEM)�۲�Ͻ���Hankģ����Һ�зֱ����5 h��3 d��ı��港ʴ��ò������EDAX���ױ�����ʴ����� �ɷ֡�
2 ���������
2.1 ��̬��Ʒ���۽ṹ
ͼ1��ʾΪMg-Zn-Ca��Ԫ��̬�Ͻ��SEM�Ͻ��Ԫ��������1���С���ͼ1��֪�����źϽ���Ca���������ӣ��Ͻ�ľ����ø��������������ߴ�Ҳ��С��������ͨ������״���ں�Ca��Ϊ3%�ĺϽ�C�пɼ����Ե���״����ṹ��˵��CaԪ�صļ��������ںϽ�ľ���ϸ�������⣬����û�г��ֵڶ������ӵ�ƫ����

ͼ1 3�ֺϽ��SEM��
Fig.1 SEM images of ternary casting alloys: (a) Alloy A; (b) Alloy B; (c) Alloy C
��1 3�ֺϽ��Ԫ�����
Table 1 Compositions of three kinds of alloys

ͼ2��ʾΪ��Ԫ�Ͻ��XRD�ס���ͼ2��֪��3��þ�Ͻ��г�þ�����⣬����MgZn��Mg2Ca�ࡣ���У�MgZn����й���ǿ����ʱЧǿ����˫�����ã��������ڸ���þ�Ͻ����ʴ���ܡ�����Ca���������ӣ��Ͻ���Mg2Ca��ķ�ǿ������ǿ��ͼ3��ʾΪ�Ͻ���ɨ��羵�µľ���ɷַ�������������ھ��紦�����˸����Ca�ɷ֡�
2.2 ������ʧ��ʴ�͵绯ѧ��ʴ
��2����Ϊ3�ֺϽ���ģ����Һ�к���37 ����������9 d��3��ƽ�����������ƽ����ʴ���ʡ�

ͼ2 3�ֺϽ��XRD��
Fig.2 XRD patterns of ternary alloys: (a) Alloy C; (b) Alloy A; (c) Alloy B
��2 �Ͻ��������ʧ��ʴ����
Table 2 Mass loss rates of alloys for corrosion

�ɱ�2��֪�Ͻ�A����ʴ������ã�����ǺϽ�B���Ͻ�C�ĸ�ʴ�������ʱȺϽ�A�Ŀ��˽�4����˵��CaԪ�صļ�������Ӱ����Ԫþ�Ͻ�Ŀ���ʴ ���ܡ�
ͼ4��ʾΪ3�ֺϽ�����ƶ��绯ѧ��ʴ���ߡ�ͨ���������������߱�ʾˮ��ԭ���������������������̣������������߱�ʾ����þ���ܽ����[16]��һ������£���ʴ��λԽ������ʴ�����ܶ�ԽС������ϵĸ�ʴ����ԽС�������ϵ���ʴ����Խǿ�������ƶ����߿�֪��3�ֺϽ���Ը�ʴ��λ��-1.64 ~ -1.67 V�������þ�ı��缫��λ(-2.34 V(vs SHE))����ʴ��λ���д���ȵ����ƣ�˵���Ͻ��������ƺ���ǿþ��������ʴ���ܡ������ƶ����ߵ�б�ʽ�������Ӧ�ĵ����ܶȼ����Լ�������������ĵ绯ѧ��ʴ���ʡ�
��3����Ϊ�������ƶ���������Ը�ʴ�����ܶȡ��Ը�ʴ��λ��ʴ���ʡ��ӱ�3�ɼ������źϽ���Ca���������ӣ��Ͻ���ֳ��Ŀ���ʴ���ܱ�3�ֺϽ�ĵ绯ѧ��ʴ���ʴӸߵ��͵�˳��Ϊ�Ͻ�C���Ͻ�B�ͺϽ�A���Ͻ�A����ʴ������ã���������ʧ��ʴ���ⶨ�Ľ��һ�¡�ֵ��ע����ǣ�����������

ͼ3 �Ͻ紦������ͼ
Fig.3 EDAX spectra at grain boundary of alloys: (a) Alloy A; (b) Alloy B; (c) Alloy C
����������ɨ�赽2.0 Vʱ���������߱��ֳ��Ͻ�������ܽ��û�г��ֶۻ������������Hankģ����Һ�д��ڽϸ�Ũ�ȵ��������йأ�˵����������Ũ�ȸߴ�0.145 mol/L����Һ�У�����������þ�Ͻ���������γ����ܵĶۻ�����Ĥ����һ���γɾͱ������ӿ��ٻ���[17-18]����Ҳ��������������ʧ��ʴ�ⶨʱ���ӳ�����ʱ�����۲쵽þ�Ͻ�����Ĵ����������

ͼ4 �Ͻ�绯ѧ��ʴ�����ƶ�����
Fig.4 Tafel curves of alloys in electrochemical corrosion
��3 3�ֺϽ�ĵ绯ѧ��ʴ����
Table 3 Data of three kinds of alloys for electrochemical corrosion

��������ʧ��ʴ�͵绯ѧ��ʴ�ⶨ�Ľ����֪���Ͻ���Ca�ļ�����Ӱ��Ͻ����ʴ���ܣ����2.1�ںϽ���۽ṹ�������Ͻ�B��C����ʴ�ԽϺϽ�A���ԭ��Ӧ�ù����ڴ���Mg2Ca��Ĵ��ڣ���һ�Ʋ�Ҳ������[13-14, 19-20]֤ʵ��KIM��[19]�о�Mg-Ca��Ԫ�Ͻ�ʱ����Mg2Ca�ĺ�����ֲ��ܹ����ƺϽ�Ŀ���ʴ���ܺ������IJ������ʡ�����[21]����Mg2Ca��ĸ�ʴ��λΪ-1.54 V(vs SCE)��������þ ��ƽ���λΪ-2.61 V(vs SCE)[22]����ˣ���Mg2Ca�������þ���Ͻ�����ʱ������Һ��Ͻ���Ľ��洦���Ͻ��е�Mg2Ca�ཫ��Ϊ���������þ������Ϊ��������ԭ��أ�����þ����ĸ�ʴ����������þ���ӽ�����Һ�����źϽ���Ca���������ӣ�Mg2Ca��ĺ���Ҳ��Ӧ���ӣ����������γ�Mg-Mg2Caԭ��أ��Ӷ��ӿ�þ����ĸ�ʴ����ͽ����˺�Ca��Ϊ3%�ĺϽ�C����������ʴ�����ԭ���ɴ˿ɼ������� ͨ������Ca�ļ���������Ч����þ�Ͻ�ĸ�ʴ�������ʡ�
2.3 �Ͻ���Hankģ����Һ�еĸ�ʴ����
�о����ֽ��Ͻ���Ʒ����ģ����Һ��2~3 min�Ͻ����ܿ��������������ֲ���ʼ�������Եĵ�ʴ���ټ������ݵ�5 h����SEM����ͼ5(a)��ʾ��ͼ5(b)��ʾΪ����3 d��Ͻ��SEM����ʾ���Ͻ����IJ������ݡ����ʵ��۲���ͼ5��֪���ڸ�ʴ���ڣ�����þ���ӵ��γɲ�������Һ����Ʒ����ֲ���������ʴ�ƻ���ͬʱ������������IJ�����ͼ5(a)��ʾ�ı���������������Ʒ��������е���ˮ���£����ֱ�����Ȼ�������������Ž���ʱ����ӳ���ʴ����Ŀ�����ӣ���ʴ�ƻ������������ʴ���̴ӱ������ڲ����룬������ʴ�����ڱ��渽�ų������������ڱ���þ�������ȫ��ʴ�ƻ������±��㲿�����䡣

ͼ5 �Ͻ�A��ģ����Һ�н���5 h��3 d���SEM��
Fig.5 SEM images of alloy A after being immersed in Hank��s SBF for 5 h (a) and 3 d (b)
�ںϽ��������ݵij��ڣ����۲쵽��ͼ6(a)��ʾ�Ľᾧ״�������ںϽ�����������ͼ6(b)��ʾ��EDAX��������ʾ�ó������и���������Cl-��CO32-��þ���ӣ�����û����������ӣ��ɴ��Ʋ�ýᾧ״�������Ǻ��Ⱥ�̼������ӵ�þ�Σ�����ܵĻ�ѧ��Ӧʽ���£�
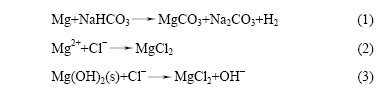

ͼ6 �Ͻ�A��ģ����Һ�н���5 h���SEM���EDAX��
Fig.6 SEM image (a) and EDAX spectrum (b) of alloy A after being immersed in SBF for 5 h
ͼ7��ʾΪ�Ͻ�B��ģ����Һ����������3 d���SEM���Լ���Ӧ�ڱ�����ڲ�������EDAX���ס�ͬͼ5(b)��ʾ�ĺϽ�A�ĸ�ʴ��òһ�����ںϽ�B�ı�������˴��������ﲢ�����˱�������������ݣ�������ָ��������ڲ���������Ҫ�ɷ��Ǻ��ƺ�þ�������Ρ���Ȼ���о�[13]����þ������ģ����Һ�н���һ��ʱ����������������ǻ���ʯ(HA)�����ǵĽ����ʾ����������γ������Ca��P������Ϊ1.21���ڲ�������γ������Ca��P������Ϊ1.18���ң���С���γ��ǻ���ʯ����Ca��P������Ϊ1.67��������
����������������Ϊþ�Ͻ���ĸ�ʴ����������һ�ֵ绯ѧ��Ӧ���̡����ںϽ���Mg2Ca���ƽ���λ�Ͻ���þ�������ö࣬Mg2Ca������þ�����ԭ���Mg-Mg2Ca��þ�Ͻ�ĸ�ʴ���̿��Ա������¡�
1) ���ȣ��Ͻ�����Ϊ������þ�����ϵĽ���þ��ʽ(4)��ʾ�ķ�Ӧ�ܽ��þ���ӽ�����Һ�У�����Ϊþ����ĵ�ʴ����Ϊ������Mg2Ca����������������

ͼ7 �Ͻ�B��ģ����Һ�н���3 d���SEM���Լ���Ӧ��EDAX��
Fig.7 SEM image (a) and EDAX spectra ((b) and (c)) of alloy B after being immersed in SBF for 3 d corresponding to correlated areas A and B in Fig.7(a)
��ʽ(5)�ķ�Ӧ��ʾ��ͬʱ�����ɵ�������þ��ɫ�����ﰴʽ(6)��ʾ�ķ�Ӧ�ںϽ����������
2) �ڸ�ʴ���ڣ�����ģ����Һ�й��������Cl-��CO32-������������þ�������Լ�þ���ཫ��Cl-��CO32-��Ӧ�γ�MgCl2��MgCO3�����Ÿ�ʴ���̵ļ���������ֲ������MgCl2��MgCO3���Ͷ���������MgCl2��MgCO3�ɺ�ʱ��MgCl2��MgCO3�ξͻ��ںϽ���Ʒ����ᾧ������
3) ���Ÿ�ʴ��Ӧ�Ľ��У���Һ��ͨ�����ɵij������������ڲ�ĺϽ��壬ʹ�ڲ�þ��������������ʴ��Ӧ���ܽ��þ����Ҳͨ�����ɵij�����Ǩ�Ƶ��Ͻ���棬ͬʱ��Һ��pHֵ��ʴ����(��ʽ(5)�ķ�Ӧ)����OH-���������Ͻ����ʾֲ������ʱMg2 +��OH-���һ������Mg(OH)2������
4) ���ŷ�Ӧ(4)~(6)�IJ����ظ���Mg(OH)2��������Խ��Խ����Һ�д��ڵĸ����Ӻ����������������Mg(OH)2���������γ��������������ͬʱ�Ͻ�����ֲ��Ͻ�����þ�������ȫ��ʴ��������������ݡ�

3 ����
1) �Ʊ���Mg-Zn-Ca��Ԫþ�Ͻ�������ϲ����ֺϽ�Ԫ��Ca�ļ���������ϸ��þ�Ͻ�ľ������Ͻ����γɵ�Mg2Ca��������Ӱ��Ͻ�Ŀ���ʴ���ܡ�
2) ��Ca��Ϊ1%��þ�Ͻ���ֳ����õĿ���ʴ���ܣ�����Ca�ļ�����γɴ�����Mg2Ca�࣬����������þ�Ͻ����ʴ���ܡ�
3) þ�Ͻ�ĸ�ʴ�Ǵ�þ����ĵ�ʴ��ʼ�ģ��ڸ�ʴ���ڣ�þ���Ȼ����̼���νᾧ�������������Ÿ�ʴ�����룬����ֲ��������������������þ�������ڸ�ʴ���ڣ��д�����þ�Ƶ������γ�������������������������䡣
REFERENCES
[1] ������. ����ҽ�ò��ϵ���[M]. �人: �人��ҵ��ѧ������, 2000: 52-71.
LI Shi-pu. Introduction of biomedical materials[M]. Wuhan: Wuhan University of Technology Press, 2000: 52-71
[2] ����, ������. Ӧ���ڵ�ЧӦ��Ѱ�Ҷ�ʧ��Կ��[J]. �л����˹ǿ���־, 2002(4): 62-64.
LIU Zhen-dong, FAN Qing-yu. Stress shield effect��Search the lost key[J]. Chinese Wound and Bone, 2002(4): 62-64.
[3] KIM S G, INOUE A, MASUMOTO T. Increase of mechanical strength of a Mg85Zn12Ce3 amorphous alloy by dispersion of ultrafine hcp-Mg particles[J]. Mater Trans, 1991, 32(9): 875-878.
[4] KIM S R, LEE J H, KIM Y T. Synthesis of Si, Mg substituted hydroxyapatites and their sintering behaviors[J]. Biomaterials, 2003, 24(8): 1389-1398.
[5] ������, ����÷, ������. �ѺϽ���ֲ���ٴ����ѵ�ԭ�����[J]. ϡ�н��������빤��, 2004, 33(4): 442-444.
WANG Qing-tao, ZHANG Yu-mei, HU Nai-sai. Microstructure analysis of fractured Ti alloy implant[J]. Rare Metal Materials and Engineering, 2004, 33(4): 442-444.
[6] ��ͤ͢, ̷����, �ܵ���, �ű���, �� ��. ҽ��þ�������ϵ��о���չ[J]. ���ϵ���, 2008, 22(1): 110-129.
YAN Ting-ting, TAN Li-li, XIONG Dang-sheng, ZHANG Bing-chun, YANG Ke. Researching progress of biomedical Mg alloys[J]. Material Review, 2008, 22(1): 110-129.
[7] WITTE F, KAESE V, HAFERKAMP H, SWITZER E, MEYER L A, WIRTH C J, WINDHAGEN H. In vivo corrosion of four magnesium alloys and the associated bone response[J]. Biomaterials, 2005, 26: 3557-3563.
[8] HAUDRECHY P, FOUSSEREAU J, MANTOUT B, BAROUX B. Nickel release from 304 and 316 stainless steels in synthetic sweat: Comparison with nickel and nickel-plated metals[J]. Corros Science, 1993, 35: 329-336.
[9] K?STER R, SOMMERAUER M, K?HLER J, BALDUS S, MEINERTZ T, HAMM C W. Nickel and molybdenum contact allergies in patients with coronary in-stent restenosis[J]. The Lancet, 2000, 356(9245): 1895�C1897.
[10] SONG G L. Control of biodegradation of biocompatible magnesium alloys[J]. Corrosion Science, 2007, 49: 1696�C1701.
[11] �ҳ�, �� ɳ, ����Ӣ, �� ��. þ��þ�Ͻ��ڷ�����Һ�еĸ�ʴ������Ϊ[J]. �й���֯�����о����ٴ�����, 2007(18): 3584�C3586.
GAO Jia-cheng, WU Sha, QIAO Li-ying, WANG Yong. Corrosion behavior of magnesium and its alloy in simulated body fluid[J]. Journal of Clinical Rehabilitative Tissue Engineering Research, 2007(18): 3584�C3586.
[12] ���ӽ�, �� ��, ¦˼Ȩ, ֣���. þ�ƺϽ��ϸ�������о�[J]. �й�����ؽ�������־, 2007, 9(22): 740�C742.
LI Zi-jian, ZHANG Ke, LOU Si-quan, ZHENG Yu-feng. A cellular study on cytotoxicity of magnesium-calcium alloy[J]. Chinese Journal of Bone and Joint Injury, 2007, 9(22): 740�C742.
[13] LI Z J, GU X N, LOU S Q, ZHENG Y F. The development of binary Mg-Ca alloys for use as biodegradable materials within bone[J]. Biomaterials, 2008, 29: 1329-1344.
[14] ������, ������, ���ٷ�. ��������þ�Ͻ��е�����[J]. ����, 2003, 54(14): 246-248.
LIU Sheng-fa, FAN Xiao-ming, WANG Zhong-fan. The effect of Ca in the process of casting Mg alloys[J]. Foundry, 2003, 54(14): 246-248.
[15] LIU C, XIN Y, TANG G, CHU P K. Influence of heat treatment on degradation behavior of bio-degradable die-cast AZ63 magnesium alloy in simulated fluid[J]. Mater Sci Eng A, 2007, 456: 350-357.
[16] JIAN W C, XING W G, PENG H F, LI M P, WEN J D. Effect of heat treatment on corrosion and electrochemical behavior of Mg-3Nd-0.2Zn-0.4Zr (wt%) alloy[J]. Electrochim Acta, 2007, 52: 3160-3167.
[17] ������, �ҳ�, �� ��. ҽ��þ�Ͻ�ĸ�ʴ��Ϊ��������[J]. ���ϵ���, 2003, 17(10): 29-32.
LI Long-chuan, GAO Jia-cheng, WANG Yong. The corrosion behavior and surface modification of biomedical Mg alloys[J]. Material Review, 2003, 17(10): 29-32.
[18] ������, �ƾ���, �� ��, �ű���, Ҧ־��, �� �. ��þ�����︯ʴ�о�[J]. ����ѧ��, 2005, 41(11): 1228-1232
REN Yi-bing, HUANG Jing-jing, YANG Ke, ZHANG Bing-chun, YAO Zhi-ming, WANG Hao. Study of biocorrosion of pure magnesium[J]. Acta Metall Sinca, 2005, 41(11): 1228-1232.
[19] KIM W C, KIM J G, LEE J Y, SEOK H K. Influence of Ca on the corrosion properties of magnesium for biomaterials[J]. Materials Letters, 2008, 62: 4146-4148.
[20] ZHANG E L, YANG L. Microstructure, mechanical properties and bio-corrosion properties of Mg-Zn-Mn-Ca alloy for biomedical application[J]. Mater Sci Eng A, 2008, 497: 111-118.
[21] KIM J G, KIM Y W. Advanced Mg-Mn-Ca sacrificial anode materials for cathodic protection[J]. Mater Corros, 2001, 52: 137-139.
[22] JONES D A. Principles and prevention of corrosion[M]. 2nd ed. London: Prentice-Hall, 1996.
(�༭ �� ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(50721003)�����ϴ�ѧ��ĩұ������ص�ʵ���ҿ��Ż���������Ŀ
�ո����ڣ�2009-03-09�������ڣ�2009-08-25
ͨ�����ߣ��� �������ڣ���ʿ���绰��13203176590��E-mail: tlei@mail.csu.edu.cn