文章编号:1004-0609(2008)01-0177-10
杂环化合物对热浸镀锌铝合金镀层在稀盐酸中的缓蚀作用
鞠 虹1, 2,李 焰1
(1. 中国科学院 海洋研究所,青岛 266071;2. 中国科学院 研究生院,北京 100039)
摘 要:为找到在热浸镀钢材表面清洗处理过程中替代铬酸使用的缓蚀剂,通过质量损失测试、电化学测试和扫描电镜分析等方法研究了烟酸、吖啶和小檗碱对热浸镀5%铝?锌和55%铝?锌合金镀层在盐酸介质中的缓蚀作用。结果表明,3种杂环化合物在盐酸介质中对两种锌铝合金镀层均具有良好的缓蚀作用,其中小檗碱的缓蚀作用最好;它们通过单分子层、化学吸附方式吸附在镀层表面从而阻滞酸液对镀层的腐蚀,其吸附遵从Langmuir吸附等温式。在盐酸介质中,烟酸、吖啶和小檗碱对5%铝?锌和55%铝?锌合金镀层钢材均为有效的环境友好型缓蚀剂。
关键词:缓蚀剂;杂环化合物;盐酸;电化学阻抗谱
中图分类号:TG 174.42 文献标识码:A
Corrosion inhibition of hot dipping Zn-Al alloy coated steels by heterocyclic compounds in diluted HCl solutions
JU Hong1, 2, LI Yan1
(1. Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China;
2. Graduate School, Chinese Academy of Sciences, Beijing 100039, China)
Abstract: In order to find chromate-substituting inhibitor in finishing process of hot dipping coated steels, the inhibition effects of nicotinic acid, acridine and berberine on the corrosion of hot dipping 5%Al-Zn and 55%Al-Zn alloy coated steels in diluted HCl solution were investigated using mass loss test, electrochemical measurement, and scanning electronic microscope analysis. The results indicate that these three heterocyclic compounds, especially berberine, can act as good inhibitors for both kinds of Zn-Al alloy coatings in HCl solutions. These compounds can adsorb on the coating surface by chemical adsorption with single molecular layer by following Langmuir adsorption isotherm. Nicotinic acid, acridine and berberine, therefore, are effective and environmental friendly corrosion inhibitors for 5%Al-Zn and 55%Al-Zn alloy coated steels in diluted HCl solutions.
Key words:inhibitor; heterocyclic compounds; hydrochloric acid; EIS
用高浓度铬酸溶液[1?2]去除热浸镀层表面的腐蚀产物[3],易造成对人体和自然环境的毒害作用[4];在热浸镀钢板的涂装前处理生产线上,如果不能在去除镀层表面氧化膜和锈点的酸洗液中添加合适的缓蚀剂,将难以控制镀层的溶解速度和酸液的消耗。因此,研究和开发用于热浸镀钢材的环境友好型缓蚀、清洗剂具有较高的应用价值和重要意义。
近年来,钢材的绿色酸洗缓蚀剂研究已取得了长足的进步[5?8],但有关热浸镀钢材的缓蚀研究仍鲜见报道。本文作者近期就热镀锌钢板在稀盐酸中的缓蚀行为进行了研究,并通过量子化学计算等方法筛选出烟酸等3种环境友好的杂环化合物作为热镀锌钢板在稀盐酸中的高效酸洗缓蚀剂,可广泛应用于彩瓦厂、钢结构厂的涂装前处理生产线上,具有可观的经济效益和社会效益,同时也为镀层腐蚀产物的无害化去除提供了一种新方法。
与热镀锌钢材相比,5%铝?锌合金镀层钢材具有更好的防腐、成形和涂装性能,55%铝?锌合金镀层钢材具有优异的防腐和耐热性能[9],因此,这两种锌铝合金镀层在国民经济各领域的应用也越来越广泛。为此,本文作者在前期工作的基础上,通过质量损失、电化学测试和扫描电镜分析等方法,进一步对比研究了烟酸、吖啶和小檗碱等杂环化合物对热浸镀锌铝合金镀层在盐酸中的缓蚀作用。
1 实验
1.1 试样制备
实验所用样品为市售热浸镀5%铝?锌(Galfan,GF)和55%铝?锌(Galvalume,GL)合金镀层钢板,钢材基体为低碳钢。其中5%铝?锌合金镀层钢板样品厚2.0 mm,镀层厚15 μm;55%铝?锌合金镀层钢板样品厚1.0 mm,镀层厚25 μm。质量损失实验所用试样的尺寸为5.2 cm×5.2 cm,经脱脂、清洗、干燥、称量质量后,用环氧树脂密封切边,使钢板两侧暴露的工作面均为5.0 cm×5.0 cm。电化学测试所用试样的尺寸为1.5 cm×1.5 cm,经脱脂、清洗、干燥、环氧封装后,工作电极的暴露面积为1.0 cm×1.0 cm,经超声清洗清洗、干燥后备用。
1.2 试剂
烟酸从惠兴生化试剂有限公司购买,纯度为99%;吖啶从Sigma-Aldrich公司购买,纯度为98%;小檗碱由青岛黄海制药有限公司提供,纯度为99%以上;盐酸为分析纯的浓盐酸(37%)。
1.3 开路电位测试
使用高阻万用表监测热浸镀5%铝?锌和55%铝?锌合金镀层钢板在不同浓度盐酸中的腐蚀电位(OCP)随时间的变化。工作电极为上述两种锌铝合金镀层钢板,参比电极为带鲁金毛细管的饱和甘汞电极。盐酸溶液浓度分别为0.05、0.10、0.20、0.50、1.00、1.50和2.00 mol/L。
1.4 质量损失测试
质量损失测试参照国家标准GB10124?88执行。盐酸溶液的浓度以及浸泡时间根据OCP测试确定;杂环化合物的使用浓度范围为1.0×10?5~1.0×10?2 mol/L。将试样浸泡在空白底液以及含不同浓度杂环化合物的盐酸溶液中,实验完毕后将试样取出,经流水冲洗、无水乙醇脱水、环氧镶嵌去除、丙酮清洗、吹干后称量。根据试样在加入杂环化合物后的质量损失mi和空白底液中的质量损失m0按下式计算缓蚀效率η:

1.5 电化学测试
电化学测试采用EG&G Parstat 2273电化学测试系统在室温下进行,盐酸溶液和杂环化合物的浓度同质量损失测试。实验采用三电极体系,两种锌铝合金镀层钢板为工作电极,铂电极为对电极,饱和甘汞电极为参比电极。当开路电位稳定后进行电化学阻抗测试,扰动电位为10 mV,频率范围为95 kHz~0.050 Hz。线性极化曲线扫描范围(vs. OCP)为?20~20 mV,扫描速度为0.166 mV/s。根据试样在加入杂环化合物后的极化电阻Rp, i和空白底液中的极化电阻Rp, 0按下式计算缓蚀效率η:

1.6 扫描电镜实验
两种锌铝合金镀层试样分别浸入空白底液和含1.0×10?3 mol/L杂环化合物的盐酸中一段时间,取出经无水乙醇清洗、真空干燥,以KYKY?2800B扫描电子显微镜观察表面形貌,加速电压为25 kV。
2 结果与讨论
2.1 两种锌铝合金镀层的OCP测试
为确定质量损失和电化学测试的实验条件,本研究首先监测了两种锌铝合金镀层钢板在不同浓度盐酸中的OCP―t曲线,见图1。图中曲线可分为3个区域:在第一个区域,镀层的开路电位保持在?1.0 V左右,反映了镀层表面锌元素的优先溶解;接着电位产生突跃,镀层中的铝将和锌同时溶解;随后是铁和铝同时溶解的区域,电位在?0.6~?0.7 V内变化。SIMPSON[10]在镀层材料的加速腐蚀实验中也得到过类似的结果。根据OCP测试结果,可确定质量损失实验的最佳条件为:5%铝?锌合金镀层,盐酸浓度为0.20 mol/L,控制时间为1.0 h;55%铝?锌合金镀层,盐酸浓度为0.50 mol/L,控制时间为1.5 h。
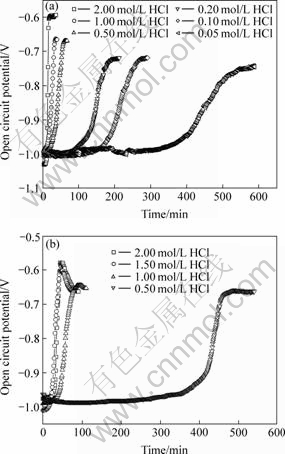
图1 镀层在盐酸中的开路电位随时间的变化
Fig.1 Open circuit potential―time curves for hot dip coatings in hydrochloric acid with different concentration: (a) 5%Al-Zn alloy coating; (b) 55%Al-Zn alloy coating
2.2 质量损失测试
锌铝合金镀层钢板试样在室温下浸入到含不同浓度杂环化合物的盐酸中的缓蚀效率数据列于表1。可
以看出,3种杂环化合物对两种锌铝合金镀层钢材均有良好的缓蚀作用。随着杂环化合物浓度的增加,镀层钢板的质量损失迅速减少,而缓蚀效率则不断增加。当杂环化合物浓度高于1.0×10?3 mol/L时,缓蚀效率增加的幅度减小。当浓度达到1.0×10?2 mol/L 时,缓蚀效率达到最高。对于5%铝?锌合金镀层,烟酸的缓蚀效率最高达88%,而吖啶和小檗碱的最高缓蚀效率均接近94%;对于55%铝?锌合金镀层,缓蚀效果似乎更理想,烟酸的最高缓蚀效率达到93%,而吖啶和小檗碱的最高缓蚀效率可达97%。
表1 质量损失测试得到的缓蚀效率
Table 1 Inhibition efficiency obtained from mass loss test (η/%)

在含有1.0×10?3 mol/L杂环化合物的盐酸中,温度对两种锌铝合金镀层缓蚀效率的影响如图2和图3所示。可以看出,随着温度的升高3种杂环化合物的缓蚀效率降低。这说明这3种化合物通过吸附在镀层材料表面的方式来起到减缓腐蚀的作用。当温度升高时,杂环化合物分子的脱附加剧,吸附在镀层材料表面的杂环化合物分子减少,缓蚀效率降低。通过Arrehenius公式[11]可计算得到表面吸附活化能Ea:

式中 Rcorr为质量损失实验得到的腐蚀速率;A为Arrehenius常量;R为摩尔气体常数;T为绝对温度。3种杂环化合物在5%铝?锌合金镀层表面吸附的活化能分别为:烟酸42.3 kJ/mol; 吖啶51.2 kJ/mol;小檗碱55.0 kJ/mol。而在55%铝?锌合金镀层表面吸附的活化能则为:烟酸48.8 kJ/mol;吖啶54.1 kJ/mol;小檗碱54.8 kJ/mol。由表面吸附活化能的数据可以推断:烟酸、吖啶和小檗碱分子均通过化学吸附方式[12] 吸附在两种锌铝合金镀层钢板表面。

图2 温度对5%铝?锌合金镀层在含1.0×10?3 mol/L缓蚀剂的0.20 mol/L盐酸中的缓蚀效率的影响
Fig.2 Effect of temperature on η of 5%Al-Zn coated steels immersed in 0.20 mol/L hydrochloric acid containing 1.0×10?3 mol/L inhibitors: (a) Nicotinic acid; (b) Acridine; (c) Berberine

图3 温度对55%铝?锌合金镀层在含1.0×10?3 mol/L缓蚀剂的0.50 mol/L盐酸中的缓蚀效率的影响
Fig.3 Effect of temperature on η of 55%Al-Zn coated steels immersed in 0.50 mol/L hydrochloric acid containing 1.0×10?3 mol/L inhibitors: (a) Nicotinic acid; (b) Acridine; (c) Berberine
2.3 交流阻抗和线性极化测试
两种锌铝合金镀层在含不同浓度杂环化合物的盐酸中的电化学阻抗谱如图4和5所示,由两个容抗弧组成。其中高频区的容抗弧是由电荷传递和双电层充电过程引起的,而低频区的容抗弧则是由离子扩散过程引起的。这是因为锌铝合金镀层存在选择性腐蚀,当其浸入盐酸时,镀层中的锌将优先溶解[10]。这种有选择性的溶解使得锌离子在镀层表面与酸液反应的位置富集,随着镀层表面与溶液中锌离子浓度梯度的产生,锌离子会从镀层表面富集的位置扩散到溶液中去,从而产生低频区由扩散阻抗控制的容抗弧。相应的等效电路如图6所示,解析的电化学参数见表2和表3,其中Rs为工作电极和参比电极之间的溶液电阻,Cdl为双电层电容,Rp为极化电阻,Zd为有限扩散阻抗。
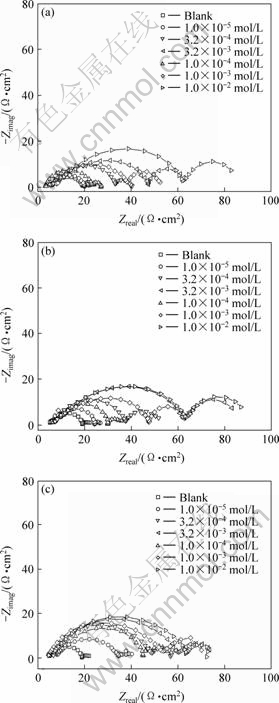
图4 5%铝?锌合金镀层在含不同浓度杂环化合物的0.20 mol/L盐酸中的电化学阻抗谱
Fig.4 Nyquist diagram of 5%Al-Zn alloy coated steels immersed in 0.20 mol/L hydrochloric acid containing inhibitors with different concentrations: (a) Nicotinic acid; (b) Acridine; (c) Berberine

图5 55%铝?锌合金镀层在含不同浓度杂环化合物的0.50 mol/L盐酸中的电化学阻抗谱
Fig.5 Nyquist diagram of 55%Al-Zn alloy coated steels immersed in 0.50 mol/L hydrochloric acid containing inhibitors with different concentrations: (a) Nicotinic acid; (b) Acridine; (c) Berberine
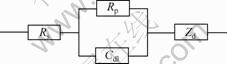
图6 5%铝?锌和55%铝?锌合金镀层钢材在盐酸中腐蚀的等效电路图
Fig.6 Equivalent circuit for 5%Al-Zn and 55%Al-Zn alloy coated steels in HCl solution
表2 5%铝?锌镀层钢材在添加缓蚀剂的0.20 mol/L盐酸及空白底液中腐蚀的电化学参数
Table 2 Electrochemical parameters for 5%Al-Zn alloy coated steels in free and inhibited 0.20 mol/L HCl solution
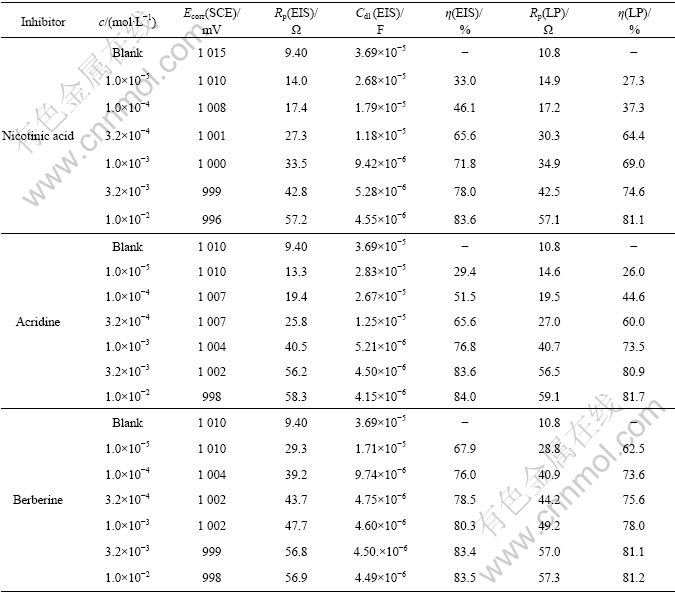
表 3 55%铝?锌镀层钢材在添加缓蚀剂的0.50 mol/L盐酸及空白底液中腐蚀的电化学参数
Table 3 Electrochemical parameters for 55%Al-Zn alloy coated steels in free and inhibited 0.50 mol/L HCl solution

由表2和表3可知,随着缓蚀剂浓度的增加,Ecorr没有出现较大变化,说明这3种缓蚀剂是混合型缓蚀剂;同时,随着缓蚀剂浓度的增加,Rp增大,而Cdl减小。这说明表面有吸附层吸附而且随着缓蚀剂浓度的升高两种锌铝合金镀层在酸液中的腐蚀受到抑制。为对比交流阻抗测试得到的数据,还进行了线性极化测量。由线性极化与交流阻抗测试得到的电化学参数以及由此计算的缓蚀效率数据并列于表2和3中,可见,由两种方法得到的极化电阻具有良好的一致性;对比表1还可发现,由电化学测试和质量损失测试得到的缓蚀效率数据吻合得很好。3种杂环化合物在盐酸中对两种锌铝合金镀层均具有较高的缓蚀效率,且缓蚀效率随着杂环化合物浓度的增加而提高,缓蚀作用良好。
用来表征金属表面被吸附的有机分子占据分数的参数――表面相对覆盖度θ可由下式计算得到:

作者尝试将表面覆盖度θ对各种吸附等温式[13?14],包括Frumkin, Langmuir, El-Awady和 Freundluich等进行拟合。结果发现这3种缓蚀剂在镀层材料表面吸附遵从Langmuir吸附等温式,如图7和图8所示。由此可以推断:烟酸、吖啶和小檗碱在5%铝?锌和55%铝?锌合金镀层表面主要呈单分子层吸附,且吸附分子之间的相互作用力可以被忽略不计。
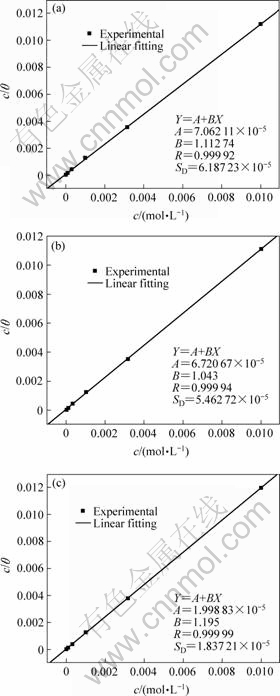
图7 杂环化合物在5%铝?锌合金镀层表面对Langmuir吸附等温式的拟合
Fig.7 Langmuir adsorption isotherm fitting for heterocyclic compounds on surface of 5%Al-Zn alloy coated steels: (a) Nicotinic acid; (b) Acridine; (c) Berberine

图8 杂环化合物在55%铝?锌合金镀层表面对Langmuir吸附等温式的拟合
Fig.8 Langmuir adsorption isotherm fitting for heterocyclic compounds on surface of 55%Al-Zn alloy coated steels: (a) Nicotinic acid; (b) Acridine; (c) Berberine
同时,表征吸附分子与金属表面相互作用的标准吉布斯自由能可由下式计算得到:

3种杂环化合物在0.20 mol/L盐酸中与5%铝?锌合金镀层相互作用的标准吉布斯自由能分别为:烟酸?33.63 kJ/mol;吖啶?33.75 kJ/mol;小檗碱?36.76 kJ/mol。在0.50 mo/L盐酸中与55%铝?锌合金镀层相互作用的标准吉布斯自由能分别为:烟酸?32.40 kJ/mol;吖啶?34.14 kJ/mol;小檗碱?35.05 kJ/mol。吉布斯自由能的数值表明,3种有机缓蚀剂分子在两种锌铝合金镀层表面的吸附为很强的化学吸附[12, 15]。
2.4 表面形貌的扫描电镜分析
两种锌铝合金镀层试样在浸入添加缓蚀剂的盐酸及空白底液后的表面腐蚀形貌如图9和10所示。可以看出,在空白底液中清洗时,两种锌铝合金镀层均发生了较为严重的腐蚀;而将1.0×10?3 mol/L的烟酸、吖啶或小檗碱添加到相同浓度的盐酸后,镀层表面的腐蚀得到有效的抑制,镀层表面完整,且无明显的锈点残留。结合质量损失和电化学数据可以得出这样的锌铝合金镀层表面形成一层保护膜,以保护镀层表面结论:烟酸、吖啶和小檗碱通过化学吸附方式在两种免受酸液的侵蚀,具有良好的缓蚀、清洗作用,其中以小檗碱的缓蚀、清洗效果最好。

图9 5%铝?锌合金镀层钢板浸入含1.0×10?3 mol/L缓蚀剂的0.20 mol/L盐酸及空白底液1 h后的表面形貌
Fig.9 Surface morphologies of 5%Al-Zn alloy coated steels immersed in 0.20 mol/L hydrochloric acid with and without 1.0×10?3 mol/L inhibitor for 1 h: (a) Blank; (b) Nicotinic acid; (c) Acridine; (d) Berberine

图10 55%铝?锌合金镀层钢板浸入添加1.0×10?3 mol/L缓蚀剂的0.50 mol/L盐酸及空白底液1.5 h后的表面形貌
Fig.10 Surface morphologies of 55%Al-Zn alloy coated steels immersed in 0.50 mol/L hydrochloric acid with and without 1.0×10?3 mol/L inhibitor for 1.5 h: (a) Blank; (b) Nicotinic acid; (c) Acridine; (d) Berberine
3 结 论
在盐酸介质中,烟酸、吖啶和小檗碱对5%铝?锌和55%铝?锌合金镀层钢材均是有效的缓蚀、清洗剂,其中小檗碱的效果最好。这3种化合物通过单分子层、化学吸附方式吸附在镀层表面形成一层保护膜,从而起到保护镀层表面的作用。
REFERENCES
[1] KING G A, O’BRIEN D J. The influence of marine environments on metals and fabricated coated metal products, freely exposed and partially sheltered[C]//Atmospheric Corrosion, ASTM STP 1239. Philadelphia: American Society for Testing and Materials, 1995: 167?192.
[2] ZOCCOLA J C, TOWNSEND H E, BORZILLO A R, HORTON J B. Atmospheric corrosion behavior of aluminum-zinc alloy-coated steel[C]//Atmospheric Factors Affecting the Corrosion of Engineering Metals, ASTM STP 646. Philadelphia: American Society for Testing and Materials, 1978: 165?184.
[3] 李 焰, 邢少华, 李 鑫, 魏绪钧. 热浸镀层在青岛站的海水腐蚀行为对比(Ⅰ)―全浸区[J]. 中国有色金属学报, 2006, 16(12): 2083?2091.
LI Yan, XING Shao-hua, LI Xin, WEI Xu-jun, Seawater corrosion behavior of hot-dip coatings at Qingdao test station (Ⅰ)―Immersion zone[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(12): 2083?2091.
[4] LI Yan, WANG Hong-ren, HOU B-rong, FENG Fa-lun, WEI Xu-jun. Chromate passivation of hot dipped Zn25Al alloy coatings[J]. British Corrosion Journal, 2001, 36(1): 56?58.
[5] SRIVASTAVA K, SRIVASTAVA P. The effect of some natural inhibitors on the corrosion of mild steel in acidic environments[J]. British Corrosion Journal, 1981, 16(4): 221?223.
[6] SALCH R M. Corrosion inhibition by naturally occurring substances: The effect aqueous extracts of some leaves & fruitpeels on the corrosion of steel, Al, Zn and Cu in acid[J]. British Corrosion Journal, 1982, 17(3): 131?135.
[7] BETHENCOURT M, BOTANA F J, CALVINO J J, MARCOS M, RODR?GUEZ-CHAC?N M A. Lanthanide compounds as environmentally-friendly corrosion inhibitors of aluminium alloys: A review[J]. Corrosion Science, 1998,40(11): 1803?1819.
[8] EL-ETRE A Y, ABDALLAH M. Natural honey as corrosion inhibitor for metals and alloys (Ⅱ): C-steel in high saline water[J]. Corrosion Science,2000,42(4): 731?738.
[9] MARDER A R. The metallurgy of zinc-coated steel[J]. Progress in Materials Science, 2000, 45(3): 191?271.
[10] SIMPSON T C. Accelerated corrosion test for aluminum-zinc alloy coating[J]. Corrosion, 1993, 49(7): 550?560.
[11] BOUKLAH M, BENCHAT N, HAMMOUTI B, AOUNITI A, KERTIT S. Thermodynamic characterisation of steel corrosion and inhibitor adsorption of pyridazine compounds in 0.5 M H2SO4[J]. Materials Letters, 2006, 60(15): 1901?1905.
[12] LEBRINI M, LAGREN?E M, VEZIN H, GENGEMBRE L, BENTISS F. Electrochemical and quantum chemical studies of new thiadiazole derivatives adsorption on mild steel in normal hydrochloric acid medium[J]. Corrosion Science, 2005, 47(2): 485?505.
[13] BOUKLAH M, OUASSINI A, HAMMOUTI B, EL IDRISSI A. Corrosion inhibition of steel in sulphuric acid by pyrrolidine derivatives[J]. Applied Surface Science, 2006, 252(6): 2178?2185.
[14] SAYED S, HAMDI H H, MOHAMMED A A. The corrosion inhibition study of sodium dodecyl benzene sulphonate to aluminium and its alloys in 1.0 M HCl solution[J]. Materials Chemistry and Physics, 2003, 78(2): 337?348.
[15] OGUZIE E E, OKOLUE B N, EBENSO E E, ONUOHA G N, ONUCHUKWU A I. Evaluation of the inhibitory effect of methylene blue dye on the corrosion of aluminium in hydrochloric acid[J]. Materials Chemistry and Physics, 2004, 87(2): 394?401.
基金项目:国家自然科学基金资助项目(40306013,40576038)
收稿日期:2007-05-08;修订日期:2007-09-20
通讯作者:李 焰;电话:0532-82898832;E-mail: yanlee@ms.qdio.ac.cn
(编辑 陈爱华)