文章编号:1004-0609(2007)02-0331-05
生物因素对次生硫化铜矿堆浸过程动力学的影响
李宏煦1, 苍大强1, 陈景河2, 邱冠周2
(1. 北京科技大学 冶金与生态工程学院,教育部生态与循环冶金重点实验室,北京100083;
2. 中南大学 资源加工与生物工程学院,长沙 410083)
摘 要:假定生物浸出过程细菌的作用是间接作用,以实验室柱浸模拟次生硫化铜矿生物堆浸,基于细菌生长Monod方程及收缩核模型建立细菌生长动力学因子影响硫化矿浸出速率的动力学模型,研究铜浸出速率、溶液总铁、溶液中细菌浓度与时间的关系、细菌产出率和细菌饱和系数对浸出速率影响的动力学规律。动力学研究表明,在浸出早期,氧化浸出速率、溶液中总铁浓度以及溶液中的细菌数量增长较快,而在浸出后期则增长较慢。计算与实际结果表明,细菌最大生长比速率、细菌产出率、细菌饱和常数及溶液中Fe离子的浓度均对硫化矿的氧化浸出速率有明显影响,尤其在浸出早期影响较大。应用动力学模型仿真结果与实际基本符合,可分析生物因素对浸出的影响趋势。
关键词:生物冶金;细菌浸出;生物堆浸;次生硫化铜矿;动力学
中图分类号:TF 111 31; Q 939 99; TF 803 21 文献标识码:A
Effect of biological factors on heap bioleaching kinetics of secondary copper sulfide
LI Hong-xu1, CANG Da-qiang1, CHEN Jing-he2, QIU Guan-zhou2
(1. School of Metallurgical and Ecological Engineering, University of Science and Technology,
The Key Ecology and Recycling Metallurgy Laboratory of Education Ministry, Beijing 100083, China;
2. School of Resource Processing and Biology, Central South University, Changsha 410083, China)
Abstract: Based on the indirect function of bacteria in the leaching process, Monod equation and Shrink core kinetics equation, the bacteria growth and sulfide bioleaching kinetics model about secondary copper sulfide column bioleaching simulating heap bioleaching were proposed, and the variation rules of copper leaching rate and bacteria and total iron concentration in the solution by the time were determined, and the kinetics of leaching speed affected by bacteria maximal growth specified rates and bacteria yield rate and bacteria saturated coefficient respectively were studied. The results show that in the prophase time of leaching process, the leaching rate, total iron concentration and bacteria cells increase rather quicker than those in the anaphase time of leaching, and the biological factors affect the leaching process when in the prophase time. The results of calculated and experimented of mining heap bioleaching show a good consistence, and it proves that the primary kinetics model can give an availability description about heap bioleaching process.
Key words: biohydrometallurgy; bioleaching; heap leaching; secondary copper sulfide; kinetics model
目前次生硫化铜矿的大规模生物堆浸在智利等国已广泛应用,但在国内尚不多见。尽管次生硫化铜矿生物堆浸已经工业化,从国内外应用情况来看,仍然存在后期浸出速率过慢、浸出率往往低于预期值等问题,原因在于对生物堆浸过程的存在许多问题尚不清楚[1-3]。目前国内外生物冶金研究主要集中在浸矿微生物的选育与培养、生物与矿物相互作用机理等方面,而浸出过程动力学方面研究较少,尤其是对于实际堆浸过程的研究[4-6]。
生物堆浸过程影响因素多,情况复杂,研究难度大。本文作者以实验室辉铜矿柱浸模拟实际堆浸,应用柱浸数据,基于细菌生长动力学与浸出反应动力学原理,找出一些经典细菌生长动力学参数与铜矿物氧化浸出速率的关系,以期说明细菌生长状况对浸出影响的定量关系。本研究仅涉及细菌生长、Fe2+、Fe3+浓度变化与硫化矿氧化等基本的动力学过程,忽略气体、液体等流体的扩散、温度场的分布等复杂动力学问题。
1 动力学模型的建立与参数的选择
目前研究表明,细菌在硫化矿浸出过程的主要作用是细菌的间接作用,即细菌在浸出中的作用是细菌在溶液中和在矿物表面吸附的状态下,将溶液或矿物表面的Fe2+氧化为Fe3+,而Fe3+为强氧化剂,可氧化浸出硫化矿,硫化矿氧化分解时释放出Fe2+,细菌又将释放出的Fe2+氧化为Fe3+,如此循环,即细菌作用过程是一个不断氧化释放Fe3+的过程。同时,细菌在氧化Fe2+时,完成细菌的生长代谢和大量繁殖,并使堆中细菌数量变化和换代更新。所以整个浸出与溶液中的Fe3+、Fe2+浓度相关[8-10],此时次生硫化矿堆浸过程的反应主要包括次生硫化矿物的分解,黄铁矿的氧化,细菌对Fe2+和元素硫的氧化。次生硫化铜矿和铜蓝的氧化反应分别为[11-12]

细菌生长对Fe2+氧化反应(溶液和矿物表面)

反应式(1)、 (2)为硫化铜矿氧化浸出反应,而代表黄铁矿氧化矿的反应式(3)和关于Fe2+氧化的反应式(4)可以被认为是与细菌生长相关的反应。 如前所述,当认为氧、氮、二氧化碳、其它无机盐充足恒定,而Fe2+浓度为细菌生长限制性因素时,溶液和吸附细菌的Monod生长动力学方程可写为[13-14]
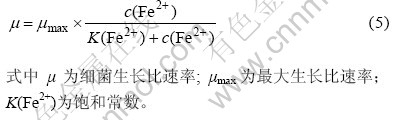
而矿物表面细菌数量的变化可表示为

溶液中细菌数量的变化为

在式(6)、(7)中,Xa为细菌吸附在矿物颗粒表面浓度;Xs为溶液中细菌浓度; Xsat为可到达矿物表面的饱和细菌浓度; Kads和Kdes分别为细菌吸附与脱附动力学系数,细菌氧化Fe2+速率可表示为
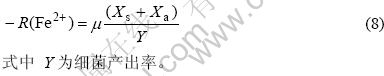
细菌产出率和细菌生长最大比速率、细菌饱和常数均为标志细菌生长状况的动力学参数,它们的变化说明细菌生长状况,它们大小反应了细菌活性、数量、生长趋势和对Fe2+及硫化矿的氧化,而其和矿物氧化的动力学方程可直接通过溶液中Fe3+、Fe2+浓度联系起来。
假定柱内温度场分布均匀、矿物被浸出液完全浸润、柱内气体充足,基于未反应收缩核模型,未反应矿物颗粒半径减小速率可表示为

式(9)右边分母项中的第一项为与矿物本身氧化溶解动力学相关的阻力项;第二项则是Fe3+在脉石矿物内及矿石颗粒内空隙间的扩散阻力,有效扩散系数Deff可认为随对流增加而减小;最后一项代表Fe3+在矿物表面静态液相薄层中的扩散。这些相关阻力随着浸出过程的进行而变化。
为了能较充分描述多种矿物的浸出过程,根据浸出过程矿物组分的变化,需要对式(9)表示的反应速率方程进行修正。在堆浸过程中,反应速率较快的组分较反应慢的组分消耗得更快,因而随着浸出的进行,内反应动力学因子β随之减小。不同矿物组分对β的影响可通过其不同的动力学系数βi和瞬时比例因子gi表示


组分i对矿物总反应的贡献为

式中 gi0为组分i对矿物铜品位的初始贡献; n为矿物总铜瞬时浸出量; Ki为组分反应常数。对于给定组分i矿物的浸出率特征与未反应核半径有如下关系:

其中黄铁矿氧化速率与辉铜矿及铜蓝氧化速率的关系可依据下式[15]:

氧化溶解离子物质平衡可用如下液相浓度微分方程表示:

式(14)用于计算溶液中Fe3+、Fe2+和Cu2+浓度。
根据堆浸过程的实际情况和查经典动力学相关数据[7, 11-15],该过程部分动力学参数列于表1。对于上述细菌生长、矿物分解和溶液离子变化的动力学方程应用四阶龙格库塔法求解,应用CFD软件包进行计算。
实验室柱高2 m,直径0.3 m,柱内液体完全浸润矿物,柱浸过程通气以保证氧气和二氧化碳,其它条件列于表1。
表1 动力学研究所用数据及参数值
Table 1 Bio heap leaching practical data and other common kinetics parameter values

2 计算结果与动力学规律
2.1 铜浸出速率与时间的关系
图1所示为实际及用动力学数学仿真计算的矿物总铜浸出速率随时间变化的趋势。从图中可知,计算结果与实际符合较好,说明了动力学仿真结果的可靠性。由图可见,在浸出前期,尤其在40~50 d时间内,有大量辉铜矿氧化溶解,而在之后的时间内氧化溶解的速度减慢。应用动力学数学计算结果和实际基本符合。说明在不考虑其他因素的条件下,建立的矿物氧化溶解的速率方程可以反应浸出过程铜氧化浸出速率与时间的关系。
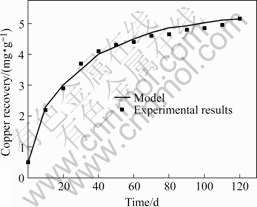
图1 铜浸出速率随时间的变化
Fig.1 Variation of copper recovery with bio heapleaching time
2.2 溶液总铁与时间的关系
图2所示为实际与计算的总铁浓度随时间的变化趋势。同样,在浸出早期,由于大量硫化矿特别是黄铁矿的氧化,溶液中的总铁浓度较快上升,而到后期,随着黄铁矿的氧化和消耗,溶液中总铁浓度上升速率下降。考虑到部分时间内存在铁的沉淀现象,实际测量结果和应用动力学数学计算结果基本相符合,说明动力学模型可以用来描述浸出过程铁浸出速率的变化。
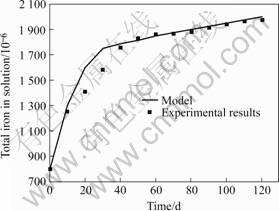
图2 溶液中的总铁浓度随时间的变化
Fig.2 Variation of total iron ion concentration of leached solution with bio heapleaching time
2.3 溶液中细菌浓度与时间的关系
图3所示为实际及计算的细菌浓度随时间的变化趋势。由图可知,在浸出早期,由于黄铁矿的大量氧化,溶液中铁的浓度较高,且Fe2+数量较多,细菌生长较快,此时存在于溶液中的细菌数量较多。随着浸矿的进行,溶液中总铁下降,同时Fe2+数量减少,大量细菌吸附于矿物表面,造成溶液中细菌数量的急剧下降。应用细菌生长动力学模型计算结果与实际测定结果吻合较好,说明基于Fe2+氧化的细菌生长动力学模型能较好描述堆浸过程细菌生长趋势。

图3 溶液中细菌浓度随时间的变化
Fig.3 Variation of bacteria cells concentration of leached solution with bio heapleaching time
2.4 细菌生长比速率对浸出速率的影响
图4所示为计算所得细菌最大生长比速率与铜浸出率的关系。由图可知,在浸出早期,细菌生长的动力学参数对于铜矿物氧化浸出具有重要的影响,此时,溶液中Fe2+的氧化速率是浸出反应速率的限制性环节。细菌经过短暂的适应期后,开始大量繁殖,于是有大量Fe2+被氧化为Fe3+,Fe3+浓度的上升使硫化矿物浸出速率增加,再过一段时间后,细菌生长速率减慢,此时,铜的浸出速率亦减缓。同时,比较细菌不同最大生长比速率可以看出,当细菌最大生长比速率下降时,此时Fe2+的氧化速率下降,溶液中的Fe3+浓度减小,从而导致铜的浸出速率下降。

图4 不同细菌最大生长比速率下铜浸出速率与时间的关系
Fig.4 Relations of copper recovery and bio heapleaching time under different bacteria ultimate specific growth rates
2.5 细菌产出率对浸出速率的影响
图5所示为不同细菌产出率下铜浸出速率与时间的关系。图5中曲线说明了早期细菌产出速率对铜硫化物浸出的影响较大,即早期细菌的数量与铜硫化矿物浸出速率关系密切。与图4相比较,细菌产出率的变化对铜硫化矿物的浸出速率的影响较大,对其最大生长比速率的影响较小。由于细菌产出率是细菌最大生长比速率的函数,其大小受其它因素的限制,所以其计算的结果差异较小。

图5 不同细菌产出率下铜浸出速率与时间的关系
Fig.5 Relations of copper recovery and bio heapleaching time under different bacteria yields
2.6 细菌饱和系数对氧化浸出的影响
图6所示为不同细菌饱和系数下铜浸出速率随时间的变化规律。由图可见,在浸出早期,细菌饱和系数的变化对铜硫化矿物浸出速率影响较大,即随着饱和系数的降低,浸出速率加快。这说明当细菌饱和系数小时,体系中能容纳的细菌数目越多,就会有越多的Fe2+会被氧化为Fe3+,则铜硫化矿的浸出速率越大。随着浸出时间的延长,溶液中的细菌逐渐达到饱和,于是饱和系数的变化对细菌生长及矿物的氧化浸出的影响减小。这与实际的浸出过程发展趋势是相符合的。
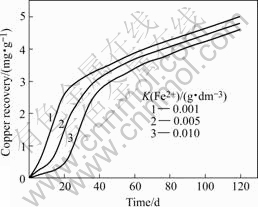
图6 不同细菌饱和系数下铜浸出速率与时间的关系
Fig.6 Relations of copper recovery and bio heapleaching time under different bacteria saturation coefficients
REFERENCES
[1] Mooiman M B, Sole K C, Kinneberg D J. Challenging the traditional hydrometallurgy curriculum an industry perspective[J]. Hydrometallurgy, 2005, 79: 80-88.
[2] Habashi F. A short history of hydrometallurgy[J]. Hydrometallurgy, 2005, 79: 15-22.
[3] Brierley J A, Brierley C L. Present and future commercial applications of biohydrometallurgy[J]. Hydrometallurgy, 2001, 59: 233-239.
[4] Ehrlich H L. Past, present and future of biohydrometallurgy[J]. Hydrometallurgy, 2001, 59: 127-134.
[5] YANG Song-rong, XIE Ji-yuan, QIU Guan-zhou, HU Yue-hua. Research and application of bioleaching and biooxidation technologies in China[J]. Minerals Engineering, 2002, 15: 361-363.
[6] Akcil A. Potential bioleaching developments towards commercial reality[J]. Minerals Engineering, 2004, 17(3): 477-480.
[7] 李宏煦, 陈景河, 王淀佐. 福建紫金矿业股份有限公司硫化铜矿生物堆浸过程[J]. 有色金属, 2004, 56(4): 66-69.
LI Hong-xu, CHEN Jing-he, WANG Dian-zuo. Copper sulf ide dump bioleaching in Fujian Zijin Mining Industry Corporation[J]. Nonferrous Metals, 2004, 56(4): 66-69.
[8] Sand W, Gehrke T, Jozsa P G, Schippers A. Biochemistry of bacterial leaching―direct vs Indirect bioleaching[J]. Hydrometallurgy, 2001, 59: 159-175.
[9] 李宏煦, 王淀佐, 陈景河. 细菌浸矿的间接作用分析[J]. 有色金属, 2003, 55(4): 98-100.
LI Hong-xu, WANG Dian-zuo, CHEN Jing-he. Discussion on indirect mechanism of bioleaching[J]. Nonferrous Metals, 2003, 55(4): 98-100.
[10] 李宏煦, 王淀佐, 陈景河. 细菌浸矿作用分析[J]. 有色金属, 2003, 55(3): 68-71.
LI Hong-xu, WANG Dian-zuo, CHEN Jing-he. Description of microbe effects on sulf ide mineral bioleaching[J]. Nonferrous Metals, 2003, 55(3): 68-71.
[11] 李宏煦, 王淀佐. 生物冶金中的微生物及其作用[J]. 有色金属, 2003, 55(2): 60-63.
LI Hong-xu, WANG Dian-zuo. Review of investigation on microorganism behaviors in ore bio-leaching[J]. Nonferrous Metals, 2003, 55(2): 60-63.
[12] LI Hong-xu, WANG Dian-zuo, QIU Guan-zhou, et al. Growth kinetics of Thiobacillus ferrooxidans in bioelectrochemical cell[J]. J Cent Technol, 2004, 11(1): 36-40.
[13] Gatti M N, Milocco R H, Giaveno A. Modeling the bacterial oxidation of ferrous iron with Acidithiobacillus ferrooxidans using kriging interpolation[J]. Hydrometallurgy, 2003, 71(1/2): 89-96.
[14] James A. Brierley response of microbial systems to thermal stress in biooxidation-heap pretreatment of refractory gold ores[J]. Hydrometallurgy, 2003, 71(1/2): 13-19.
[15] Sidborn M, Casas J, Martínez J. Two-dimensional dynamic model of a copper sulphide ore bed[J]. Hydrometallurgy, 2003, 71(1/2): 67-74.
基金项目:国家重点基础研究发展规划资助项目(2004CB619205); 国家自然科学基金资助项目(50204001)
收稿日期:2006-07-06;修订日期:2006-10-28
通讯作者:李宏煦,副教授; 电话: 010-62332786;E-mail: lihongxu2001@126.com;lihongxu20001@sian.com
(编辑 陈爱华)