
DOI�� 10.11817/j.issn.1672-7207.2021.01.014
Ce����Fe-Mn�����������ѹ������������о�
���ţ���ǿ����褣��ҹ�ة��¬ƽ���ܼ���
(�Ͼ�ʦ����ѧ ��Դ���е����ѧԺ������ʡ��Դϵͳ����ת������ż�������ʵ���ң����� �Ͼ���210023)
ժҪ�����ù��������Ʊ�Ce����Fe-Mn����������(Fe6Mn1-xCex)���ڹ̶���ʵ��ϵͳ����Fe6Mn1-xCex�������Ĺ�������������ʵ�飬����Ce�������������¶ȡ�SO2����Ũ�Ⱥ��������������ض��ѹ���Ӱ�죬����N2����/�Ѹ�����ǿ��(VSM)��X����������(XRD)���ֶζ������������ﻯ���Ա������������ѹ����������ԡ��о����������Fe6Mn0.8Ce0.2��150 ��ʱ������ӵ����ǿ���ѹ�������Ce�IJ�����Ż��������Ŀ�϶�ṹ����������Ce���ӻή���ѹ��������Mn�ĺ���������Fe6Mn1-xCex�ѹ����ܽ��ͣ�Ce�IJ��������Fe6Mn0.8Ce0.2�Ŀ�SO2���ܣ���SO2��O2ͬʱ����ʱ��Fe6Mn0.8Ce0.2�Ŀ�SO2�����õ�������ǿ��Fe6Mn0.8Ce0.2�������õĴ������������ܣ��������ﻯ���Ա仯��С��5������ѭ���ѹ�����ýϸ��ѹ�Ч�ʣ��ѹ�����ΪHgO��
�ؼ��ʣ��������������̶������̵������ѹ�������
��ͼ����ţ�X511 ���ױ�־�룺A ���ſ�ѧ(��Դ����)��ʶ��(OSID)
���±�ţ�1672-7207��2021��01-0144-09
Study on mercury removal and regeneration characteristics of Ce modified Fe-Mn magnetic sorbent
TAO��Xin, ZHOU��Qiang, SHANG��Yu, DI��Guancheng, LU��Ping, ZHOU��Jiaqi
(Engineering Laboratory for Energy System Process Conversion & Emission Control Technology of Jiangsu Province, School of Energy and Mechanical Engineering, Nanjing Normal University, Nanjing 210023, China)
Abstract: The co-precipitation method was used to prepare Ce-modified Fe-Mn magnetic sorbents (Fe6Mn1-xCex). The mercury adsorption and thermal regeneration experiments of Fe6Mn1-xCex adsorbent were carried out in a fixed bed experimental system. The influences of Ce addition amount, gas temperature, SO2 mass concentration and regeneration frequency on mercury removal were investigated. The physicochemical characteristics of the sorbent were characterized by N2 adsorption/desorption, vibrating magnetometer(VSM), and X-ray diffractometer(XRD), in order to analyse the mercury removal and regeneration characteristics. The results show that the Fe6Mn0.8Ce0.2 sorbent has the strongest mercury removal capability at 150 ��. The Ce incorporation can optimize the pore structure of sorbent, but excessive Ce addition reduces the content of Mn which acts as mercury removal active component, leading to the reduction of mercury removal performance of Fe6Mn1-xCex. Ce incorporation improves the resistance of Fe6Mn0.8Ce0.2 to SO2, and when SO2 and O2 co-exist, the SO2 resistance of the Fe6Mn0.8Ce0.2 is significantly enhanced. The Fe6Mn0.8Ce0.2 sorbent has good magnetic and regeneration performance. The change of physicochemical characteristics of the Fe6Mn0.8Ce0.2 after thermal regeneration is small. The Fe6Mn0.8Ce0.2 receives high mercury removal efficiency during 5 cycles with a product of HgO.
Key words: magnetic sorbents; fixed-bed; flue gas; mercury removal; regeneration
�ؽ�������һ��Σ�����彡������Ⱦ�����ľ綾���ʣ�������;��ԡ���Ǩ�ƺ����︻�����ص㡣ȼú����Ϊ��������������Ϊ���ŷ�Դ[1-2]����ǰ���ҹ����������Ͼ��Ĺ���Ⱦ��ս��2015��1��1�գ��ҹ�ʵʩ�����µġ���糧������Ⱦ���ŷű������涨���ŷ���ֵΪ30 ��g/m3��2020���ҹ�ȼú���ŷŻ�һ���ϸ�������3 ��g/m3[3]��2017��8��16�գ�ּ������ȫ���ŷŵġ����ڹ���ˮٶ��Լ����ʽ��Ч�����־�Ź����ų�Ϊ���з���Լ��Ч���Ĺ�������ȼú�����еĹ���Ϊ������(Hgp)�����۹�(Hg2+)�͵��ʹ�(Hg0)[4]������Hgp���Ա��������(ESP)��������(FF)��ȥ��Hg2+�ܹ�ͨ��ʪ������װ��(WFGD)�ѳ�����Hg0����лӷ��Լ������ԣ������Hgp��Hg2+�����Ա��ѳ�����ˣ������ŷŵĹؼ����ڿ���Hg0���ŷš�Ŀǰ������̿���似������Ϊ���������е��ѹ�����[5]�����ü���Ŀǰ�Դ���һ��������[6]���������Ļ��պ����������ѡ��ɱ��ߡ������ʵ͡�����Ҫ���ǣ��ѹ����������ͣ���ڷɻ��У�������ɹ��Ķ����ͷš�Ϊ�˽��ACI�������������⣬ʵ�����������ظ����ã�����̼���������Էɻҵ�Ӱ�죬�������Ϳ������ѹ��������ѳ�Ϊ��ǰ�о��ȵ㡣��-��(Fe-Mn)���ѹ���������ɴŷ��롢���������ͳɱ������ԣ��ܵ��˹㷺��ע��YANG��[7]���ù��������Ʊ���Mn/��-Fe2O3��������ָ��������������õĴ��ԣ�����150 ��ʱ10 h�ڵ�ƽ���ѹ��ʿɴ�52%��ZENG��[8]���ù��������Ʊ���FeMnOx�����ѹ���������FeMnOx���������нϸ��ѹ�Ч�ʣ�YANG��[9]�Ʊ�����MnOx/-Fe2O3չ�ֳ�����Ĺ��ѳ����ܺͳ�ǿ�Ĺ��������������Ҹ�����������ʵ���������á�Ȼ����Fe-Mn������������SO2�ж���ZENG��[8]������������ͨ��400��10-6 SO2������£�FeMnOx���������ѳ�Ч�ʴ�87.6%��Ϊ59.7%����Ҫ��Ϊ������SO2����Hg0����������������ռ���ѹ�����λ��Mn4+����ˣ���ѧ�߳�����Fe-Mn�������в�������ֹ��ɽ���[10-11]���������Fe-Mn���������ѹ����ܺͿ�SO2���ܡ�XU��[12]�Ʊ���Fe-Sn-Mn�ѹ������������ֲ���Sn�������������ıȱ������ͬʱFe-Sn-Mn�������õ�SO2�����ԡ����ɽ�����(Ce)�ѱ�֤ʵ����һ����SO2�ж�����[13-16]����Ҫ��Ϊ����S֮��ӵ�и����������SO2������CeO2���ữ���Ӷ��������ڵĻ��Գɷ�MnO2��Ȼ��������Ce��Fe-Mn�������������и��Ե�����о��dz����ޣ�ֵ�������о�����ˣ���������������ù��ɽ���Ce��Fe-Mn�������������и��ԣ����ù��������Ʊ������ѹ�������Fe6Mn1-xCex����ģ�����������½���Fe6Mn1-xCex�������Ĺ�������������ʵ�飬����Ce�������������¶ȡ�SO2����Ũ�Ⱥ����������ȶ��ѹ���Ӱ�죬����N2����/�Ѹ�����ǿ��(VSM)��X����������(XRD)���ֶζ������������ﻯ���Ա������������ѹ����������ԡ����ĵ��о������Ϊȼú�������ѳ����������������ü����ķ�չ�ṩ�ο���
1 ʵ��
1.1�����������Ʊ�
���ù�ͬ�������Ʊ�Fe6Mn1-xCex�����������ľ����������£��ֱ�ȡ0.03 mol FeCl3��6H2O��0.03 mol FeSO4��7H2O�Ͷ���MnSO4��H2O��Ce(NO3)3��6H2O���壬�ܽ���200 mLȥ����ˮ�У�ʹ�����Һ�����ʵ�����n(Fe2+):n(Fe3+):n(Mn2++Ce3+)=3:3:1�������NH3��H2O��Һ��Ϊ������������2 h�������������ں�������105 �����12 h��������¯����400 ������4 h�������顢ɸ�ֺ��Ƶô���������Fe6Mn1-xCex������xΪCe��������(���ʵ���)��xԽС����Ce������ԽС��������Fe6Mn1-xCex������������ΪFe6Mn1-xCex-R��
1.2��ʵ��װ��
��ͼ1��ʾ��װ��ϵͳ����ɴ���Fe6Mn1-xCex������������������ʵ�顣ʹ��VM3000���߲��(Mercury Instrument ��˾���¹�)�ⶨ�����еĹ�Ũ�ȡ����ƹ̶�����ڹ�������ʼ����Ũ�Ⱥ㶨��(33��0.5) ��g/m3������������Ϊ2 L/min���ع�N2Ϊ300 mL/min���̶�������Ϊ��е�ɻ���(200 mg��������ĩ��2 gʯӢɰ)������ʱ��Ϊ2.5 h���ѹ������������ȡ������ͼ1��ʾ�Ĺ̶����Ͻ�������������������������Ϊ2 L/min�����������Ϊ79% N2��21% O2��ɣ�����ʱ��Ϊ3 h���¶�Ϊ500 �棻Hg���������Ѹ�(Hg-TPD)����ʽ��ʽ¯�Ͻ��У�����ΪN2��������Ϊ2 L/min����������Ϊ5 ��/min��
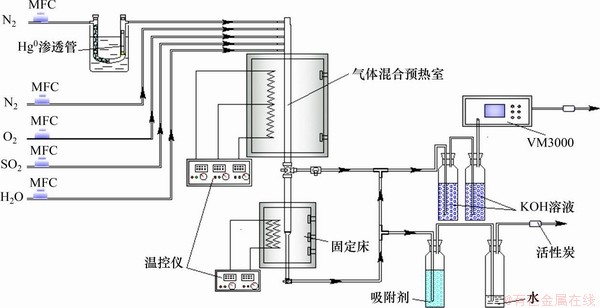
ͼ1���̶���������/��������װ��ϵͳ
Fig. 1��Schematic diagram of fixed bed mercury adsorption/regeneration device
�������������۲����ѹ�Ч�ʦǺ͵�λ�����������ۻ���������q��ʾ��
 (1)
(1)
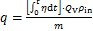 (2)
(2)
ʽ�У���inΪ���Ԫ�ع�����Ũ�ȣ���g/m3����outΪ����Ԫ�ع�����Ũ�ȣ���g/m3��qΪ��λ�����������ۻ�������������g/g��tΪʱ�䣬min��QVΪ������������L/min��mΪ������������g��
1.3����������
����N2����/�Ѹ��������������бȱ��������϶�ṹ����(ASAP-2020M��Micromeritics)���������Ĵ�������(MPMS-VSM��MPMS-XL)��ǿ�Ʋ��������������ľ���ṹ��(D8 Advance, Bruker)�����ⶨ��
2 ���������
2.1���̶������ѳ�ʵ����
2.1.1��Ce��������Ӱ�졡
ͼ2��ʾΪ���¶�Ϊ150 ��ʱCe���������������ѹ�Ч�ʵ�Ӱ�졣��ͼ2��֪��Fe6Mn0.8Ce0.2���ѹ�Ч�����Fe6Mn0.5Ce0.5���ѹ�Ч������͡��ɼ�������������Ce(x=0.2)�������Fe6Mn1-xCex���������ѹ��������������ӹ�����Ce�ᵼ��Fe6Mn1-xCex���ѹ��������͡�ͼ3��ʾΪCe�������Ե�λ������������������(qt)��Ӱ�졣��ͼ3���Կ�����Fe6Mn0.8Ce0.2��Fe6Mn1���������Ÿ��õ��ѹ�Ч������Ce���������ӻᵼ����������λ��������������С���о�����[16]��CeԪ�صIJ����ܹ���ɢHg0����λ�㣬�������������Mn4+�ı�������ǿ��������������ԭ����������Fe6Mn1-xCex�������е��ѹ�����λ����Mn�����������Ce����ή��Mn���������еı�������ˣ������Ce���뵼�����������ѹ����ܵĽ��͡�
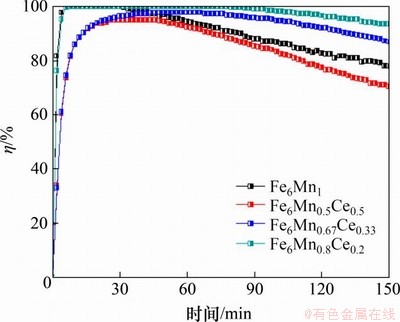
ͼ2��Ce���������������ѹ�Ч�ʵ�Ӱ��
Fig. 2��Effect of Ce addition amount on mercury removal efficiency

ͼ3��Ce�������Ե�λ��������������������Ӱ��
Fig. 3��Effect of Ce addition amount on mercury adsorption capacity of per unit mass sorbent
2.1.2�������¶ȵ�Ӱ�졡
ʵ�鿼����N2�����������¶�Ϊ100��150��200��250 ����������ѹ���Ӱ�죬��ͼ4��ʾ����ͼ4��֪��150 ��ʱ��Fe6Mn0.8Ce0.2���ѹ�Ч�����150 minʱ����ά��93.4%���ѹ�Ч�ʣ������¶���200 ��ʱ�ѹ�Ч�����Խ��ͣ����������¶ȴﵽ250 ��ʱ���ѹ�Ч���轵��29%��ͼ5��ʾΪ�¶ȶԵ�λ��������������������Ӱ�졣��ͼ5��֪�����¶�Ϊ150 ��ʱ����λ�����������Ĺ���������ﵽ45.36 ��g/g������Ҫ����Ϊ�������ѹ����̴������������ͻ�ѧ����2�ַ�ʽ[17-18]�����¶Ƚϵ�ʱ�������������ý�ǿ����ѧ�������ʽ�����������������������Ч�ʵ�Ӱ���С���¶����ߣ���ǿ�˲��뷴Ӧ���ʵĻ��ԣ������Hg0���������������λ��ĽӴ����ʣ��Ӷ��ٽ�����������Fe6Mn0.8Ce0.2�������ѳ�Hg0��Ҫ�ǻ�ѧ������Hg0���������е�O��ϳ�HgO���������������Ӧ�����У�Mn�ļ�̬�ή�ͣ���������������Ce������Ĵ��ڣ��ܹ���Mn������֮��ͨ���������ԭת�Ƶ���[19]���Ӷ�ʵ��Mn����λ�����������ˣ���һ���¶ȷ�Χ�ڣ���������¶��ܹ���Ч�ٽ������ѳ���Ȼ������������������Ӧ���棬���»ᵼ������������������Ĺ��Ѹ����������ߵ��¶�Ҳ��ʹ�����������ս������ƻ����϶�ṹ��

ͼ4�������¶ȶ��������ѹ�Ч�ʵ�Ӱ��
Fig. 4��Effect of temperature on mercury removal efficiency
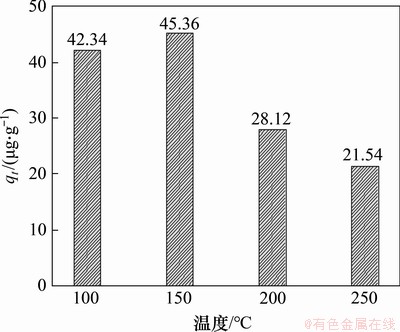
ͼ5���¶ȶԵ�λ��������������������Ӱ��
Fig. 5��Effect of temperature on mercury adsorption amount of per unit mass sorbent
2.1.3��SO2��Ӱ�졡
ͼ6��ʾΪSO2���������ѹ�Ч�ʵ�Ӱ�졣���У�O2���������Ϊ6%��SO2������Ũ��Ϊ1 200 mg/m3���¶�Ϊ150 �棬ƽ����ΪN2����ͼ6��֪��Fe6Mn1�Լ�Fe6Mn0.8Ce0.2�ڴ�N2�����¾����ָ���75%���ѹ�Ч�ʣ�Fe6Mn0.8Ce0.2�����Fe6Mn1���Ÿ��ߵ��ѹ�Ч�ʡ���������ֻ����1 200 mg/m3��SO2��Fe6Mn1��������150 min���ѹ�Ч��ֻ��33.03%��SO2��Fe6Mn1���������ż�����������á�һ��������ΪSO2��Hg0֮������������������[17, 20-24]����һ���棬SO2���������MnO2������Ӧ�����ѹ�����λ�����γ������������ʣ�ʹMnO2ʧȥ�ѹ�����[25]��Ȼ������Fe6Mn0.8Ce0.2���ѹ�����Ҳ�ܵ������ƣ�������ܱ�����50%���ҵ��ѹ�Ч�ʣ�˵��Ce�IJ��������Fe6Mn0.8Ce0.2�Ŀ�SO2���ܣ���Ҫ��ΪCe�������Խ�����SO2������Ce�������ﷴӦ���Ӷ��ܹ�����Mn����λ�㲻��SO2��������ģ��������ͬʱ�ټ���6%(�������)O2��Fe6Mn1��Fe6Mn0.8Ce0.2���ѹ����ܾ�������ߣ��ý��������һ��[8, 25-26]����ʱ��Fe6Mn0.8Ce0.2���ѹ��ʽӽ���N2�����µ��ѹ��ʣ��ɼ���O2����ʱ��Ce���������������SO2�������ԡ�
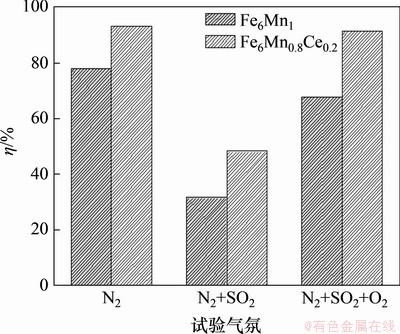
ͼ6��SO2���������ѹ�Ч�ʵ�Ӱ��
Fig. 6��Effect of SO2 on mercury removal efficiency
ͼ7��ͼ8��ʾ�ֱ�ΪO2���������Ϊ6% ʱ��SO2����Ũ�ȶ�Fe6Mn0.8Ce0.2�������ѹ�Ч�ʺ͵�λ��������������������Ӱ�졣��ͼ7��ͼ8��֪����SO2������Ũ��Ϊ1 200 mg/m3ʱ��Fe6Mn0.8Ce0.2���ѹ�Ч���Լ���λ���������������������SO2������Ũ��Ϊ600 mg/m3��1 200 mg/m3�����£����������ѹ�Ч�ʼ���λ������������������������٣�������SO2����Ũ�Ƚ�һ��������Fe6Mn0.8Ce0.2���ѹ�Ч���������ͣ�����������SO2����Ũ��Ϊ2 400 mg/m3������70%���ѹ�Ч�ʣ�˵���������Ŀ�SO2Ч�����ã�����һ����Ϊ�����Ŀ�SO2����Ũ�����䡣

ͼ7��SO2����Ũ�ȶ��������ѹ�Ч�ʵ�Ӱ��
Fig. 7��Effect of SO2 mass concentration on mercury removal efficiency
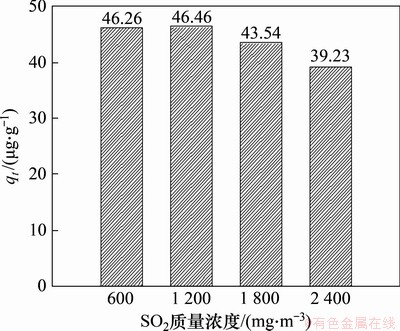
ͼ8��SO2����Ũ�ȶԵ�λ��������������������Ӱ��
Fig. 8��Effect of SO2 mass concentration on mercury adsorption capacity of per unit mass sorbent
2.1.4��Fe6Mn0.8Ce0.2�������ѹ����ԡ�
ͼ9��ʾΪFe6Mn0.8Ce0.2�����������������Ѹ�����ͼ����ͼ9���Կ����������߽���1����ֵΪ380 ��ķ壬���¶��¶�Ӧ�Ĺ���������̬ΪHgO[27]��HgO��380 �����һ�ֽ����ɵ��ʹ���˵��Hg��Fe6Mn0.8Ce0.2����������Ҫ�γ���HgO[28]�������Ѹ������ϲ�δ�۲쵽�����壬˵���˹�����ֻ��ǿ�����õ���HgO����������ʽ�Ĺ���������γɣ��¶ȸ���150 ��ʱ��ʼ������Hg0���ݳ���˵���������������������Ĺ���
ͼ10��ʾΪ����������Fe6Mn0.8Ce0.2��N2�������ѹ�Ч�ʵ�Ӱ�졣��ͼ10��֪������5������ѭ��������Fe6Mn0.8Ce0.2���ѹ�Ч�ʾ�������95%���ϣ����������������нϺõ��������ԡ���Ҫ��ΪCe���н�ǿ�ľ������������������������ܱ���ԭ�е�����ṹ�ͻ�ѧ���ԣ����������У������������HgO��ַֽ⣬��O2�ij�ֲ����£��ѹ�������ֵõ��˺ܺõĻָ����Ӷ�ʵ�����������ĸ�Ч������

ͼ9��Fe6Mn0.8Ce0.2�����������Ѹ�����
Fig. 9��Mercury temperature programmed desorption curve of Fe6Mn0.8Ce0.2 sorbent

ͼ10�������������ѹ�Ч�ʵ�Ӱ��
Fig. 10��Effect of regeneration times on mercury removal efficiency
2.2����������������
2.2.1����϶�ṹ��
ͼ11��ͼ12��ʾ�ֱ�Ϊ��������N2����/�Ѹ�����������ֲ�(BJH)��ͼ12�У�dV/ddΪ��λ���µĿ��ݻ�����ͼ11���Կ������Ʊ����õ��������������Ƶ�N2����/�Ѹ����ߡ������ѹ��p/p0��Сʱ������������Ļ�������˵�����dz��٣�����p/p0����0.6ʱ��������������������ӣ�˵�����������д����пʹ�ס�������������ƽ������֪�����������п�����Ϊ����

ͼ11��N2����/�Ѹ�������
Fig. 11��N2 adsorption/desorption isotherm curves
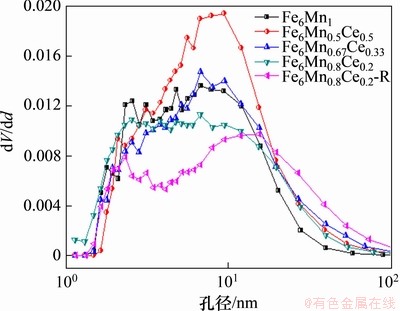
ͼ12�����ֲ�(BJH)
Fig. 12��Pore size distribution (BJH)
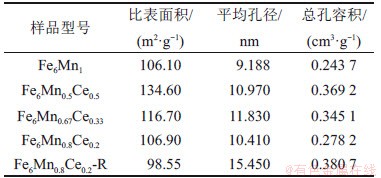
��1��ʾΪ�������Ŀ�϶�ṹ�������ӱ�1���Կ�����CeԪ�صIJ���������������ıȱ������ƽ�����Ϳ��ݻ������������ıȱ��������Ce���������Ӷ����ӣ�����2.1.1�ڿ�֪��Ce�������Ӳ������������������ѹ�Ч�ʡ��ɼ���CeԪ�صIJ�������Ż��������Ŀ�϶����������Ce���������ӽ������ѹ��������Mn�ĺ������Ӷ��������������ѹ�Ч�ʷ�����С��5���������Fe6Mn0.8Ce0.2����������ȱ�������н��ͣ���ƽ�������ܿ��ݻ���������ǰ�Ĵ�
��1���������Ŀ�϶�ṹ����
Table 1��Pore structure parameters of sorbent
2.2.2�����Է�����VSM����
ͼ13��ʾΪ�������Ĵ��ͻ���(VSM)��ͼ����ͼ13���Կ�����Fe6Mn1��Fe6Mn0.8Ce0.2��Fe6Mn0.8Ce0.2-R�ıȱ��ʹŻ�ǿ�ȷֱ�Ϊ51.1��45.8��42.8 A��m2/kg��3�������������ֳ���˳���ԣ���������С���Ż��ͺ���Ժ��Բ��ơ�Ce�ļ���ʹ��Fe6Mn1�������Ĵ������н��ͣ�������5�����������Fe6Mn0.8Ce0.2-R����״̬��Fe6Mn0.8Ce0.2�Ľӽ�����Ҳ��ζ������������Ӱ���������Ĵ��ԡ��Ż����Ա�֤�˴���Fe6Mn0.8Ce0.2��������¶���ⲿ�ų������ôŻ�����ˣ����ų����Ƴ�ʱ�������������������·�ɢ�����ۼ�����������������������Բ�δ�����ϴ�ı仯����֤�������������������յĿ��ܡ�

ͼ13����������VSMͼ
Fig. 13��VSM diagram of sorbent
2.2.3��XRD������
ͼ14��ʾΪFe6Mn1-xCex��XRDͼ�ס���ͼ14���Է����������д��ڶྦྷ�ṹ������ֵλ��2��Ϊ29.8�㣬35.5�㣬43.6�㣬56.7���64.4��ʱ�����Ӧ������ΪFe3O4��ͼ14��δ�������Ե��й�Ce��Mn�ľ���ṹ��������Ce��Mn�Ѿ�ȫ�����뵽�������У���ˣ��������Ĵ�����Ҫ��Fe3O4�ṩ[29]����MnO2�������������ѹ�����Ҫ�������ʣ�CeO2�ڵ�ʧ�������ܹ����õ�������������������ԭ��������ͬCe���������������еľ���ṹ������������û�����Ե����𣬿�������ΪCe�ĺ����Ƚ�С��Fe6Mn0.8Ce0.2����������-����ѭ����XRDͼ����ʾ������ǰ��û�����Ա仯����������������������ָֻ��˼��ߵ��ѹ�������˵��������������Ce��Mn�����������������ԭ��Ӧ�������˸��̵ĺ�����Ϊ�����ѹ��ṩ��֧�֡�

ͼ14����������XRDͼ��
Fig. 14��XRD patterns of sorbent
3 ����
1) ��150 ��ʱ��Fe6Mn0.8Ce0.2ӵ����ǿ���ѹ�������Ce������Ż��������Ŀ�϶�ṹ����������Ce���ӻή���ѹ��������Mn�ĺ���������Fe6Mn1-xCex���ѹ����ܽ��͡�
2) Ce�IJ��������Fe6Mn0.8Ce0.2�Ŀ�SO2���ܣ���SO2��O2ͬʱ����ʱ��Fe6Mn0.8Ce0.2�Ŀ�SO2�����õ�������ǿ��
3) Fe6Mn0.8Ce0.2�������ô������������ܣ��������ﻯ���Ա仯��С��5������ѭ���ѹ�����ýϸ��ѹ�Ч�ʣ��ѹ�����ΪHgO��
�ο����ף�
[1] ZHAO Shilin, PUDASAINEE D, DUAN Yufeng, et al. A review on mercury in coal combustion process: content and occurrence forms in coal, transformation, sampling methods, emission and control technologies[J]. Progress in Energy and Combustion Science, 2019, 73: 26-64.
[2] ZHOU Qiang, DUAN Yufeng, CHEN Mingming, et al. Studies on mercury adsorption species and equilibrium on activated carbon surface[J]. Energy & Fuels, 2017, 31(12): 14211-14218.
[3] China Council for International Cooperation on Environment and Development(CCICED). Special policy study on mercury management in China[R]. Beijing: CCICED, 2011: 447-448.
[4] ZHAO Shilin, DUAN Yufeng, CHEN Lei, et al. Study on emission of hazardous trace elements in a 350 MW coal-fired power plant. Part 1: mercury[J]. Environmental Pollution, 2017, 229: 863-870.
[5] HU Changxing, ZHOU Jinsong, HE Sheng, et al. Effect of chemical activation of an activated carbon using zinc chloride on elemental mercury adsorption[J]. Fuel Processing Technology, 2009, 90(6): 812-817.
[6] ¬ƽ, ʷ����, Ҷ����, ��. ��������ȼ���ܵ������ѹ�����[J]. ������չ, 2019, 38(5): 2471-2478.
LU Ping, SHI Jiateng, YE Yangtian, et al. In-duct injection mercury removal characteristics of biochar prepared under biomass reburning condition[J]. Chemical Industry and Engineering Progress, 2019, 38(5): 2471-2478.
[7] YANG Shijian, GUO Yongfu, YAN Naiqiang, et al. Elemental mercury capture from flue gas by magnetic Mn�CFe spinel: effect of chemical heterogeneity[J]. Industrial & Engineering Chemistry Research, 2011, 50(16): 9650-9656.
[8] ZENG Xiaobo, XU Yang, ZHANG Bi, et al. Elemental mercury adsorption and regeneration performance of sorbents FeMnOx enhanced via non-thermal plasma[J]. Chemical Engineering Journal, 2017, 309: 503-512.
[9] YANG Shijian, GUO Yongfu, YAN Naiqiang, et al. Capture of gaseous elemental mercury from flue gas using a magnetic and sulfur poisoning resistant sorbent Mn/��-Fe2O3 at lower temperatures[J]. Journal of Hazardous Materials, 2011, 186(1): 508-515.
[10] LIAO Y, XIONG Shangchao, DANG H, et al. The centralized control of elemental mercury emission from the flue gas by a magnetic rengenerable Fe-Ti-Mn spinel[J]. Journal of Hazardous Materials, 2015, 299: 740-746.
[11] XIONG Shangchao, XIAO Xin, HUANG Nan, et al. Elemental mercury oxidation over Fe-Ti-Mn spinel: performance, mechanism, and reaction kinetics[J]. Environmental Science & Technology, 2017, 51(1): 531-539.
[12] XU Haomiao, XIE Jiangkun, MA Yongpeng, et al. The cooperation of FeSn in a MnOx complex sorbent used for capturing elemental mercury[J]. Fuel, 2015, 140: 803-809.
[13] TAO Shasha, LI Caiting, FAN Xiaopeng, et al. Activated coke impregnated with cerium chloride used for elemental mercury removal from simulated flue gas[J]. Chemical Engineering Journal, 2012, 210: 547-556.
[14] WANG Yan, LI Caiting, ZHAO Lingkui, et al. Study on the removal of elemental mercury from simulated flue gas by Fe2O3-CeO2/AC at low temperature[J]. Environmental Science and Pollution Research, 2016, 23(6): 5099-5110.
[15] XIE Yine, LI Caiting, ZHAO Lingkui, et al. Experimental study on HgO removal from flue gas over columnar MnOx-CeO2 activated coke[J]. Applied Surface Science, 2015, 333: 59-67.
[16] �ų�, �⽭, ������. ��̼������TiO2�ѳ���������ʵ���о�[J]. �Ϻ�����ѧԺѧ��, 2016, 32(2): 135-139.
ZHANG Chong, WU Jiang, CHEN Xiantuo. Experiment research of mercury removal using Ce, C-TiO2 from flue gas[J]. Journal of Shanghai University of Electric Power, 2016, 32(2): 135-139.
[17] ��ǿ. ���������������ѹ���ʵ�鼰�����о�[D]. �Ͼ������ϴ�ѧ��Դ�뻷��ѧԺ, 2016: 27-28.
ZHOU Qiang. Experimental and mechanism researches of in-duct mercury removal by modified sorbent injection[D]. Nanjing: Southeast University. School of Energy and Environment, 2016: 27-28.
[18] ����. MnxOy/Al2O3�������ѹ������������о�[D]. �Ͼ������ϴ�ѧ��Դ�뻷��ѧԺ��2017: 25-26.
XU Jing. Study on characteristics of MnxOy/Al2O3 regenerable mercury adsorbent[D]. Nanjing: Southeast University. School of Energy and Environment, 2017: 25-26.
[19] WU Huiyu, LI Caiting, ZHAO Lingkui, et al. Removal of gaseous elemental mercury by cylindrical activated coke loaded with CoOx-CeO2 from simulated coal combustion flue gas[J]. Energy & Fuels, 2015, 29(10): 6747-6757.
[20] WAN Qi, DUAN Lei, HE Kebin, et al. Removal of gaseous elemental mercury over a CeO2-WO3/TiO2 nanocomposite in simulated coal-fired flue gas[J]. Chemical Engineering Journal, 2011, 170(2/3): 512-517.
[21] YANG W, HUSSAIN A, ZHANG J, et al. Removal of elemental mercury from flue gas using red mud impregnated by KBr and KI reagent[J]. Chemical Engineering Journal, 2018, 341: 483-494.
[22] YANG Wei, LI Ying, SHI Shuo, et al. Mercury removal from flue gas by magnetic iron-copper oxide modified porous char derived from biomass materials[J]. Fuel, 2019, 256: 115977.
[23] ����. ���������±������������ʽ��ѳ�ȼú�������ʹ����о�[D]. ��: ���մ�ѧ��Դ�붯������ѧԺ, 2018: 42-43.
XU Wen. Study on mercury removal from coal-fired flue gas by metal oxide/halide modified bio-chars[D]. Zhenjiang: Jiangsu University. School of Energy and Power Engineering, 2018: 42-43.
[24] TONG Li, XU Wenqing, ZHOU Xuan, et al. Effects of multi-component flue gases on HgO removal over HNO3-modified activated carbon[J]. Energy & Fuels, 2015, 29(8): 5231-5236.
[25] DONG Lu, HUANG Yaji, CHEN Hao, et al. Magnetic ��-Fe2O3-loaded attapulgite sorbent for HgO removal in coal-fired flue gas[J]. Energy & Fuels, 2019, 33(8): 7522-7533.
[26] TAN Zengqiang, SU Sheng, QIU Jianrong, et al. Preparation and characterization of Fe2O3-SiO2 composite and its effect on elemental mercury removal[J]. Chemical Engineering Journal, 2012, 195/196: 218-225.
[27] RUMAYOR M, DIAZ-SOMOANO M, LOPEZ-ANTON M A, et al. Mercury compounds characterization by thermal desorption[J]. Talanta, 2013, 114: 318-322.
[28] ZHANG Shibo, DIAZ-SOMOANO M, ZHAO Yongchun, et al. Research on the mechanism of elemental mercury removal over Mn-based SCR catalysts by a developed Hg-TPD method[J]. Energy & Fuels, 2019, 33(3): 2467-2476.
[29] HOSSEINI M, MEMARI Z, GANJALI M R, et al. A novel mercury-sensitive fluorescent nano-chemosensor using new functionalized magnetic core-shell Fe3O4@SiO2 nanoparticles[J]. International Journal of Environmental Research, 2014, 8(4): 861-870.
(�༭ ����ƽ)
�ո����ڣ� 2020 -06 -08; �����ڣ� 2020 -08 -23
������Ŀ(Foundation item)��������Ȼ��ѧ����������Ŀ(51906115)������ʡ��Ȼ��ѧ����������Ŀ(BK20190709)������ʡ��У��Ȼ��ѧ����������Ŀ(17KJD470003)���й���ʿ���ѧ����������Ŀ(2017M621780) (Project(51906115) supported by the National Natural Science Foundation of China; Project(BK20190709) supported by the Natural Science Foundation of Jiangsu Province; Project(17KJD470003) supported by the University Natural Science Foundation of Jiangsu Province; Project(2017M621780)supported by the Postdoctoral Science Foundation of China)
ͨ�����ߣ���ǿ����ʿ����ʦ������ȼú����Ⱦ���ŷſ����о���E-mail��zhouqiang8@njnu.edu.cn
���ø�ʽ�� ����, ��ǿ, ���, ��. Ce����Fe-Mn�����������ѹ������������о�[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2021, 52(1): 144-152.
Citation: TAO Xin, ZHOU Qiang, SHANG Yu, et al. Study on mercury removal and regeneration characteristics of Ce modified Fe-Mn magnetic sorbent[J]. Journal of Central South University(Science and Technology), 2021, 52(1): 144-152.